Цистеин

| |||
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
Cistein
| |||
| Други називи
2-Амино-3-меркаптопропанска киселина
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| Абревијација | Cis, C | ||
| ChemSpider | |||
| ECHA InfoCard | 100.000.145 | ||
| Е-бројеви | Е920 (глазинг агентс, ...) | ||
| МеСХ | Цyстеине | ||
| |||
| Својства | |||
| C3H7NO2S | |||
| Моларна маса | 121,15 g·mol−1 | ||
| Агрегатно стање | бели кристали или прах | ||
| Тачка топљења | 240 ºC decomp. | ||
| растворљив | |||
| Хирална ротација [α]D | +9.4º (H2O, ц = 1.3) | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||
Цистеин (Cys или C)[4] је α-аминокиселина са хемијском формулом HO2CCH(NH2)CH2SH. Она је неесенцијална аминокиселина, што значи да се она може биосинтетисати у људском телу. Њени кодони су УГУ и УГЦ. Бочни ланац цистеина, тиол, је неполаран и зато се цистеин обично класификује као хидрофобна аминокиселина. Тиолни бочни ланац често учествује у ензиматским реакцијама, служећи као нуклеофил. Тиол је подложан оксидацији којом се формира дисулфидни дериват цистин, који има важну структурну улогу у многим протеинима. Цистеин је добио име по цистину.
Извори[уреди | уреди извор]
Прехрамбени извори[уреди | уреди извор]
Мада је класификована као неесенцијална аминокиселина, у ретким случајевима, цистеин може да буде есенцијалан за децу, старије особе, и индивидуе са специфичним метаболичким болестима, или код оболелих од синдрома малапсорпције. Људско тело обично може да синтетише цистеин под нормалним физиолошким условима, ако је довољна количина метионина доступна. Цистеин је подложан катаболизи у гастроинтестиналном тракту и крвној плазми. За разлику од реактивног цистеина, цистин неизмењен пролази кроз ГИ тракт и крвну плазму, а по уласку у ћелије он се брзо редукује у два молекула цистеина.
Цистеин се налази у већини високопротеинских извора хране. Неки од њих су:
- Животињски извори: свињетина, месо кобасица, пилетина, ћуретина, јаја, млеко, протеин сурутке, сир, јогурт
- Биљни извори: црвене паприке, бели лук, црни лук, броколи, кељ, овас, гранола, клице жита, комбуха
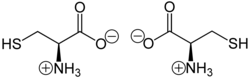
Као и друге аминокиселине, цистеин има амфотерни карактер.
Индустријски извори[уреди | уреди извор]
L-Цистеин се некад индустријски добијао путем хидролизе косе и кератина. У данашње време главни индустријски приступ је ферментација уз употребу мутиране Е. цоли. Wacker Chemie је увео начин добијања ис субституисаних тиазолина.[5] У складу са том технологијом, L-цистеин се производи хидролизом рацемиске 2-амино-Δ2-тхиазолин-4-карбоксилне киселине користећи Псеудомонас тхиазолинопхилум.[6]
Биосинтеза[уреди | уреди извор]

Код животиња, биосинтеза почиње са аминокиселином серином. Сумпор долази из метионина, који се конвертује у хомоцистеин кроз интермедиар С-аденозил метионин. Цистатионин бета-синтетаза након тога комбинује хомоцистеин и серин у форму асиметричног тиоетра цистатионина. Ензим цистатионин гама-лијаза конвертује цистатионин у цистеин и алфа-кето бутират. У биљкама и бактеријама, биосинтеза цистеина исто почиње од серина, који се конвертује у О-ацетил серин ензимом серин трансацетилаза. Ензим О-ацетилсерин (тиол)-лијаза, користећи сулфидне изворе, конвертује овај естер у цистеин, ослобађајући ацетат.[7]
Биолошке функције[уреди | уреди извор]
Тиол група цистеина има нуклеофилни карактер, и лако се оксидује. Реактивност је појачана кад је тиол јонизован. pKa вредности цистеинских остатака у протеинима су близо неутралности, тако да су они често у њиховом реактивном тиолатном облику унутар ћелије.[8] Због високе реактивности тиол групе, цистеин има бројне биолошке функције.
Прекурзор антиоксиданта глутатиона[уреди | уреди извор]
Као последица склоности тиола да подлеже редокс реакцијама, цистеин поседује антиоксидансне особине. Цистеинске антиоксидансне особине долазе до изражаја на пример у случају трипептида глутатиона, који је присутан у људском телу, као и код низа других организама. Системска доступност оралног глутатиона (ГСХ) је незнатна. Из тог разлога он се мора биосинтетизовати из конститутивних аминокиселина: цистеина, глицина, и глутаминске киселине. Глутаминска киселина и глицин су лако доступни из хране, док је расположивост цистеина може бити ограничавајући фактор.
Дисулфидне везе[уреди | уреди извор]
Дисулфидне везе играју важну улогу у савијању и стабилности неких протеина, поготову протеина излучених у екстрацелуларни медијум.[9] Пошто већина ћелијских компартмана има редукујуће окружење, дисулфидне везе су генерално нестабилне у цитосолу.

Дисулфидне везе протеина се формирају оксидацијом тиол групе цистеинских остатака. Друга аминокиселина која садржи сумпор, метионин, не може да формира дисулфидне везе. Агресивнији оксиданти конвертују цистеин у кореспондирајућу сулфинску и сулфонску киселина. Цистеин остаци играју важну улогу у умрежавања протеина, што повећава крутост протеина и исто тако доприноси стварању протеолитичке отпорности. Унутар ћелије, дисулфидни мостови између цистеинских остатака унутар полипептида подржавају протеинску секундарну структуру. Инсулин је пример протеина са цистин умрежавањем, где су два независна пептидна ланца повезана паром дисулфидних веза.
Протеин дисулфид изомераза катализује коректну формацију дисулфидних веза; ћелија преноси де-хидро аскорбинску киселину у ендоплазматични ретикулум, што оксидира средину. У таквом окружењу, цистеини су углавном оксидизовани до цистина који не функциониши као нуклеофили.
Прекурзор гвожђе-сумпор кластера[уреди | уреди извор]
Цистеин је важан извор сулфида у људском метаболизму. Сулфид у гвожђе-сумпор кластеру, и у нитрогенази, је екстрахован из цистеина, који се истовремено конвертује у аланин.[10]
Везивање за металне јоне[уреди | уреди извор]
Сем протеина са гвожђе-сумпорним мотивом, многи други метални кофактори су у ензимима везани за тиолат субституент цистеинил остатака. Примери таквих констракта су цинк у цинковом прсту и алкохол дехидрогенази, бакар у плавим бакарним протеинима, и никл у [НиФе]-хидрогенази.[11] Тиолна група има јак афинитет за тешке метале, тако да се протеини који садрже цистеин, као што је металотионеин, чврсто везују за метале као што је жива, олово, и кадмијум.[12]
Пост-транслационе модификације[уреди | уреди извор]
Поред оксидације у цистин, цистеин учествује у многим пост-транслационим модификацијама. Нуклеофилна тиол група омогућава цистеину да се коњугује са другим групама, нпр., у пренилацији. Убиквитин лигазе трансферирају убиквитин на њихове зависне протеине и каспазе, који учествује у протеолизи у апоптотичном кругу. Интеини често функционишу уз помоћ каталитичког цистеина. Улоге су типично ограничене на део интрацелуларног миљеа, где је окружење редукујуће, и цистеин није оксидован у цистин.
Примена[уреди | уреди извор]
Цистеин, првенствено L-енантиомер, је прекурзор у прехрамбеној, фармацеутској, и козметичкој индустрији. Јеан од најобимнијих апликација је производња зачина. На пример, реакција цистеина са шећерима у Maillard reakciji производи укус меса.[13] L-цистеин се користи као помоћно средство за печење хране.[14]
У пољу козметике, цистеин се користи у перманентни талас апликацијама углавном у Азији. У овој врсти примене цистеин се користи за раскидање дисулфидних веза у кератину косе.
Цистеин је веома популаран циљ за експерименте усмереног обележавања којима се испитује биомолекулска структура и динамика. Малеимиди се селективно причвршћују на цистеин путем ковалентног Мицхаел додавања. Положајем усмерено спинско обележавање за ЕПР, или пара-магнетном релаксацијом побољшан НМР, такође користи цистеин екстензивно.
У извештају из 1994 од стране пет топ произвођача цигарета, цистеин је један од 599 адитива за цигарете. Као и за већину других адитива цигарета сврха његове употреба или улога је непозната.[15]
Овце[уреди | уреди извор]
Цистеин је неоходан у узгоју оваца да би оне могле да производе вуну. То је есенцијална аминокиселина која се мора узимати као храна из траве. Консеквентно, у току суше, овце престану да производе вуну. Трансгенетске овце које могу да стварају цистеин су развијене.[16]
Референце[уреди | уреди извор]
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Еван Е. Болтон; Yанли Wанг; Паул А. Тхиессен; Степхен Х. Брyант (2008). „Цхаптер 12 ПубЦхем: Интегратед Платформ оф Смалл Молецулес анд Биологицал Ацтивитиес”. Аннуал Репортс ин Цомпутатионал Цхемистрy. 4: 217—241. дои:10.1016/С1574-1400(08)00012-1.
- ^ Wеаст, Роберт C., ур. (1981). ЦРЦ Хандбоок оф Цхемистрy анд Пхyсицс (62нд изд.). Боца Ратон, ФЛ: ЦРЦ Пресс. ИСБН 0-8493-0462-8..
- ^ „Номенцлатуре анд сyмболисм фор амино ацидс анд пептидес (ИУПАЦ-ИУБ Рецоммендатионс 1983)”, Пуре Аппл. Цхем., 56 (5): 595—624, 1984, дои:10.1351/пац198456050595
- ^ Мартенс, Јüрген; Офферманнс, Хериберт; Сцхерберицх, Паул (1981), „Фациле Сyнтхесис оф Рацемиц Цyстеине”, Ангеw. Цхем. Инт. Ед. Енгл., 20 (8): 668, дои:10.1002/ание.198106681
- ^ -Драуз, Карлхеинз; Граyсон, Иан; Клееманн, Аxел; Криммер, Ханс‐Петер; Леуцхтенбергер, Wолфганг; Wецкбецкер, Цхристопх (2007). „Амино Ацидс”. Уллманн'с Енцyцлопедиа оф Индустриал Цхемистрy. ИСБН 9783527303854. дои:10.1002/14356007.а02_057.пуб2.
- ^ Хелл, Рüдигер (1997), „Молецулар пхyсиологy оф плант сулфур метаболисм”, Планта, 202 (2): 138—48, ПМИД 9202491, С2ЦИД 2539629, дои:10.1007/с004250050112.
- ^ Булај, Грзегорз; Кортемме, Тања; Голденберг, Давид П. (1998), „Ионизатион-реацтивитy релатионсхипс фор цyстеине тхиолс ин полyпептидес.”, Биоцхемистрy, 37 (25): 8965—72, ПМИД 9636038, дои:10.1021/би973101р.
- ^ Севиер, Царолyн С.; Каисер, Цхрис А. (2002), „Форматион анд трансфер оф дисулпхиде бондс ин ливинг целлс” (ПДФ), Натуре Рев. Мол. Целл. Биол., 3 (11): 836—47, ПМИД 12415301, С2ЦИД 2885059, дои:10.1038/нрм954.
- ^ Лилл, Роланд; Мüхленхофф, Улрицх (2006), „Ирон-Сулфур Протеин Биогенесис ин Еукарyотес: Цомпонентс анд Мецханисмс”, Анн. Рев. Целл Дев. Биол., 22: 457—86, ПМИД 16824008, дои:10.1146/аннурев.целлбио.22.010305.104538.
- ^ Липпард, Степхен Ј.; Берг, Јеремy M. (1994), Принциплес оф Биоинорганиц Цхемистрy, Милл Валлеy, ЦА: Университy Сциенце Боокс, ИСБН 978-0-935702-73-6.
- ^ Бакер, Давид Х.; Цзарнецки-Маулден, Гаил L. (1987), „Пхармацологиц роле оф цyстеине ин амелиоратинг ор еxацербатинг минерал тоxицитиес”, Ј. Нутр., 117 (6): 1003—10, ПМИД 3298579, дои:10.1093/јн/117.6.1003.
- ^ Хуи, Нип W.; Рогерс, Р. (2001), Хуи, Y., ур., Меат сциенце анд апплицатионс, ЦРЦ Пресс, стр. 74, ИСБН 978-0-8247-0548-0.
- ^ Фоод Ингредиентс анд Цолорс, У.С. Фоод анд Друг Администратион, 2004, Архивирано из оригинала 12. 05. 2009. г., Приступљено 6. 9. 2009.
- ^ Мартин, Террy (25. 6. 2009), Тхе Лист оф Аддитивес ин Цигареттес, абоут.цом, Архивирано из оригинала 23. 05. 2006. г., Приступљено 6. 9. 2009.
- ^ Поwелл БЦ, Wалкер СК, Баwден ЦС, Сивапрасад АВ, Рогерс ГЕ (1994). „Трансгениц схееп анд wоол гроwтх: поссибилитиес анд цуррент статус.”. Репрод Фертил Дев. 6 (5): 615—23. ПМИД 7569041. дои:10.1071/рд9940615.
Литература[уреди | уреди извор]
Види још[уреди | уреди извор]
Спољашње везе[уреди | уреди извор]
- Интернационални институт за камен на бубрегу Архивирано на сајту Wayback Machine (13. мај 2019)
- Цистеин Архивирано на сајту Wayback Machine (10. новембар 2016)
- Хидрофобна природа цистеина
- 978-952-10-3056-7 Могућа хемопревенција рака цистеином
- Бионет школа
 Медији везани за чланак Цистеин на Викимедијиној остави
Медији везани за чланак Цистеин на Викимедијиној остави


