Policistična bolest bubrega
| Policistična bolest bubrega | |
|---|---|
 | |
| Klasifikacija i spoljašnji resursi | |
| Specijalnost | medicinska genetika |
| Patient UK | [https://patient.info/doctor/autosomal-dominant-polycystic-kidney-disease autosomal-dominant-polycystic-kidney-disease Policistična bolest bubrega] |
Policistična bolest bubrega (akronim PBB) je genetski poremećaj kod kojeg se u bubrezima razvijaju i rastu ciste. Ovaj nasledni monogenski poremećaj može da utiče i na druge organe, uključujući jetru, pankreas, mozak i krvne sudove. Zbog cistama uvećanih bubrega, onemogućena je njihova odgovarajuća funkcija što rezultuje otkazom funkcija bubrega, a samim tim i potrebom za nadoknadu bubrežne funkcije: dijalizom ili transplantacijom bubrega.
Rana dijagnoza asimptomatskih osoba sa policističnom bolesti bubrega pruža mogućnost maksimalne preventivne nege kao što je: stroga kontrola krvnog pritiska, praćenje vanbubrežnih (ekstrarenalnih) manifestacijama (npr kongenitalna fibroza jetre, kardiovaskularnih bolesti), izbegavanje potencijalnih prehrambenih i životih faktora koji utiču na progresiju bolesti i mogućnost prilagođavanja terapije u skladu sa stadijuma bolesti. Sve intervencije kod policistične bolesti bubrega odlažu dijalizu ili transplantaciju bubrega i time poboljšavaju kvalitet života bolesnika.
Istorija[uredi | uredi izvor]
Pariski hirurg Feliks Lejars (1863—1932) prvi je upotrebio izraz policistični bubrezi u svojoj disertaciji iz 1888. godine.[1][2]
Kanadski lekar Villijem Osler nekoliko decenija kasnije detaljnije je opisao bolest (1915).[3][4]
Do sredine 20. veka objavljeno je samo nekoliko publikacija koje su se bavile ovom bolešću.
Dalgard je bio prvi istraživač koji je prepoznao da se policističnih bolest bubrega nasleđuje autosomno dominantno, i to je prikazao u svojoj disertaciji 1957. godine.[5] Potom su Rider i saradnici 1985. godine otkrili gen lokus PBB1 na humanom hromozomu 16.[6]
Epidemiologija[uredi | uredi izvor]
Krajnji stadijum bolesti najčešće nastupa u periodu od četvrte do šeste decenije života. Policistična bolest bubrega javlja se u celom svetu i pogađa jednu od 400 do 1.000 osoba.[7][8][9]
Kod oko 50% pacijenata, bolest u poslednjoj fazi zahteva dijalizu ili transplantaciju bubrega.
Patogeneza[uredi | uredi izvor]
Nastanak i razvoj cističnih bubrega zasniva se na cističkoj degeneraciji tubula (mokraćnih kanala) u bubrezima. U slučaju autozomno dominantnog nasleđene PBB, dolazi do sve većeg uvećanja bubrega tokom decenija. To može dovesti do funkcionalnog ograničenja do potpunog gubitka funkcije bubrega.[2]
Oba bubrega su podjednako pogođena, a u svakom organu može se formirati nekoliko stotina cista, koje izgledaju debele i elastične. Masa i zapremina bubrega mogu se značajno povećati kao rezultat stvaranja cisti. Dok zdrav bubreg ima prosečnu masu od 160 g, policistični bubrezi mogu težiti do 8 kg i meriti do 40×25×20 cm (ili do 20 litara) zapremine (zdrav bubreg meri: 12×6×3 cm 3 = 0,216 litara). I pored značajno povećane potrebe izmenjenih organa za prostorom, funkcionalni poremećaji od strane susednih organa se javljaju relativno retko.[10]
Ciste se nalaze i na meduli bubrega (lat. Medulla renis) i na korteksu bubrega (lat. Cortex renalis ). U principu, bilo koje područje nefrona može formirati cistu. Međutim, posebno su pogođeni glomeruli i Henleova petlja. Ciste su ispunjene onim što je poznato kao cevasti urin. Prečnik jedne ciste može značajno da varira od nekoliko milimetara do preko 100 mm. Velike ciste mogu sadržati nekoliko stotina mililitara tubularnog urina. Unutrašnjost ciste se sastoji od jednoslojnog skvamoznog ili jednoslojnog izopizmatičnog (kubnog) epitela. Kako bolest napreduje, može se povećati i broj i veličina prisutnih cista.[2]
Etiologija[uredi | uredi izvor]

Policistične promene na bubrezima su klinička slika koja se javlja kod niza bolesti. Mogu nastati sporadično kao odstupanje od normalnog razvoja bubrega ili se mogu steći u odraslom životu ( stečeni cistični bubrezi ). Mnogo češći uzrok (etiologija) ove bolesti su nasledni defekti određenih gena ( nasledni cistični bubrezi ).
Autozomno dominantna bolest policističnih bubrega ( ADPBB ) čini daleko najveći udeo.[2] Ova bolest je najčešći nasledni uzrok hronične bubrežne insuficijencije: od nje boluje oko 7% svih pacijenata na dijalizi.[11]
Razne druge – mnogo ređe – nasledne bolesti takođe izazivaju policistične bubrege. Mogu se javiti i stečeni cistični bubrezi, posebno kod pacijenata na dijalizi.[12] Pošto je velika većina cističnih bubrega uzrokovana ADPBB, termin „policistični bubreg“ se često koristi kao sinonim za ADPBB.
Oblici[uredi | uredi izvor]

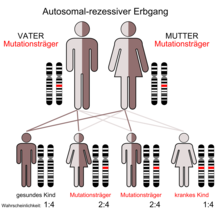
Autozomna dominantna policistična bolest bubrega[uredi | uredi izvor]
Autozomno dominantna (adultna) policistična bolest bubrega (skraćeno ADPBB) je dominantno nasledna anomalija koja se karakteriše cističnom dilatacijom (širenjem) svih delova nefrona. Osim u bubrezima, siste se mogu pojaviti i u jetri, gušterači i drugim organima.[13]
Autozomno dominantna (adultna) policistična bolest bubrega je učestalijiji obik policistične boleste bubrega, ali se klinička slika najčešće ne razvijaja sve do 30 ili 40 godine života pacijenta. Zato se nekad ADPBB naziva i adultni oblik PBB.
Izazvana je mutacijom PBB1 i PBB2 gena koji kodiraju policistin-1 (PC-1) ili policistin-2 (PC-2).[14][15]
Autozomna recesivna policistična bolest bubrega[uredi | uredi izvor]
Autozomna recesivna (infantilna) policistična bolest bubrega (skraćeno ) je recesivno nasledni poremećaj koji karakteriše cistična dilatacija sabirnih kanalića bubrega i kongenitalna fibroza jetre. Poznat je i pod zastarelim nazivom infantilni oblik PBB-a.
Autozomna recesivna (infantilna) policistična bolest bubrega je znatno ređi oblik koji pogađa decu.[16] Ona izaziva mutacija u PKHD1, genu koji kodira kompleks proteina fibrocistin/poliduktin (FPC). Mada je glavna klinička manifestacija bilateralni razvoj cista, ova mutacija, u kombinaciji sa drugim mutacijama, može biti uzrok veće težine bolesti i širokih fenotipskih varijacija.[17]
Dijagnoza[uredi | uredi izvor]

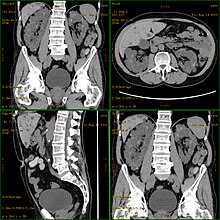
Dijagnoza se obično postavlja pomoću sonografije („ultrazvuka“)[18] ili drugih metoda snimanja, kao što je magnetna rezonanca.[19]
Uz savremenu opremu, ultrazvuk se može koristiti za dijagnostikovanje cista do veličine od 5 mm. Stopa ranog otkrivanja kod 20-godišnjih pacijenata je oko 90%.[20] Iako kompjuterska tomografija nudi veću rezoluciju uz bolji kvalitet slike, ona se ne koristi za skrining pacijenata, uglavnom zbog izloženosti zračenju, već samo za posebna dijagnostička pitanja.[2]
Biopsija, u kojoj se uklanja mala količina tkiva bubrega i jetre, koristi se u detinjstvu da se napravi razlika između ARPBB i ADPBB ( rani početak ). To znači da se morfološke promene u bazalnoj membrani mogu otkriti u vrlo ranoj fazi. ARPBB se dijagnostikuje određivanjem kongenitalne fibroze jetre.[2]
Pored patoanatomskog opisa bubrega i jetre, važnu ulogu ima i porodična anamneza (anamneza). Genetski zasnovani termini autozomno dominantni i autozomno recesivni se stoga uglavnom koriste za nasledne slučajeve bubrežnih cista.[21]
Identifikovanjem potencijalno zahvaćenih gena moguća je neinvazivna molekularna genetička dijagnostika. U mnogim slučajevima ova procedura može zameniti invazivnu biopsijsku dijagnostiku i omogućiti etiološku klasifikaciju. Ova klasifikacija zauzvrat otvara puteve za različite terapijske opcije za lečenje bolesti. Osetljivost za pravi pozitivan rezultat je oko 95%.[2]
Korelacija između genotipa i fenotipa je moguća samo u ograničenoj meri.[2] Analiza mutacije PKD1 gena je teška zbog njegove veličine (46 kodirajućih egzona i 14,2 kb transkripta). Pored toga, u zahvaćenom hromozomu 16 na genskom lokusu p13.1, prva 33 egzona PKD1 u tri homologne kopije (HG-A ˜21 kb, HG-B ˜17 kb i HG-C ˜8,5 kb; HG = homologno gen) su prisutni. Ovo čini specifično amplifikaciju korišćenjem lančane reakcije polimeraze (PCR) znatno težim.[2]
Poseban problem predstavlja molekularna genetička dijagnostika. Rana dijagnoza genetske predispozicije pacijenata omogućava preventivne mere i ranu suportivnu terapiju s jedne strane. S druge strane, rođaci i pacijenti mogu se već suočiti sa verovatnoćom da izbije bolest koja je opasna po život za nekoliko decenija kada je osoba još uvek dete. Stoga se rizici i koristi moraju pažljivo odmeriti pre postavljanja dijagnoze.[22]
Kod pacijenata sa porodičnom anamnezom (predispozicija), dijagnoza se može postaviti sonografskim putem od 20. godine života ako se mogu otkriti najmanje dve bubrežne ciste po bubregu. Nasuprot tome, odsutne ciste isključuju bolest kod osoba starijih od 30 godina.[23]
Diferencijalna dijagnoza[uredi | uredi izvor]
Uporedna genetika, klinička i radiološka slika karakteristična za ADPKD i ARPKD.
| Stanje | Slika | Genetika | Klinička i patološka slika | Radiološka slika |
|---|---|---|---|---|
| Autozomna recesivna policistična bolest bubrega | 
|
PKHD1 (6p12): fibrocistin / poliduktin |
|
|
| Autozomna dominantna policistična bolest bubrega | 
|
PKD1 (16p13,3): policistin-1 PKD2 (4q22): policistin-2 |
|
|
Terapija[uredi | uredi izvor]
Trenutno postoji samo jedan odobren lek za lečenje policistične bolesti bubrega ( tolvaptan). Oko 50% svih pacijenata sa akutnim oblikom PBB - koji čine većinu pacijenata sa policističnom bolešću bubrega - biće potrebna terapija zamene bubrega tokom svog života. Lečenje je moguće samo transplantacijom bubrega .
Simptomatska terapija[uredi | uredi izvor]
Regulacija arterijskog krvnog pritiska, obično uz pomoć ACE inhibitora, je od posebnog značaja kao pomoćna mera kod policističnih bubrega. Pored toga, postoji niz preporuka za pacijente sa cističnim bubrezima, koje ne omogućavaju izlečenje, ali usporavaju progresiju bolesti što je povoljnija za pacijenta.
Pošto se sumnja da kofein ubrzava rast cista, pacijenti treba da izbegavaju pića koja sadrže kofein ako je moguće.
Dijeta sa malo soli pomaže u snižavanju krvnog pritiska, što je povezano sa poremećenim izlučivanjem jona natrijuma.
Nesteroidne antiinflamatorne lekove , mešane analgetike , određene antibiotike i druge lekove toksične za bubrege treba u velikoj meri izbegavati.
Infekcije cista, s druge strane, leče se što je ranije moguće antibioticima koji prodiru u žuč .
Terapija zamene bubrega[uredi | uredi izvor]

Samo terapija zamene bubrega, odnosno dijaliza ili transplantacija bubrega, obezbeđuje opstanak pacijenta u slučajevima završnog stadijuma bubrežne insuficijencije. U većini slučajeva dijaliza ima oblik hemodijalize, pošto je trbušna šupljina veoma skučena zbog prevelikih bubrega - a često i jetre - i peritonealna dijaliza stoga nije moguća.
Ako je moguće, transplantacija bubrega je poželjnija od dijalize. Omogućava pacijentima da povrate svoje fizičke performanse, kvalitet života i socijalnu integraciju. Takođe značajno produžava očekivani životni vek u poređenju sa dijalizom. Duga vremena čekanja na bubrege donora su problematična zbog malog broja dostupnih donorskih bubrega.
U poređenju sa prethodnom praksom, policistični bubrezi se uklanjaju pre transplantacije samo u izuzetnim slučajevima, na primer kada zapremina bubrega dostigne kritičnu veličinu.
Budući terapijski pristupi[uredi | uredi izvor]
Lečenje pacijenata sa cističnim bubrezima samo u Sjedinjenim Američkim Državama košta preko milijardu dolara godišnje. Ova suma u suštini proizilazi iz troškova terapije zamene bubrega neophodne za završnu bubrežnu insuficijenciju.
Proliferacija i povećanje veličine cista sa tankim zidovima, ispunjenih tečnošću, zavise od dva procesa: proliferacije ćelija epitela ciste i izlučivanja tečnosti u ciste. Oba procesa zavise od cikličnog adenozin monofosfat (cAMP). Ciklični adenozin monofosfat stimuliše put Ras/MAP kinaze, što dovodi do abnormalnog rasta ćelija. Pored toga, cAMP aktivira CFTR hloridni kanal i tako podstiče izlučivanje tečnosti u ciste. Terapijski pristupi koji se trenutno testiraju ciljaju oba procesa zavisna od cAMP kako bi se usporilo formiranje i rast cista.
Takođe se istražuje moguće učešće C-Met proteina i povezana terapija inhibitorima C-Met, koja je dala obećavajuće rezultate u eksperimentima na životinjama sa miševima .
Prognoza[uredi | uredi izvor]
Policistična bolest bubrega je teško zdravstveno stanje koje može pogoditi osobe bilo kojeg životnog uzrasta.
Bitno narušava kvalitet života jer je potrebna stalna kontrola stanja, posebno hipertenzije sa ciljem što dužeg odganja zadnjeg—terminalnog stadijuma hroničnog bubrežnog zastoja.
Više od polovine pacijenata sa policističnom bolesti bubrega podvrgava se postupku dijalize, odnosno transplantacije bubrega.
Prevencija[uredi | uredi izvor]
Prenatalna dijagnostika, kao deo genetskog informisanja, pruža mogućnost rane prenatalne dijagnoze bolesti i omogućava objektivno genetsko savetovanje roditelja. Ovo savetovanje traba da omogući roditeljima da nakon dobijenih iscrpnih informacija, donesu odgovornu odluku o daljoj sudbini ploda, u skladu sa njihovim etičkim, verskim i drugim stavovima i interesima deteta.
Galerija[uredi | uredi izvor]
Izvori[uredi | uredi izvor]
- ^ F. Lejars: Du gros reins polykystique de l'adulte. Dissertation, 1888, Paris
- ^ a b v g d đ e ž z „Lexikon: Zystenniere”. www.bestmed.at. Pristupljeno 2022-02-07.
- ^ W. Osler: The diagnosis of polycystic kidney. In: Internat Clin. Philadelphia, 2, 1915, S. 1–5.
- ^ L. P. Brendan u. a.: Did Sir William Osler Perform an Autopsy at The Johns Hopkins Hospital? In: Archives of Pathology & Laboratory Medicine 2, 132, 2007, S. 261–264.
- ^ O. Z. Dalgaard: Bilateral polycystic disease of the kidneys. In: Acta Med Scand. 328, 1957, S. 1–255
- ^ Reeders, S. T.; Breuning, M. H.; Davies, K. E.; Nicholls, R. D.; Jarman, A. P.; Higgs, D. R.; Pearson, P. L.; Weatherall, D. J. (1985). „A highly polymorphic DNA marker linked to adult polycystic kidney disease on chromosome 16”. Nature. 317 (6037): 542—544. Bibcode:1985Natur.317..542R. PMID 2995836. S2CID 4319860. doi:10.1038/317542a0.
- ^ Torres, Vicente (20. 5. 2009). „Autosomal dominant polycystic kidney disease: the last 3 years”. Kidney International. 76 (2): 149—168. PMC 2812475
 . PMID 19455193. doi:10.1038/ki.2009.128.
. PMID 19455193. doi:10.1038/ki.2009.128.
- ^ DALGAARD, OZ (1957). „Bilateral polycystic disease of the kidneys; a follow-up of two hundred and eighty-four patients and their families”. Acta Med. Scand. Suppl. 328: 1—255. PMID 13469269.
- ^ „Policistični bubrezi”. Stetoskop. 12. 6. 2007. Arhivirano iz originala 16. 09. 2011. g. Pristupljeno 16. 8. 2011.
- ^ Fried, L. F.; Palevsky, P. M.; Johnston, J. R. (1998). „Duodenal obstruction in polycystic kidney disease. Case report and review of the literature”. American Journal of Nephrology. 18 (4): 318—320. PMID 9653836. S2CID 72794736. doi:10.1159/000013357.
- ^ U. Frei und H. J. Schober-Halstenberg: http://www.bundesverband-niere.de/files/QuaSi-Niere-Bericht_2005-2006.pdf Nierenersatztherapie in Deutschland. (PDF; 1,4 MB) In: QuaSi-Niere Jahresbericht 2005/2006 Berlin, Deutschland
- ^ Fick, G. M.; Gabow, P. A. (1994). „Hereditary and acquired cystic disease of the kidney”. Kidney International. 46 (4): 951—964. PMID 7861721. doi:10.1038/ki.1994.354.
- ^ Grantham, Jared (2. 10. 2008). „Autosomal Dominant Polycystic Kidney Disease”. New England Journal of Medicine. 359 (14): 1477—1485. PMID 18832246. doi:10.1056/NEJMcp0804458.
- ^ Lee K, Battini L, Gusella GL. Cilium, centrosome and cell cycle regulation in polycystic kidney disease. Biochimica et biophysica acta. 2011;1812(10):1263-71
- ^ Pirson Y. Extrarenal manifestations of autosomal dominant polycystic kidney disease. Advances in chronic kidney disease. 2010;17(2):173-80.
- ^ Wen J. Congenital hepatic fibrosis in autosomal recessive polycystic kidney disease. Clinical and translational science. 2011;4(6):460-5.
- ^ Buscher R, Buscher AK, Weber S, Mohr J, Hegen B, Vester U, et al. Clinical manifestations of autosomal recessive polycystic kidney disease (ARPKD): kidney-related and non-kidney-related phenotypes. Pediatric nephrology (Berlin, Germany). 2014;29(10):1915-25.
- ^ P. A. Gabow u. a.: http://jasn.asnjournals.org/cgi/reprint/8/1/105 Utility of ultrasonography in the diagnosis of autosomal dominant polycystic kidney disease in children. In: J Am Soc Nephrol 8, 1997, S. 105–110. Gabow, P. A.; Kimberling, W. J.; Strain, J. D.; Manco-Johnson, M. L.; Johnson, A. M. (1997). „Utility of ultrasonography in the diagnosis of autosomal dominant polycystic kidney disease in children”. Journal of the American Society of Nephrology : Jasn. 8 (1): 105—110. PMID 9013454. doi:10.1681/ASN.V81105.
- ^ O'Neill, W. C.; Robbin, M. L.; Bae, K. T.; Grantham, J. J.; Chapman, A. B.; Guay-Woodford, L. M.; Torres, V. E.; King, B. F.; Wetzel, L. H.; Thompson, P. A.; Miller, J. P. (2005). „Sonographic assessment of the severity and progression of autosomal dominant polycystic kidney disease: The Consortium of Renal Imaging Studies in Polycystic Kidney Disease (CRISP)”. American Journal of Kidney Diseases : The Official Journal of the National Kidney Foundation. 46 (6): 1058—1064. PMID 16310571. doi:10.1053/j.ajkd.2005.08.026.
- ^ K. M. Koch u. a.: Klinische Nephrologie. Urban&Fischer-Verlag, 1999, S. 437–459. ISBN 978-3-437-21730-2
- ^ Hermanns, B.; Alfer, J.; Fischedick, K.; Stojanovic-Dedic, A.; Rudnik-Schöneborn, S.; Büttner, R.; Zerres, K. (2003). „Pathology and genetic hereditary kidney cysts”. Der Pathologe. 24 (6): 410—420. PMID 14605845. S2CID 25441269. doi:10.1007/s00292-003-0646-5.
- ^ F. Hildebrandt und M. Wolf: Pathologie und Genetik hereditärer Zystennieren. In: Medizinische Therapie Springer, 2005, S. 927–939. ISBN 978-3-540-21226-3
- ^ Elles, R. G.; Hodgkinson, K. A.; Mallick, N. P.; O'Donoghue, D. J.; Read, A. P.; Rimmer, S.; Watters, E. A.; Harris, R. (1994). „Diagnosis of adult polycystic kidney disease by genetic markers and ultrasonographic imaging in a voluntary family register”. Journal of Medical Genetics. 31 (2): 115—120. PMC 1049671
 . PMID 8182715. doi:10.1136/jmg.31.2.115.
. PMID 8182715. doi:10.1136/jmg.31.2.115.
Literatura[uredi | uredi izvor]
- Nedima ATIĆ, Izeta SOFTIĆ, Jasminka TVICA, Anomalije urinarnog trakta u djece Pedijatrija danas 2007;3(2):149-163
Spoljašnje veze[uredi | uredi izvor]
| Klasifikacija | |
|---|---|
| Spoljašnji resursi |
- Dečja hirurgija Arhivirano na sajtu Wayback Machine (9. maj 2021)
- Slikoviti prikaz dimenzija policističnih bubrega Arhivirano na sajtu Wayback Machine (14. novembar 2020)
- National Kidney & Urologic Diseases Information Clearinghouse: Polycystic Kidney Disease (jezik: engleski)
- U.S. National Library of Medicine National Institutes of Health: Genes and Disease (језик: енглески)
 | Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |






