Kumarin

| |
| |

| |
| Nazivi | |
|---|---|
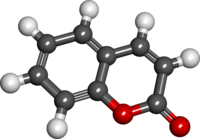
| IUPAC naziv
2H-chromen-2-one
| |
| Drugi nazivi
1-benzopiran-2-on
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.001.897 |
| KEGG[1] | |
| UNII | |
| |
| Svojstva | |
| C9H6O2 | |
| Molarna masa | 146,15 g·mol−1 |
| Gustina | 0,935 g/cm3 (20 °C) |
| Tačka topljenja | 71 °C (160 °F; 344 K) |
| Tačka ključanja | 301 °C (574 °F; 574 K) |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Kumarin (2H-hromen-2-on) je hemijsko jedinjenje sa benzopironskom osnovom[4][5][6][7] koje daje miris mnogim biljkama. Prisutno je u visokim koncentracijama u Dipteryx odorata, vanila travi (Anthoxanthum odoratum), lazarkinji (Galium odoratum), divizmi (Verbascum spp.), slatkoj travi (Hierochloe odorata), kineskom cimetu (Cinnamomum aromaticum) i slatkoj detelini. Ime potiče od franc. coumarou, za Dipteryx odorata.
On ima sladak miris, koji se lako prepoznaje kao miris novo pokošenog sena, i koji se koristi u parfemima od 1882. Lazarkinja, slatka trava i detelina su posebno prepoznatljive po tom mirisu, koji je posledica visokog sadržaja ove supstance. On se koristio kao pojačivač arome duvana za lulu i pojedinih alkoholnih pića, mada je generalno zabranjen kao aditiv hrane, zbog moguće hepatotoksičnosti, koja je uočena na životinjskim modelima. Kad se javi u javi u visokim koncentracijama u krmnom bilju, kumarin deluje kao gorki supresant apetita, te se smatra da ga biljke proizvode kao vid odbrambenog mehanizma.
Mada sam kumarin nema antikoagulansne osobine, njega transformišu u prirodni antikoagulans dikumarol brojne vrste gljiva. Do toga dolazi kao rezultat formiranja 4-hidroksikumarina, zatim dalje (u prisustvu prirodnog formaldehida) u sami antikoagulans dikumarol, fermentacionog produkta i mikotoksina. Ta supstanca je odgovorna za bolest krvavljenja, koja je poznata kao bolest slatke deteline kod marve koja jede silažu od buđave deteline.[8]
Kumarin se koristi u farmaceutskoj industriji kao prekursorni molekul u sintezi mnogobrojnih sintetičkih antikoagulansnih lekova sličnih dikumarolu, kao što su varfarin (kumadin), i neki potentni rodenticidi koji deluju putem istog antikoagulansnog mehanizma. Svi ti agensi su otkriveni putem analize bolesti slatke deteline.
Sam kumarin ima klinički medicinski značaj kao modifikator otoka. Za kumarin i druge benzopirone, poput 5,6 benzopirona, 1,2 benzopirona i diosmina, je poznato da stimulišu makrofage da degradiraju ekstracelularni albumin, omogućavajući bržu resorpciju otočnih fluida.[9][10]. Druge biološke aktivnosti sa mogućom medicinskom primenom su poznate.
Kumarin se takođe koristi kao pojačavajući medijum u nekim laserima s bojom[11][12][13], i kao pojačavač osetljivosti u starijim fotonaponskim tehnologijama[14].
Vidi još[уреди | уреди извор]
Reference[уреди | уреди извор]
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ McMurry John E. (1992). Fundamentals of Organic Chemistry (3rd изд.). Belmont: Wadsworth. ISBN 0-534-16218-5.
- ^ Morrison Robert Thornton; Boyd Robert Neilson (2006). Organic chemistry. Engelwood Cliffs, New Jersey: Prentice Hall. ISBN 8120307658.
- ^ Katritzky A.R.; Pozharskii A.F. (2000). Handbook of Heterocyclic Chemistry (Second изд.). Academic Press. ISBN 0080429882.
- ^ Bye, A., King, H. K., 1970. The biosynthesis of 4-hydroxycoumarin and dicoumarol by Aspergillus fumigatus Fresenius. Biochemical Journal 117, 237-245.
- ^ John R. Casley-Smith; Robert Gwyn Morgan & Neil B. Piller (14. 10. 1993). „Treatment of Lymphedema of the Arms and Legs with 5,6-Benzo-[alpha]-pyrone”. 329 (6): 1158—1163.
- ^ „Review of benzypyrone drugs and edema”. Архивирано из оригинала 20. 03. 2012. г. Приступљено 28. 09. 2011.
- ^ F. P. Schäfer (Ed.), Dye Lasers, 3rd Ed. (Springer-Verlag, Berlin, 1990).
- ^ F. J. Duarte and L. W. Hillman (Eds.), Dye Laser Principles (Academic, New York, 1990).
- ^ F. J. Duarte, Tunable Laser Optics (Elsevier-Academic, New York, 2003) Appendix of Laser Dyes.
- ^ U.S. Pat. No. 4175982 to Loutfy et al, issued Nov 27 1978 to Xerox Corp.
Literatura[уреди | уреди извор]
Spoljašnje veze[уреди | уреди извор]
- Kumarin
- Kumarin u tabaku
- Kumarin kao sastojak perfema.
- Zakon kojim se reguliše upotreba kumarina kao prehrambenog aditiva
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
