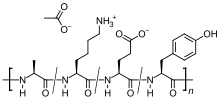
Глатирамер ацетат
 | |
| IUPAC име | |
|---|---|
ацетиц ацид; (2С)-2-амино-3-(4-хyдроxyпхенyл)пропаноиц ацид; (2С)-2-аминопентанедиоиц ацид; (2С)-2-аминопропаноиц ацид; (2С)-2,6-диаминохеxаноиц ацид | |
| Клинички подаци | |
| Drugs.com | Монографија |
| Подаци о лиценци |
|
| Категорија трудноће |
|
| Начин примене | Субкутана ињекција |
| Правни статус | |
| Правни статус |
|
| Идентификатори | |
| CAS број | 147245-92-9 |
| ATC код | L03AX13 (WHO) |
| PubChem | CID 3081884 |
| DrugBank | DB05259 |
| ChemSpider | - |
| UNII | 5M691HL4BO |
| ChEMBL | CHEMBL1201507 |
| Хемијски подаци | |
| Формула | C25H45N5O13 |
| Моларна маса | 623.65 г/мол |
Глатирамер ацетат (Цопаxоне или Цополyмер 1, Тева Фармацеутичка Индустрија) је имуномодулаторни лек за третман мултипле склерозе. [1][2] То је полимер следеће четири аминокиселине: L-глутаминске киселине, L-аланин, L-лизин и L-тирозин, и ацетата (со), нађене у мијелин протеину. Његова структурна формула је: (Glu, Ala, Lys, Tyr)x•xCH3COOH, или (C5H9NO4•C3H7NO2•C6H14N2O2•C9H11NO3)x•xC2H4O2. Ова смеша може да функционише као заваравајуће средство за имунски систем. Клиничка дефиниција мултипле склерозе захтева две или више епизода симптома и знакова. Глатирамер ацетат је одобрен за третман након једне епизоде, и такође за релапсно ремитирајућу мултиплу склерозу.[3] Он се администрира супкутаном ињекцијом.
Механизам акције[уреди | уреди извор]
Глатирамер ацетате је рандомни полимер (средње молекулске масе 6.4 kD) који се састоји од четири аминокиселине које се налазе у основном протеину мијелина. Механизам акције глатирамера је непознат, мада их је више било предложено. Администрација глатирамера мења популацију Т ћелија из проинфламаторних Th1 ћелија у регулаторне Th2 ћелије које потискују инфламаторни одговор.[4] Узимајући у обзир сличност са основним протеином мијелина, глатирамер може такође да дејствује попут мамца, одвраћајући аутоимуни одговор против мијелина. Интегритет крвно-мождане баријере, међутим, није подложан приметном утицају глатирамера, бар не у току првих ступњева третмана. За глатирамер ацетат је било показано на клиничким испитивањима да умањује број и озбиљност погоршања.[5][3]
Студије на животињама и ин-витро системима указују да су након употребе, глатирамер ацетат специфичне супресор Т-ћелије индуковане и активиране на периферији. [6]
Развој[уреди | уреди извор]
Глатирамер ацетате је откривен на Веизмановом Институту за Науку у Израелу. Ефикасност и безбедност глатирамер ацетата су демонстрирани у три клиничка испитивања: Прво испитивање, предвођено професором M. Борнстеином, је изведено у једном центру, као дупло-слепо, плацебо контролисано испитивање на 50 пацијената. Друго испитивање је било једна двогодишња студија, спроведена у више центара, као рандомизовано, дупло-слепо, плацебо контролисано испитивање. Оно је спроведено у једанаест америчких центара на 251 пацијента. Треће испитивање је била дупло-слепо, мулти-центарска, међународна студија, у 29 МС центара у шест европских земаља и у Канади, са учешћем 239 пацијената.[1]
Продаја и дистрибуција[уреди | уреди извор]
Глатирамер ацетат је одобрен за продају у 47 земаља, укључујући САД, Израел, Канаду, 22 земље Европске уније, Швајцарску, Аустралију, Русија, Бразил, и Аргентину.
Нуспојаве[уреди | уреди извор]

Могуће нуспојаве су квржица на месту ињекције код приближно 30% корисника[7], и болови, температура, језа (симптоми попут грипа) код 10% корисника.[8] Нуспојаве су углавном благе. Реакција која укључује црвенило, краткоћу даха, тескобу и убрзан рад срца је пријављена да се јавља краткотрајно након ињекције код око 5% пацијената (обично након убризгавање директно у вену). Ове нуспојаве се повуку у року од тридесет минута. Током времена, видљив траг на мјесту ињекције се може јавити због локалног уништења масног ткива, познат као липоатропија.
Озбиљније нуспојаве су забележене за глатирамер ацетат, према ФДА прописаном етикети, то укључује озбиљне нуспојаве на кардиоваскуларном систему, пробавном систему (укључујући јетру), хематолошком и лимфном систему, коштано-мишићном систему, живчаном систему, респираторном систему, чулима (посебно очима), и урогениталном систему. Такође су пријављени метаболички и нутрициони поремећаји, међутим веза између глатирамер ацетата и тих негативних ефеката није била дефинитивно успостављена.[9]
Ефективност[уреди | уреди извор]
Докази који поткрепљују ефикасност глатирамер ацетата у смањењу учесталости релапса код болесника са релапсно-ремитирајућом мултиплом склерозом (МСРР) потичу из две плацебо-контролисане студије. Обе студије су користиле глатирамер ацетат дозе од 20 мг / дан. (Друге дозе или режими дозирања нису студиране у плацебо-контролисаним испитивањима РРМС).[10] А цомпаративе триал оф тхе аппровед 20 мг досе анд тхе 40 мг досе схоwед но сигнифицант дифференце ин еффицацy бетwеен тхесе досес[11].
У свом кључном испитивању[12] на 251 пацијента, након 2 године Copaxon није показао предност у заустављању прогресије инвалидности (78% третираних пацијената су били без прогреса у односу на 75% пацијената у истој категорији на плацебу).
Међутим, 2004. Кокранов Медицински преглед [13] је истакао да "Глатирамер ацетат није показао благотворни утицај на главни исход МС мерења, тј. напредовање болести, и да нема значајног утицаја на ризик клиничког релапса."
Као резултат тога[14], ФДА продајна етикета за Copaxon још увек не садржи индикацију за редуцирање прогресивне инвалидности.
Истраживање[уреди | уреди извор]
За глатирамер је нађено да има заштитни ефекат у моделу церебралне маларије на мишевима.[15]
Глатирамер је тренутно у фази I клиничких испитивања за суву сенилну дегенерацију макуле (АМД).
Референце[уреди | уреди извор]
- ^ а б Цоми Г, Мартинелли V, Родегхер M, Моиола L, Бајенару О, Царра А, Еловаара I, Фазекас Ф, Хартунг ХП, Хиллерт Ј, Кинг Ј, Комолy С, Лубетзки C, Монталбан X, Мyхр КМ, Равнборг M, Риецкманн П, Wyнн D, Yоунг C, Филиппи M (2009). ПреЦИСе студy гроуп.. „Еффецт оф глатирамер ацетате он цонверсион то цлиницаллy дефините мултипле сцлеросис ин патиентс wитх цлиницаллy исолатед сyндроме (ПреЦИСе студy): а рандомисед, доубле-блинд, плацебо-цонтроллед триал”. Ланцет. 374: 1503—11. ПМИД 19815268.
- ^ Јохнсон, КП (2010). „Рискс вс бенефитс оф глатирамер ацетате: а цхангинг перспецтиве ас неw тхерапиес емерге фор мултипле сцлеросис”. Тхер Цлин Риск Манаг. волуме=15 (6): 153—72. ПМИД 20421914.
- ^ а б Кеитх Паркер; Лауренце Брунтон; Гоодман, Лоуис Санфорд; Лазо, Јохн С.; Гилман, Алфред (2006). „Цхаптер 52. Иммуносуппрессантс, толерогенс, анд иммуностимулантс, А цасе студy: Иммунотхерапy фор мултипле сцлеросис”. Гоодман & Гилман'с Тхе Пхармацологицал Басис оф Тхерапеутицс (11. изд.). Неw Yорк: МцГраw-Хилл. ИСБН 0071422803.
- ^ „Тхе цхемистрy оф тхе Цопаxоне друг” (ПДФ). Архивирано из оригинала (ПДФ) 13. 8. 2006. г.
- ^ „www.мулт-сцлеросис.орг”.
- ^ „Фулл пресцрибинг информатион цопаxоне (глатирамер ацетате)” (ПДФ).
- ^ „иГуард.орг ТСQМ сурвеy ресултс (н=1700+):”.[мртва веза]
- ^ „Цопаxоне Сиде Еффецтс”.
- ^ „ФДА Цопаxоне Лабел” (ПДФ).
- ^ „Пресцрибинг Информатион” (ПДФ). Архивирано из оригинала (ПДФ) 7. 3. 2010. г. Приступљено 11. 6. 2010.
- ^ Цохен, ЈА; et al. (2007). „Тхе 9006 триал”. Неурологy. 68: 939—944.
- ^ „ФДА маркетинг лабел” (ПДФ). Архивирано из оригинала (ПДФ) 7. 3. 2010. г. Приступљено 11. 6. 2010.
- ^ „Цоцхране Медицал ревиеw оф Цопаxоне”.
- ^ „Цопаxоне маркетинг материалс”. Архивирано из оригинала 17. 5. 2008. г. Приступљено 11. 6. 2010.
- ^ Лацкнер П, Парт А, Бургер C, Диетманн А, Броесснер Г, Хелбок Р, Реиндл M, Сцхмутзхард Е, Беер Р (2009). „Глатирамер ацетате редуцес тхе риск фор еxпериментал церебрал малариа: а пилот студy.”. Малар Ј. 8. ПМИД 19250545.
Спољашње везе[уреди | уреди извор]
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
