Инхибитор ензима

Инхибитор ензима је молекул који се везује за ензим и умањује његову активност. Пошто блокирање ензимске активности може да узрокује угинуће патогена или да коригује метаболичку неуравнотеженост, стога су многи лекови инхибитори ензима. Инхибитори ензима се такође користе као пестициди. Нису сви молекули који се везују за ензиме инхибитори; активатори ензима се везују за ензиме и повећавају њихову активност, док се ензимски супстрати везују и бивају конвертовани до продуката у нормалном каталитичком циклусу ензима.
Везивање инхибитора може да спречи приступ супстрата ензимском активном месту и/или омете ензим при катализи биохемијске реакције. Везивање инхибитора може да буде реверзибилно или иреверзибилно. Иреверзибилни инхибитори обично реагују са ензимом и хемијски га мењају (нпр. формирањем ковалентне везе), те модификују кључне аминокиселинске остатке неопходне за ензиматску активност. Насупрот овоме, реверзибилни инхибитори се везују нековалентно, те се различити типови инхибиције јављају зависно од тога да ли се инхибитори везују за ензим, за ензимско-супстратни комплекс, или за обоје.[1]
Многи молекули лекова су инхибитори ензима, тако да је њихово откривање и побољшање активна област истраживања у биохемији и фармакологији. Медицински ензимски инхибитори се често вреднују по својој специфичности (свом одсуству везивања за друге протеине) и својој потентности (својој константи дисоцијације, која је индикатор концентрације неопходне за инхибицију ензима). Висока специфичност и потентност су предуслови да лек испољава мали број нуспојава и стога ниску токсичност.
Ензимски инхибитори се исто тако јављају у природи и учествују у регулацији метаболизма. На пример, ензими у метаболичком путу могу да буду инхибирани продуктима даљих корака пута. Овај тип повратне спреге успорава ћелијску производну линију кад продукти почну да се накупљају, и то је један од важних начина одржавања хомеостазе у ћелијама. Други ћелијски ензимски инхибитори су протеини, који се специфично везују за и инхибирају ензимску мету. То може да помогне у контроли ензима, који би иначе могли да оштете ћелију, као што су протеазе или нуклеазе. Једна детаљно окарактерисана класа инхибиторних молекула су рибонуклеазни инхибитори, који се везују за рибонуклеазе формирајући једну од најчвршћих познатих протеин—протеин интеракција.[2] Природни ензимски инхибитори такође могу да буду отрови и да се користе као вид одбране од предатора, или као начин убијања плена.
Реверзибилни инхибитори[уреди | уреди извор]
Типови реверзибилних инхибитора[уреди | уреди извор]
Реверзибилни инхибитори се везују за ензиме путем нековалентних интеракција као што су водоничне везе, хидрофобне интеракције и јонске везе. Вишеструке слабе везе између инхибитора и активног места се комбинују и производе јако и специфично везивање. За разлику од супстрата и иреверзибилних инхибитора, реверзибилни инхибитори генерално не подлежу хемијским реакцијама при везивању за ензим и могу лако да се уклоне разблаживањем или дијализом.
Постоје четири врсте реверзибилних ензимских инхибитора. Класификују се на основу утицаја променљиве концентрације ензимског супстрата на инхибитор.[3]

- У конкурентној инхибицији, супстрат и инхибитор не могу истовремено да се вежу за ензим, као што је то приказано на слици десно. То је обично последица тога да инхибитор има афинитет за активно место ензима за које се такође везује супстрат; супстрат и инхибитор се надмећу за приступ активном месту ензима. Овај тип инхибиције се може превазићи применом довољно високих концентрација супстрата (Vmax остаје константно), од. путем надмашивања концентрације инхибитора. Међутим, долази до повећања појавне вредности Km, јер је потребна већа концентрација супстрата да би се досегла тачка Km, или половина вредности Vmax.[4] Конкурентни инхибитори су обично структурно слични реалном супстрату (види примере испод).
- У неконкурентној инхибицији, инхибитор се једино везује за супстратно-ензимски комплекс. Овај тип инхибиције узрокује снижење вредности Vmax (максимална брзина се смањује услед уклањања активираног комплекса) и вредности Km (услед повећане ефикасности везивања која произилази из Ле Шатељеовог принципа и ефективне елиминације ES комплекса чиме се умањује Km, што је индикатор повећаног афинитета везивања).[4]
- У бесконкурентној инхибицији, везивањем инхибитора за ензим редукује се његова активност, мада то нема утицаја на везивање супстрата. Резултат овога је да степен инхибиције једино зависи од концентрације инхибитора. Вредност Vmax се смањује, јер се реакција одвија мање ефикасно, док се вредност Km не мења, пошто се само везивање супстрата — по дефиницији — и даље нормално одвија.[4]
- У мешовитој инхибицији, инхибитор се може везати за ензим истовремено са супстратом ензима. Међутим, овакво везивање инхибитора утиче на везивање супстрата, и обрнуто. Ова врста инхибиције се може умањити, али не и превазићи повећањем концентрације супстрата. Мада постоји могућност да се инхибитори мешовитог типа вежу на активном месту, овај тип инхибиције генерално произилази из алостерног дејства, при чему се инхибитор везује на различитом месту на ензиму. Везивање инхибитора за алостерно место мења конформацију (тј. терцијарну структуру или тродимензионални облик) ензима, тако да је афинитет супстрата за активно место умањен.[4]
Квантитативни опис реверзибилне инхибиције[уреди | уреди извор]
Реверзибилна инхибиција се може квантитативно описати у погледу везивања инхибитора за ензим и за ензимско-супстратни комплекс, као и његовог утицаја на кинетичке константе ензима. У класичној Михаелис—Ментениној шеми испод, ензим (E) везује се за свој супстрат (S) и формира ензимско-супстратни комплекс ES. Након катализе, овај комплекс се разлаже и ослобађају се продукт P и слободни ензим. Инхибитор (I) може се везати или за E или за ES са константама дисоцијације Ki или Ki′, редом.
Када ензим има вишеструке супстрате, инхибитори могу да испоље различите типове инхибиције у зависности од тога који се супстрат посматра. До овога долази зато што активно место садржи два различита места везивања, по једно за сваки супстрат. На пример, инхибитор се може надметати са супстратом A за прво место везивања, а бити бесконкурентни инхибитор супстрата B у другом месту везивања.[5]
Мерење константи дисоцијације реверзибилног инхибитора[уреди | уреди извор]
Као што је напоменуто изнад, ензимски инхибитор се описује путем својих двеју константи дисоцијације: Ki и Ki′, за ензим и ензимско-супстратни комплекса, редом. Ензимско-инхибиторска константа Ki се може директно мерити различитим методима. Један од изузетно прецизних метода је изотермална титрациона калориметрија, у којој се инхибитор титрира у раствор ензима; потом се мери ослобођена или апсорбована топлота.[6] Међутим, другу константу дисоцијације Ki′ је тешко директно мерити, пошто је ензимско-супстратни комплекс краткотрајан и подлеже хемијској реакцији којом се формира продукт. Стога се Ki′ обично индиректно мери, и то путем посматрања ензимске активности при различитим концентрацијама супстрата и инхибитора, те постављањем података[7] у модификовану Михаелис—Ментенину једначину.
где су модификујући фактори α и α′ дефинисани путем концентрације инхибитора и његових двеју константи дисоцијације:

Стога, у присуству инхибитора, ензимске ефективне вредности Km и Vmax постају (α/α′)Km и (1/α′)Vмаx, редом. Треба имати у виду да модификована Михаелис—Ментенина једначина подразумева да је остварена равнотежа везивања инхибитора за ензим, што може да буде веома спор процес за инхибиторе са поднаномоларним константама дисоцијације. У тим случајевима, обично је практичније да се третира чврсто везујући инхибитор као иреверзибилни инхибитор (види испод); мада, још увек може да постоји опција кинетичког процењивања Ki′, ако се независно измери Ki.
Утицаји различитих типова реверзибилних инхибитора ензима на ензиматску активност се могу приказати користећи графичке репрезентације Михаелис—Ментенине једначине, као што су Лајнвивер—Берков и Еди—Хофстијев дијаграм. На пример, на Лајнвивер—Берковом дијаграму приказаном десно, линије конкурентне инхибиције секу се на y-оси, што илуструје да такви инхибитори немају утицаја на Vmax. Аналогно, линије бесконкурентне инхибиције секу се на x-оси, што показује да ови инхибитори не утичу на Km. Међутим, често је тешко прецизно проценити Ki и Ki′ са дијаграма,[8] па се препоручује коришћење поузданијих метода нелинеарне регресије за процену константи (описано изнад).
Реверзибилни инхибитори[уреди | уреди извор]
Традиционално се реверзибилни инхибитори ензима класификују као конкурентни, неконкурентни или бесконкурентни, на основу њиховог утицаја на параметре Km и Vmax. Ти различити утицаји директно произилазе из начина везивања инхибитора за ензим E, ензимско-супстратни комплекс ES, или оба. Подела у ове класе проистиче из проблема са одређивањем параметара и ствара потребу за коришћењем различитих константи везивања за описивање чина везивања. Везивање инхибитора и његов утицај на ензиматску активност су две потпуно различите свари, што је још један проблем који традиционалне једначине не одражавају. Код неконкурентне инхибиције везивање инхибитора следствено једначинама једино доводи до потпуне (100%) инхибиције ензима, и једначине не остављају могућност постојања било чега између тих крајности.[9] Заједнички облик инхибиторног члана такође замагљује однос између везивања инхибитора за ензим и његовог односа са другим члановима везивања, било да је то Михаелис—Ментенина једначина или дозно-респонсна крива асоцирана са везивањем лиганда за рецептор. Да би се демонстрирао однос, може се створити следеће прераспоређивање:
Додајући нулу на дно ([I]−[I]):
... и делећи са [I]+Ki добија се:
Ова једначина демонстрира да је слично Михаелис—Ментениној једначини, где брзина реакције зависи од процента ензимске популације која међуделује са супстратом:
разломак ензимске популације везане супстратом
разломак ензимске популације везане инхибитором
... утицај инхибитора резултат процента популације ензима која међуделује са инхибитором. Једини проблем са овом једначином у њеној тренутној форми је што подразумева апсолутну инхибицију ензима везивањем инхибитора, док се у стварности може јавити широк опсег утицаја: од 100% инхибиције супстрата до само извесног процента, > 0%. Да би се ово узело у обзир, једначина се може једноставно модификовати увођењем члана делта Vmax, тако да дозвољава различите степене инхибиције:
... или:
Овај члан може онда да дефинише резидуални проценат ензиматске активности кад инхибитор интерагује са индивидуалним ензимима у популацији. Уврштавање овог члана има додатну предност дозвољавања могућности активације ако се испостави да је секундарни члан Vmax већи од иницијалног члана. Да би се у обзир такође узела могућност активације, једначина се може прилагодити замењивањем инхибиторске ознаке „I” општом ознаком односно модификаторским чланом који је овде означен са „X”:
Док ова терминологија доводи до поједностављеног начина руковања кинетичким ефектима везаним за максималну брзину Михаелис—Ментенине једначине, она исто тако наглашава потенцијалне проблеме са члановима који се користе за описивање ефеката везаних за Km. Вредност Km везана за афинитет ензима за супстрат је у већини случаја повезана са могућим променама места везивања ензима, што је директна последица интеракције ензима и инхибитора. Стога је члан сличан горенаведеном члану за корекцију Vmax подесан у већини случајева:[10][11]
Специјални случајеви[уреди | уреди извор]
- Механизам парцијално конкурентне инхибиције је сличан оном бесконкурентне, изузев што EIS комплекс има каталитичку активност, која може да буде нижа или чак виша (парцијално компетитивна активација) од активности ензимско-супстратног (ES) комплекса. Ова инхибиција типично испољава нижу вредност Vmax, док се вредност Km не мења.[5][12]
- Неконкурентна инхибиција се јавља када се инхибитор везује само за ензимско-супстратни комплекс, не и за слободни ензим; комплекс EIS је каталитички неактиван. Овај начин инхибиције је редак и узрокује смањивање обеју вредности, и Vmax и Km.[5]
- Инхибиција супстрата и продуката се јавља кад било супстрат или продукт ензиматске реакције инхибира ензимску активност. Овај облик инхибиције може да следи компетитивне, некомпетитивне или мешовите обрасце. При супстратној инхибицији долази до прогресивног смањења активности при високим концентрацијама супстрата. То може да буде индикација постојања два места везивања супстрата на ензиму. При ниским концентрацијама супстрата, место високог афинитета је окупирано и нормална кинетика долази до изражаја. Међутим, при вишим концентрацијама долази до заузећа секундарног, инхибиторног места, чиме се инхибира ензим.[13] Продукт инхибиције често служи као регулаторно својство при метаболизму и може да формира негативну повратну спрегу.[14]
- Спора непропусна инхибиција се јавља кад иницијални комплекс ензима и инхибитора (EI) подлеже изомеризацији до другог, чвршће пакованог (непропусног) комплекса, EI*, иако је свеукупни процес инхибиције реверзибилан.[15] Ово се манифестује као споро растућа инхибиција ензима. Под овим условима, традиционална Михаелис—Ментенина кинетика даје погрешну вредност за Ki, јер је она зависна од времена. Тачна вредност Ki се може добити путем комплексније анализе константи брзина асоцијације (kon) и дисоцијације (koff) инхибитора. Додатне информације су доступне у одељку о иреверзибилној инхибицији.
Примери реверзибилних инхибитора[уреди | уреди извор]

Ензими су еволуционо развили способност чврстог везивања својих супстрата; како се већина реверзибилних инхибитора везује за активно место ензима, није изненађујуће да неки од тих инхибитора имају веома сличне структуре са супстратима своје мете. Један од примера опонашања супстрата су протеазни инхибитори. Они су веома успешна класа антиретровиралних лекова који се користе за лечење инфекције ХИВ.[16] Структура ритонавира, протеазног инхибитора који је базиран на пептиду и који садржи три пептидне везе, приказана је са десне стране. Овај лек наликује на протеин који је супстрат ХИВ протеазе; надмеће са овим супстратом за приступ активном месту ензима.
Ензимски инхибитори се често дизајнирају тако да опонашају прелазно стање или интермедијер ензимски катализоване реакције. Тиме се осигурава да инхибитор искористи стабилизујући ефекат прелазног стања ензима, што доводи до побољшаног афинитета везивања (ниже Ki вредности) него што је то случај са дизајнима заснованим на супстрату. Пример оваквог инхибитора прелазног стања је антивирални лек оселтамивир; овај лек опонаша планарну структуру прстена оксонијумског јона у реакцији виралног ензима неураминидазе.[17]
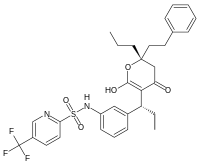
Међутим, нису сви инхибитори базирани на структурама супстрата. На пример, структура другог инхибитора ХИВ протеазе типранавира приказана је на левој страни. Овај молекул није заснован на пептиду и није очигледну структурну сличност са протеинским супстратом. Ови непептидни инхибитори могу да буду стабилнији од инхибитора који садрже пептидне везе, пошто они не могу да буду супстрати пептидаза и много мање су склони деградацији.[18]
При дизајну лекова је важно да се узму у обзир концентрације супстрата којима су изложени циљни ензими. На пример, неки инхибитори протеинских киназа имају хемијске структуре које су сличне аденозин-трифосфату, једном од супстрата поменутих ензима. Међутим, лекови који су једноставни компетитивни инхибитори ће морати да се надмећу са високим концентрацијама АТП молекула у ћелији. Протеинске киназе се исто тако могу инхибирати конкурисањем за места везивања на којима киназе међуделују са својим супстратним протеинима, а већина протеина је присутна у ћелијама са далеко нижим концентрацијама од концентрације АТП молекула. Последично, ако се два инхибитора протеинске киназе везују за активна места са сличним афинитетом — а само један од њих треба да се надмеће са АТП молекулима, онда ће компетитивни инхибитор на месту протеинског везивања ефективније инхибирати ензим.[19]
Иреверзибилни инхибитори[уреди | уреди извор]
Типови иреверзибилне инхибиције (ковалентна инактивација)[уреди | уреди извор]

Иреверзибилни инхибитори обично ковалентно модификују ензим, те инхибиција стога не може да буде повратна. Иреверзибилни инхибитори често садрже реактивне функционалне групе, као што су азотни иперити, алдехиди, халоалкани, алкени, Мајклови акцептори, фенил сулфонати или флуорофосфонати. Те електрофилне групе реагују са аминокиселинским бочним ланцима и формирају ковалентне додатке. Модификовани остаци су они са бочним ланцима који садрже нуклеофиле као што су хидроксилне или сулфхидрилне групе; ту се убрајају аминокиселине серин (нпр. DFP молекули, приказано на десној страни), цистеин, треонин или тирозин.[20]
Иреверзибилна инхибиција се разликује од иреверзибилне ензимске инактивације. Иреверзибилни инхибитори су генерално специфични за једну класу ензима и не инактивирају све протеине; не функционишу уништавајући протеинске структуре него специфичним измењивањем активног места своје мете. На пример, екстреми вредности pH или температуре обично узрокују денатурацију свих протеинских структура, што је неспецифичан ефекат. Поједини неспецифични хемијски третмани аналогно уништавају протеинску структуру: на пример, загревање у концентрованој хлороводоничној киселини ће хидролизовати пептидне везе које протеине држе на окупу, ослобађајући овиме слободне аминокиселине.[21]
Иреверзибилни инхибитори испољавају временски зависну инхибицију и њихова потентност се стога не може окарактерисати помоћу IC50 вредности. Разлог за ово је што се количина активног ензима при датој концентрацији иреверзибилног инхибитора разликује у зависности од тога колико дуго је инхибитор био преинкубиран са ензимом. Због овога, уместо IC50 користе се kobs/[I] вредности,[22] где је kobs уочена брзина инактивације псеудопрвог реда (изведена ис графика зависности логаритамске вредности постотне активности од времена) а [I] концентрација инхибитора. Параметер kobs/[I] је валидан докле год се инхибитор не засити везивањем за ензим (у ком случају је kobs = kinact).
Анализа иреверзибилне инхибиције[уреди | уреди извор]

Као што је приказано на шеми лево, иреверзибилни инхибитори формирају реверзибилни нековалентни комплекс са ензимом (EI или ESI), и затим долази до реакције којом се формира ковалентно модификовани неактивни комплекс EI*. Брзина којом се EI* формира се назива брзином инактивације, или kinact. Пошто формирање ЕИ може да се надмеће са ES, везивање иреверзибилних инхибитора се може спречити конкуренцијом било са супстратом или са другим, реверзибилним инхибитором. Овај протекциони ефекат је добра потврда специфичности реакције иреверзибилног инхибитора са активним местом.
Кораци везивања и инактивације ове реакције се испитују путем инкубације ензима са инхибитором и утврђивањем степена активности која преостаје током времена. Активност ће опадати на временски зависан начин, обично следећи експоненцијални распад. Уклапањем ових података у једначину брзине добија се брзина инактивације при датој концентрацији инхибитора. Ово се ради за неколико различитих концентрација инхибитора. Ако долази до формирања реверзибилног EI комплекса, биће уочљиво засићење брзине инактивације и из одговарајуће криве биће могуће извести kinact и Ki.[23]
Други метод који је у широкој употреби у овим анализама је масена спектрометрија. Овде прецизно мерење масе немодификованог природног ензима и инактивираног ензима даје повећање масе узроковано реакцијом са инхибитором и показује стехиометрију реакције.[24] То се обично ради користећи MALDI-TOF масени спектрометар. У комплементарној техници званој пептидни масени отисци прстију врши се разлагање природног и модификованог протеина дејством протеазе, као што је трипсин. Тиме настаје сет пептида који се могу анализирати користећи масени спектрометар. Пептиди који промене масу након реакције са инхибитором су они који садрже место модификације.
Специјални случајеви[уреди | уреди извор]

Не формирају сви иреверзибилни инхибитори ковалентне додатке на својим ензимским метама. Неки реверзибилни инхибитори се тако чврсто вежу за своје циљне ензиме да су у суштини иреверзибилни. Ови потентно везујући инхибитори могу да испоље кинетику сличну ковалентним иреверзибилним инхибиторима. Неки од ових инхибитора се брзо везују за ензим у EI комплексу ниског афинитета и затим долази до спорог прераспоређивања до веома чврсто везаног EI* комплекса (погледајте леву слику изнад). Овакво кинетичко понашање се назива спорим везивањем.[26] Спори реаранжман након везивања често обухвата конформациону промену при чему се ензим обавије око молекула инхибитора. Примери споро везујућих инхибитора су неки важни лекови, као што је метотрексат,[27] алопуринол[28] и активирани облик ацикловира.[29]
Примери иреверзибилних инхибитора[уреди | уреди извор]
Диизопропилфлуорофосфат (DFP) приказан је као пример иреверзибилног протеазног инхибитора на десној слици изнад. Ензим хидролизује фосфорно-флуорну везу, али фосфатни остатак остаје везан за серин у активном месту, чиме се ензим деактивира.[30] Слично овоме, DFP такође реагује са активним местом ацетилхолинске естеразе у синапсама неурона; последично је потентан неуротоксин, са смртном дозом мањом од 100 mg.[31]
Самоубилачка инхибиција је необични тип иреверзибилне инхибиције где ензим конвертује инхибитор у реактивну форму у свом активном месту. Пример таквог једињења је инхибитор полиаминске биосинтезе, α-дифлуорометилорнитин или DFMO, који је аналоган аминокиселини орнитин и користи се за лечење афричке трипаносомијазе (болест спавања). Орнитинска декарбоксилаза може да катализује декарбоксилацију DFMO уместо орнитина, као што је приказано изнад. Међутим, овој реакцији декарбоксилације следи елиминација атома флуора, чиме се овај каталитички интермедијер конвертује у конјуговани имин, који је веома електрофилно једињење. Ова реактивна форма DFMO молекула затим реагује или са цистеином или са лизином у активном месту, да би се ензим иреверзибилно инактивирао.[25]
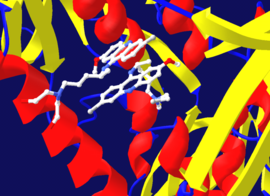
Пошто иреверзибилна обично обухвата првобитно формирање нековалентног EI комплекса, понекад је могуће да се инхибитор веже за ензим на више од једног начина. На пример, на слици лево на којој је приказана трипанотионска редуктаза из људског протозоанског паразита Trypanosoma cruzi, два молекула инхибитора званог квинакрински иперит везана су у активном месту овог ензима. Горњи молекул је реверзибилно везан, док је доњи везан ковалентно пошто је реаговао са аминокиселинским остатком путем азотноиперитне групе.[32]
Откриће и дизајн инхибитора[уреди | уреди извор]

Нови лекови су продукти дуготрајног процеса развоја лекова. Први корак у том процесу је често откриће новог ензимског инхибитора. У прошлости је једини начин да се открију нови инхибитори био приступ покушаја и грешке: тестирање огромних колекција једињења на циљном ензиму у нади да ће се доћи корисних молекула. Овај приступ грубе силе је још увек успешан и био је унапређен применом приступа комбинаторне хемије којима се омогућава брза производња огромног броја нових једињења, као и технологијом високопропусног скрининга да би се брзо тестирале огромне хемијске колекције (библиотеке) с циљем налажења инхибитора.[33]
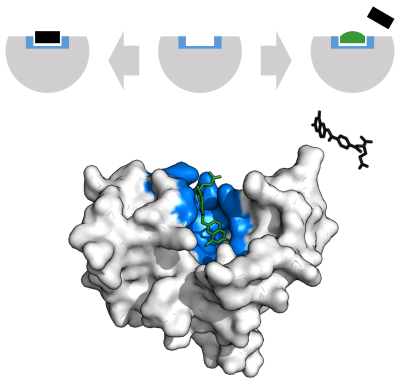
Један од скорашњих алтернативних приступа је рационални дизајн лекова, при чему се користи тродимензионална структура активног места ензима да би се предвидело који молекули би могли да буду инхибитори.[34] Та предвиђања се затим тестирају. Нови инхибитори се након тога користе за добијање структуре ензима у комплексу инхибитор/ензим, да би се потврдило на који начин су молекули везани за активно место. На бази структура је могуће дизајнирати измењене инхибиторе с циљем даље оптимизације везивања. Овај циклус тестирања и побољшања се затим понавља док се не дође до довољно потентних инхибитора.[35] Низ приступа базираних на примени рачунара за предвиђање афинитета инхибитора за ензим такође је у развоју. Примери оваквих метода су молекуларни докинг[36] и молекулска механика.[37][38]
Употребе инхибитора[уреди | уреди извор]
Ензимски инхибитори се могу наћи у природи. Осим њих постоји и знатан број инхибитора који су дизајнирани и производе се за фармаколошке сврхе и биохемијска истраживања. Природни отрови су често ензимски инхибитори који су еволуирали да штите биљке или животиње од предатора. Ти природни токсини обухватају неке од најсмртоноснијих отрова. Вештачки инхибитори се често користе као лекови, мада исто тако могу да буду и инсектициди као што је малатион, хербициди као што је глифосат, или дезинфектанти као што је триклосан. Део вештачких ензимских инхибитора блокира ацетилхолинестеразу, ензим који разлаже ацетилхолин; користе се као нервни агенси у бојним отровима.
Хемиотерапија[уреди | уреди извор]
 |
 |
 |
Ензимски инхибитори се најчешће користе као лекови за третман болести. Многи од њих делују на људске ензиме с циљем кориговања патолошког стања. Међутим, нису сви лекови ензимски инхибитори. Неки, као што су антиепилептички лекови, мењају активност ензима узрокујући да се ензим производи у мањој или већој количини. Ови ефекти се називају ензимска индукција и инхибиција[42] и представљају промене у изражавању гена. То није дирекно повезано са типом ензимске инхибиције о којем се овде говори. Други лекови међуделују са ћелијским метама које нису ензими, као што су јонски канали или мембрански рецептори.
Пример медицинског ензимског инхибитора је силденафил (вијагра), популарни лек за мушку еректилну дисфункцију. Ово једињење је потентни инхибитор cGMP специфичне фосфодиестеразе типа 5, ензима који деградира сигнални молекул циклични гуанозин монофосфат.[43] Овај сигнални молекул подстиче релаксацију глатких мишића и омогућава проток крви у corpus cavernosum, што узрокује ерекцију. Пошто лек умањује активност ензима који зауставља сигнал, продужава се трајање сигнала.
Још један пример структурне сличности појединих инхибитора са супстратима ензима на које делују је приказан на слици десно на којој се пореди лек метотрексат са фолном киселином (витамин Б9). Фолна киселина је супстрат дихидрофолатне редуктазе, ензима који учествује у формирању нуклеотида и који бива потентно инхибиран метотрексатом. Метотрексат блокира дејство дихидрофолатне редуктазе и тиме зауставља продукцију нуклеотида. Ова блокада нуклеотидне биосинтезе је токсичнија за брзорастуће ћелије него за оне које се не деле, зато што брзорастуће ћелије морају да изводе репликацију ДНК. Стога се метотрексат обично користи за хемотерапију канцера.[44]
Антибиотици[уреди | уреди извор]
Лекови се исто тако користе за инхибирање ензима неопходних за опстанак патогена.[45][46] На пример, бактерије су окружене дебелим ћелијским зидом сачињеним из полимера који наликује на мрежу и зове се пептидогликан. Многи антибиотици, као што су пеницилин и ванкомицин, инхибирају ензиме који производе и потом умрежавају нити тог полимера.[47] Последица њиховог дејства је да бактеријски ћелијски зид губи јачину и бактерије се распрсну.[48] На слици, молекул пеницилина (приказан у форми „кугли и штапића”) везан је за свој циљни ензим, транспептидазу из бактерије Streptomyces R61 (протеин је приказан као тракасти дијаграм).[49]
Антибиотички дизајн лекова је олакшан кад је ензим који је есенцијалан за опстанак патогена одсутан или веома различит код људи.[50] У примеру изнад, људско тело не прави пептидогликан, и стога су инхибитори тог процеса селективно токсични за бактерије. Селективна токсичност се такође остварује код антибиотика кроз искоришћавање разлика у структури рибозома код бактерија,[51] или начина на који праве масне киселине.[52]
Метаболичка контрола[уреди | уреди извор]
Ензимски инхибитори су важни у метаболичкој контроли.[53] Многи ћелијски метаболички путеви су инхибирани метаболитима, који контролишу ензимску активност путем алостерне регулације или инхибиције супстрата. Добар пример је алостерна регулација гликолитичког пута.[54] Овај катаболички пут конзумира глукозу и производи ATP, NADH и пируват.[55][56] Кључни корак у регулацији гликолизе је једна рана реакција пута која је катализована фосфофруктокиназом-1 (PFK1).[57][58] Кад се ATP ниво повиси, ATP се везује за алостерно место на PFK1 чиме се смањује брзина ензимске реакције; гликолиза се инхибира и опада продукција ATP. Овај облик контроле негативном повратном спрегом помаже у одржавању стабилног нивоа концентрације ATP молекула у ћелији.[59] Међутим, метаболички путеви се не регулишу само инхибицијом, већ је активација ензима једнако важна. У односу на PFK1, фруктоза 2,6-бисфосфат и ADP представљају примере метаболита који делују као алостерини активатори.[60]
Физиолошка ензимска инхибиција се такође може произвести путем специфичних протеинских инхибитора. Овај механизам се јавља у панкреасу, који синтетише мноштво дигестивних прекурсорских ензима, познатих као зимогени.[61][62] Многи од њих се активирају дејством протеазе трипсин,[63] тако да је важно да се инхибира активност трипсина у панкреасу да би се спречила могућност да орган почне да пробавља сам себе.[64] Један начин контроле активности трипсина је продукција специфичног и потентног протеинског инхибитора трипсина у панкреасу.[65] Тај инхибитор се чврсто везује за трипсин, спречавајући активност трипсина која би иначе била штетна за орган.[66] Мада је трипсински инхибитор протеин, он избегава да постане супстрат протеазе тако што уклања воду из активног места трипсина и тиме дестабилизује прелазно стање.[67] Други примери физиолошких ензимских инхибиторних протеина су барстар који је инхибитор бактеријске рибонуклеазе барназе[68][69][70][71] и инхибитори протеинских фосфатаза.[72]
Пестициди и хербициди[уреди | уреди извор]
Многи пестициди су ензимски инхибитори.[73] Ацетилхолинестераза (AChE) ензим је који је присутан у животињама од инсеката до људи.[74][75] Есенцијалан је за функцију нервних ћелија.[76] Овај ензим делује тако што разлаже неуротрансмитер ацетилхолин у његове конституенте, ацетат и холин.[77][78] Ацетилхолин је донекле јединствен међу неуротрансмитерима у смислу да се већина њих, укључујући серотонин, допамин, и норепинефрин, апсорбује из синаптичког отвора уместо да буде разграђена. Велики број AChE инхибитора се користи у медицини и агрикултури.[77][78] Реверзибилни конкурентни инхибитори, као што је едрофонијум,[79] физостигмин и неостигмин, користе се за третман миастеније гравис[80][81][82] и за анестезију.[83] Карбаматни пестициди су такође примери реверзибилних AChE инхибитора.[84] Органофосфатни пестициди као што су малатион, паратион и хлорпирифос иреверзибилно инхибирају ацетилхолинестеразу.[85]
Хербицид глифосат је инхибитор 3-фосфошикимат 1-карбоксивинилтрансферазе.[86][87][88] Други хербициди, као што су сулфонилуреје, инхибирају ензим ацетолактатну синтазу.[89][90] Оба ова ензима су неопходна да би биљке правиле аминокиселине са разгранатим бочним ланцем. Хербициди инхибирају многе друге ензиме, укључујући ензиме који су неопходни за биосинтезу липида[91] и каротеноида,[92] као и за процесе фотосинтезе и оксидативне фосфорилације.[93]

Природни отрови[уреди | уреди извор]
Животиње и биљке су током еволуције развиле способност да синтетишу широк опсег отровних продуката укључујући секундарне метаболите,[94] пептиде и протеине који могу да делују као инхибитори. Природни токсини су обично мали органски молекули и толико су разноврсни да су вероватно природни инхибитори већине метаболичких процеса.[95][96] Метаболички процеси на које делују природни отрови обухватају не само ензиме метаболичких путева, него и инхибицију рецептора, канала и структурних протеинских функција у ћелији.[97] На пример, паклитаксел (таксол),[98] органски молекул присутан у пацифичкој тисовини, чврсто се везује за тубулинске димере и инхибира њихово уклапање у микротубуле цитоскелетона.[99][100][101]
Многи природни отрови делују као неуротоксини који могу да узрокују парализу доводећи до смрти и користе се за одбрану од предатора или за лов и хватање плена. Неки од ових природних инхибитора су, упркос својим токсичним својствима, корисни за терапеутске сврхе при ниским дозама.[102] Пример неуротоксина су гликоалкалоиди, из биљних врста фамилије Solanaceae (која обухвата кромпир,[103] парадајз и плави патлиџан), који су инхибитори ацетилхолинестеразе. Инхибиција овог ензима узрокује неконтролисано повишење нивоа неуротрансмитера ацетилхолина, мишићну парализу и затим смрт. Неуротоксичност такође може да буде последица инхибиције рецептора; на пример, атропин из велебиља (Atropa belladonna) који функционише као конкурентни антагонист мускариничких ацетилхолинских рецептора.[104]
Иако су многи природни токсини секундарни метаболити, ови отрови обухватају и многе пептиде и протеине. Пример токсичног пептида је алфа-аманитин,[105] који се налази у сродним врстама печурке зелена пупавка. У питању је потентан ензимски инхибитор. У овом случају долази до спречавања ензима РНК полимераза II да транскрибује ДНК.[106] Токсин из алги микроцистин је такође пептид. Он инхибира протеинске фосфатазе.[107] Овај токсин може да контаминира залихе воде након цветања алги; познати је карциноген који узрокује акутно крварење јетре и смрт при већим дозама.[108]
Протеини могу да буду буду природни отрови или антинутријенти, као што су трипсински инхибитори (описани изнад), који су присутни у неким махунама, као што је приказано на левој слици изнад. Мање заступљена класа токсина су токсични ензими: они делују као иреверзибилни инхибитори својих циљних ензима и хемијски модификују супстратне ензиме. Пример оваквог ензима је рицин, екстремно потентан протеински токсин присутан у биљци Ricinus communis.[109][110][111] Овај ензим је гликозидаза[112][113] која инактивира рибозоме. Пошто је рицин каталитички иреверзибилан инхибитор, могућ је сценарио где само један молекул рицина може да убије ћелију.[114]
Метални комплекси као инхибитори ензима[уреди | уреди извор]
Један од приступа откривању лекова се састоји од испитивања потенцијалних терапеутских комплекса за биолошку активност, те накнадног бављења питањем механизма. За многе лекове, начин деловања још увек није јасан, чак ни након много година клиничке употребе. У последњих неколико година, велики напредак у расветљавању молекуларних структура омогућио је прецизно одређивање интеракција између протеина и терапијских средства. Овим је појашњен механизам многих агенаса и омогућено је информисано предвиђање потенцијалних места везивања лека. Идентификација тачне природе интеракција лека је кључна за контролисање његове специфичности, а тиме и за смањење нежељених дејстава (нуспојава).[115]
Детаљне структурне информације се могу користити за дизајнирање молекула који се везују за специфичне циљеве, а већина ових напора је усмерена на ензиме. Супстратна специфичност ензима која омогућава препознавање појединачних молекула, пружа могућност конструисања лекова са добро дефинисаним понашањем.[116] Сматра се да су ензими природне мета неорганских лекова,[117] пошто метали имају кључне структурне улоге у многим ензимима, на пример у цинковим металоензимима.[118][119] Пертурбације ендогеног метала који је од виталног значаја за ензимско дејство могу да доведу до инактивације ензима. Ови поремећаји могу да буду изазвани утицајима као што је координација егзогених лиганада за металом, супституција метала, или уклањање метала. Неоргански комплекси такође могу да утичу на ензиме који нису металоензими. Метали се могу координирати са остацима активног места и тиме блокирати супстратну интеракцију, или се могу координирати са остацима изван активног места и тиме утицати на структурни интегритет. Иако је листа инхибитора ензима који се користе као терапеутски агенси у великој мери попуњена органским молекулима, ти агенси међуделују са циљевима путем слабих веза као што су водоничне везе и Ван дер Валсови контакти. То потенцијално може да доведе до нуспојава услед кратког интервала задржавања лекова у активном месту мета, те су могуће неспецифичне интеракције са молекулима који нису жељена мета. Координациона способност метала може да произведе јаче интеракције, као што су ковалентне и јонске везе.
Примена на нормалну и абнормалну физиологију[уреди | уреди извор]
Канцер[уреди | уреди извор]
Један од најзначајнијих успеха неорганских лекова је била ефикасност комплекса платине против рака тестиса.[120][121] Тај напредак је подстакао талас истраживања с циљем идентификације нових неорганских агенаса за употребу у хемотерапији, који би имали побољшану специфичност и мање изражене токсичне нуспојаве. Механизам антинеопластичног дејства цисплатина и његових деривата је идентификован као директна интеракција са ДНК, мада бројни извештаји сугеришу да платина исто тако има ензимске мете.[122] Инхибиција РНК полимеразе,[123] ДНК полимеразе (могућег ометања функционисања цинковог прста),[124] илеалне моноаминске оксидазе (што је везано за споредне ефекте хемотерапије: мучнину и повраћање),[125] ЦТП синтазе,[126] аденилат циклазе (у вези са степеном ототоксичности хемотерапије)[127][128] и других респираторних ензима,[129] били су уочени. Преинкубација пречишћеног ензима са комплексима платине показала је да долази до директне интеракције између њих, али је у многим случајевима везивање платине за циљни ензим такође допринело инхибицији. Инхибиција ензима може да допринесе неким од нежељених токсичних ефеката лекова на бази платине; боље разумевање интеракција са тим комплексима је потребно да бе се умањиле нежељене последице хемотерапије.
Платински лекови су један од примера у коме је примећен терапеутски ефекат лека пре него што је откривен механизам дејства. Алтернативни приступ је дизајн лека са одређеном метом на уму. Тражени су специфични циљеви који играју кључне улоге у метаболизму ћелија рака, који су јединствени за ћелије канцера или су различито изражени у ћелијама рака. Рибонуклеотидна редуктаза је један такав молекул који се показао као обећавајућа мета за терапију рака.
Рибонуклеотидна редуктаза обавља кључни корак који ограничава брзину синтезе ДНК путем контроле производње четири дезоксирибонуклеотидна грађевна блока. Овај ензим редукује 2' угљеник рибозе на дифосфатном нивоу.[130] Ензим се састоји од две димерне подјединице (зване M1 и M2 у старијим извештајима, или R1 и R2 у скоријим публикацијама), које су кодиране са два различита гена под засебном регулаторном контролом. Активност самог ензима је зависна од комплексне алостерне регулације различитим нуклеотидима. R1 садржи места везивања супстрата и регулаторних ефектора, док R2 садржи она бинуклеарних, нехемни центар гвожђа и слободног тирозинског радикала, који су неопходни за функционисање ензима. Рибонуклеотидна редуктаза контролише равнотежу дезоксирибонуклеотиде доступности, а промене њене активности могу да промене спонтану мутациону брзину ћелија.[130] Повећана активност рибонуклеотидне редутазе доводи се у везу са стањима болести, укључујући рак;[130][131] инхибиција овог ензима је атрактивна мета за терапију рака.
Известан напредак је направљен у коришћењу галијум нитрата у инхибицији рибонуклеотидне редуктазе.[132][133][134] Галијум има сличан јонски радијус као и гвожђе и сматра се да омета доступност гвожђа у R2 подјединици. Инхибиторни ефекат галијума се повећава када се испоручује у комплексу са есенцијалним молекулом транспорта гвожђа, трансферином. Ћелијске студије показују да третман са трансферин-галијумом (Tf-Ga) блокира ћелијску апсорпцију 59Fe и инхибира пролиферацију.[133] Умањена активност рибонуклеотидне редуктазе огледа се у инхибицији ESR сигнала из тирозинског слободног радикала на R2 подјединицу рибонуклеотидне редуктазе. Ови ефекти могу бити преокренути излагањем фероамонијум сулфату, што указује да инхибиција утиче на процес зависан од гвожђа. Ови резултати не искључују ефекте на другим путевима зависним од гвожђа, што такође може да утиче на пролиферацију ћелија. Студије у систему без ћелија у којима се директно тестира активност ензима показују да галијум инхибира активност ензима; аутори претпостављају да галијум формира галијум-CDP, или галијум-ADP комплексе, чиме компетитивно инхибира интеракцију супстрата са ензимом.[134] Ни једна од ових студија не даје одговор на питање да ли се галијум може заменити гвожђем у R2 подјединици и да ли је тако супституисани ензим и даље активан. Галијум такође синергистички делује са бројним другим инхибиторима рибонуклеотидне редуктазе на онемогућавању ћелијске пролиферације. Његово дејство је антагонистичко у односу на друге инхибиторе рибонуклеотидне редуктазе.[132] Ове опсервације имају значајне последице за комбиновану терапију, мада прецизан механизам синергизма није познат.
Други јони су такође истраживани у погледу утицаја на рибонуклеотидне редуктазе. Познато је да гвожђе, бакар и цинк утичу на раст ћелија и регулишу компоненте циклуса транспорта гвожђа. Студије о утицају тих јона на рибонуклеотидну редуктазу у свеже изолованим нормалним и леукемијским људским лимфоцитима показале су да цинк инхибира ензим у оба типа ћелија, док Fe и Cu имају стимулативне ефекте.[130][131] Ови резултати могу имати импликације за модулацију ефеката инхибитора рибонуклеотидне редуктазе траговима метала.
| Примене на третман канцераа | |||
|---|---|---|---|
| Комплекс | Метал | Ензим | |
| трансферин-Ga | јони Ga | рибонуклеотидна редуктаза[133][134] | |
| карботиоамид | Fe, Cu | рибонуклеотидна редуктаза[135][136] | |
| тиосемикарбазони | Cu | рибонуклеотидна редуктаза, РНК- -зависне ДНК полимеразе[137] | |
| јони | Zn | рибонуклеотидна редуктаза[131] | |
| јони | Ga | рибонуклеотидна редуктаза[132] | |
| антрациклин, јони | Cu | протеинска киназа C[138] | |
| селеноцистеин/глутатион | Se | протеинска киназа C[139][140] | |
| металоцени | Mo, V | протеинска киназа C, топоизомераза II[141] | |
| бипиридински фенантролин | Pt, Pd | РНК полимераза[123] | |
| стрептонигрин | Fe, Cu, Pd, Cd, Zn | топоизомераза III, реверзна транскриптаза (путем формирања слободних радикала)[142] | |
| PtCl2, cis-DDP | Pt | ДНК полимераза[124] | |
| цисплатин, бакар сулфат | Pt, Cu | илеална моноаминска оксидаза[125] | |
| cis-DDP, K2PtCl4 | Pt | CTP синтаза[126] | |
| јони | Zn | каспаза-3[143][144] | |
| разни | Ga | орнитинска декарбоксилаза[145] | |
| cis-DDP, тетраплатин, карбоплатин | Pt | респираторни ензими[128] | |
| цисплатин | Pt | аденилатна циклаза[127] | |
| тетраплатин | Pt | аденилатна циклаза[128] | |
| ванадат, пероксованадијум | V | протеинске тирозинске фосфатазе[146][147] | |
| јон | Zn | Ser/Thr фосфопротеинска фосфатаза[148] | |
| метални хелатор | Cd | матрилизин[149] | |
а Напомена: У овој и наредним табелама оксидационо стање металног јона није приказано ради јасноће. Додатне информације су дате у тексту.
| |||
За металне комплексе карботиоамида[135][136][150] и тиосемикарбазона[137] је утврђено да инхибирају рибонуклеотидну редуктазу и имају антиканцерогено дејство. Утврђено је да метални комплекси α-(N)-хетероцикличних карбоксиалдехидних тиосемикарбазона (α-HCAT) инхибирају раст ћелија у већој мери него слободни лиганд.[136] Метални комплекси 2,2'-бипиридил-6-карботиоамида (BPYTA), који су структурно и функционално слични α-HCAT, не показују тако јасно дејство. Студије гвожђа и бакра у комплексу са BPYTA су показале да BPYTA има већи афинитет за бакар; бакарни комплекс показује израженије антитуморско дејство од слободног лиганда или комплекса гвожђа. Студије са слободним лигандом међутим нису јасне, јер је вероватно да лиганд формира комплексе са расположивим металним јонима у раствору. Сматра се да дозиметрија BPYTA комплекса може да утиче на учинак. На пример, бакарни комплекс има најјачи антипролиферативни ефекат на култивисаним мишјим леукемијским ћелијама након пулсног контакта, док је у случају континуираног контакта мање активан од слободног лиганда. Осим тога, изгледа да различити метални комплекси делују различитим механизмима. Док се антипролиферативни ефекат комплекса гвожђа може објаснити инхибицијом рибонуклеотидне редуктазе и верује се да заправо уништава R2 подјединицу, постоје индикације да комплекс бакра такође делује на друге циљеве.[150][151] Потврђено је да BPYTA синергистички делује са инхибитором рибонуклеотидне редуктазе хидроксиурејом (HU), што сугерише могућност комбиноване терапије.
Још једна ензимска мета за агенсе против канцера је протеинска киназа C (PKC). PKC је фамилија серин/треонинских киназа које се активирају секундарним гласницима попут Ca2+ и продуктима фосфолипидне хидролизе (из каскаде инозитол трифосфата). Девет различитих чланова ове породице је до сада окарактерисано и они учествују у различитим ћелијским активностима, укључујући трансдукцију сигнала, раст ћелија/диференцијацију и хормонску секрецију.[138] Они су такође познати као рецептори форболних естара (познатих хемијских активатора), а активирају се и у одговору на оксидативне промотере тумора.[139] Инхибиција PKC је од интереса као начин спречавања формирања тумора. Недавни докази указују на то да је PKC регулаторни домен, који има два хомологна региона са шест очуваних цистеина и два конзервисана хистидина, те садржи непремошћена Zn2+ места.[152] Противтуморска средства која делују на PKC обухватају антрациклине, чије је дејство посредовано координацијом с прелазним металима. Једна студија на пречишћеном PKC је показала да антрациклин-Cu(II) комплекс ефикасније инхибира PKC него појединачне компоненте и да је тај ефекат посредован директном интеракцијом између Cu(II) и PKC (овај закључак је изведен из EPR студија).[138] Исто тако је показано да антрациклини имају различите ефекте на ДНК топоизомерази II,[153] мада још увек нема извештаја о дејству комплекса прелазних метала са антрациклинима у овом виду примене.
Поједина једињења селенијума имају инхибиторни ефекат на PKC, а такође имају канцерпревентивно дејство.[139][140] Резултати истраживања сугеришу да та једињења инактивирају PKC путем редокс механизма, реагујући са цистеинима унутар PKC каталитичког домена.[139] У једној студији је показано да једињења селенијума инхибирају PKC, док на друге тестиране протеинске киназе немају утицаја (на фосфорилазну киназу и протеинску фосфатазу 2А). Међутим, постоји могућност да ова једињења реагују са другим протеинима који садрже кластере цистеина.
Металоцени су класа антитуморних агенаса који не садрже платину и који делују на различит начин од лекова базираних на платини.[154][141] Поједини металоцени се везују за терминалне фосфате и/или базе нуклеотида, док други не међуделују са нуклеотидима.[141][155][156] Из тог разлога је предложен низ алтернативних циљева. Показано је да V(IV) и Mo(IV) једињења инхибирају PKC и топоизомеразу II.[141] Једињења ниобијума (Nb) не везују се за нуклеотиде или аминокиселине.[155] Механизам дејства ове класе захтева даља истраживања.
Једињења ванадијума, која су најбоље позната као инсулински миметици, исто тако испољавају антиканцерне ефекте. Ова једињења, конкретно комплекси ванадата и пероксованадијума, компетитивни су инхибитори протеинске тирозинске фосфатазе (PTP). Ванадати делују као аналози прелазног стања реверзибилним везивањем за тиолну групу у каталитичком домену, док пероксованадијумски комплекси оксидују критичне цистеинске остатке у каталитичком домену.[146] У серин/треонинским фосфатазама, ванадати се везују за хидроксилну групу у активном месту, док су пероксованадијумски комплекси неактивни у одсуству цистеина. Пероксованадијумски комплекси могу да блокирају ћелијски циклус у фази G2-M транзиције (G2 = фаза раста 2, препараторна фази митозе; M = митоза, период активне ћелијске поделе); сматра се да је то узроковано инхибицијом PTP, чије функционисање је есенцијално за прогресију митозе.[146][147] Могуће је да је ова блокада повезана са њиховим цитотоксичним дејством. Серин/треонинске фосфатазе су такође инхибиране бројним јонима прелазих метала д-блока, међу којима су најефективнији Zn2+, Hg2+, Cu2+, Yb2+ и Sc2+ (μM Ki).[148]
Бројне друге ензимске мете за антиканцерне агенсе такође су истраживане. Орнитинска декарбоксилаза, која се може индуковати форболним естрима и која учествује у ћелијској трансформацији, може се инхибирати једињењима галијума.[145] Трансформација је повезана са ћелијском транзицијом у канцерозно стање. Та једињења инхибирају раст тумора и сматра се да исто тако делују на рибонуклеотидне редуктазе. Матричне металопротеиназе учествују у ремоделовању екстрацелуларне матрице, што је кључно за инвазију тумора и метастазу у ткивима. Људска матрична металопротеиназа матрилизин је ензим цинка за који је показано да се инактивира у раствору кадмијума, који формира неактивни Cd/Zn хибрид.[149] Матрилизин се исто тако може инхибирати агенсима металног везивања, као што је 1,10-фенантролин, који формира ензим-хелат-метал комплекс уз накнадно уклањање каталитичког јона цинка.[149]
Апоптоза, која је постала проминентно поље истраживања последњих година, процес је „програмиране” ћелијске смрти. Постоји корелација између дефеката апоптозних процеса и бројних болести, укључујући канцер. Познато је да Zn2+ спречава апоптозу и показано је да до тога долази путем инхибирања каспазе-3, апоптотичке протеазе која учествује у протеолизи поли(ADP-рибоза) полимеразе (PARP).[143][144] Конфликтни извештаји не узимају у обзир инхибиторно дејство цинка на каспазу-3.[157] Сматра се да су несугласице последица разлика у експерименталним условима: инхибиција уочена у случају пречишћеног рекомбинантног протеина али не и код протеина у присуству E. coli лизата, сугеришу постајање фактора у лизату који ометају дејство цинка.
Постоје бројни агенси који делују путем инхибиције ензима који делују на ДНК. Ова инхибиција је често последица везивања за место којим ензим формира интеракције са ДНК и није резултат директне инактивације ензима.[153][158][159][160]
Имајући у виду природу интеракција ензима и супстрата, избор ензима као циљева антиканцерних лекова омогућава изузетно специфично препознавање циљева. Развој софистициранијих техника моделовања и доступност детаљнијих информација о структурама ензима довели су до ригорозне карактеризације интеракција лека и ензима, те разјашњавања механизма дејства. Већина публикација у литератури о канцеру се бави инхибицијом специфичних ензима, повремено оних који учествују у метаболичким процесима. У тим истраживањима се користе пречишћени ензими или тестови којима се испитују појединачни ензими од значаја. Док је круцијално да се одреде инхибиторне особине на циљном молекулу, исто тако је неопходно да се демонстрира да једињење није активно на другим ензимима. Овај тип студија је тегобан пошто се може тестирати само релативно мали број репрезентативних ензима, па се лако може пропустити ензим који негира специфичност. Пажљивим разматрањем места деловања лека може да се омогући извођење релативно добрих прогноза о могућим интеракцијама са другим ензимима. Додатни изазов је да су ензимске мете често присутне и у нормалним ћелијама. Дизајн ефективних антиканцерних агенаса је компликован процес који не обухвата само инхерентна инхибиторна својства лека, него и његову испоруку, дозиметрију и време задржавања ин виво. Метални комплекси превазилазе неке од ових изазова формирањем јаких ковалентних веза са циљним ензимима.
Примене везане за хем[уреди | уреди извор]
- Хипербилирубинемија
| Хипербилирубинемија | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| јони | Sn | цитохром P-450, ω-хидролаза[161] | |
| протопорфирин (PP) | Sn, Zn | 11β-хидроксилаза, 21R-хидроксилаза, цитохром P-450, хем оксигеназа[162][163][164] | |
| мезопорфирин (MP) | Sn | хем оксигеназа (танко црево)[165] | |
| деутеропорфирин 2,4-бисгликол (BG) | Zn | хем оксигеназа (пацов)[166] | |
| MP | Zn | хем оксигеназа (пацов)[167] | |
| MP | Co | хем оксигеназа слезине (мождане мембране пацова)[168] | |
| PP, BG, MP | Cr | хем оксигеназа (пацов)[169] | |
| разни порфирини | Zn, Sn, Cu | γ-аминолевулинатна синтаза (ћелије јетре кокошјег ембриона), хем оксигеназа 56 | |
| разни порфирини | Zn, Sn, Cr, Mg | хем оксигеназа (епител танког црева)[170] | |
| мезопорфирин | Sn | клиничка супресија хипербилирубинемије[171][172] | |

Инхибитор ензима је молекул који се везује за ензим и умањује његову активност. Пошто блокирање ензимске активности може да узрокује угинуће патогена или да коригује метаболичку неуравнотеженост, стога су многи лекови инхибитори ензима. Инхибитори ензима се такође користе као пестициди. Нису сви молекули који се везују за ензиме инхибитори; активатори ензима се везују за ензиме и повећавају њихову активност, док се ензимски супстрати везују и бивају конвертовани до продуката у нормалном каталитичком циклусу ензима.
Везивање инхибитора може да спречи приступ супстрата ензимском активном месту и/или омете ензим при катализи биохемијске реакције. Везивање инхибитора може да буде реверзибилно или иреверзибилно. Иреверзибилни инхибитори обично реагују са ензимом и хемијски га мењају (нпр. формирањем ковалентне везе), те модификују кључне аминокиселинске остатке неопходне за ензиматску активност. Насупрот овоме, реверзибилни инхибитори се везују нековалентно, те се различити типови инхибиције јављају зависно од тога да ли се инхибитори везују за ензим, за ензимско-супстратни комплекс, или за обоје.[1]
Многи молекули лекова су инхибитори ензима, тако да је њихово откривање и побољшање активна област истраживања у биохемији и фармакологији. Медицински ензимски инхибитори се често вреднују по својој специфичности (свом одсуству везивања за друге протеине) и својој потентности (својој константи дисоцијације, која је индикатор концентрације неопходне за инхибицију ензима). Висока специфичност и потентност су предуслови да лек испољава мали број нуспојава и стога ниску токсичност.
Ензимски инхибитори се исто тако јављају у природи и учествују у регулацији метаболизма. На пример, ензими у метаболичком путу могу да буду инхибирани продуктима даљих корака пута. Овај тип повратне спреге успорава ћелијску производну линију кад продукти почну да се накупљају, и то је један од важних начина одржавања хомеостазе у ћелијама. Други ћелијски ензимски инхибитори су протеини, који се специфично везују за и инхибирају ензимску мету. То може да помогне у контроли ензима, који би иначе могли да оштете ћелију, као што су протеазе или нуклеазе. Једна детаљно окарактерисана класа инхибиторних молекула су рибонуклеазни инхибитори, који се везују за рибонуклеазе формирајући једну од најчвршћих познатих протеин—протеин интеракција.[2] Природни ензимски инхибитори такође могу да буду отрови и да се користе као вид одбране од предатора, или као начин убијања плена.
Реверзибилни инхибитори[уреди | уреди извор]
Типови реверзибилних инхибитора[уреди | уреди извор]
Реверзибилни инхибитори се везују за ензиме путем нековалентних интеракција као што су водоничне везе, хидрофобне интеракције и јонске везе. Вишеструке слабе везе између инхибитора и активног места се комбинују и производе јако и специфично везивање. За разлику од супстрата и иреверзибилних инхибитора, реверзибилни инхибитори генерално не подлежу хемијским реакцијама при везивању за ензим и могу лако да се уклоне разблаживањем или дијализом.
Постоје четири врсте реверзибилних ензимских инхибитора. Класификују се на основу утицаја променљиве концентрације ензимског супстрата на инхибитор.[3]

- У конкурентној инхибицији, супстрат и инхибитор не могу истовремено да се вежу за ензим, као што је то приказано на слици десно. То је обично последица тога да инхибитор има афинитет за активно место ензима за које се такође везује супстрат; супстрат и инхибитор се надмећу за приступ активном месту ензима. Овај тип инхибиције се може превазићи применом довољно високих концентрација супстрата (Vmax остаје константно), од. путем надмашивања концентрације инхибитора. Међутим, долази до повећања појавне вредности Km, јер је потребна већа концентрација супстрата да би се досегла тачка Km, или половина вредности Vmax.[4] Конкурентни инхибитори су обично структурно слични реалном супстрату (види примере испод).
- У неконкурентној инхибицији, инхибитор се једино везује за супстратно-ензимски комплекс. Овај тип инхибиције узрокује снижење вредности Vmax (максимална брзина се смањује услед уклањања активираног комплекса) и вредности Km (услед повећане ефикасности везивања која произилази из Ле Шатељеовог принципа и ефективне елиминације ES комплекса чиме се умањује Km, што је индикатор повећаног афинитета везивања).[4]
- У бесконкурентној инхибицији, везивањем инхибитора за ензим редукује се његова активност, мада то нема утицаја на везивање супстрата. Резултат овога је да степен инхибиције једино зависи од концентрације инхибитора. Вредност Vmax се смањује, јер се реакција одвија мање ефикасно, док се вредност Km не мења, пошто се само везивање супстрата — по дефиницији — и даље нормално одвија.[4]
- У мешовитој инхибицији, инхибитор се може везати за ензим истовремено са супстратом ензима. Међутим, овакво везивање инхибитора утиче на везивање супстрата, и обрнуто. Ова врста инхибиције се може умањити, али не и превазићи повећањем концентрације супстрата. Мада постоји могућност да се инхибитори мешовитог типа вежу на активном месту, овај тип инхибиције генерално произилази из алостерног дејства, при чему се инхибитор везује на различитом месту на ензиму. Везивање инхибитора за алостерно место мења конформацију (тј. терцијарну структуру или тродимензионални облик) ензима, тако да је афинитет супстрата за активно место умањен.[4]
Квантитативни опис реверзибилне инхибиције[уреди | уреди извор]
Реверзибилна инхибиција се може квантитативно описати у погледу везивања инхибитора за ензим и за ензимско-супстратни комплекс, као и његовог утицаја на кинетичке константе ензима. У класичној Михаелис—Ментениној шеми испод, ензим (E) везује се за свој супстрат (S) и формира ензимско-супстратни комплекс ES. Након катализе, овај комплекс се разлаже и ослобађају се продукт P и слободни ензим. Инхибитор (I) може се везати или за E или за ES са константама дисоцијације Ki или Ki′, редом.
Када ензим има вишеструке супстрате, инхибитори могу да испоље различите типове инхибиције у зависности од тога који се супстрат посматра. До овога долази зато што активно место садржи два различита места везивања, по једно за сваки супстрат. На пример, инхибитор се може надметати са супстратом A за прво место везивања, а бити бесконкурентни инхибитор супстрата B у другом месту везивања.[5]
Мерење константи дисоцијације реверзибилног инхибитора[уреди | уреди извор]
Као што је напоменуто изнад, ензимски инхибитор се описује путем својих двеју константи дисоцијације: Ki и Ki′, за ензим и ензимско-супстратни комплекса, редом. Ензимско-инхибиторска константа Ki се може директно мерити различитим методима. Један од изузетно прецизних метода је изотермална титрациона калориметрија, у којој се инхибитор титрира у раствор ензима; потом се мери ослобођена или апсорбована топлота.[6] Међутим, другу константу дисоцијације Ki′ је тешко директно мерити, пошто је ензимско-супстратни комплекс краткотрајан и подлеже хемијској реакцији којом се формира продукт. Стога се Ki′ обично индиректно мери, и то путем посматрања ензимске активности при различитим концентрацијама супстрата и инхибитора, те постављањем података[7] у модификовану Михаелис—Ментенину једначину.
где су модификујући фактори α и α′ дефинисани путем концентрације инхибитора и његових двеју константи дисоцијације:

Стога, у присуству инхибитора, ензимске ефективне вредности Km и Vmax постају (α/α′)Km и (1/α′)Vмаx, редом. Треба имати у виду да модификована Михаелис—Ментенина једначина подразумева да је остварена равнотежа везивања инхибитора за ензим, што може да буде веома спор процес за инхибиторе са поднаномоларним константама дисоцијације. У тим случајевима, обично је практичније да се третира чврсто везујући инхибитор као иреверзибилни инхибитор (види испод); мада, још увек може да постоји опција кинетичког процењивања Ki′, ако се независно измери Ki.
Утицаји различитих типова реверзибилних инхибитора ензима на ензиматску активност се могу приказати користећи графичке репрезентације Михаелис—Ментенине једначине, као што су Лајнвивер—Берков и Еди—Хофстијев дијаграм. На пример, на Лајнвивер—Берковом дијаграму приказаном десно, линије конкурентне инхибиције секу се на y-оси, што илуструје да такви инхибитори немају утицаја на Vmax. Аналогно, линије бесконкурентне инхибиције секу се на x-оси, што показује да ови инхибитори не утичу на Km. Међутим, често је тешко прецизно проценити Ki и Ki′ са дијаграма,[8] па се препоручује коришћење поузданијих метода нелинеарне регресије за процену константи (описано изнад).
Реверзибилни инхибитори[уреди | уреди извор]
Традиционално се реверзибилни инхибитори ензима класификују као конкурентни, неконкурентни или бесконкурентни, на основу њиховог утицаја на параметре Km и Vmax. Ти различити утицаји директно произилазе из начина везивања инхибитора за ензим E, ензимско-супстратни комплекс ES, или оба. Подела у ове класе проистиче из проблема са одређивањем параметара и ствара потребу за коришћењем различитих константи везивања за описивање чина везивања. Везивање инхибитора и његов утицај на ензиматску активност су две потпуно различите свари, што је још један проблем који традиционалне једначине не одражавају. Код неконкурентне инхибиције везивање инхибитора следствено једначинама једино доводи до потпуне (100%) инхибиције ензима, и једначине не остављају могућност постојања било чега између тих крајности.[9] Заједнички облик инхибиторног члана такође замагљује однос између везивања инхибитора за ензим и његовог односа са другим члановима везивања, било да је то Михаелис—Ментенина једначина или дозно-респонсна крива асоцирана са везивањем лиганда за рецептор. Да би се демонстрирао однос, може се створити следеће прераспоређивање:
Додајући нулу на дно ([I]−[I]):
... и делећи са [I]+Ki добија се:
Ова једначина демонстрира да је слично Михаелис—Ментениној једначини, где брзина реакције зависи од процента ензимске популације која међуделује са супстратом:
разломак ензимске популације везане супстратом
разломак ензимске популације везане инхибитором
... утицај инхибитора резултат процента популације ензима која међуделује са инхибитором. Једини проблем са овом једначином у њеној тренутној форми је што подразумева апсолутну инхибицију ензима везивањем инхибитора, док се у стварности може јавити широк опсег утицаја: од 100% инхибиције супстрата до само извесног процента, > 0%. Да би се ово узело у обзир, једначина се може једноставно модификовати увођењем члана делта Vmax, тако да дозвољава различите степене инхибиције:
... или:
Овај члан може онда да дефинише резидуални проценат ензиматске активности кад инхибитор интерагује са индивидуалним ензимима у популацији. Уврштавање овог члана има додатну предност дозвољавања могућности активације ако се испостави да је секундарни члан Vmax већи од иницијалног члана. Да би се у обзир такође узела могућност активације, једначина се може прилагодити замењивањем инхибиторске ознаке „I” општом ознаком односно модификаторским чланом који је овде означен са „X”:
Док ова терминологија доводи до поједностављеног начина руковања кинетичким ефектима везаним за максималну брзину Михаелис—Ментенине једначине, она исто тако наглашава потенцијалне проблеме са члановима који се користе за описивање ефеката везаних за Km. Вредност Km везана за афинитет ензима за супстрат је у већини случаја повезана са могућим променама места везивања ензима, што је директна последица интеракције ензима и инхибитора. Стога је члан сличан горенаведеном члану за корекцију Vmax подесан у већини случајева:[10][11]
Специјални случајеви[уреди | уреди извор]
- Механизам парцијално конкурентне инхибиције је сличан оном бесконкурентне, изузев што EIS комплекс има каталитичку активност, која може да буде нижа или чак виша (парцијално компетитивна активација) од активности ензимско-супстратног (ES) комплекса. Ова инхибиција типично испољава нижу вредност Vmax, док се вредност Km не мења.[5][12]
- Неконкурентна инхибиција се јавља када се инхибитор везује само за ензимско-супстратни комплекс, не и за слободни ензим; комплекс EIS је каталитички неактиван. Овај начин инхибиције је редак и узрокује смањивање обеју вредности, и Vmax и Km.[5]
- Инхибиција супстрата и продуката се јавља кад било супстрат или продукт ензиматске реакције инхибира ензимску активност. Овај облик инхибиције може да следи компетитивне, некомпетитивне или мешовите обрасце. При супстратној инхибицији долази до прогресивног смањења активности при високим концентрацијама супстрата. То може да буде индикација постојања два места везивања супстрата на ензиму. При ниским концентрацијама супстрата, место високог афинитета је окупирано и нормална кинетика долази до изражаја. Међутим, при вишим концентрацијама долази до заузећа секундарног, инхибиторног места, чиме се инхибира ензим.[13] Продукт инхибиције често служи као регулаторно својство при метаболизму и може да формира негативну повратну спрегу.[14]
- Спора непропусна инхибиција се јавља кад иницијални комплекс ензима и инхибитора (EI) подлеже изомеризацији до другог, чвршће пакованог (непропусног) комплекса, EI*, иако је свеукупни процес инхибиције реверзибилан.[15] Ово се манифестује као споро растућа инхибиција ензима. Под овим условима, традиционална Михаелис—Ментенина кинетика даје погрешну вредност за Ki, јер је она зависна од времена. Тачна вредност Ki се може добити путем комплексније анализе константи брзина асоцијације (kon) и дисоцијације (koff) инхибитора. Додатне информације су доступне у одељку о иреверзибилној инхибицији.
Примери реверзибилних инхибитора[уреди | уреди извор]

Ензими су еволуционо развили способност чврстог везивања својих супстрата; како се већина реверзибилних инхибитора везује за активно место ензима, није изненађујуће да неки од тих инхибитора имају веома сличне структуре са супстратима своје мете. Један од примера опонашања супстрата су протеазни инхибитори. Они су веома успешна класа антиретровиралних лекова који се користе за лечење инфекције ХИВ.[16] Структура ритонавира, протеазног инхибитора који је базиран на пептиду и који садржи три пептидне везе, приказана је са десне стране. Овај лек наликује на протеин који је супстрат ХИВ протеазе; надмеће са овим супстратом за приступ активном месту ензима.
Ензимски инхибитори се често дизајнирају тако да опонашају прелазно стање или интермедијер ензимски катализоване реакције. Тиме се осигурава да инхибитор искористи стабилизујући ефекат прелазног стања ензима, што доводи до побољшаног афинитета везивања (ниже Ki вредности) него што је то случај са дизајнима заснованим на супстрату. Пример оваквог инхибитора прелазног стања је антивирални лек оселтамивир; овај лек опонаша планарну структуру прстена оксонијумског јона у реакцији виралног ензима неураминидазе.[17]

Међутим, нису сви инхибитори базирани на структурама супстрата. На пример, структура другог инхибитора ХИВ протеазе типранавира приказана је на левој страни. Овај молекул није заснован на пептиду и није очигледну структурну сличност са протеинским супстратом. Ови непептидни инхибитори могу да буду стабилнији од инхибитора који садрже пептидне везе, пошто они не могу да буду супстрати пептидаза и много мање су склони деградацији.[18]
При дизајну лекова је важно да се узму у обзир концентрације супстрата којима су изложени циљни ензими. На пример, неки инхибитори протеинских киназа имају хемијске структуре које су сличне аденозин-трифосфату, једном од супстрата поменутих ензима. Међутим, лекови који су једноставни компетитивни инхибитори ће морати да се надмећу са високим концентрацијама АТП молекула у ћелији. Протеинске киназе се исто тако могу инхибирати конкурисањем за места везивања на којима киназе међуделују са својим супстратним протеинима, а већина протеина је присутна у ћелијама са далеко нижим концентрацијама од концентрације АТП молекула. Последично, ако се два инхибитора протеинске киназе везују за активна места са сличним афинитетом — а само један од њих треба да се надмеће са АТП молекулима, онда ће компетитивни инхибитор на месту протеинског везивања ефективније инхибирати ензим.[19]
Иреверзибилни инхибитори[уреди | уреди извор]
Типови иреверзибилне инхибиције (ковалентна инактивација)[уреди | уреди извор]

Иреверзибилни инхибитори обично ковалентно модификују ензим, те инхибиција стога не може да буде повратна. Иреверзибилни инхибитори често садрже реактивне функционалне групе, као што су азотни иперити, алдехиди, халоалкани, алкени, Мајклови акцептори, фенил сулфонати или флуорофосфонати. Те електрофилне групе реагују са аминокиселинским бочним ланцима и формирају ковалентне додатке. Модификовани остаци су они са бочним ланцима који садрже нуклеофиле као што су хидроксилне или сулфхидрилне групе; ту се убрајају аминокиселине серин (нпр. DFP молекули, приказано на десној страни), цистеин, треонин или тирозин.[20]
Иреверзибилна инхибиција се разликује од иреверзибилне ензимске инактивације. Иреверзибилни инхибитори су генерално специфични за једну класу ензима и не инактивирају све протеине; не функционишу уништавајући протеинске структуре него специфичним измењивањем активног места своје мете. На пример, екстреми вредности pH или температуре обично узрокују денатурацију свих протеинских структура, што је неспецифичан ефекат. Поједини неспецифични хемијски третмани аналогно уништавају протеинску структуру: на пример, загревање у концентрованој хлороводоничној киселини ће хидролизовати пептидне везе које протеине држе на окупу, ослобађајући овиме слободне аминокиселине.[21]
Иреверзибилни инхибитори испољавају временски зависну инхибицију и њихова потентност се стога не може окарактерисати помоћу IC50 вредности. Разлог за ово је што се количина активног ензима при датој концентрацији иреверзибилног инхибитора разликује у зависности од тога колико дуго је инхибитор био преинкубиран са ензимом. Због овога, уместо IC50 користе се kobs/[I] вредности,[22] где је kobs уочена брзина инактивације псеудопрвог реда (изведена ис графика зависности логаритамске вредности постотне активности од времена) а [I] концентрација инхибитора. Параметер kobs/[I] је валидан докле год се инхибитор не засити везивањем за ензим (у ком случају је kobs = kinact).
Анализа иреверзибилне инхибиције[уреди | уреди извор]

Као што је приказано на шеми лево, иреверзибилни инхибитори формирају реверзибилни нековалентни комплекс са ензимом (EI или ESI), и затим долази до реакције којом се формира ковалентно модификовани неактивни комплекс EI*. Брзина којом се EI* формира се назива брзином инактивације, или kinact. Пошто формирање ЕИ може да се надмеће са ES, везивање иреверзибилних инхибитора се може спречити конкуренцијом било са супстратом или са другим, реверзибилним инхибитором. Овај протекциони ефекат је добра потврда специфичности реакције иреверзибилног инхибитора са активним местом.
Кораци везивања и инактивације ове реакције се испитују путем инкубације ензима са инхибитором и утврђивањем степена активности која преостаје током времена. Активност ће опадати на временски зависан начин, обично следећи експоненцијални распад. Уклапањем ових података у једначину брзине добија се брзина инактивације при датој концентрацији инхибитора. Ово се ради за неколико различитих концентрација инхибитора. Ако долази до формирања реверзибилног EI комплекса, биће уочљиво засићење брзине инактивације и из одговарајуће криве биће могуће извести kinact и Ki.[23]
Други метод који је у широкој употреби у овим анализама је масена спектрометрија. Овде прецизно мерење масе немодификованог природног ензима и инактивираног ензима даје повећање масе узроковано реакцијом са инхибитором и показује стехиометрију реакције.[24] То се обично ради користећи MALDI-TOF масени спектрометар. У комплементарној техници званој пептидни масени отисци прстију врши се разлагање природног и модификованог протеина дејством протеазе, као што је трипсин. Тиме настаје сет пептида који се могу анализирати користећи масени спектрометар. Пептиди који промене масу након реакције са инхибитором су они који садрже место модификације.
Специјални случајеви[уреди | уреди извор]

Не формирају сви иреверзибилни инхибитори ковалентне додатке на својим ензимским метама. Неки реверзибилни инхибитори се тако чврсто вежу за своје циљне ензиме да су у суштини иреверзибилни. Ови потентно везујући инхибитори могу да испоље кинетику сличну ковалентним иреверзибилним инхибиторима. Неки од ових инхибитора се брзо везују за ензим у EI комплексу ниског афинитета и затим долази до спорог прераспоређивања до веома чврсто везаног EI* комплекса (погледајте леву слику изнад). Овакво кинетичко понашање се назива спорим везивањем.[26] Спори реаранжман након везивања често обухвата конформациону промену при чему се ензим обавије око молекула инхибитора. Примери споро везујућих инхибитора су неки важни лекови, као што је метотрексат,[27] алопуринол[28] и активирани облик ацикловира.[29]
Примери иреверзибилних инхибитора[уреди | уреди извор]

Диизопропилфлуорофосфат (DFP) приказан је као пример иреверзибилног протеазног инхибитора на десној слици изнад. Ензим хидролизује фосфорно-флуорну везу, али фосфатни остатак остаје везан за серин у активном месту, чиме се ензим деактивира.[30] Слично овоме, DFP такође реагује са активним местом ацетилхолинске естеразе у синапсама неурона; последично је потентан неуротоксин, са смртном дозом мањом од 100 mg.[31]
Самоубилачка инхибиција је необични тип иреверзибилне инхибиције где ензим конвертује инхибитор у реактивну форму у свом активном месту. Пример таквог једињења је инхибитор полиаминске биосинтезе, α-дифлуорометилорнитин или DFMO, који је аналоган аминокиселини орнитин и користи се за лечење афричке трипаносомијазе (болест спавања). Орнитинска декарбоксилаза може да катализује декарбоксилацију DFMO уместо орнитина, као што је приказано изнад. Међутим, овој реакцији декарбоксилације следи елиминација атома флуора, чиме се овај каталитички интермедијер конвертује у конјуговани имин, који је веома електрофилно једињење. Ова реактивна форма DFMO молекула затим реагује или са цистеином или са лизином у активном месту, да би се ензим иреверзибилно инактивирао.[25]
Пошто иреверзибилна обично обухвата првобитно формирање нековалентног EI комплекса, понекад је могуће да се инхибитор веже за ензим на више од једног начина. На пример, на слици лево на којој је приказана трипанотионска редуктаза из људског протозоанског паразита Trypanosoma cruzi, два молекула инхибитора званог квинакрински иперит везана су у активном месту овог ензима. Горњи молекул је реверзибилно везан, док је доњи везан ковалентно пошто је реаговао са аминокиселинским остатком путем азотноиперитне групе.[32]
Откриће и дизајн инхибитора[уреди | уреди извор]

Нови лекови су продукти дуготрајног процеса развоја лекова. Први корак у том процесу је често откриће новог ензимског инхибитора. У прошлости је једини начин да се открију нови инхибитори био приступ покушаја и грешке: тестирање огромних колекција једињења на циљном ензиму у нади да ће се доћи корисних молекула. Овај приступ грубе силе је још увек успешан и био је унапређен применом приступа комбинаторне хемије којима се омогућава брза производња огромног броја нових једињења, као и технологијом високопропусног скрининга да би се брзо тестирале огромне хемијске колекције (библиотеке) с циљем налажења инхибитора.[33]
Један од скорашњих алтернативних приступа је рационални дизајн лекова, при чему се користи тродимензионална структура активног места ензима да би се предвидело који молекули би могли да буду инхибитори.[34] Та предвиђања се затим тестирају. Нови инхибитори се након тога користе за добијање структуре ензима у комплексу инхибитор/ензим, да би се потврдило на који начин су молекули везани за активно место. На бази структура је могуће дизајнирати измењене инхибиторе с циљем даље оптимизације везивања. Овај циклус тестирања и побољшања се затим понавља док се не дође до довољно потентних инхибитора.[35] Низ приступа базираних на примени рачунара за предвиђање афинитета инхибитора за ензим такође је у развоју. Примери оваквих метода су молекуларни докинг[36] и молекулска механика.[37][38]
Употребе инхибитора[уреди | уреди извор]
Ензимски инхибитори се могу наћи у природи. Осим њих постоји и знатан број инхибитора који су дизајнирани и производе се за фармаколошке сврхе и биохемијска истраживања. Природни отрови су често ензимски инхибитори који су еволуирали да штите биљке или животиње од предатора. Ти природни токсини обухватају неке од најсмртоноснијих отрова. Вештачки инхибитори се често користе као лекови, мада исто тако могу да буду и инсектициди као што је малатион, хербициди као што је глифосат, или дезинфектанти као што је триклосан. Део вештачких ензимских инхибитора блокира ацетилхолинестеразу, ензим који разлаже ацетилхолин; користе се као нервни агенси у бојним отровима.
Хемиотерапија[уреди | уреди извор]
 |
 |
 |
Ензимски инхибитори се најчешће користе као лекови за третман болести. Многи од њих делују на људске ензиме с циљем кориговања патолошког стања. Међутим, нису сви лекови ензимски инхибитори. Неки, као што су антиепилептички лекови, мењају активност ензима узрокујући да се ензим производи у мањој или већој количини. Ови ефекти се називају ензимска индукција и инхибиција[42] и представљају промене у изражавању гена. То није дирекно повезано са типом ензимске инхибиције о којем се овде говори. Други лекови међуделују са ћелијским метама које нису ензими, као што су јонски канали или мембрански рецептори.
Пример медицинског ензимског инхибитора је силденафил (вијагра), популарни лек за мушку еректилну дисфункцију. Ово једињење је потентни инхибитор cGMP специфичне фосфодиестеразе типа 5, ензима који деградира сигнални молекул циклични гуанозин монофосфат.[43] Овај сигнални молекул подстиче релаксацију глатких мишића и омогућава проток крви у corpus cavernosum, што узрокује ерекцију. Пошто лек умањује активност ензима који зауставља сигнал, продужава се трајање сигнала.
Још један пример структурне сличности појединих инхибитора са супстратима ензима на које делују је приказан на слици десно на којој се пореди лек метотрексат са фолном киселином (витамин Б9). Фолна киселина је супстрат дихидрофолатне редуктазе, ензима који учествује у формирању нуклеотида и који бива потентно инхибиран метотрексатом. Метотрексат блокира дејство дихидрофолатне редуктазе и тиме зауставља продукцију нуклеотида. Ова блокада нуклеотидне биосинтезе је токсичнија за брзорастуће ћелије него за оне које се не деле, зато што брзорастуће ћелије морају да изводе репликацију ДНК. Стога се метотрексат обично користи за хемотерапију канцера.[44]
Антибиотици[уреди | уреди извор]
Лекови се исто тако користе за инхибирање ензима неопходних за опстанак патогена.[45][46] На пример, бактерије су окружене дебелим ћелијским зидом сачињеним из полимера који наликује на мрежу и зове се пептидогликан. Многи антибиотици, као што су пеницилин и ванкомицин, инхибирају ензиме који производе и потом умрежавају нити тог полимера.[47] Последица њиховог дејства је да бактеријски ћелијски зид губи јачину и бактерије се распрсну.[48] На слици, молекул пеницилина (приказан у форми „кугли и штапића”) везан је за свој циљни ензим, транспептидазу из бактерије Streptomyces R61 (протеин је приказан као тракасти дијаграм).[49]
Антибиотички дизајн лекова је олакшан кад је ензим који је есенцијалан за опстанак патогена одсутан или веома различит код људи.[50] У примеру изнад, људско тело не прави пептидогликан, и стога су инхибитори тог процеса селективно токсични за бактерије. Селективна токсичност се такође остварује код антибиотика кроз искоришћавање разлика у структури рибозома код бактерија,[51] или начина на који праве масне киселине.[52]
Метаболичка контрола[уреди | уреди извор]
Ензимски инхибитори су важни у метаболичкој контроли.[53] Многи ћелијски метаболички путеви су инхибирани метаболитима, који контролишу ензимску активност путем алостерне регулације или инхибиције супстрата. Добар пример је алостерна регулација гликолитичког пута.[54] Овај катаболички пут конзумира глукозу и производи ATP, NADH и пируват.[55][56] Кључни корак у регулацији гликолизе је једна рана реакција пута која је катализована фосфофруктокиназом-1 (PFK1).[57][58] Кад се ATP ниво повиси, ATP се везује за алостерно место на PFK1 чиме се смањује брзина ензимске реакције; гликолиза се инхибира и опада продукција ATP. Овај облик контроле негативном повратном спрегом помаже у одржавању стабилног нивоа концентрације ATP молекула у ћелији.[59] Међутим, метаболички путеви се не регулишу само инхибицијом, већ је активација ензима једнако важна. У односу на PFK1, фруктоза 2,6-бисфосфат и ADP представљају примере метаболита који делују као алостерини активатори.[60]
Физиолошка ензимска инхибиција се такође може произвести путем специфичних протеинских инхибитора. Овај механизам се јавља у панкреасу, који синтетише мноштво дигестивних прекурсорских ензима, познатих као зимогени.[61][62] Многи од њих се активирају дејством протеазе трипсин,[63] тако да је важно да се инхибира активност трипсина у панкреасу да би се спречила могућност да орган почне да пробавља сам себе.[64] Један начин контроле активности трипсина је продукција специфичног и потентног протеинског инхибитора трипсина у панкреасу.[65] Тај инхибитор се чврсто везује за трипсин, спречавајући активност трипсина која би иначе била штетна за орган.[66] Мада је трипсински инхибитор протеин, он избегава да постане супстрат протеазе тако што уклања воду из активног места трипсина и тиме дестабилизује прелазно стање.[67] Други примери физиолошких ензимских инхибиторних протеина су барстар који је инхибитор бактеријске рибонуклеазе барназе[68][69][70][71] и инхибитори протеинских фосфатаза.[72]
Пестициди и хербициди[уреди | уреди извор]
Многи пестициди су ензимски инхибитори.[73] Ацетилхолинестераза (AChE) ензим је који је присутан у животињама од инсеката до људи.[74][75] Есенцијалан је за функцију нервних ћелија.[76] Овај ензим делује тако што разлаже неуротрансмитер ацетилхолин у његове конституенте, ацетат и холин.[77][78] Ацетилхолин је донекле јединствен међу неуротрансмитерима у смислу да се већина њих, укључујући серотонин, допамин, и норепинефрин, апсорбује из синаптичког отвора уместо да буде разграђена. Велики број AChE инхибитора се користи у медицини и агрикултури.[77][78] Реверзибилни конкурентни инхибитори, као што је едрофонијум,[79] физостигмин и неостигмин, користе се за третман миастеније гравис[80][81][82] и за анестезију.[83] Карбаматни пестициди су такође примери реверзибилних AChE инхибитора.[84] Органофосфатни пестициди као што су малатион, паратион и хлорпирифос иреверзибилно инхибирају ацетилхолинестеразу.[85]
Хербицид глифосат је инхибитор 3-фосфошикимат 1-карбоксивинилтрансферазе.[86][87][88] Други хербициди, као што су сулфонилуреје, инхибирају ензим ацетолактатну синтазу.[89][90] Оба ова ензима су неопходна да би биљке правиле аминокиселине са разгранатим бочним ланцем. Хербициди инхибирају многе друге ензиме, укључујући ензиме који су неопходни за биосинтезу липида[91] и каротеноида,[92] као и за процесе фотосинтезе и оксидативне фосфорилације.[93]

Природни отрови[уреди | уреди извор]
Животиње и биљке су током еволуције развиле способност да синтетишу широк опсег отровних продуката укључујући секундарне метаболите,[94] пептиде и протеине који могу да делују као инхибитори. Природни токсини су обично мали органски молекули и толико су разноврсни да су вероватно природни инхибитори већине метаболичких процеса.[95][96] Метаболички процеси на које делују природни отрови обухватају не само ензиме метаболичких путева, него и инхибицију рецептора, канала и структурних протеинских функција у ћелији.[97] На пример, паклитаксел (таксол),[98] органски молекул присутан у пацифичкој тисовини, чврсто се везује за тубулинске димере и инхибира њихово уклапање у микротубуле цитоскелетона.[99][100][101]
Многи природни отрови делују као неуротоксини који могу да узрокују парализу доводећи до смрти и користе се за одбрану од предатора или за лов и хватање плена. Неки од ових природних инхибитора су, упркос својим токсичним својствима, корисни за терапеутске сврхе при ниским дозама.[102] Пример неуротоксина су гликоалкалоиди, из биљних врста фамилије Solanaceae (која обухвата кромпир,[103] парадајз и плави патлиџан), који су инхибитори ацетилхолинестеразе. Инхибиција овог ензима узрокује неконтролисано повишење нивоа неуротрансмитера ацетилхолина, мишићну парализу и затим смрт. Неуротоксичност такође може да буде последица инхибиције рецептора; на пример, атропин из велебиља (Atropa belladonna) који функционише као конкурентни антагонист мускариничких ацетилхолинских рецептора.[104]
Иако су многи природни токсини секундарни метаболити, ови отрови обухватају и многе пептиде и протеине. Пример токсичног пептида је алфа-аманитин,[105] који се налази у сродним врстама печурке зелена пупавка. У питању је потентан ензимски инхибитор. У овом случају долази до спречавања ензима РНК полимераза II да транскрибује ДНК.[106] Токсин из алги микроцистин је такође пептид. Он инхибира протеинске фосфатазе.[107] Овај токсин може да контаминира залихе воде након цветања алги; познати је карциноген који узрокује акутно крварење јетре и смрт при већим дозама.[108]
Протеини могу да буду буду природни отрови или антинутријенти, као што су трипсински инхибитори (описани изнад), који су присутни у неким махунама, као што је приказано на левој слици изнад. Мање заступљена класа токсина су токсични ензими: они делују као иреверзибилни инхибитори својих циљних ензима и хемијски модификују супстратне ензиме. Пример оваквог ензима је рицин, екстремно потентан протеински токсин присутан у биљци Ricinus communis.[109][110][111] Овај ензим је гликозидаза[112][113] која инактивира рибозоме. Пошто је рицин каталитички иреверзибилан инхибитор, могућ је сценарио где само један молекул рицина може да убије ћелију.[114]
Метални комплекси као инхибитори ензима[уреди | уреди извор]
Један од приступа откривању лекова се састоји од испитивања потенцијалних терапеутских комплекса за биолошку активност, те накнадног бављења питањем механизма. За многе лекове, начин деловања још увек није јасан, чак ни након много година клиничке употребе. У последњих неколико година, велики напредак у расветљавању молекуларних структура омогућио је прецизно одређивање интеракција између протеина и терапијских средства. Овим је појашњен механизам многих агенаса и омогућено је информисано предвиђање потенцијалних места везивања лека. Идентификација тачне природе интеракција лека је кључна за контролисање његове специфичности, а тиме и за смањење нежељених дејстава (нуспојава).[115]
Детаљне структурне информације се могу користити за дизајнирање молекула који се везују за специфичне циљеве, а већина ових напора је усмерена на ензиме. Супстратна специфичност ензима која омогућава препознавање појединачних молекула, пружа могућност конструисања лекова са добро дефинисаним понашањем.[116] Сматра се да су ензими природне мета неорганских лекова,[117] пошто метали имају кључне структурне улоге у многим ензимима, на пример у цинковим металоензимима.[118][119] Пертурбације ендогеног метала који је од виталног значаја за ензимско дејство могу да доведу до инактивације ензима. Ови поремећаји могу да буду изазвани утицајима као што је координација егзогених лиганада за металом, супституција метала, или уклањање метала. Неоргански комплекси такође могу да утичу на ензиме који нису металоензими. Метали се могу координирати са остацима активног места и тиме блокирати супстратну интеракцију, или се могу координирати са остацима изван активног места и тиме утицати на структурни интегритет. Иако је листа инхибитора ензима који се користе као терапеутски агенси у великој мери попуњена органским молекулима, ти агенси међуделују са циљевима путем слабих веза као што су водоничне везе и Ван дер Валсови контакти. То потенцијално може да доведе до нуспојава услед кратког интервала задржавања лекова у активном месту мета, те су могуће неспецифичне интеракције са молекулима који нису жељена мета. Координациона способност метала може да произведе јаче интеракције, као што су ковалентне и јонске везе.
Примена на нормалну и абнормалну физиологију[уреди | уреди извор]
Канцер[уреди | уреди извор]
Један од најзначајнијих успеха неорганских лекова је била ефикасност комплекса платине против рака тестиса.[120][121] Тај напредак је подстакао талас истраживања с циљем идентификације нових неорганских агенаса за употребу у хемотерапији, који би имали побољшану специфичност и мање изражене токсичне нуспојаве. Механизам антинеопластичног дејства цисплатина и његових деривата је идентификован као директна интеракција са ДНК, мада бројни извештаји сугеришу да платина исто тако има ензимске мете.[122] Инхибиција РНК полимеразе,[123] ДНК полимеразе (могућег ометања функционисања цинковог прста),[124] илеалне моноаминске оксидазе (што је везано за споредне ефекте хемотерапије: мучнину и повраћање),[125] ЦТП синтазе,[126] аденилат циклазе (у вези са степеном ототоксичности хемотерапије)[127][128] и других респираторних ензима,[129] били су уочени. Преинкубација пречишћеног ензима са комплексима платине показала је да долази до директне интеракције између њих, али је у многим случајевима везивање платине за циљни ензим такође допринело инхибицији. Инхибиција ензима може да допринесе неким од нежељених токсичних ефеката лекова на бази платине; боље разумевање интеракција са тим комплексима је потребно да бе се умањиле нежељене последице хемотерапије.
Платински лекови су један од примера у коме је примећен терапеутски ефекат лека пре него што је откривен механизам дејства. Алтернативни приступ је дизајн лека са одређеном метом на уму. Тражени су специфични циљеви који играју кључне улоге у метаболизму ћелија рака, који су јединствени за ћелије канцера или су различито изражени у ћелијама рака. Рибонуклеотидна редуктаза је један такав молекул који се показао као обећавајућа мета за терапију рака.
Рибонуклеотидна редуктаза обавља кључни корак који ограничава брзину синтезе ДНК путем контроле производње четири дезоксирибонуклеотидна грађевна блока. Овај ензим редукује 2' угљеник рибозе на дифосфатном нивоу.[130] Ензим се састоји од две димерне подјединице (зване M1 и M2 у старијим извештајима, или R1 и R2 у скоријим публикацијама), које су кодиране са два различита гена под засебном регулаторном контролом. Активност самог ензима је зависна од комплексне алостерне регулације различитим нуклеотидима. R1 садржи места везивања супстрата и регулаторних ефектора, док R2 садржи она бинуклеарних, нехемни центар гвожђа и слободног тирозинског радикала, који су неопходни за функционисање ензима. Рибонуклеотидна редуктаза контролише равнотежу дезоксирибонуклеотиде доступности, а промене њене активности могу да промене спонтану мутациону брзину ћелија.[130] Повећана активност рибонуклеотидне редутазе доводи се у везу са стањима болести, укључујући рак;[130][131] инхибиција овог ензима је атрактивна мета за терапију рака.
Известан напредак је направљен у коришћењу галијум нитрата у инхибицији рибонуклеотидне редуктазе.[132][133][134] Галијум има сличан јонски радијус као и гвожђе и сматра се да омета доступност гвожђа у R2 подјединици. Инхибиторни ефекат галијума се повећава када се испоручује у комплексу са есенцијалним молекулом транспорта гвожђа, трансферином. Ћелијске студије показују да третман са трансферин-галијумом (Tf-Ga) блокира ћелијску апсорпцију 59Fe и инхибира пролиферацију.[133] Умањена активност рибонуклеотидне редуктазе огледа се у инхибицији ESR сигнала из тирозинског слободног радикала на R2 подјединицу рибонуклеотидне редуктазе. Ови ефекти могу бити преокренути излагањем фероамонијум сулфату, што указује да инхибиција утиче на процес зависан од гвожђа. Ови резултати не искључују ефекте на другим путевима зависним од гвожђа, што такође може да утиче на пролиферацију ћелија. Студије у систему без ћелија у којима се директно тестира активност ензима показују да галијум инхибира активност ензима; аутори претпостављају да галијум формира галијум-CDP, или галијум-ADP комплексе, чиме компетитивно инхибира интеракцију супстрата са ензимом.[134] Ни једна од ових студија не даје одговор на питање да ли се галијум може заменити гвожђем у R2 подјединици и да ли је тако супституисани ензим и даље активан. Галијум такође синергистички делује са бројним другим инхибиторима рибонуклеотидне редуктазе на онемогућавању ћелијске пролиферације. Његово дејство је антагонистичко у односу на друге инхибиторе рибонуклеотидне редуктазе.[132] Ове опсервације имају значајне последице за комбиновану терапију, мада прецизан механизам синергизма није познат.
Други јони су такође истраживани у погледу утицаја на рибонуклеотидне редуктазе. Познато је да гвожђе, бакар и цинк утичу на раст ћелија и регулишу компоненте циклуса транспорта гвожђа. Студије о утицају тих јона на рибонуклеотидну редуктазу у свеже изолованим нормалним и леукемијским људским лимфоцитима показале су да цинк инхибира ензим у оба типа ћелија, док Fe и Cu имају стимулативне ефекте.[130][131] Ови резултати могу имати импликације за модулацију ефеката инхибитора рибонуклеотидне редуктазе траговима метала.
| Примене на третман канцераа | |||
|---|---|---|---|
| Комплекс | Метал | Ензим | |
| трансферин-Ga | јони Ga | рибонуклеотидна редуктаза[133][134] | |
| карботиоамид | Fe, Cu | рибонуклеотидна редуктаза[135][136] | |
| тиосемикарбазони | Cu | рибонуклеотидна редуктаза, РНК- -зависне ДНК полимеразе[137] | |
| јони | Zn | рибонуклеотидна редуктаза[131] | |
| јони | Ga | рибонуклеотидна редуктаза[132] | |
| антрациклин, јони | Cu | протеинска киназа C[138] | |
| селеноцистеин/глутатион | Se | протеинска киназа C[139][140] | |
| металоцени | Mo, V | протеинска киназа C, топоизомераза II[141] | |
| бипиридински фенантролин | Pt, Pd | РНК полимераза[123] | |
| стрептонигрин | Fe, Cu, Pd, Cd, Zn | топоизомераза III, реверзна транскриптаза (путем формирања слободних радикала)[142] | |
| PtCl2, cis-DDP | Pt | ДНК полимераза[124] | |
| цисплатин, бакар сулфат | Pt, Cu | илеална моноаминска оксидаза[125] | |
| cis-DDP, K2PtCl4 | Pt | CTP синтаза[126] | |
| јони | Zn | каспаза-3[143][144] | |
| разни | Ga | орнитинска декарбоксилаза[145] | |
| cis-DDP, тетраплатин, карбоплатин | Pt | респираторни ензими[128] | |
| цисплатин | Pt | аденилатна циклаза[127] | |
| тетраплатин | Pt | аденилатна циклаза[128] | |
| ванадат, пероксованадијум | V | протеинске тирозинске фосфатазе[146][147] | |
| јон | Zn | Ser/Thr фосфопротеинска фосфатаза[148] | |
| метални хелатор | Cd | матрилизин[149] | |
а Напомена: У овој и наредним табелама оксидационо стање металног јона није приказано ради јасноће. Додатне информације су дате у тексту.
| |||
За металне комплексе карботиоамида[135][136][150] и тиосемикарбазона[137] је утврђено да инхибирају рибонуклеотидну редуктазу и имају антиканцерогено дејство. Утврђено је да метални комплекси α-(N)-хетероцикличних карбоксиалдехидних тиосемикарбазона (α-HCAT) инхибирају раст ћелија у већој мери него слободни лиганд.[136] Метални комплекси 2,2'-бипиридил-6-карботиоамида (BPYTA), који су структурно и функционално слични α-HCAT, не показују тако јасно дејство. Студије гвожђа и бакра у комплексу са BPYTA су показале да BPYTA има већи афинитет за бакар; бакарни комплекс показује израженије антитуморско дејство од слободног лиганда или комплекса гвожђа. Студије са слободним лигандом међутим нису јасне, јер је вероватно да лиганд формира комплексе са расположивим металним јонима у раствору. Сматра се да дозиметрија BPYTA комплекса може да утиче на учинак. На пример, бакарни комплекс има најјачи антипролиферативни ефекат на култивисаним мишјим леукемијским ћелијама након пулсног контакта, док је у случају континуираног контакта мање активан од слободног лиганда. Осим тога, изгледа да различити метални комплекси делују различитим механизмима. Док се антипролиферативни ефекат комплекса гвожђа може објаснити инхибицијом рибонуклеотидне редуктазе и верује се да заправо уништава R2 подјединицу, постоје индикације да комплекс бакра такође делује на друге циљеве.[150][151] Потврђено је да BPYTA синергистички делује са инхибитором рибонуклеотидне редуктазе хидроксиурејом (HU), што сугерише могућност комбиноване терапије.
Још једна ензимска мета за агенсе против канцера је протеинска киназа C (PKC). PKC је фамилија серин/треонинских киназа које се активирају секундарним гласницима попут Ca2+ и продуктима фосфолипидне хидролизе (из каскаде инозитол трифосфата). Девет различитих чланова ове породице је до сада окарактерисано и они учествују у различитим ћелијским активностима, укључујући трансдукцију сигнала, раст ћелија/диференцијацију и хормонску секрецију.[138] Они су такође познати као рецептори форболних естара (познатих хемијских активатора), а активирају се и у одговору на оксидативне промотере тумора.[139] Инхибиција PKC је од интереса као начин спречавања формирања тумора. Недавни докази указују на то да је PKC регулаторни домен, који има два хомологна региона са шест очуваних цистеина и два конзервисана хистидина, те садржи непремошћена Zn2+ места.[152] Противтуморска средства која делују на PKC обухватају антрациклине, чије је дејство посредовано координацијом с прелазним металима. Једна студија на пречишћеном PKC је показала да антрациклин-Cu(II) комплекс ефикасније инхибира PKC него појединачне компоненте и да је тај ефекат посредован директном интеракцијом између Cu(II) и PKC (овај закључак је изведен из EPR студија).[138] Исто тако је показано да антрациклини имају различите ефекте на ДНК топоизомерази II,[153] мада још увек нема извештаја о дејству комплекса прелазних метала са антрациклинима у овом виду примене.
Поједина једињења селенијума имају инхибиторни ефекат на PKC, а такође имају канцерпревентивно дејство.[139][140] Резултати истраживања сугеришу да та једињења инактивирају PKC путем редокс механизма, реагујући са цистеинима унутар PKC каталитичког домена.[139] У једној студији је показано да једињења селенијума инхибирају PKC, док на друге тестиране протеинске киназе немају утицаја (на фосфорилазну киназу и протеинску фосфатазу 2А). Међутим, постоји могућност да ова једињења реагују са другим протеинима који садрже кластере цистеина.
Металоцени су класа антитуморних агенаса који не садрже платину и који делују на различит начин од лекова базираних на платини.[154][141] Поједини металоцени се везују за терминалне фосфате и/или базе нуклеотида, док други не међуделују са нуклеотидима.[141][155][156] Из тог разлога је предложен низ алтернативних циљева. Показано је да V(IV) и Mo(IV) једињења инхибирају PKC и топоизомеразу II.[141] Једињења ниобијума (Nb) не везују се за нуклеотиде или аминокиселине.[155] Механизам дејства ове класе захтева даља истраживања.
Једињења ванадијума, која су најбоље позната као инсулински миметици, исто тако испољавају антиканцерне ефекте. Ова једињења, конкретно комплекси ванадата и пероксованадијума, компетитивни су инхибитори протеинске тирозинске фосфатазе (PTP). Ванадати делују као аналози прелазног стања реверзибилним везивањем за тиолну групу у каталитичком домену, док пероксованадијумски комплекси оксидују критичне цистеинске остатке у каталитичком домену.[146] У серин/треонинским фосфатазама, ванадати се везују за хидроксилну групу у активном месту, док су пероксованадијумски комплекси неактивни у одсуству цистеина. Пероксованадијумски комплекси могу да блокирају ћелијски циклус у фази G2-M транзиције (G2 = фаза раста 2, препараторна фази митозе; M = митоза, период активне ћелијске поделе); сматра се да је то узроковано инхибицијом PTP, чије функционисање је есенцијално за прогресију митозе.[146][147] Могуће је да је ова блокада повезана са њиховим цитотоксичним дејством. Серин/треонинске фосфатазе су такође инхибиране бројним јонима прелазих метала д-блока, међу којима су најефективнији Zn2+, Hg2+, Cu2+, Yb2+ и Sc2+ (μM Ki).[148]
Бројне друге ензимске мете за антиканцерне агенсе такође су истраживане. Орнитинска декарбоксилаза, која се може индуковати форболним естрима и која учествује у ћелијској трансформацији, може се инхибирати једињењима галијума.[145] Трансформација је повезана са ћелијском транзицијом у канцерозно стање. Та једињења инхибирају раст тумора и сматра се да исто тако делују на рибонуклеотидне редуктазе. Матричне металопротеиназе учествују у ремоделовању екстрацелуларне матрице, што је кључно за инвазију тумора и метастазу у ткивима. Људска матрична металопротеиназа матрилизин је ензим цинка за који је показано да се инактивира у раствору кадмијума, који формира неактивни Cd/Zn хибрид.[149] Матрилизин се исто тако може инхибирати агенсима металног везивања, као што је 1,10-фенантролин, који формира ензим-хелат-метал комплекс уз накнадно уклањање каталитичког јона цинка.[149]
Апоптоза, која је постала проминентно поље истраживања последњих година, процес је „програмиране” ћелијске смрти. Постоји корелација између дефеката апоптозних процеса и бројних болести, укључујући канцер. Познато је да Zn2+ спречава апоптозу и показано је да до тога долази путем инхибирања каспазе-3, апоптотичке протеазе која учествује у протеолизи поли(ADP-рибоза) полимеразе (PARP).[143][144] Конфликтни извештаји не узимају у обзир инхибиторно дејство цинка на каспазу-3.[157] Сматра се да су несугласице последица разлика у експерименталним условима: инхибиција уочена у случају пречишћеног рекомбинантног протеина али не и код протеина у присуству E. coli лизата, сугеришу постајање фактора у лизату који ометају дејство цинка.
Постоје бројни агенси који делују путем инхибиције ензима који делују на ДНК. Ова инхибиција је често последица везивања за место којим ензим формира интеракције са ДНК и није резултат директне инактивације ензима.[153][158][159][160]
Имајући у виду природу интеракција ензима и супстрата, избор ензима као циљева антиканцерних лекова омогућава изузетно специфично препознавање циљева. Развој софистициранијих техника моделовања и доступност детаљнијих информација о структурама ензима довели су до ригорозне карактеризације интеракција лека и ензима, те разјашњавања механизма дејства. Већина публикација у литератури о канцеру се бави инхибицијом специфичних ензима, повремено оних који учествују у метаболичким процесима. У тим истраживањима се користе пречишћени ензими или тестови којима се испитују појединачни ензими од значаја. Док је круцијално да се одреде инхибиторне особине на циљном молекулу, исто тако је неопходно да се демонстрира да једињење није активно на другим ензимима. Овај тип студија је тегобан пошто се може тестирати само релативно мали број репрезентативних ензима, па се лако може пропустити ензим који негира специфичност. Пажљивим разматрањем места деловања лека може да се омогући извођење релативно добрих прогноза о могућим интеракцијама са другим ензимима. Додатни изазов је да су ензимске мете често присутне и у нормалним ћелијама. Дизајн ефективних антиканцерних агенаса је компликован процес који не обухвата само инхерентна инхибиторна својства лека, него и његову испоруку, дозиметрију и време задржавања ин виво. Метални комплекси превазилазе неке од ових изазова формирањем јаких ковалентних веза са циљним ензимима.
Примене везане за хем[уреди | уреди извор]
- Хипербилирубинемија
| Хипербилирубинемија | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| јони | Sn | цитохром P-450, ω-хидролаза[161] | |
| протопорфирин (PP) | Sn, Zn | 11β-хидроксилаза, 21R-хидроксилаза, цитохром P-450, хем оксигеназа[162][163][164] | |
| мезопорфирин (MP) | Sn | хем оксигеназа (танко црево)[165] | |
| деутеропорфирин 2,4-бисгликол (BG) | Zn | хем оксигеназа (пацов)[166] | |
| MP | Zn | хем оксигеназа (пацов)[167] | |
| MP | Co | хем оксигеназа слезине (мождане мембране пацова)[168] | |
| PP, BG, MP | Cr | хем оксигеназа (пацов)[169] | |
| разни порфирини | Zn, Sn, Cu | γ-аминолевулинатна синтаза (ћелије јетре кокошјег ембриона), хем оксигеназа 56 | |
| разни порфирини | Zn, Sn, Cr, Mg | хем оксигеназа (епител танког црева)[170] | |
| мезопорфирин | Sn | клиничка супресија хипербилирубинемије[171][172] | |

Хипербилирубинемија је обољење које узрокује прекомерну акумулацију билирубина у крви и ткивима.[173] Билирубин је продукт катаболизма хема, при чему се хем деградира посредством хем оксигеназе (HO) и формира се биливердин, који се затим редукује помоћу биливердин редуктазе до билирубина.[174] Након конјугације са глукуронском киселином, помоћу ензима билирубин глукуронид трансфераза, и формирања растворљивијег конјугата, билирубин се излучује. Прекомерно разлагање хема и недовољна активност трансферазе могу да доведу до акумулације билирубина. Ово накупљање је познато као неонатална жутица код беба са недовољно развијеном јетром и превремено рођене деце, која брзо разграђују хем (при прелазу са феталног на регуларни хемоглобин) али им недостају адекватне трансферазе. Хипербилирубинемија се такође јавља код генетичког Криглер—Најаровог синдрома, где долази до комплетног одсуства трансферазног дејства у јетри[171] и других болести као што су таласемија и конгениталне анемије.[174] Инхибиција разлагања хема у хем оксигеназном кораку је могући начин спречавања хипербилирубинемије.
Металопорфирини су екстензивно изучавани и добро познати инхибитори хем оксигеназе. Ови инхибитори се везују за каталитичко место, али нису ефективни супстрати. Знатан број металопорфирина има инхибиторно дејство, а има и оних који индукују хем оксигеназу. Најзначајнији инхибитори хем оксигеназе су калајни и цинкови порфирини. Неки од ових порфирина су нашли клиничку примену у сузбијању продукције билирубина.[171][172] Недавна истраживања су разјаснила природу инхибиције, утицај на друге биохемијске путеве, као и опсег биодистрибуције лекова.
Студије цинкових и калајних протопорфирина индицирају да је калајни протопорфирин (Sn-PP) исто тако ефективан инхибитор адреналне стероидогенезе, док цинков протопорфирин (Zn-PP) нема утицаја на тај пут.[162][163] Синтеза стероида је посредована бројним хемопротеинима, цитохромима P-450, те постоји комплексна међузависност између пута синтезе хема и стероидогенезе. Концентрација цитохрома је везана за промене у синтези и деградацији хема. У тестовима, користећи моделе на пацовима, утврђено је да Sn-PP знатно редукује активност стероидних биосинтетичких ензима митохондријске 11β-хидроксилазе и микрозомалне 21R-хидроксилазе; такође је уочено смањење садржаја микрозомалног цитохрома P-450.[162][163] У поменутој студији је исто тако запажено драстично смањење садржаја HO-2, неиндуцибилног изозима хем оксигеназе који је далеко превалентнији од индуцибилног HO-1, те се претпоставља да Sn-PP заправо уништава HO-2 уместо да га инхибира. Zn-PP, насупрот овога, инхибира активност HO али нема утицаја на ензиме стероидне биосинтезе.[162][163]
Даља истраживање поређењем дејства Zn-PP и Sn-PP са HO-1 и HO-2 показала су да су оба једнако инхибиторна за HO-1 без утицаја на интегритет протеина (што је утврђено вестерн блот анализом), као и да индукују повишење нивоа HO-1 транскрипије. Међутим, Sn-PP и Zn-PP се разликују у погледу своје активности спрам HO-2.[164] Мада оба инхибирају HO-2, разликују се у степену инхибиције. Степен инхибиције Zn-PP је исти за обе форме HO, док Sn-PP испољава знатнију инхибицију HO-2 него HO-1. Сматра се да Sn-PP поремећује интегритет HO-2 протеина (вестерн блот), док Zn-PP нема тај ефекат. Механизам који узрокује разлике активности Sn-PP и Zn-PP на HO формама није познат.
Утврђено је да разни порфирини инхибирају интестиналну хем оксигеназу и умањују преузимање гвожђа из црева, доводећи до повећаног излучивања овог метала. То може да буде корисно у третману случајева хемохроматозе.[170][165] Овај ефекат је уочен код свих парентерално администрираних порфирина, али су само Sn-MP, Sn-PP и Cr-MP били орално ефективни (на интестиналној HO; нису нађени на реналним, сплинским или хепатичим ткивима). Показано је да је Zn-MP ефективан у третману акутне порфирије (поремећаја изазваног дефицијенцијом хема), а студије дистрибуције у ткиву су показале да брзо бива уклоњен из плазме и да се првенствено задржава у јетри и слезини, где инхибира HO током периода од скоро недељу дана након једне инјекције.[167] Zn-MP не пролази кроз крвно-мождану баријеру, за разлику од Sn-PP за који је показано да штетно утиче на HO-2 интегритет и активност у мозгу пацова.[175] Металопорфирини делују као појачивачи фотосензитивности с варирајућим степенима[176] (они се такође користе у фотодинамичкој терапији). Познато је да Zn-PP у мањој мери подстиче фотосензитивност од Sn-PP, што је још једно својство које сугерише да су цинкове форме инхибитора вероватно подесније за клиничку примену.[166]
Co-MP и Cr-MP такође ефективно инхибирају HO.[168][169] Утврђено је да Co-MP не посредује липидну пероксидацију у можданим мембранама пацова након фотоирадијације (што је показано користећи малондиалдехидни тест); стога, он не подстиче фотосензитивност.[168] Cr-MP ефективно инхибира хепатичку HO након оралне администрације, док на сплинску HO нема утицаја.[169] Показано је да Zn-MP инхибира хепатичку 5-аминолевулинатну синтазу (ALAS), ензим који ограничава брзину пута биосинтезе хема. Овај ефекат се увећава кад се хем дода са порфирином.[177] Познато је да гвожђе и хем повратно регулишу ALAS путем инхибирања mРНК транскрипције/транспорта.[178] Уочено је да је ALAS транслација под контролом елемената респосивних на гвожђе.[179]
Употреба металопорфирина за третман хипербилирубинемије је узнапредовала даље у процесу развоја лекова у односу на антиканцерне агенсе описане у претходном одељку. Ови порфирини имају познат биолошки циљ, хем оксигеназу, те је њихова клиничка ефективност већ показана. Међутим, њихова главна биолошка мета је део комплексног пута, који је у великој мери повезан са другим процесима, као што је стероидна синтеза. Неопходно је праћење тих других процеса да би се спречили нежељени утицаји на њих.
- Трансдукција азот-моноксидног сигнала
| Трансдукција азот-моноксидног сигнала | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| PP | Zn | растворна гуанилатна циклаза (пречишћена)[180] | |
| PP, BG | Zn, Sn | растворна гуанилатна циклаза (пацови)[181] | |
| натријум нитропрусид (SNP) | Fe | азот-моноксид синтаза (неутрофили пацова)[182] | |
| SNP | Fe | NOS (церебрални кортикални синаптозоми)[183] | |
| јони | Cu, Zn, Co, Ni, Fe | NOS (пречишћена)[184] | |
| јон | Zn | NOS (пречишћени nNOS)[185] | |
| SNP | Fe | екто-5'-нуклеотидаза (ренално епителијална)[186] | |
| SNP | Fe | индоламин 2,3-диоксигеназа (мононуклеарни фагоцити)[187] | |
| SNP | Fe | метионин синтаза[188] | |
| SNP | Fe | (Na+/K+)-ATPаза[189] | |
Азот-моноксид (NO) игра улогу гласника у мноштву система. У имунском систему, NO posreduje respons belih krvnih zrnaca na patogene; u kardiovaskularnom sistemu, NO индукује релаксацију ћелија глатких мишића у крвним судовима; и у нервном систему, NO учествује у неуротрансмисији и неуромодулацији.[190][188][191] NO се формира из L-аргинина посредством азот-моноксидне синтазе (NOS), хем протеина који се јавља у више изоформи и за чије дејство је неопходан NADPH као донор електрона. Постоје три NOS изоформе: конститутивне изоформе присутне у мозгу (nNOS, тип I) и ендотелним ћелијама (eNOS, тип III) за чије дејство је неопходан калцијум/калмодулин, и цитокином индуковане форме (iNOS, тип II) за чије дејство није неопходан калцијум али које имају калмодулин као чврсто везану подјединицу.[192] Обе класе се јављају у облику хомодимера при чему свака подјединица садржи 1 еквивалент FAD, FMN, (6R)-5,6,7,8-тетрахидро-L-биоптерина (H4B) и протопорфирин IX хема.[184][193] Постоји дуга листа NOS инхибитора која обухвата селеноорганска једињења (која се везују за тиолне групе), Zn порфирине, те цинк (везује се за хем места).[193] У каскади преноса сигнала, познато је да NO стимулише гуанилатну циклазу и да индукује акумулацију секундарног гласника, cAMP. Многи аспекти NO сигнализације су испитани студирањем рамификација увођења NO донора у систем или путем NOS инхибирања NOS чиме се обуставља NO продукција.
NO је нашао широку примену као лиганд у гвожђе-хемним комплексима у неорганској хемији, и стога се намеће питање да ли NO може да буде ауторегулисан NOS инхибицијом (хемни је протеин).[192] Студије са NO донором, натријум нитропрусидом (SNP), Na2Fe(CN)5NO•2H2O, показују да NO може да инхибира NOS.[182][182] У студијама са неутрофилима пацова, липополисахарид се користи за индуковање активности NOS и ова индукција се инхибира помоћу SNP.[182] SNP испитивања користећи кортикалне синаптозоме пацова су указала на постојање концентрационо зависне NOS инхибиције NOS активности.[182] У овим студијама се NOS активност одређује праћењем формирања [3H]цитрулина из [3H]аргинина.[194] Познато је да прелазни метали инхибирају NOS,[184] као и да пречишћени Cu2+, Ni2+, Zn2+ и Co2+ делују као инхибитори индуцибилног NOS ензима, док нехемно гвожђе повећава каталитичку активност. За Cu2+ јон је утврђено да инхибира пречишћени неуронални NOS (други метали нису тестирани на nNOS). Из ових налаза произилази да нехемно гвожђе NOS ензима учествује у катализи, те да NOS вероватно садржи активно место за нехемно гвожђе/H4B.
Zn2+ реверзибилно инхибира активност nNOS (Ki = 30 μM).[185] Уочена је инхибиција NADPH-зависне редукције гвожђа хема и од калмодулина (CaM)-зависна редукција цитохрома c. Није уочена инхибиција CaM-независне редуктазе цитохром c редуктазе (мерено релативним бројем каталитичких циклуса цитохрома c). Међутим, чак и у одсуству Zn2+, CaM-независни пут има више него десет пута слабију активност од CaM-зависног пута. nNOS спектри разлика типа II демонстрирају смањење количине високоспинског гвожђа хема у присуству Zn2+. На основу ових резултата, закључено је да до инактивације ензима долази услед везивања Zn2+ за сулфхидриле у близини хем лиганда и накнадног поремећаја окружења око гвожђа хема.
SNP и NO продукција доприносе инхибицији низа других ензима. Индоламин 2,3-диоксигеназа (IDO) ензим је који садржи хем и који је део интерфероном γ (IFNγ) индукованог респонса мононуклеарних фагоцита на патогене.[187] IDO је ензим који ограничава брзину у путу деградације триптофана. Исцрпљивање триптофана, најмање доступне есенцијалне аминокиселине, може да допринесе антипатогеној активности мононуклеарних фагоцита. У студијама на изолованим IFNγ-третираним људским периферним крвним мононуклеарним ћелијама и из моноцита изведеним макрофагама, уочено је да SNP инхибира IDO активност.[187] Такође је показано да се IDO може инхибирати дејством Zn-MP.[195] Други ензими које инхибира SNP обухватају метионинску синтазу у хепатоцитима пацова,[188] (Na+/K+)-ATPазе[189] и екто-5'-нуклеотидазе у реналним епителијалним ћелијама.[186] Метионинска синтаза се састоји од метилкобаламина као кофактора, деривата витамина Б-12 који је у знатној мери сличан хемоглобину, а до инхибиције може доћи путем формирања NO-кобаламинског комплекса. Сматра се да до инхибиције екто ензима долази путем S-нитрозилације. Механизам инхибиције (N+/К+)-ATPазе није познат.
Постоје индикације да је угљен-моноксид (CO) физиолошки регулатор, који делује на сличан начин као и NO, укључујући способност стимулације гуанилил циклазе. CO се формира посредством HO, при конверзији хема до биливердина и CO. Многе студије улоге CO су извршене користећи HO инхибиторе, као што су Zn-PP и Sn-PP, да би се показало да супресија HO (и стога CO продукције) инхибира гуанилил циклазу. Међутим, недавне студије су показале да сами металопорфирини инхибирају гуанилил циклазу, те стога студије које користе те комплексе за испитивање утицаја CO вероватно треба преиспитати.[180][181] У другим студијама су коришћени порфирини за испитивање улоге CO у просторном учењу и дугорочној потенцијацији у хипокампусу.[196][197] Порфирини су коришћени под претпоставком да они искључиво делују као супресори CO продукције посредством HO; међутим, имајући у виду да је дејство порфирина вишестрано, тешко је претпоставити улогу CO искључиво на бази тих експеримената. Ове студије демонстрирају неке од проблема са којима се истраживачи суочавају кад специфичност инхибитора није апсолутна и илуструју неке од компликујућих фактора у анализи података кад се користе „индиректни” ефектори (нпр. инхибирање ензима који формира CO, уместо директног уклањања CO).
Хипертензивне примене[уреди | уреди извор]
| Хипертензивне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| сулфонамид | Cu | карбонатна анхидраза[198] | |
| хетероциклични сулфонамиди | Zn, Cu | карбонатна анхидраза[199] | |
| хетероциклични меркаптани, сулфенамиди, сулфонамиди | Zn, Cu | карбонатна анхидраза[200] | |
| разни сулфонамиди | Ge, Sb | карбонатна анхидраза[201] | |
| хлоротиазид | Hg, Pb | карбонатна анхидраза[202] | |
| каптоприл | Zn | ангиотензин конвертујући ензим[203] | |
| лисиноприл | Cu | ангиотензин конвертујући ензим[204] | |
Системи везани за хем који су разматрани у претходном одељку блиско су повезани са хипертензивним применама. Натријум нитропрусид је у широкој употреби као хипотензивни агенс,[188][205] а хем оксигеназа је имплицирана у одржавање крвног притиска.[161] Утврђено је да SnCl2 индукује HO-1 транскрипцију и стога инхибира дејство цитохром P450-арахидонска киселина ω/ω-1 хидроксилазе, што доводи до смањеног формирања ö/ö-1 хидроксилазних метаболита и нижег крвног притиска.[161] Хидроксилаза је хемни протеин чији су нивои контролисани доступношћу хема. Кад се индукује хем оксигеназа исцрпи се доступни хем; томе следи опадање нивоа ензима, а тиме и количине ензимских метаболита. Метаболити, односно 19[S]-хидроксиеикозатетраеноинска киселина (HETE) и 20-HETE, делују као прохипертензиви јер стимулишу Na+/K+-ATPазу и констрикцију крвних судова.
Још један од примарних ензимских циљева за хипертензију је карбонатна анхидраза (CAs). Она катализује хидрацију CO2 до бикарбоната и учествује у широком опсегу биолошких процеса, укључујући pH хомеостазу, продукцију окуларних и цереброваскуларних флуида, те секрецију електролита. У очима, на пример, карбонатна анхидраза игра критичну улогу у одржавању интраокуларног притиска. Познато је седам изоензима карбонатне анхидразе и неколико сродних протеина. Ови изоензими су присутни у цитосолу (CA I, II, III и VII), везани за ћелијске мембране (CA IV), у митохондријама (CA V) и у секреторној форми у пљувачки (CA VI).[206][207] Они имају различите улоге и веома различиту ткивну дистрибуцију, кинетичка својства и осетљивост на инхибиторе. CA ензими су металоензими, а многи инхибитори тих ензима су метал комплексирајући анјони који се директно координирају са цинком у активном месту ензима.
Карбонатне анхидразе, изузев CA III, такође инхибирају сулфонамиди који се везују за цинк путем супституције каталитички важног молекула воде.[200] Сулфонамиди су коришћени за третман глаукома дуги низ година јер снижавају интраокуларни притисак (IOP). Прецизни механизам снижавања притиска није познат, али се сматра да до тога долази услед редукције концентрације бикарбоната у постериорној комори ока, те да пратеће премештање бикарбонатних јона доводи до кретања флуида и смањења концентрације натријума.[208] Метални комплекси сулфонамида такође потентно инхибирају карбонатне анхидразе. Zn(II), Cu(II), Ni(II), Co(II), Fe(III) и Al-(III) комплекси адамантил сулфонамидних деривата имају инхибиторно дејство на три CA изозима (hCA I, hCA II и bCA IV) са nM Ki вредностима.[199] Zn(II) и Cu(II) комплекси, најјачи инхибитори у серији, топикално су били примењивани на зечји модел ока и утврђено је да снижавају IOP. Топикално примењени сулфонамид не снижава IOP, из чега следи да присуство металних јона критично мења својства инхибитора. Претпоставља се да метал мења растворљивост комплекса, чиме се повећава доступност лека. Hg(II) комплекси хлоротиазида, диуретика који се користи као антихипертензив, исто тако показују јаку инхибицију CA[202] као и Ge(IV) и Sb(III) комплекси арилсулфониламида[201] и Cu(II) комплекси ацетазоламидних деривата.[198] За металне комплексе се сматра да делују на CA на два начина: 1. инхибицијом са слободним сулфонамидом и 2. интеракцијом металних јона са хистидином у активном месту.[198]
Велики део литературе о хипертензивним агенсима је посвећен инхибиторима ангиотензин-конвертујућег ензима (ACE), компоненти ренин-ангиотензин система. Ренин-ангиотензин систем учествује у одржавању крвног притиска. ACE катализује конверзију ангиотензина I до ангиотензина II, вазоконстриктора који учествује у хипертензији. Ангиотензин I се формира конверзијом јетреног продукта посредством ренина, ензима који излучују бубрези.[209][210] Постоје рецепторска места на многим органима за ангиотензин II. Тај систем може да буде блокиран на више нивоа, познати β-блокатори блокирају отпуштање ренина, аналози ренин-супстрата и ренински инхибитори блокирају ренин, ангиотензин II рецепторе блокира саларзин, а ACE инхибитори блокирају ACE. Већина поменутих једињења не садржи метале, мада неки ACE инхибитори формирају металне комплексие ин виво. На пример, каптоприл је дизајниран да се надмеће са ангиотензином за јоне цинка у ензиму и да везује цинк путем тиолне групе.[203] Лисиноприл, још један ACE инхибитор, везује цинк путем аминокарбоксилатне гурпе.[204] Лисиноприл се конјугује са Rh(III) и Pd(II) (иминофосфорано)фосфинима, а конјугати имају нешто већу инхибиторну активност од родитељског једињења (долази до 18-струког смањења вредности IC50, наномоларни опсег).[211] Ова дериватизација у виду синтезе 105Rh и 109Pd радио-обележених једињења омогућава ин виво праћење дистрибуције лека.
Третмани за хипертензију су обично дугорочни и стога је стабилност интеракција коју пружа ковалентно везивање металних комплекса привлачна опција. Највећи део литературе у овој области се бави органским једињењима; међутим, знатан број тих једињења је зависан од интеракције са металима за испољавање свог дејства.
Серинскопротеазне примене[уреди | уреди извор]
| Серинскопротеазне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| аминокиселинске и пептидне лигације | Co | α-химотрипсин[212][213] | |
| Шифова база | Co | тромбин, термолизин[214][215][216] | |
| разне боронске киселине | B | трипсин[217] | |
| пептид | B | α-литичка протеаза[218] | |
| фенилборонска киселина | B | α-химотрипсин[219] | |
| трипептид | B | трипсин, α-литичка протеаза, трипсину сличне протеазе[220] | |
| BABIM | Zn | серинске протеазе[221][222][223][224] | |
| титанил сулфати | Ti | трипсин[225] | |
Серинске протеазе обухватају главну фамилију протеолитичких ензима са разноврсним опсегом функција. Серинске протеазе играју кључне улоге у каскади коагулације крви, у активацији комплемента, бактеријској патогенези, те фибринолизи.[217] Серинске протеазе су постале проминентни циљеви за дизајн лекова у антивирусним и антибактеријским истраживањима.[225] Велика класа инхибитора серинских протеаза су боронске киселине и пептид-боронске киселине.[157][200][226][227] Сматра се да боронил групе опонашању прелазно стање реакције, док пептидна порција усмерава специфичност на специфичне протеазе.
Серије 15N и 1H студија комплекса протеазних инхибитора дале су увид у интеракције између трипсина или α-литичких протеаза и разних боронскокиселинских инхибитора. У α-литичким протеазама и трипсину, супстратни аналози теже да формирају серинске адукте, док несупстратни аналози обично формирају хистидинске адукте,[217] мада и супстратни аналози могу понекад да формирају хистидинске адукте.[218][228] Даље, 11B NMR студије на хистидинским адуктима α-литичких протеаза и серинских адуката химотрипсина и α-литичких протеаза показале су да је атом бора тетраедралан у хистидинским и серинским адуктима.[218] Из рада са фенилборонском киселином произилази да адиција шећера (D-моносахарида) повећава инхибиторно дејство на α-химотрипсин.[219] Тај закључак је изведен на основу ацидификације атома бора путем самокомплексације са D-моносахаридима. Овај синергистички ефекат је pH зависан и није уочен изнад pH 9,5 (ензимска инхибиција дејством саме борне киселине такође није уочена). До јаке инхибиције ензима долази између pH 4 и pH 9 у присуству фенилборне киселине и фруктозе са највећим шећерно индукованим појачањем инхибиције на приближно неутралном pH. Разни трипептиди боронатних естара такође делују као инхибитори серинске протеазе.[220] Утврђено је да додатни пептидно-метални комплекси делују као серин протеазни инхибитори. Познато је да Co(III)-везане аминокиселине и дипептиди могу да инхибирају химотрипсин и трипсин.[212][213] Ове студије су провођене да би се испитали ефекти пентамин кобалта(III), који се користи као хидрофилна карбоксилна заштитна група у ензиматској пептидној синтези. Раније је примећено да присуство ове групе на аминокиселинама непосредно поред везе која је подложна ензимском дејству блокира каталитичку конверзију. Инхибиција пречишћеног химотрипсина и трипсина лигираним пептидима је компетитивна и реверзибилна. Накнадне студије ове хемијске групе сугеришу да се лигирани пептиди везују за ензим путем Кулонових интеракција.[213] Кобалт(III)-лигирани пептиди разних дужина су тестирани на трипсину, химотрипсину и протеинази K. На основу резултата моделовања химотрипсина, растојање између два негативно наелектрисана Asp остатка (Asp-35 и Asp-64) у S' везујућем и Ser-195 у активном месту одговара дужини инхибитора пептида оптималне дужине. Редослед инхибиционих ефикасности је металопептид > амид > слободни пептид, што се подудара са очекивањима имајући у виду постојање два негативно наелектрисана бочна ланца у месту везивања. У присуству повишених концентрација NaCl, инхибиција металопептидима је мање ефикасна, док се инхибиција слободних пептида побољшава. До промене инхибиције амида не долази. Ови резултати су конзистентни са електростатичким интеракцијама између инхибитора и активног места. Насупрот овоме, трипсин има два позитивно наелектрисана остатка (Lys-60 и Arg-62) у S' везујућем региону и сходно томе инхибиција слободним пептидима је ефективнија од позитивно наелектрисаних металопептида. Опсервације на протеинази K нису конзистентне са обрасцем ефикасности уоченим за друга два ензима, што сугерише да једно позитивно наелектрисање (Arg-218) у S' региону не одређује везивање. Те студије демонстрирају да адиција металног једињења може да промени афинитет везивања супстрата путем електростатичких ефеката.
У студијама комплекса Co(III) Шифове базе и пептидних конјугата тих комплекса показано је да ефективно инхибирају тромбин и термолизин.[214][215][216] Пептидни конјугат селективно инхибира тромбин у смеши са две друге серинске протеазе (Kи = μM). Селективност проистиче из интеракције пептидне компоненте, док је сама инхибиција последица кобалт(III) координације са хистидинима активног места. Алтернативно, кобалт се може координирати са хистидинима у близини али не и у самом активном месту, чиме се пептид закључава у месту везивања супстрата. Такође, показано је да ови комплекси имају способност везивања хистидина у модел систему пептида из цинковог прста HIV нуклеокапсидног протеина.[229] У овим студијама је помоћу 1H NMR спектроскопије демонстрирана директна интеракција између кобалтних комплекса и хистидина у цинковом прсту, што доводи до ремећења структуре цинковог прста. Из поменутих студија проистиче да ови комплекси могу да инхибирају цинкове металопротеазе.
Након што је класа инхибитора цинк-посредованих серинских протеаза окарактерисана,[221][222][223][224] у кристалографским студијама на трипсину је уочено да се ти инхибитори тетраедрално координирају са егзогеним јоном цинка између два хелирајућа атома азота инхибитора и два остатка активног места (His57 и Ser195).[222] Присуство цинка појачава инхибицију за скоро три реда величине, и у случају појединих инхибитора производи селективност. Ова класа инхибитора представља јединствен приступ у којем сам инхибитор није метални комплекс али је присуство прелазног метала од кључног значаја за инхибицију.
Серинске протеазе су имплициране у процесе бројних болести, а инхибиција ових ензима активно је поље изучавања.[222][224] Присуство хистидина у активном месту и афинитет јаких киселина за азот чини инхибицију серинских протеаза помоћу металних комплекса логичним избором. Нов приступ дизајну инхибитора, као што је описано изнад, везује органска једињења за активна места путем цинковог јона као „моста” (граничне Луисове киселине), што сугерише да цинк можда делује као регулаторни елемент. Ови мали молекули представљају потенцијални оквир за конструисање бројних других инхибитора, где инхибиторна порција молекула остаје непромењена, док се остатак молекула може прилагођавати да би се променила специфичност.
Неуролошке примене[уреди | уреди извор]
| Неуролошке примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| јон | Li | аденилатна циклаза, триптофанска хидроксилаза, Ca2+-ATPаза[230] | |
| јон | Al | серинске протеазе, α-химотрипсин[231] | |
| јон | Al | моноаминооксидаза А[232] | |
| јон | Al | калпаин[233] | |
| јон | Al | калпаин, хексокиназа, глукоза-6-фосфат дехидрогеназа[234] | |
| порфирини | Fe, Zn | ацетилхолинестераза[235] | |
| порфирини | Cr, Zn | хем оксигеназа, азот-моноксид синтаза[196] | |
| протопорфирин | Sn | хем оксигеназа[197] | |
| цисплатин, цоппер сулфате | Pt, Cu | моноаминооксидаза[125] | |
| јон | Cu, Cd, Pb, Mg, Zn | лизозомна, цитопласмична протеиназа, калпаин I и II[236] | |
| јон | Zn | матричне металопротеиназе, секретазе, цитохром c оксидаза, азот-моноксидна синтаза, ендонуклеаза[237] | |
Једна од најбоље познатих области примене металних инхибитора у неурологији је употреба литијума као третмана за биполарни поремећај (манично-депресивну болест). Литијумска терапија је уведена 1949. године, али прецизни механизам њеног терапеутског дејства није био познат. Последњих година су објављени извештаји који индицирају да литијум утиче на путеве инозитол фосфолипидне хидролизе (мада није јасно да ли је то услед инхибиције инозитол-1-фосфатазе) и да инхибира аденилатну циклазу.[230]
Улога алуминијума у Алцхајмеровој болести и детаљни механизам његовог учешћа у развоју болести нису потпуно разјашњени. Повезаност алуминијума са болешћу је имплицирана стицајем околности услед повишених нивоа алуминијума у мозгу пацијената са Алцхајмеровом болешћу и амиотрофичном латералном склерозом.[231][234][233] Алуминијумски садржај је висок у плаковима, неурофибриларним свежњевима и неуритским наслагама карактеристичним за поменута обољења. Алуминијум инхибира мождане хексокиназе[238] и некомпетитивно инхибира мождану митохондријску моноаминску оксидазу-A (MAO-A)[232] (као што је то случај са цревном MAO, у контексту канцера). Постоје индикације да алуминијум активира серинске протеазе, и да су тако активиране протеазе накнадно отпорне на дејство других инхибитора.[231][234] Серинске протеазе пресецају β-амилоидне прекурсорске протеине (APP) и формирају β-амилоидне пептиде. Предложен је модел по којем алуминијум супресује инхибиторски домен протеаза, чиме поспешује протеолитичко формирање пептида који се затим акумулирају и иницирају формирање плакова.[231]
Низ других метала је био имплициран у формирање амилоидних плакова. Примећено је да Zn2+, Fe2+ и Cu2+ (μM), као и Al2+ (mM), узрокују агрегацију при физиолошким концентрацијама β-амилоидних протеина.[239][240][237][241][242][243] Хистидински модификован људски A бета(1-40) не подлеже агрегацији посредством Zn2+, Fe2+ или Cu2+, из чега произилази да хистидини учествују у металом индукованој агрегацији.[239] Постоје индикације да метали делују путем различитих механизама. Fe2+-индукована агрегација је инхибирана присуством антиоксиданаса, док они немају утицаја на Zn2+-индуковану агрегацију. Овај несклад сугерише да Fe2+ узрокује агрегацију путем оксидативног механизма.[240] Познато је да оксидација може да индукује агрегацију,[244] те да β-амилоиди имају прооксидантна својства — посебице у присуству алуминијума.[245] Азот-моноксидни донори као што је SNP (који NO формирају услед оксидативног стреса) могу да посредују акумулацију цинка у хипокампалним ћелијама, те постоји могућност да су оксидативни ефекти повезани са цинковим ефектима.[237] За разлику од тога, механизам Zn2+-индуковане агрегације није зависан од оксидације, него се заснива на директним интеракцијама са пептидима.[239][240][242][243] Поред свог агрегационог дејства, Zn2+ инхибира бројне протеолитичке ензиме који учествују у трансформацијама амилоида, укључујући матрикс металопротеиназе (MMP) одговорне за деградацију амилоидних пептида, а вероватно и α-секретазе одговорне за пресецање амилоидног прекурсорског протеина.[237] Инхибиција протеолизе се остварује путем два различита вида дејства метала на супстрате: 1. APP има место везивања за Zn2+ и након везивања долази до инхибиције пресецања на α-секретазном месту, и 2. MMP ензими не пресецају агрегиране амилоиде. За бакар и кобалт (50 μM) утврђено је да инхибирају APP пресецање.[246] Директна интеракција са секретазама није потврђена у APP студијама.
Осим амилоидних плакова, Алцхајмерово мождано ткиво карактеришу неурофибриларни сплетови. Истражује се мноштво различитих фактора да би се утврдио узрок овог феномена, укључујући абнормални транспорт неурофиламената и абнормалну деградацију. Показано је да алуминијум инхибира калцијумом активирану неутралну протеиназу (калпаин II) која посредује разлагање неурофиламентних подјединица и цитоскелеталних протеина.[233] AlCl3 и алуминијум лактат инхибирају пречишћени калпаин II, из људског церебралног кортекса, са IC50 вредношћу од 200 μM и 400 μM, редом. Инхибиција дејства калпаина је последица директне интеракције са ензимом, пошто преинкубација супстрата [14C]метилазоказеина са алуминијумом нема ефекта на инхибиторну ефикасност. Алуминијумска инхибиција исто тако обухвата интеракцију са цитоскелеталним протеинима, и у неким случајевима (нпр. код неурофиламентних подјединица NF-H и NF-M) алуминијум индукује формирање нерастворних комплекса урее. Стога је инхибиција протеолизе алуминијумом вишеструки процес који обухвата директно везивање за ензим, везивање за супстрат чиме се омета протеолиза, те формирање супстратних комплекса који су отпорни на протеолизу. Алуминијум има висок афинитет за фосфате и сматра се да се везује за фосфорилисане групе на неурофиламентним протеинима.[233] Упркос овим интеракцијама, механизам инхибиције калпаинина није расветљен.
Такође је показано да алуминијум инхибира метаболичке ензиме у мозгу, чиме се производе метаболичке грешке. Могуће је да акумулација таквих метаболичких грешака доприноси неуролошким поремећајима као што је Алцхајмерова болест. Хексокиназа, Mg(II)-зависни ензим, катализује први корак у циклусу гликолизе, којим се глукоза разлаже уз ослобађање енергије. Инхибиција хексокиназе је посредована везивањем алуминијума за супстрат; ATP има 107 пута већи афинитет за Al(III) него Mg(II).[234] Док највећи део глукозе подлеже гликолизи, 15—20% се подвргава хексозомонофосфатном шанту. Један од кључних ензима у овом путу, глукоза-6-фосфат дехидрогеназа (G6PD), инхибира се посредством Al(III) (μM распон).[234] До тога долази услед директне интеракције са ензимом; Al(III)-везани ензим подлеже конформационој промени до насумичније уређене структуре (судећи по налазима циркуларне дихроизне спектроскопије).

Тренутно се органски ацетилхолинестеразни инхибитори користе у третману Алцхајмерове болести; међутим, порфирини цинка и гвожђа исто тако инхибирају ацетилхолинестеразу.[235] Број и позиције флуоринских група на порфиринском прстену имају огроман ефекат на инхибиторну активност.[247]
С обзиром да постоји евиденција да долази до акумулације металних јона у неколико болести централног нервног система (CNS), од знатног интереса је да се утврди да ли ова акумулација има улогу у патогенези болести, а ако је то случај и да се одреди биохемијска природа њиховог учешћа. У једној недавној студији, велики број лизозомалних и цитоплазмичних протеиназа које су присутне у церебралном кортексу тестиран је за инхибицију металним јонима.[236] Утврђено је да милимоларне концентрације Cu2+, Cd2+, Pb2+, Hg2+ и Zn2+ инхибирају све тестиране лизозомалне протеиназе. Ови јони исто тако инхибирају цитоплазмичне протеиназе у различитим мерама а у зависности од металног јона. Пролинска ендонуклеаза и леуцилна аминопептидаза се инхибирају 50% или више са Zn2+ и Cu2+, редом. Аланил-, леуцил- и трипептидиламинопептидазе су инхибитиране са 0,05 mM Fe2+. Пироглутамилна пептидаза се инхибира са 0,05 mM Cu2+, Cd2+, Mn2+, Hg2+ или Zn2+. Аланил- и рипептидиламинопептидазе, пролинска ендопептидаза, те пироглутамил аминопептидаза, инхибиране су у различим мерама са Co2+ и Mn2+. Cd2+, Hg2+, Mn2+, Zn2+ и Al3+ инхибирају калпаин I и II у различитим мерама при концентрацији 5 mM. Импликације ових налаза о металним јонама су предмент истраживања.
Из ових радова следи да је улога металних јона у неуролошким болестима комплексна и разнолика. Метални јони демонстрирају разноврстан асортиман ефеката, од кинетичких до структурних. Кинетички ефекти могу да буду инхибиторни или активирајући. Структурни ефекти могу да подстакну агрегацију или отежају везивање. Ови ефекти наговештавају да метални јони могу да буду интиматно укључени у процес ензимске регулације. Да би се спровела ин виво испитивања било би неопходно да се остваре милимоларне концентрације метала у ткивима, што је нормално случај под физиолошким условима. Другим речима, потребно је правити разлику између потенцијално регулаторних процеса и токсичних ефеката.
Артритисне примене[уреди | уреди извор]
| Артритисне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| Ауранофин, натријум тиомалат | Au | протеинска киназа C[248][249] | |
| триметиламински карбоксиборани | B, Cu, Fe | еластаза, колагеназа, липоксигеназа, катепсин, циклооксигеназа[250] | |
| јон | Al | калпаин I[251] | |
| амински карбоксиборанеи и њихови естри | B | инозин монофосфат, де ново регулаторни ензими у синтези липида[252] | |
Једињења злата, као што је ауранофин, екстензивно су коришћена за третман реуматоидног артритиса, мада механизам њиховог дејства још увек није утврђен. Многе студије су демонстрирале инхибицију лизозомалних ензима[253][254] и протеинске киназе C, што може да објасни имуносупресивно дејство соли злата.[248][249]
Комплекси бакра[255][256] и бакарни комплекси антиинфламаторних лекова[257] показали су се ефективним као антиинфламаторни агенси. Постоје индикације да ови комплекси утичу на више ензимских система, а могуће је и да сам бакар има улогу у патогенези болести. Оболели од артритиса имају повишене просечне серумске или плазмене концентрације бакра, што је у директној корелацији са јачином и активношћу болести.[255] Утврђено је да бакар инхибира глутатион-S-трансферазу, а умањена GST активност је симптоматична за хронични артритис. Познато је да су бројни од бакра зависни ензими неопходни за опоравак од упале ткива.
Ензими протеолитичког пута су фреквентно имплицирани у деструкцију хрскавице оболелих од артритиса. Они су металопротеиназе, серинске протеазе и цистеинске протеазе, генерално присутни у везаном облику са природним инхибиторима. Систем калпаин-калпастатина је значајан јер је калпастатин (инхибитор калпаина) аутоантиген код скоро 50% реуматоидних артритисних пацијената и постоји евиденција да је калпаин прекомерно изражен код артритисних болесника.[258] Калпаин је Ca(II)-зависна цистеинска протеаза која се јавља у виду две изоформе: 1. калпаин I, за чију активацију се неопходне ниске концентрације калцијума, и 2. калпаин II, коме су потребне високе концентрације. Јони алуминијума различито утичу на ове две изоформе у калцијум-зависном маниру.[259] У присуству милимоларне концентрације калцијума, Al инхибира калпаин II у концентрационо зависном маниру, док је калпаин I максимално инхибиран унутар уског концентрационог опсега (0,1—0,5 mM Al). У одсуству калцијума, алуминијум активира калпаин II (који је иначе неактиван).
Имајући у виду ефективност борана као серинскопротеазних инхибитора, али и улогу протеаза у артритису, није изненађујуће да је утврђено да су бројни амински карбоксиборани антиинфламаторни агенси. Комплекси бакра и гвожђа триметиламинских карбоксиборана инхибирају активност лизозомалних и протеолитичких ензима у макрофагама,[250] као и неки од самих аминских карбоксиборана.[252] Међу инхибираним ензимима су неутрални катепсин, трипсин, еластаза, колагеназе I и II, простагландинска синтаза, циклооксигеназа (индукована код инфламаторног артритиса)[260] и 5'-липоксигеназа. Сви су инхибирани при микромоларним концентрацијама.[250] Такође је утврђено да амински карбоксиборани имају мноштво других ефеката, укључујући инхибицију регулаторних ензима који учествују у де ново синтези липида, ДНК и РНК. Путем ин виво експеримената је исто тако утврђено да амински карбоксиборани врше различите утицаје, укључујући снижавање серумског холестерола, блокирање калцијумске ресорпције (што је проблематично код остеопорозе) и редуковање инфламација.[252] Даља истраживања су неопходна да би се утврдила специфичност ових агенаса и структурна својства која утичу на разна терапеутска својства. Артритис је добар пример болести у којој су метални комплекси екстензивно коришћени као терапија иако механизам дејства није познат.
Примена на инфекције[уреди | уреди извор]
Виралне примене[уреди | уреди извор]
| Виралне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| полиоксоволфрамати | W | HIV реверзна транскриптаза, РНК полимераза, ДНК полимераза[261] | |
| тиосемикарбазони | Sn | реверзна транскриптаза вируса леукемије[262] | |
| TSAO | Si | HIV реверзна транскриптаза[263] | |
| трифлуоперазин | V, Cu, Ni, Pd, Sn | реверзна транскриптаза вируса леукемије[264] | |
| стрептонигрин | Zn | топоизомераза, HIV реверзна транскриптаза[142] | |
| јони | Fe, U, V, Ti, Pb, Cu, Pd | протеиназа[265] | |
| батокупроинска дисулфонска киселина | Cu | протеаза, интеграза[266] | |
| јони | Zn | протеаза[267] | |
| јони | Zn | ренин, протеаза[265] | |
| инхибиторни хелат | Cu | протеаза[268] | |
| фенантролин, неокупроин, батокупроински комплекси | Cu | интеграза[269] | |
| ароматични полихидроксилати | Mn | интеграза, други ензими којима је потребан метал[270] | |
| порфирини | Fe, Co | хем оксигеназа[195] | |


Вируси користе релативно мали број, јединствених ензима за одржавање свог животног циклуса, што чини те ензиме атрактивним метама за антивирусне лекове.[271] На пример, геном вируса људске имунодефицијенције (HIV) кодира три критична ензима: 1. реверзну транскриптазу која конвертује инфекциону виралну ssРНК у dsДНК, 2. интегразу која умеће dsДНК у домаћинов геном, и 3. протеазу која пресеца вирусне генске продукте до њихових крајњих форми.[272] Вирусни ензими су генерално у већој мери конзервирани, а то је посебно случај са њиховим активним местима у односу на покровне протеине, још једну класу металекова; стога су мање склони развоју мутационе отпорности на лекове. Током последњих неколико декада огромни напори су уложени у истраживање начина спречавања пропагације HIV вируса, а један од главних терапијских циљева је била реверзна транскриптаза.
Реверзна транскриптаза (RT) проминентна је мета за инхибиторе јер је дистинктна у односу на нормалне полимеразе ћелија домаћина и физички одвојена од репликационе машинерије домаћина (вирална транскриптаза је цитоплазматична, а не једрена). Реверзна транскриптаза је мултифункционални ензим. Она делује као полимераза која формира плус и минус ланце ДНК и као рибонуклеаза Х која разлаже РНК порцију РНК-ДНК хибрида.[273] Инхибиција може да буде усмерена на било коју од тих функција или места везивања ензима, мада сви тренутно одобрени инхибитори утичу на полимеразну функцију.[274] Многи нуклеозидни аналози и ненуклеозидни инхибитори су развијени током последњих година, али релативно мали број тих инхибитора су метални комплекси.
Полиоксоволфрамати, а посебно серије силиковолфрамата из кегинске групе, класа су неорганских једињења за које је показано да имају антивирално дејство.[261] Ова једињења инхибирају виралну репликацију у HIV-ом инфектираним ћелијама и испољавају компетитивну и некомпетитивну инхибицију пречишћене или поли(етилен гликолом) преципитиране реверзне транскриптазе. Инхибиција РНК-зависне ДНК полимеразне функције се остварује на 3—6 пута нижој концентрацији него за ДНК-зависну ДНК полимеразну активност. Тестови на другим пречишћеним ДНК полимеразама индицирају да су силиковолфрамова једињења најсензитивнија против вируса леукемије мишева (IC50 = 0,0035 μM), мање ефективна против HIV-1 RT (IC50 = 3 μM) и релативно неефективна против људске ДНК полимеразе 1 (IC50 = 43 μM). Мада је ДНК полимераза α донекле сензитивнија на инхибицију од HIV-1 RT, тестови у култури су показали антивиралну активност без цитотоксичности; концентрације неопходне за производњу цитотоксичности су неколико редова величине више од концентрације неопходне за елиминацију вируса. Мада специфичност тих једињења против RT није установљена и тачно место инхибиције на RT није познато, њихово антивирално дејство у културама подстиче даља истраживања.
Тиосемикарбазони су већ дуже време познати као антивирални агенси. Диорганокалај(IV) комплекси пиридил тиосемикарбазона су недавно окарактерисани и утврђено је да инхибирају RT.[262] Комплекси бакра и кобалта истог лиганда (L) такође су испитани.[275] Sn(Bu)2(L) и Sn(Ph)2(L) комплекси су најефективнији против RT, али нису тестирани на другим полимеразама да би се утврдила специфичност инхибиције. Стога се на бази ових студија антивирално дејство једињења не може искључиво приписати њиховој инхибицији RT. Такође је познато да тиосемикарбазони инхибирају рибонуклеотидне редуктазе, РНК-зависну ДНК полимеразу, те дихидрофолатну редуктазу.[137]
Трифлуоперазини (TFP), деривати психотерапеутског лека фенотиазина, такође имају потврђено антивирално дејство. Метални комплекси TFP су тестирани на RT вируса леукемије мишева, и установљено је да метали поспешују инхибицију у редоследу VO(IV) > Ni(II) > Pd(II) > Cu(II) > Sn(IV) > слободни лиганд.[264] Ови комплекси су ефективни против реверзних транскриптаза више ретровируса. Стрептонигрин је антибиотик који је потенцијално могао да делује као антитуморски агенс за разне људске канцере; међутим, токсичне нуспојаве третмана стрептонигрином су довеле до прекида клиничких испитивања. Стрептонигрин такође селективно инхибира TT птичјег мијелобластозног вируса (AMV) и HIV без инхибирања ћелијских полимераза.[142] Механизам дејства стрептонигрина је испитан након прекида клиничких испитивања. Преглед резултата тих студија, укључујући детаљну структурну карактеризацију неколико металних комплекса лека, показао је да је метална јомплексација кључна за биолошку активност лека.[142] Међутим, прецизни механизам његовог терапеутског ефекта је још увек непознат.
Примена метал-хелирајућих деривата TSAO-T, а [2',5'-bis-O-(терт-бутилдиметилсилил)-β-дрибофуранозил]-3'-спиро-5-(4-амино-1,2-оксатиол-2,2-диоксид) нуклеозидног деривата тимина представља један другачији приступ побољшању инхибиције реверзне транскриптазе.[276] Родитељско једињење, TSAO, везује се за алостерно место лоцирано поред RT каталитичког места.[263] Ово место везивања инхибитора формира интеракције са оближњим Mg2+ местом везивања.[277] Нова класа једињења је дизајнирана са везаним инхибитором, TSAO-T, за металну хелирајућу групу, јер се сматрало да ће формирати бидентатни инхибитор са већим афинитетом за ензим. Неколико деривата је било синтетисано, а за оне са кратким алкилним ланцима је утврђено да су знатно ефективнији антивирални агенси. Неколико деривата који су једнако активни као родитељско једињење има знатно мању токсичност (10 пута мање концентрације резултују са 50% повећања ћелијске одрживости). Ова класа једињења је пример инхибитора који не садрже метал и инхибирају путем формирања металног комплекса.
HIV-1 протеаза је аспартилна протеаза која формира зреле протеине из продуката gag гена (групно специфичних гена) и pol гена (ДНК полимеразе). Отпорност на протеазне инхибиторе се теже остварује код вируса него отпорност на RT инхибиторе,[278] те су развијени многи пептидни инхибитори.[227] Утврђено је да бројни метални јони делују као инхибитори HIV-1 протеазе, а да су најефективнији тешки јони (Fe3+, UO22+, VO3−/VO43−, TiCp2Cl2, Pb2+), као и да су они углавном тетраедрално координирани.[265] Метали некомпетитивно инхибирају ензим, тако што симултано са супстратом заузимају активно место. Сматра се да се метали координирају са карбоксилатним бочним ланцима активних остатака Asp25 и Asp125, мада то није дефинитивно потврђено. Могуће је да ће ове обзервације подстаћи дизајн инхибитора HIV-1 протеаза који ће садржати метале који се везују за ензим јонским или ковалентним везама, те да ће стога бити знатно јаче везани од пептидних инхибитора.
Гореописана студија металних јона је наизглед у конфликту са резултатима једне раније студије која је показала да јони цинка и сребра некомпетитивно — а јони бакра компетитивно инхибирају протеазе и ренин из HIV-1.[265] Ranija studija je sprovedena na rekombinantnoj proteazi izolovanoj iz E. coli, док је каснија студија користила синтетичку SF2 секвенцу протеазе, у којој је аминобутирна киселина замењена цистеинским остатком.[183][227][279][280] Није сасвим јасно у којој мери синтетички ензим опонаша природни ензим. Исто тако, студије су изведене на различитим pH вредностима, раније студије на неутралном pH а касније на pH 5. Раније студије су заправо показале да је инхибиција цинком у великој мери зависна од pH. Процењује се долази до надметања цинка са протоном за групу са pKa = 7,0. Молекуларне динамичке симулације изведене на протеази у присуству цинка индицирају да се јони цинка везују за каталитички активно место на остацима Asp25 и Asp25' без поремећаја структуре ензима.[267]
Утврђено је да је CuCl2 ефективан инхибитор протеазе, али не и мутиране протеазе у којој су аланини супституисани цистеинима.[281] Мутирана протеаза може инхибирати CuCl2 у присуству бакарних хелатора. Утврђено је да је батокупроин сулфонска киселина Cu(I), BCSD-Cu(I), компетитивни инхибитор протеазе.[266] Сама BCSD не инхибира ензим, нити инхибиција комплекса може да буде блокирана помоћу EDTA. Из овога следи да је метални комплекс активни инхибитор, а не слободни лиганд нити слободни метал. Комплекс исто тако инхибира мутирану протеазу којој недостају цистени. Други бакарни хелати инхибрају HIV-1 протеазу. Утврђено је да је диаква[бис(2-пиридилкарбонил)амидо]бакар(II) нитрат дихидрат компетитивни инхибитор протеазе.[268] Ова студија такође сугерише да су молекули воде у активном месту који су присутни између Asp25 и Asp125 важни за структуру ензима. Ова чињеница може да утиче на дизајн инхибитора који не садрже хидроксилне супституенте.
Утврђено је да бакарни комплекси инхибирају HIV интегразу.[269] Долази до некомпетитивне инхибиције механизмом који се разликује од једноставног блокирања везивања супстрата или везивања ДНК. Инхибиција мутаната C- и N-терминалног брисања овим комплексима указује на чињеницу да се ови комплекси везују за сржни регион интегразе. Селективност комплекса за интегразе до сада није демонстрирана. Интегразе садрже мотиве цинковог прста у близини N-терминуса и конзервирани мотив аспартатних и глутаматних остатака који вероватно учествују у ДНК везивању или пресецању.[272] Они такође могу да представљају места потенцијалних интеракција са металним комплексима. За велики број антрахинона и сродних полихидроксилисаних фенолних молекула је показано да инхибирају интегразе при наномоларним концентрацијама.[270] Ова једињења реагују и са другим ензимима за чије дејство су неопходни метали (реверзне транскриптазе мишјег леукемијског вируса, MoMLV, и рестрикциони ензими Pvu II и EcoRI), али не и са ензимима којима нису потребни метали. Из ове чињенице произилази да метали учествују у инхибиторном механизму. За нека од тестираних једињења је познато да су метални хелатори. MoMLV инхибиција је ефикаснија у присуству Mn2+ него Mg2+ (до 26 пута мање вредности IC50 у зависности од једињења). Овај ефекат је уочен и код интегразе.[282] Познато је да каталитички домен интегразе везује метале, а инхибиција може да обухвати формирање терцијарног комплекса инхибитора, метала и ензима; међутим, то ово још увек није доказано.
Описани инхибитори виралних ензима углавном немају ексклузивну специфичност. Изузев деривата TSOA-T, инхибитори ове класе нису дизајнирани за интеракцију са специфичним местима. Многи инхибитори су идентификовани скринингом прво за инхибицију виралне репликације а затим за активност на пречишћеним ензимима.
Невиралне примене[уреди | уреди извор]
- Бактерије, глијвице и паразити
| Антимикробне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| 1-амино-3-(2-пиридил)изохинолин, јони | Cu | NADH оксидаза, лактатна дехидрогеназа[283] | |
| сулфадиазин | Ag | фосфоманозна изомераза[284] | |
| тровалентна једињења арсена | As | трипанотионска редуктаза, глутатионска редуктаза[285] | |
| [XxMxOoHh]n- | Mo, V | киселинска фосфатаза[286] | |
| шећерни комплекси | Ni | хитиназа[287] | |
| тровалентна једињења амонијака | Sb | фосфофруктокиназа[288] | |
| пентостам | Sb | клинички демо[289] | |
| тиосемикарбазони | Cu | дихидрофолатна редуктаза[137] | |
| јон | V | ектокиселинска фосфатаза[290] | |
| титанил сулфати | Ti | серинске протеазе[225] | |
Неке од најранијих примена неорганских једињења у медицини су биле у виду антисептика и антимикробних агенаса.[205][226][291] Заправо, органоарсенична једињења су била прва једињења која су успешно примењена за третман сифилиса (она су касније замењена пеницилином), а коришћена су као адитиви сточне хране за спречавање бактеријских и паразитских инфекција.[226] Сулфаниламиди су велика класа једињења која испољава антибактеријску ефективност, а познато је и неколико металних јона који имају антимикробно дејство.[292] Органометална једињења се рутински тестирају за антимикробне ефекте ради идентификације могућих лекова. Осим агенаса који инхибирају ензиме, постоји мноштво агенаса чији механизам није познат.[293][294][295][296][279]
Једна недавна студија се бавила испитивањем инхибиције серинских протеаза код бактерија и гљивица ради развоја антимикробиних агенаса. Скрининг великог броја металних јона на трипсину из разних извора (пречишћених и у бактеријским лизатима) и говеђем панкреасном химотрипсинину показао је да само Ti(IV) у облику титанилног сулфата инхибира трипсин, док други метали или увећавају активност (Ca2+, Mn2+) или немају ефекта.[225] Ова инхибиција је компетитивна, што значи да се инхибитор везује за активно место. Инхибиција химотрипсина није уочена, те је предложено да се Ti(IV) везује за Asp-198 у супстратном месту везивања за остатак који није присутан код химотрипсина. Утврђено је да су титанилни алкохолни комплекси мање инхибиторни (25% инхибиторне активности) него сулфати. Петокоординатна геометрија Ti(IV) била је разматрана као могуће објашњење уочене активности Ti(IV) против бактерија у односу на друге металне јоне и геометрије.
Тривалентни арсенични лекови, као што је меларзопрол, још увек се рутински користе у третману трипанозомом посредованих болести, као што је афричка болест спавања. Механизам њиховог дејства није испитан, мада се сматра да је последица интеракције са протеинским дитиолима. Познато је да тривалентна једињења арсена формирају стабилне адукте са дитиол трипанотионом, те да се ти адукти ефективније надмећу за активно место трипанотион редуктазе.[297] Трипанотион, који је аналоган глутатиону код сисара, јединствен је за трипанозоме. Једна недавна студија је испитала утицај неколико једињења арсеника на трипанотионску и глутатионску редуктазу, два ензима која садрже каталитичке сулфидрилне групе.[285] Инхибиција оба ензима је знатно сензитивнија у присуству НАДПХ, што је индикација да цистеински сулфидрили морају да буду редуковани да би формирали интеракције са лековима. Трипанотионска редуктаза је сензитивнија на инхибицију од глутатионске редуктазе. Инхибицију обуставља дихидротрипанотион. Иако једињења арсена инхибирају ензим, пошто је дихидротрипанотион ин виво доступан у знатно вишим концентрацијама од трипанотионске редуктазе, мало је вероватно да би инхибиција овог ензима могла да има терапеутски учинак на трипанозомијазу.
Антимонијали су дуго коришћени као антипаразитици,[226][291] и још увек се користе у третману слузокожне лишманијазе.[289] Низ других метала се испитује за њихову активност против лишманијазе. Постоје индикације да киселинске фосфатазе (ACP) доприносе патогености трипаносома Leishmania. Те фосфатазе могу да инхибирају бројни прелазни метали и њихови комплекси, као што су арсенат и ванадат.[290] Студије у којима је коришћена тартратно сензитивна киселинска фосфатаза из људског семеног флуида и тартратно резистентна фосфатаза из протозое Leishmania donovani демонстрирале су да хетерополианјонски комплекси молибдена (са Ge, Fe, As, Ce, Th) селективно инхибирају ове ензиме.[286] Тестиране су четири класе комплекса, које садрже 4, 6—8, 12 или 18 атома Mo. Селективност је процењена на основу инхибиције поменутих ензима и одсуства ACP инхибиције из људске слезине. β-глукуронидазе и α-манозидазе из слезине су такође испољиле мало или нимало инхибиције услед дејства молибденат-хетерополианјона. Студије унакрсног надметања између ових инхибитора индицирају да се неки од комплекса везују за активно место, док се други везују за друго место које утиче на активно место. На пример, везивање ванадата и једног од комплекса Mo није било узајамно искључиво, а ванадат је појачавао инхибицију Mo комплекса.
Антимон се такође примењује као антишистозомијални агенс. Недавним истраживањима је утврђено да разни антимонијали инхибирају фосфофруктокиназу (PFK) из метиља Schistosoma mansoni.[288] Опстанак шистозома је зависан од велике брзине гликолизе, а PFK је кључни ензим у гликолитичком путу — садржи 20 цистеина. Упоређивањем шистозомалне и сисарске PFK је утврђено да антимонилтартарат калијум преферентно инхибира паразитов ензим. Механизам ове селективности није разјашњен.
Метални јони и метални комплекси су ефективни антифунгални агенси против патогеног квасца Candida albicans. Комплекси сребра инхибирају фосфоманозну изомеразу (PMI), кључни ензим у биосинтези квашчаних ћелијских зидова, са nM Ki.[284] PMI мутант код кога је Cys150 замењен са аланином понаша се на сличан начин као и природни ензим, али не бива инхибиран једињењима сребра и 1000 пута је мање сензитиван на живу. Из овога произилази да је Cys150 место интеракције инхибитора. Јони сребра инхибирају PMI са 210 пута вишом бимолекуларном константом брзине за људски ензим. Ова једињења редукују специфичност за људски ензим до 1,3 : 1. I док их ово не квалификује као инхибиторе који су селективни за паразите, може се претпоставити да је могуће развити лек путем модификација органских група. Комплекси никла инхибирају хитиназу, која такође учествује у биохемији ћелијског зида квасца-гљиве C. albicans.[287] Поменути комплекси садрже N-гликозиде изведене из аминошећера, који инхибирају у компетитивном маниру.
Микоплазми недостаје чврст ћелијски зид. Јонски бакар је ефективан инхибитор микоплазичне активности и показано је да инхибира ензиме у гликолитичком путу, NADH оксидазу и лактатну дехидрогеназу.[283] 2,2'-бипиридински тип лиганда олакшава транспорт бакра кроз микоплазмичну мембрану, па је антимикоплазмично дејство бакра знатно повећано у присуству ових лиганда — мада присуство лиганда умањује инхибиторни ефекат на пречишћеним, изолованим ензимима. Ова опажања потврђују да је јон бакра токсичан материјал, а да лиганд само служи као преносник.
- Третман чирева
| Третман чирева | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| јони | Bi | фекална слузокожна сулфатаза[298] | |
| јони | Bi | H. pylori ATPаза[299] | |
Бизмутове соли су коришћене у терапији чирева. Познато је да оне инхибирају аденозинтрифосфатазу из желучане бактерије H. pylori (која учествује у развићу пептичног чира),[299] као и фекалну слузокожну сулфатазу (чије је изражавање повишено код улцерозног колитиса).[298]
Токсичност примене[уреди | уреди извор]
| Токсичност примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| ионс | Al | γ-аминолевулинска киселина[300] | |
| јони | Al | хексокиназа[301] | |
| јони | Cd, Cu, Hg, Zn, Pb | хексокиназа[302] | |
| јони | Al | глицеролна киназа[303] | |
| јони | Al, Cd, Pb | ATPаза[304] | |
| јони | As | поли-(ADP-рибоза) полимераза[305] | |
| јони | As | пируватна дехидрогеназа, ДНК лигаза[306] | |
| јони | As | метилтрансфераза[307] | |
| јони | As | метилтрансфераза[308] | |
| арсеноглутатион | As | глутатионска редуктаза[309] | |
| 3-арсонопируват | As | Фосфоенолпируватна мутаза[310] | |
| јон | Ni | ДНК полимераза[311] | |
| јон | Zn, Cd | ДНК лигаза[312] | |
| јон | Cd | О6-метилгуанин-ДНА метилтрансфераyа, ДНК полимераза β[313] | |
| cis-DDP | Pt | респираторни ензими[129] | |
| јони | V | пероксидаза рена, супероксид дисмутаза[280] | |
| јон | Ni | MutT-dGTPаза[314] | |
| јон | Pb | γ-аминолевулинатна дехидратаза[315] | |

Велика количина рада је уложена да би се одредио молекуларни механизам металне токсичности. Узрок смртности је комбинација више фактора. Разумевање путева на које метали утичу је пререквизит за спречавање токсичности, те пружа увид у потенцијалне примене у којима се токсичност искоришћава за производњу корисних ефеката. Алуминијумска токсичност индукује анемију, а сматра се да до овога долази услед пертурбације биосинтетичког пута хема.[300] Уочено је да алуминијум инхибира бројне ензиме ин витро, укључујући дехидратазу δ-аминолевулинске киселине (ака порфобилиногену синтазу),[300] хексокиназе,[301] глицеролне киназе[303] и ATPазу.[304] Механизам инхибиције се разликује од ензима до ензима. Дехидратаза δ аминолевулинске киселине која катализује други корак биосинтезе хема је металопротеин који везује осам јона цинка. Алуминијум некомпетитивно инхибира ове ензиме, из чега следи да се не везује за активно место, те да се вероватно надмеће са неким или свим јонима цинка.[300] Јонски пречник Al3+ је сличан пречнику Mg2+ или Fe3+, а могуће је да алуминијум инхибира Mg2+-зависне ензиме путем супституције за Mg2+ (на пример у хексокинази),[303] мада ово није било уочено у свим студијама.[301] За глицеролне киназе и хексокиназе је такође постулирано да се алуминијум надмеће са MgATP супстратом у облику алуминијум-ATP хелатног комплекса.[301][303] Кинетика инхибиције може да помогне у одређивању природе инхибиционог места, али су структурне студије неопходне за одређивање прецизног тока интеракције.
Друге студије су демонстрирале да Cd2+, Cu2+, Hg2+, Zn2+ и Pb2+ инхибирају хексокиназу (у ниском μM опсегу).[302] Cd2+ и Cu2+ су много ефективнији од других метала. Инхибиција помоћу Cu2+ доводи до пратећег снижења нивоа редукованог глутатиона (GSH). Преинкубација узорка са GSH заштићује ензим од Cu2+ инхибиције. Познато је да GSH формира GSH-Cu(I) комплексе, а заштитни ефекти GSH комплекса су вероватно последица једноставног уклањања Cu2+ из раствора. Предложени су бројни модели за релацију између хексокиназе, GSH и токсичности тешких метала ин виво.
Постоје индикације да је арсенична токсичност редокс зависна, тако да је пентавалентни As(V) знатно мање токсичан од тривалентне форме елемента, As(III).[309][307] Арсеник је карциноген, мада директно не оштећује ДНК. Најпроминентнија хипотеза за његов механизам деловања је инхибиција ензима путем везивања за сулфхидриле, те је знатан број студија био усредсређен на испитивање дејства арсеника на ензиме поправке и лигације ДНК. Утврђено је да As(III) инхибира ензим поли-(ADP-рибоза) полимеразу, који садржи два вицинална дитиола који посредују везивање ензима за прекиде ДНК ланаца.[305] Механизам инхибиције још увек није утврђен. Пируватну дехидрогеназу инхибира As(III) при микромоларним концентрацијама, али не и As(V). Неколико других ензима за ДНК поправку је тестирано и утврђено је да на њих As(III) нема утицаја, мада неки садрже SH групе од пресудног значаја за своју функцију.[306] Арсенит може да инхибира лигазну активност у култивисаним ћелијама али не и у нуклеарним екстрактима из тих ћелија, из чега следи да инхибиција лигаза није директна већ се јавља на неком другом нивоу поправке.[306] Спектроскопске студије As(III) инхибиције метилтрансферазе (ензима који учествује у модификацији и поправци неподударних ДНК сегмената) индицирају да се As(III) везује за Cys223, чиме индукује ефекат тешког атома (HAE) на оближњем Trp остатку. Ово је потврђено опсервацијом да се HAE не јавља код мутанта са Cys223 замењеним Ser223 остатком.[307][308] Појава HAE је заснована на налазима црвеног помака фосфоресцентног спектра и знатног скраћења животног века триплетног стања As(III)-пертурбираног триптофана. Ова интеракција не утиче на ензимску активност, тако да је инхибиција која је уочена у присуству вишка арсенита вероватно последица везивања за друге цистенске остатке ензима.
Инхибиција глутатионске редуктазе са As(III) конзистентна је са оксидацијом тиолних група у активном месту ензима.[309] Арсен формира арсеноглутатионске комплексе са глутатионом, и они делују као инхибитори мешовитог типа на глутатионској редуктази. Ензими који делују на форсфорним једињењима често препознају арсенске аналоге, нпр. аденилатна циклаза и РНК полимераза. Показано је да 3-арсонопируват компетитивно инхибира фосфоенолпируватну (PEP) мутазу са Ki = 27 μM.[310] PEP мутаза је главни ензим у биосинтетичком путу формирања C-P веза. Никл је попут арсена генотоксичан карциноген, мада прецизни механизам токсичности Ni није познат. Ni(II) служи као слаба замена за Mg(II) у неким полимеразама, док друге полимеразе бивају јако инхибиране.[311] Ефекат јона никла на инкорпорацију нуклеотида, процесивност и мисинкорпорацију проучаван је код седам различитих полимераза; изведен је закључак да је његов примарни ефекат инхибиција (микромоларни опсег). Међутим, ово зависи од бројних фактора чији значај варира од ензима до ензима. Дејство никла је комплексно, а прецизни механизам ометања полимеразне функције није установљен. Инхибиција репликације и поправке ДНК повезана је са мутагеношћу и карциногеношћу металних јона.[313] Уочено је да Ni(II) инхибира MutT-dGTPазу, која учествује у поправци 8-оксо-dGTP оштећења на ДНК (милимоларни Ki).[314] Ћелије изложене оксидативном стресу формирају 8-оксо-dGTP; присуство нуклеотида повишава мутациону фреквенцију A у C трансверзијама услед 8-оксо-dG-dA неспаривања. Инхибиција Mg(II)-зависног MutT ензима поправке може да доведе до повишене мутагенезе. Студије молекулским моделовањем указују да се Ni(II) не везује за место везивања Mg(II), него да индукује конформационе промене за које је предвиђени узрок везивање за хистидинске остатке.[314]
Уочено је да цинк и кадмијум такође инхибирају ензиме ДНК поправке.[313] Пречишћена ДНК лигаза се инхибира са 0,8 mM ZnCl2 и 0,04 mM CdCl2.[312] Оба метала инхибирају формирање интермедијера, трансферазно дејство и лигационо дејство, а немају ефекта на брзину мислигације. Другим речима, инхибиција једино утиче на ензимску активност док се тачност рада лизаге не мења. Лигазама је неопходан магнезијум као кофактор; Mg је неопходан за све три корака лигационе реакције која инхибира кадмијум и цинк. Јони Cd и Zn могу да делују путем супституисања јона Mg у месту везивања метала.
Један од метала с лошом репутацијом у очима јавности је олово. Тровање оловом заузима истакнуто место у јавној свести због мноштва инцидената узрокованих применом олова на радним местима, као и због тровања деце оловним бојама.[315] Један од механизама токсичности је инхибиција цинк металоензима, односно γ-аминолевулинатне дехидратазе (ALAD) која је такође некомпетитивно инхибирана алуминијумом. У случају олова, инхибиција се одвија путем супституције цинка оловом. Два алела ALAD ензима су идентификована код људи (ALAD1 и ALAD2) и они кодирају три дистинктна изозима. Тестирање великог броја деце (изложене ниским нивоима олова у животној средини) и радника из оловопрерађивачких фабрика показала су да ALAD2 позитивни имају повишене нивое олова у крви након сличних излагања и да су знатно сензитивнији на тровање оловом. Претпоставља се да ALAD2 јаче везује олово.[315]
Метална токсичност може да буде резултат оксидативних реакција. Ванадат учествује у мноштву таквих реакција, а недавно је објављена студија у којој је изучавано његово дејство на антиоксидантне ензиме.[280] Четири различита ензима су разматрана и утврђено је да ванадат инхибира пероксидазу рена. Ови налази додуше не дају јасну индикацију о релацији између антиоксидантске ензимске инхибиције и токсичности.
Знатан део литературе се бави једним другим механизмом инхибиције ензимске активности металним јонима: редукцијом количине ензима услед инхибирања транскрипције гена који кодирају ензим.[318][319] Највећим делом, резултати испитивања наглашавају да је токсичност узрокована металним јонима последица инхибиције која се јавља на многим нивоима у многим системима, те да је мало вероватно да било која појединачна промена може да буде самостално одговорна за токсичне ефекте.
Види још[уреди | уреди извор]
- Аналог прелазног стања
- Антиметаболит
- Фармакофор
- Инхибиција ензимских реакција
- Протеомика базирана на активности — грана протеомике која користи ковалентне инхибиторе ензима као индикаторе при изучавању ензимске активности
Референце[уреди | уреди извор]
- ^ а б Robert A. Copeland (06. 05. 2013). Evaluation of Enzyme Inhibitors in Drug Discovery: A Guide for Medicinal Chemists and Pharmacologists (II izd.). ISBN 9781118488133. doi:10.1002/9781118540398.
- ^ а б Shapiro, R; Vallee, BL (1991). „Interaction of human placental ribonuclease with placental ribonuclease inhibitor”. Biochemistry. 30 (8): 2246—55. PMID 1998683. doi:10.1021/bi00222a030.
- ^ а б Berg J.; Tymoczko J.; Stryer L. (2002). Biochemistry. W. H. Freeman and Company. ISBN 978-0-7167-4955-4.
- ^ а б в г д ђ е ж з и Cleland WW (1963). „The kinetics of enzyme-catalyzed reactions with two or more substrates or products. II. Inhibition: nomenclature and theory”. Biochim. Biophys. Acta. 67: 173—87. PMID 14021668. doi:10.1016/0926-6569(63)90226-8.
- ^ а б в г д ђ Segel, Irwin H. (1993). Enzyme Kinetics : Behavior and Analysis of Rapid Equilibrium and Steady-State Enzyme Systems (New izd.). Wiley-Interscience. ISBN 978-0-471-30309-1.
- ^ а б Holdgate, GA (2001). „Making cool drugs hot: isothermal titration calorimetry as a tool to study binding energetics” (PDF). BioTechniques. 31 (1): 164—6, 168, 170. PMID 11464510.
- ^ а б Leatherbarrow, RJ (1990). „Using linear and non-linear regression to fit biochemical data”. Trends in Biochemical Sciences. 15 (12): 455—8. PMID 2077683. doi:10.1016/0968-0004(90)90295-M.
- ^ а б Tseng, SJ; Hsu, JP (1990). „A comparison of the parameter estimating procedures for the Michaelis-Menten model”. Journal of Theoretical Biology. 145 (4): 457—64. PMID 2246896. doi:10.1016/S0022-5193(05)80481-3.
- ^ а б Walsh, R.; Martin, E.; Darvesh, S. (2011). „Limitations of conventional inhibitor classifications”. Integrative Biology. Royal Society of Chemistry. 3 (12): 1197—1201. PMID 22038120. doi:10.1039/c1ib00053e.
- ^ а б Walsh, R.; Martin, E.; Darvesh, S. (2007). „A versatile equation to describe reversible enzyme inhibition and activation kinetics: Modeling β-galactosidase and butyrylcholinesterase”. Biochimica et Biophysica Acta (BBA) – General Subjects. 1770 (5): 733—746. PMID 17307293. doi:10.1016/j.bbagen.2007.01.001.
- ^ а б Walsh, Ryan (2012). „Ch. 17. Alternative Perspectives of Enzyme Kinetic Modeling”. Ur.: Ekinci, Deniz. Medicinal Chemistry and Drug Design (PDF). InTech. str. 357—371. ISBN 978-953-51-0513-8.
- ^ а б Chris G Whiteley (30. 06. 2010). „Enzyme Kinetics: Partial and Complete Competitive Inhibition”. Biochemical Education. 25 (3).
- ^ а б Dixon, M.; Webb, E.C.; Thorne, C.J.R.; Tipton K.F. (1979). Enzymes (III izd.). London: Longman. str. 126. ASIN B001MVGNNO.
- ^ а б „Hormonal Regulation of Metabolism: The levels of glucose in the blood are regulated by the hormones insulin and glucagon from the pancreas, and T3 and T4 from the thyroid”. 26. 05. 2016.
- ^ а б John F. Morrison (1982). „The slow-binding and slow, tight-binding inhibition of enzyme-catalysed reactions”. Trends in Biochemical Sciences. 7 (3): 102—105. doi:10.1016/0968-0004(82)90157-8.
- ^ а б Hsu, JT; Wang, HC; Chen, GW; Shih, SR (2006). „Antiviral drug discovery targeting to viral proteases”. Current pharmaceutical design. 12 (11): 1301—14. PMID 16611117. doi:10.2174/138161206776361110.
- ^ а б Lew W, Chen X, Kim CU (2000). „Discovery and development of GS 4104 (oseltamivir): an orally active influenza neuraminidase inhibitor”. Curr. Med. Chem. 7 (6): 663—72. PMID 10702632. doi:10.2174/0929867003374886.
- ^ а б PM, Fischer (2003). „The design, synthesis and application of stereochemical and directional peptide isomers: a critical review”. Curr. Protein Pept. Sci. 4 (5): 339—56. PMID 14529528. doi:10.2174/1389203033487054.
- ^ а б Bogoyevitch, MA; Barr, RK; Ketterman, AJ (2005). „Peptide inhibitors of protein kinases-discovery, characterisation and use”. Biochimica et Biophysica Acta. 1754 (1—2): 79—99. PMID 16182621. doi:10.1016/j.bbapap.2005.07.025.
- ^ а б L., Lundblad R. (2004). Chemical Reagents for Protein Modification. CRC Press Inc. ISBN 978-0-8493-1983-9.
- ^ а б Price, N.; Hames, B.; Rickwood, D., ur. (1996). Proteins LabFax. Academic Press. ISBN 978-0-12-564710-6.
- ^ а б Adam, GC; Cravatt, BF; Sorensen, EJ (2001). „Profiling the specific reactivity of the proteome with non-directed activity-based probes”. Chemistry & Biology. 8 (1): 81—95. PMID 11182321. doi:10.1016/S1074-5521(00)90060-7.
- ^ а б Maurer, T; Fung, HL (2000). „Comparison of methods for analyzing kinetic data from mechanism-based enzyme inactivation: application to nitric oxide synthase”. AAPS PharmSci. 2 (1): 68—77. PMC 2751003
 . PMID 11741224. doi:10.1208/ps020108.
. PMID 11741224. doi:10.1208/ps020108.
- ^ а б Loo JA, DeJohn DE, Du P, Stevenson TI, Ogorzalek LR (1999). „Application of mass spectrometry for target identification and characterization”. Med Res Rev. 19 (4): 307—19. PMID 10398927. doi:10.1002/(SICI)1098-1128(199907)19:4<307::AID-MED4>3.0.CO;2-2.
- ^ а б в г Poulin, R; Lu, L; Ackermann, B; Bey, P; Pegg, AE (1992). „Mechanism of the irreversible inactivation of mouse ornithine decarboxylase by alpha-difluoromethylornithine. Characterization of sequences at the inhibitor and coenzyme binding sites”. The Journal of Biological Chemistry. 267 (1): 150—8. PMID 1730582.
- ^ а б Szedlacsek, SE; Duggleby, RG (1995). „Kinetics of slow and tight-binding inhibitors”. Enzyme Kinetics and Mechanism Part D: Developments in Enzyme Dynamics. Methods in Enzymology. 249. str. 144—80. ISBN 978-0-12-182150-0. PMID 7791610. doi:10.1016/0076-6879(95)49034-5.
- ^ а б Stone, SR; Morrison, JF (1986). „Mechanism of inhibition of dihydrofolate reductases from bacterial and vertebrate sources by various classes of folate analogues”. Biochimica et Biophysica Acta. 869 (3): 275—85. PMID 3511964. doi:10.1016/0167-4838(86)90067-1.
- ^ а б Pick, FM; McGartoll, MA; Bray, RC (1971). „Reaction of formaldehyde and of methanol with xanthine oxidase”. European Journal of Biochemistry / FEBS. 18 (1): 65—72. PMID 4322209. doi:10.1111/j.1432-1033.1971.tb01215.x.
- ^ а б Reardon, JE (1989). „Herpes simplex virus type 1 and human DNA polymerase interactions with 2'-deoxyguanosine 5'-triphosphate analogues. Kinetics of incorporation into DNA and induction of inhibition”. The Journal of Biological Chemistry. 264 (32): 19039—44. PMID 2553730.
- ^ а б Cohen, J.A.; Oosterbaan, R.A.; Berends, F. (1967). „[81] Organophosphorus compounds”. Enzyme Structure. Methods in Enzymology. 11. str. 686. ISBN 978-0-12-181860-9. doi:10.1016/S0076-6879(67)11085-9.
- ^ а б Brenner, G. M. (2000). Pharmacology. Philadelphia, PA: W.B. Saunders Company. ISBN 978-0-7216-7757-6.
- ^ а б Saravanamuthu, A; Vickers, TJ; Bond, CS; Peterson, MR; Hunter, WN; Fairlamb, AH (2004). „Two interacting binding sites for quinacrine derivatives in the active site of trypanothione reductase: a template for drug design”. The Journal of Biological Chemistry. 279 (28): 29493—500. PMC 3491871
 . PMID 15102853. doi:10.1074/jbc.M403187200.
. PMID 15102853. doi:10.1074/jbc.M403187200.
- ^ а б Koppitz M, Eis K; Eis (2006). „Automated medicinal chemistry”. Drug Discov. Today. 11 (11—12): 561—8. PMID 16713909. doi:10.1016/j.drudis.2006.04.005.
- ^ а б G, Scapin (2006). „Structural biology and drug discovery”. Curr. Pharm. Des. 12 (17): 2087—97. PMID 16796557. doi:10.2174/138161206777585201.
- ^ а б Gohlke H, Klebe G; Klebe (2002). „Approaches to the description and prediction of the binding affinity of small-molecule ligands to macromolecular receptors”. Angew. Chem. Int. Ed. Engl. 41 (15): 2644—76. PMID 12203463. doi:10.1002/1521-3773(20020802)41:15<2644::AID-ANIE2644>3.0.CO;2-O.
- ^ а б Glen RC, Allen SC; Allen (2003). „Ligand-protein docking: cancer research at the interface between biology and chemistry”. Curr. Med. Chem. 10 (9): 763—7. PMID 12678780. doi:10.2174/0929867033457809.
- ^ а б Allinger NL, Burkert U (1982). Molecular Mechanics. An American Chemical Society Publication. ISBN 978-0-8412-0885-8.
- ^ а б VG, Box (1997). „The Molecular Mechanics of Quantized Valence Bonds”. J Mol Model. 3 (3): 124—41. doi:10.1007/s008940050026.
- ^ а б „Sildenafil Citrate”. The American Society of Health-System Pharmacists. Pristupljeno 01. 12. 2014.
- ^ а б Peters GJ, van der Wilt CL, van Moorsel CJ, Kroep JR, Bergman AM, Ackland SP (2000). „Basis for effective combination cancer chemotherapy with antimetabolites”. Pharmacol. Ther. 87 (2—3): 227—53. PMID 11008002. doi:10.1016/S0163-7258(00)00086-3.
- ^ а б Silvaggi, N.R.; Josephine, H.R.; Kuzin, A.P.; Nagarajan, R.; Pratt, R.F.; Kelly, J.A. (2005). „Crystal structures of complexes between the R61 DD-peptidase and peptidoglycan-mimetic beta-lactams: a non-covalent complex with a "perfect penicillin"”. J.Mol.Biol. 345: 521—533. PMID 15581896. doi:10.1016/j.jmb.2004.10.076.
- ^ а б Park BK, Breckenridge AM (1981). „Clinical implications of enzyme induction and enzyme inhibition.”. Clin Pharmacokinet. 6 (1): 1—24. PMID 6113907. doi:10.2165/00003088-198106010-00001.
- ^ а б Maggi, M; Filippi, S; Ledda, F; Magini, A; Forti, G (2000). „Erectile dysfunction: from biochemical pharmacology to advances in medical therapy”. European Journal of Endocrinology. Bioscientifica. 143 (2): 143—54. PMID 10913932. doi:10.1530/eje.0.1430143.
- ^ а б McGuire, JJ (2003). „Anticancer antifolates: current status and future directions”. Current pharmaceutical design. 9 (31): 2593—613. PMID 14529544. doi:10.2174/1381612033453712.
- ^ а б „Antibiotics”. NHS. 05. 06. 2014. Pristupljeno 17. 01. 2015.
- ^ а б „Factsheet for experts”. European Centre for Disease Prevention and Control. Pristupljeno 24. 12. 2014.
- ^ а б Katz, AH; Caufield, CE (2003). „Structure-based design approaches to cell wall biosynthesis inhibitors”. Current pharmaceutical design. 9 (11): 857—66. PMID 12678870. doi:10.2174/1381612033455305.
- ^ а б Tan, Siang Yong; Tatsumura, Yvonne (01. 07. 2015). „Alexander Fleming (1881—1955): Discoverer of penicillin”. Singapore Medical Journal. 56 (7): 366—367. ISSN 0037-5675. PMC 4520913
 . PMID 26243971. doi:10.11622/smedj.2015105.
. PMID 26243971. doi:10.11622/smedj.2015105.
- ^ а б Gualerzi, Claudio O.; Brandi, Letizia; Fabbretti, Attilio; Pon, Cynthia L. (04. 12. 2013). Antibiotics: Targets, Mechanisms and Resistance. John Wiley & Sons. ISBN 9783527333059.
- ^ а б Calderon, C. B.; Sabundayo, B. P. (2007). Schwalbe, R.; Steele-Moore, L.; Goodwin, A. C., ur. Antimicrobial Classifications: Drugs for Bugs. Antimicrobial Susceptibility Testing Protocols. CRC Press. Taylor & Frances group. ISBN 978-0-8247-4100-6.
- ^ а б Srivastava A, Talaue M, Liu S, Degen D, Ebright RY, Sineva E, Chakraborty A, Druzhinin SY, Chatterjee S, Mukhopadhyay J, Ebright YW, Zozula A, Shen J, Sengupta S, Niedfeldt RR, Xin C, Kaneko T, Irschik H, Jansen R, Donadio S, Connell N, Ebright RH (2011). „New target for inhibition of bacterial RNA polymerase: 'switch region'”. Curr. Opin. Microbiol. 14 (5): 532—43. PMC 3196380
 . PMID 21862392. doi:10.1016/j.mib.2011.07.030.
. PMID 21862392. doi:10.1016/j.mib.2011.07.030.
- ^ а б Cunha, B. A. (2009). Antibiotic Essentials. Jones & Bartlett Learning. str. 180. ISBN 978-0-7637-7219-2.
- ^ а б Nicholson, Donald E. (1971). An Introduction to Metabolic Pathways by S. DAGLEY (Vol. 59, No. 2 izd.). Sigma Xi, The Scientific Research Society. str. 266.
- ^ а б Reece, Jane B. (2011). Campbell biology / Jane B. Reece ... [et al.]. (IX izd.). Boston: Benjamin Cummings. str. 143. ISBN 978-0-321-55823-7.
- ^ а б Bailey, Regina. „10 Steps of Glycolysis”.
- ^ а б Romano, AH; Conway, T (1996). „Evolution of carbohydrate metabolic pathways”. Res Microbiol. 147 (6—7): 448—55. PMID 9084754. doi:10.1016/0923-2508(96)83998-2.
- ^ а б Wegener G, Krause U (2002). „Different modes of activating phosphofructokinase, a key regulatory enzyme of glycolysis, in working vertebrate muscle”. Biochem. Soc. Trans. 30 (2): 264—270. PMID 12023862. doi:10.1042/bst0300264.
- ^ а б Raben N, Exelbert R, Spiegel R, Sherman JB, Nakajima H, Plotz P, Heinisch J (1995). „Functional expression of human mutant phosphofructokinase in yeast: genetic defects in French Canadian and Swiss patients with phosphofructokinase deficiency”. Am. J. Hum. Genet. 56 (1): 131—141. PMC 1801305
 . PMID 7825568.
. PMID 7825568.
- ^ а б Cannon, W. B. (1926). „Physiological regulation of normal states: some tentative postulates concerning biological homeostatics”. Ur.: A. Pettit(ed.). A Charles Richet : ses amis, ses collègues, ses élèves. Paris: Les Éditions Médicales. str. 91.
- ^ а б Okar, DA; Lange, AJ (1999). „Fructose-2,6-bisphosphate and control of carbohydrate metabolism in eukaryotes”. BioFactors (Oxford, England). 10 (1): 1—14. PMID 10475585. doi:10.1002/biof.5520100101.
- ^ а б Robert M. Stroud; Anthony A. Kossiakoff; John L. Chambers (1977). „Mechanisms of Zymogen Activation”. Annual Review of Biophysics and Bioengineering. 6: 177—193. doi:10.1146/annurev.bb.06.060177.001141.
- ^ а б Hans Neurath; Kenneth A. Walsh (1976). „Biochemistry Role of proteolytic enzymes in biological regulation (A Review) (limited proteolysis/zymogen activation/control mechanisms)” (PDF). Proc. Natl. Acad. Sci. USA. 73 (11): 3825—3832.
- ^ а б Rawlings ND, Barrett AJ (1994). „Families of serine peptidases”. Meth. Enzymol. Methods in Enzymology. 244: 19—61. ISBN 978-0-12-182145-6. PMID 7845208. doi:10.1016/0076-6879(94)44004-2.
- ^ а б Levilliers, J.; Péron; Arrio; Pudles (1970). „On the mechanism of action of proteolyticinhibitors: IV. Effect of 8murea on the stability of trypsin in trypsin-lnhibitor complexes”. Archives of Biochemistry and Biophysics. 140 (2): 474—483. PMID 5528741. doi:10.1016/0003-9861(70)90091-3.
- ^ а б S., Dreon M.; Ituarte S.; Heras H. (2010). „The Role of the Proteinase Inhibitor Ovorubin in Apple Snail Eggs Resembles Plant Embryo Defense against Predation”. PLoS ONE. 5 (12): e15059. PMID 21151935. doi:10.1371/journal.pone.0015059.
- ^ а б Price, Nicholas; Stevens, Lewis (1999). Fundamentals of Enzymology. Oxford University Press. ISBN 978-0-19-850229-6.
- ^ а б Smyth, TP (2004). „Substrate variants versus transition state analogues as noncovalent reversible enzyme inhibitors”. Bioorganic & Medicinal Chemistry. 12 (15): 4081—8. PMID 15246086. doi:10.1016/j.bmc.2004.05.041.
- ^ а б Hartley, RW (1989). „Barnase and barstar: two small proteins to fold and fit together”. Trends in Biochemical Sciences. 14 (11): 450—4. PMID 2696173. doi:10.1016/0968-0004(89)90104-7.
- ^ а б Serrano L, Kellis JT, Cann P, Matouschek A, Fersht AR (1992). „The folding of an enzyme. II. Substructure of barnase and the contribution of different interactions to protein stability”. J. Mol. Biol. 224 (3): 783—804. PMID 1569557. doi:10.1016/0022-2836(92)90562-X.
- ^ а б Serrano L, Matouschek A, Fersht AR (1992). „The folding of an enzyme. III. Structure of the transition state for unfolding of barnase analysed by a protein engineering procedure”. J. Mol. Biol. 224 (3): 805—18. PMID 1569558. doi:10.1016/0022-2836(92)90563-Y.
- ^ а б Matouschek A, Serrano L, Fersht AR (1992). „The folding of an enzyme. IV. Structure of an intermediate in the refolding of barnase analysed by a protein engineering procedure”. J. Mol. Biol. 224 (3): 819—35. PMID 1569559. doi:10.1016/0022-2836(92)90564-Z.
- ^ а б Oliver, CJ; Shenolikar, S (1998). „Physiologic importance of protein phosphatase inhibitors”. Frontiers in Bioscience. 3: D961—72. PMID 9727084.
- ^ а б „Types of Pesticides”. US Environmental Protection Agency. Pristupljeno 20. 02. 2013.
- ^ а б Quinn DM (1987). „Acetylcholinesterase: enzyme structure, reaction dynamics, and virtual transition states”. Chemical Reviews. 87 (5): 955—79. doi:10.1021/cr00081a005.
- ^ а б Taylor P, Radić Z (1994). „The cholinesterases: from genes to proteins”. Annual Review of Pharmacology and Toxicology. 34: 281—320. PMID 8042853. doi:10.1146/annurev.pa.34.040194.001433.
- ^ а б Katzung BG (2001). Basic and clinical pharmacology:Introduction to autonomic pharmacology (8 izd.). The McGraw Hill Companies. str. 75—91. ISBN 978-0-07-160405-5.
- ^ а б в г Sussman JL, Harel M, Frolow F, Oefner C, Goldman A, Toker L, Silman I (1991). „Atomic structure of acetylcholinesterase from Torpedo californica: a prototypic acetylcholine-binding protein”. Science. 253 (5022): 872—9. Bibcode:1991Sci...253..872S. PMID 1678899. doi:10.1126/science.1678899.
- ^ а б в г Sussman JL, Harel M, Silman I (1993). „Three-dimensional structure of acetylcholinesterase and of its complexes with anticholinesterase drugs”. Chem. Biol. Interact. 87 (1—3): 187—97. PMID 8343975. doi:10.1016/0009-2797(93)90042-W.
- ^ а б KD Tripati MD. Essentials of Medical Pharmacology (fifth izd.). Jaypee Brothers Medical Publishers(P) Ltd. str. 84. ISBN 978-81-8061-187-2.
- ^ а б Mehndiratta, Man Mohan; Pandey, Sanjay; Kuntzer, Thierry (13. 10. 2014). Acetylcholinesterase inhibitor treatment for myasthenia gravis. John Wiley & Sons, Ltd. doi:10.1002/14651858.CD006986.pub3.
- ^ а б Choices, N. H. S. (2014). „Atropine - Myasthenia-gravis medicines and drugs - NHS Choices”. Pristupljeno 11. 07. 2015.
- ^ а б Kumar, Vikas; Kaminski, Henry J. (07. 10. 2010). „Treatment of Myasthenia Gravis”. Current Neurology and Neuroscience Reports. 11 (1): 89—96. ISSN 1528-4042. PMID 20927659. doi:10.1007/s11910-010-0151-1.
- ^ а б V Priya Nair; Jennifer M Hunter (2004). „Anticholinesterases and anticholinergic drugs”. Contin Educ Anaesth Crit Care Pain. 4 (5): 164—168. doi:10.1093/bjaceaccp/mkh045.
- ^ а б J. Susan Van Dyk; Brett Pletschke (2011). „Review on the use of enzymes for the detection of organochlorine, organophosphate and carbamate pesticides in the environment”. Chemosphere. 82 (3): 291—307. doi:10.1016/j.chemosphere.2010.10.033.
- ^ а б Kambiz Soltaninejad; Mohammad Abdollahi (2009). „Current opinion on the science of organophosphate pesticides and toxic stress: a systematic review”. Med Sci Monit. 15 (3): RA75—90. eISSN 1643-3750.
- ^ а б S, Tan; Evans R; Singh B (2006). „Herbicidal inhibitors of amino acid biosynthesis and herbicide-tolerant crops”. Amino Acids. 30 (2): 195—204. PMID 16547651. doi:10.1007/s00726-005-0254-1.
- ^ а б Steinrücken HC, Amrhein N (1980). „The herbicide glyphosate is a potent inhibitor of 5-enolpyruvyl-shikimic acid-3-phosphate synthase”. Biochemical and Biophysical Research Communications. 94 (4): 1207—12. PMID 7396959. doi:10.1016/0006-291X(80)90547-1.
- ^ а б Lamberth C, Jeanmart S, Luksch T, Plant A (2013). „Current Challenges and Trends in the Discovery of Agrochemicals”. Science. 341 (6147): 742—6. PMID 23950530. doi:10.1126/science.1237227.
- ^ а б Hugh M. Brown (1990). „Mode of action, crop selectivity, and soil relations of the sulfonylurea herbicides”. 29 (3): 263—281. doi:10.1002/ps.2780290304.
- ^ а б Leonard L. Saari; Josephine C. Cotterman; Michael M. Primiani (1990). „Mechanism of Sulfonylurea Herbicide Resistance in the Broadleaf Weed, Kochia scoparia” (PDF). Plant Physiology. 93 (1): 55—61. PMID 16667465.
- ^ а б E. Patrick Fuerst (1987). „Understanding the Mode of Action of the Chloroacetamide and Thiocarbamate Herbicides”. Weed Technology. 1 (4): 270—277.
- ^ а б Frosch, S.; Jabben, M.; Bergfeld, R.; H. Kleinig; H. Mohr (1979). „Inhibition of carotenoid biosynthesis by the herbicide SAN 9789 and its consequences for the action of phytochrome on plastogenesis”. Planta. 145: 497. doi:10.1007/BF00380105.
- ^ а б SO, Duke (1990). „Overview of herbicide mechanisms of action”. Environ. Health Perspect. Brogan. 87: 263—71. JSTOR 3431034. PMC 1567841
 . PMID 1980104. doi:10.2307/3431034.
. PMID 1980104. doi:10.2307/3431034.
- ^ а б „Secondary metabolites - Knowledge Encyclopedia”. www.biologyreference.com. Pristupljeno 10. 05. 2016.
- ^ а б Tan, G; Gyllenhaal, C; Soejarto, DD (2006). „Biodiversity as a source of anticancer drugs”. Current drug targets. 7 (3): 265—77. PMID 16515527. doi:10.2174/138945006776054942.
- ^ а б Laurie C. Dolan; Ray A. Matulka; George A. Burdock (2010). „Naturally Occurring Food Toxins”. Toxins. Basel. 2 (9): 2289—2332. PMID 3153292. doi:10.3390/toxins2092289.
- ^ а б Bal Ram Singh; Anthony T. Tu, ur. (1996). Natural Toxins 2: Structure, Mechanism of Action, and Detection (NATO Asi Series) (v. 2). Springer. ISBN 978-0-06-093436-1.
- ^ а б Peltier, Sandra; Oger, Jean-Michel; Lagarce, Frédéric; Couet, William; Benoît, Jean-Pierre (2006). „Enhanced Oral Paclitaxel Bioavailability After Administration of Paclitaxel-Loaded Lipid Nanocapsules”. Pharmaceutical Research. 23 (6): 1243—50. PMID 16715372. doi:10.1007/s11095-006-0022-2.
- ^ а б Abal, M; Andreu, JM; Barasoain, I (2003). „Taxanes: microtubule and centrosome targets, and cell cycle dependent mechanisms of action”. Current cancer drug targets. 3 (3): 193—203. PMID 12769688. doi:10.2174/1568009033481967.
- ^ а б Bharadwaj, Rajnish; Yu, Hongtao (2004). „The spindle checkpoint, aneuploidy, and cancer”. Oncogene. 23 (11): 2016—27. PMID 15021889. doi:10.1038/sj.onc.1207374.
- ^ а б Brito, D. A.; Yang, Z.; Rieder, C. L. (2008). „Microtubules do not promote mitotic slippage when the spindle assembly checkpoint cannot be satisfied”. The Journal of Cell Biology. 182 (4): 623—9. PMC 2518701
 . PMID 18710927. doi:10.1083/jcb.200805072.
. PMID 18710927. doi:10.1083/jcb.200805072.
- ^ а б Hostettmann, K.; Borloz, A.; Urbain, A.; Marston, A. (2006). „Natural Product Inhibitors of Acetylcholinesterase”. Current Organic Chemistry. 10 (8): 825—847. doi:10.2174/138527206776894410.
- ^ а б Mendel Friedman (2006). „Potato Glycoalkaloids and Metabolites: Roles in the Plant and in the Diet”. J. Agric. Food Chem. 54 (23): 8655—8681. doi:10.1021/jf061471t.
- ^ а б Defrates, LJ; Hoehns, JD; Sakornbut, EL; Glascock, DG; Tew, AR (2005). „Antimuscarinic intoxication resulting from the ingestion of moonflower seeds”. The Annals of pharmacotherapy. 39 (1): 173—6. PMID 15572604. doi:10.1345/aph.1D536.
- ^ а б Hallen, H.; Luo; J.S. Scott-Craig; J.D. Walton (2007). „A gene family encoding the major toxins of lethal Amanita mushrooms.”. Proceedings of the National Academy of Sciences of the United States of America. 104 (48): 19097—19101. PMC 2141914
 . PMID 18025465. doi:10.1073/pnas.0707340104.
. PMID 18025465. doi:10.1073/pnas.0707340104.
- ^ а б Vetter, J (1998). „Toxins of Amanita phalloides”. Toxicon. 36 (1): 13—24. PMID 9604278. doi:10.1016/S0041-0101(97)00074-3.
- ^ а б Holmes, CF; Maynes, JT; Perreault, KR; Dawson, JF; James, MN (2002). „Molecular enzymology underlying regulation of protein phosphatase-1 by natural toxins”. Current medicinal chemistry. 9 (22): 1981—9. PMID 12369866. doi:10.2174/0929867023368827.
- ^ а б Bischoff, K (2001). „The toxicology of microcystin-LR: occurrence, toxicokinetics, toxicodynamics, diagnosis and treatment”. Veterinary and human toxicology. 43 (5): 294—7. PMID 11577938.
- ^ а б Waghmare; Chougule P.; Kanase A. (2004). „Extract of Ricinus communis leaves mediated alterations in liver and kidney functions against single dose of CCl
4 induced liver necrosis in albino rats.”. Journal of Ecophysiology and Occupational Health. 4 (3—4): 169—173. ISSN 0972-4397.|first1=zahteva|last1=u Authors list (pomoć) - ^ а б Sabina E.P.; Rasool M.K.; Mathew L.; Parameswari (2009). „Studies on the protective effect of Ricinus communis leaves extract on carbon tetrachloride hepatotoxicity in albino rats”. Pharmacologyonline. 2: 905—916. ISSN 1827-8620.
- ^ а б Anuradha; Parameswari C.S. (2003). „Protective effect of Ricinus communis leaf extract against paracetamol-induced hepatotoxicity”. Biomedicine. 23 (1—2): 97—105.
|first1=zahteva|last1=u Authors list (pomoć) - ^ а б Henrissat B, Callebaut I, Mornon JP, Fabrega S, Lehn P, Davies G (1995). „Conserved catalytic machinery and the prediction of a common fold for several families of glycosyl hydrolases”. Proc. Natl. Acad. Sci. U.S.A. 92 (15): 7090—7094. PMC 41477
 . PMID 7624375. doi:10.1073/pnas.92.15.7090.
. PMID 7624375. doi:10.1073/pnas.92.15.7090.
- ^ а б Henrissat B, Davies G (1995). „Structures and mechanisms of glycosyl hydrolases”. Structure. 3 (9): 853—859. PMID 8535779. doi:10.1016/S0969-2126(01)00220-9.
- ^ а б Hartley, MR; Lord, JM (2004). „Cytotoxic ribosome-inactivating lectins from plants”. Biochimica et Biophysica Acta. 1701 (1—2): 1—14. PMID 15450171. doi:10.1016/j.bbapap.2004.06.004.
- ^ а б Angelique Y. Louie; Thomas J. Meade (1999). „Metal Complexes as Enzyme Inhibitors”. Chem. Rev. 99: 2711—2734. doi:10.1021/cr9804285.
- ^ а б Waldron, K. J.; Robinson, N. J. (2009). „How do bacterial cells ensure that metalloproteins get the correct metal?”. Nat. Rev. Microbiol. 7 (1): 25—35. PMID 19079350. doi:10.1038/nrmicro2057.
- ^ а б Thomson, A. J.; Gray, H. B. (1998). „Bioinorganic chemistry”. Current Opinion in Chemical Biology. 2: 155—158. doi:10.1016/S1367-5931(98)80056-2.
- ^ а б Banci, Lucia (2013). Sigel, Astrid; Sigel, Helmut; Sigel, Roland K. O., ur. Metallomics and the Cell. Springer. ISBN 978-94-007-5561-1. ISSN 1868-0402.
- ^ а б Shriver, D. F.; Atkins, P. W. (1999). „Chapter 19, Bioinorganic chemistry”. Inorganic chemistry (III izd.). Oxford University Press. ISBN 978-0-19-850330-9.
- ^ а б Lippard, S. J. (1994). Bertini, I.; Gray, H. B.; Lippard, S. J.; Valentine, J. S., ur. Bioinorganic Chemistry (PDF). Mill Valle, CA,: University Science Books.
- ^ а б Lippard, S. (1996). Sigel, A.; Sigel, H., ur. „Metal ions in Biology”. 32. New York: M. Dekker.
- ^ а б Aull, J. L. (1980). Interactions of anticancer drugs with enzymes. New York: Marcel Dekker. ISSN 0161-5149.
- ^ а б в г Mital, R.; Shah, G. M.; Srivastava, T. S.; Bhattacharya, R. K. (1992). „The effect of some new platinum (II) and palladium (II) coordination complexes on rat hepatic nuclear transcription in vitro”. Life Sci. 50: 781—790. PMID 1371326. doi:10.1016/0024-3205(92)90183-P.
- ^ а б в г Kelley, T. J.; Moghaddas, S.; Bose, R.; Basu, S. (1993). „Inhibition of immunopurified DNA polymerase-alpha from PA-3 prostate tumor cells by platinum (II) antitumor drugs”. Cancer Biochem. Biophys. 13: 135—146. PMID 8111727.
- ^ а б в г д Endo, T.; Takahashi, M.; Minami, M.; Yoshioka, M.; Saito, H.; Parvez, S. H. (1993). „Effects of anticancer drugs on enzyme activities and serotonin release from ileal tissue in ferrets”. Biogen. Amines. 9: 479—489. ISSN 0168-8561.
- ^ а б в г Ganeva, R. L.; Spassovska, N. C.; Genchev, D. D. J. (1991). „The effect of some platinum compounds on the activity of the CTP synthetase of Ehrlich ascites tumor cells: in vitro and in vivo studies”. Inorg. Biochem. 43: 717—722. PMID 1779227. doi:10.1016/0162-0134(91)80042-G.
- ^ а б в г Koch, T.; Gloddek, B. (1991). „Inhibition of adenylate-cyclase-coupled G protein complex by ototoxic diuretics and cis-platinum in the inner ear of the guinea pig”. Eur. Arch. Oto-Rhino-Laryngol. 248: 459—464. PMID 1662964. doi:10.1007/BF00627634.
- ^ а б в г д ђ Ho, B. T.; Huo, Y. Y.; Lee, J. H.; Levin, V. A. (1991). „Inhibition of adenylate cyclase by tetraplatin”. Anti-Cancer Drugs. 2: 267—268. PMID 1802021. doi:10.1097/00001813-1991.
- ^ а б в Rosen, M.; Figliomeni, M.; Simpkins, H. (1992). „The interaction of platinum antitumor drugs with mouse liver mitochondria”. Int. J. Exp. Pathol. 73: 61—74. ISSN 0959-9673. PMC 2002465
 .
.
- ^ а б в г д ђ е ж Wright, J. A.; Chan, A. K.; Choy, B. K.; Hurta, R. A. R.; McClarty, G. A.; Tagger, A. Y. (1990). „Regulation and drug resistance mechanisms of mammalian ribonucleotide reductase, and the significance to DNA synthesis”. Cell. Biol. 68: 1364—1371. PMID 2085432.
- ^ а б в г д ђ Oblender, M.; Carpentieri, U. (1990). „Effects of iron, copper and zinc on the activity of ribonucleotide reductase in normal and leukemic human lymphocytes”. Anticancer Res. 10: 123—128. PMID 2185685.
- ^ а б в г д ђ Myette, M. S.; Elford, H. L.; Chitambar, C. R. (1998). „Interaction of gallium nitrate with other inhibitors of ribonucleotide reductase: effects on the proliferation of human leukemic cells”. Cancer Lett. 129: 199—204. PMID 9719462. doi:10.1016/S0304-3835(98)00104-9.
- ^ а б в г д ђ Chitambar, C. R.; Narasimhan, J. (1991). „Targeting Iron-Dependent DNA Synthesis with Gallium and Transferrin-Gallium”. Pathobiology. 59: 3—10. PMID 1645976.
- ^ а б в г д ђ Chitambar, C. R.; Narasimhan, J.; Guy, J.; Sem, D. S.; O’Brien, W. J. (1991). „Inhibition of ribonucleotide reductase by gallium in murine leukemic L1210 cells”. Cancer Res. 51: 6199—6201. PMID 1933878.
- ^ а б в г Nocentini, G.; Federici, F.; Grifantini, M.; Barzi, A. (1992). „2,2'-Bipyridyl-6-carbothioamide and Its Ferrous Complex: Their in Vitro Antitumoral Activity Related to the Inhibition of Ribonucleotide Reductase R2 Subunit” (PDF). Pharmacol. Res. 25: 312—313. PMID 8416745.
- ^ а б в г д ђ Nocentini, G.; Barzi, A. (1996). „The 2,2′-Bipyridyl-6-carbothioamide copper (II) complex differs from the iron (II) complex in its biochemical effects in tumor cells, suggesting possible differences in the mechanism leading to cytotoxicity”. Biochem. Pharm. 52: 65—71. PMID 8678909. doi:10.1016/0006-2952(96)00139-6.
- ^ а б в г д ђ West, D. X.; Liberta, A. E. (1993). „The cytotoxicity of copper(II) complexes of heterocyclic thiosemicarbazones and 2-substituted pyridine N-oxides”. Coord. Chem. Rev. 123: 49— 71. PMID 8098234.
- ^ а б в г д ђ Monti, E.; Monzini, F.; Morazzoni, F.; Perletti, G.; Piccini, F. (1993). „Interaction of Cu(II) and Cu(II)-anthracycline complexes with protein kinase C. Spectromagnetic assessment of the inhibitory effect”. Inorg. Chim. Acta. 205: 181—184. doi:10.1016/S0020-1693(00)85536-X.
- ^ а б в г д ђ е ж Gopalakrishna, R.; Gundimeda, U.; Chen, Z. H. (1997). „Cancer-Preventive Selenocompounds Induce a Specific Redox Modification of Cysteine-Rich Regions in Ca2+- Dependent Isoenzymes of Protein Kinase C”. Arch. Biochem. Biophys. 348: 25—36. PMID 9390171. doi:10.1006/abbi.1997.0334.
- ^ а б в г Gopalakrishna, R.; Chen, Z. H.; Gundimeda, U. (1997). „Selenocompounds Induce a Redox Modulation of Protein Kinase C in the Cell, Compartmentally Independent from Cytosolic Glutathione: Its Role in Inhibition of Tumor Promotion”. Arch. Biochem. Biophys. 348: 37—48. PMID 9390172. doi:10.1006/abbi.1997.0335.
- ^ а б в г д ђ е ж Kuo, L. Y.; Liu, A. H.; Marks, T. J. (1996). Sigel, A.; Sigel, H., ur. Metal Ions in biological systems. 33. New York: M. Dekker.
- ^ а б в г д Harding, M. M.; Long, G. V. (1997). „Solution conformation of the antitumor drug streptonigrin”. Curr. Med. Chem. 4: 405—420. PMID 8230091. doi:10.1021/jm00073a003.
- ^ а б в г Perry, D. K.; Smyth, M. J.; Stennicke, H. R.; Salvesen, G. S.; Duriez, P.; Poiriez, G. G.; Hannun, Y. A. (1997). „Zinc Is a Potent Inhibitor of the Apoptotic Protease, Caspase-3 - A novel target for zink in the inhibition of apoptosis”. J. Biol. Chem. 30: 18530—18533. PMID 9228015. doi:10.1074/jbc.272.30.18530.
- ^ а б в г Maret, W.; Jacob, C.; Vallee, B. L.; Fischer, E. H. (1999). „Inhibitory sites in enzymes: Zinc removal and reactivation by thionein”. Proc. Natl. Acad. Sci. 96: 1936—1940. PMID 10051573. doi:10.1073/pnas.96.5.1936.
- ^ а б в г Shlyakhovenko, V. A.; Milinevskaya, V. A.; Zagorujko, L. I.; Yanish, Y. V.; Kozak, V. V.; Kokozey, V. N.; Chernova, A. S. (1997). „Antitumor activity of some gallium-containing coordination compounds”. Exp. Oncol. 19: 348—352. ISSN 0204-3564.
- ^ а б в г д ђ Morinville, A.; Maysinger, D.; Shaver, A. (1998). „From Vanadis to Atropos: vanadium compounds as pharmacological tools in cell death signalling”. Trends Pharmacol. Sci. 19: 452—460. PMID 9850609. doi:10.1016/S0165-6147(98)01257-7.
- ^ а б в г Faure, R.; Vincent, M.; Dufour, M.; Shaver, A.; Posner, B. I. J. (1995). „Arrest at the G2/M transition of the cell cycle by protein-tyrosine phosphatase inhibition: Studies on a neuronal and a glial cell line”. Cell Biochem. 58: 389—401. PMID 8567756. doi:10.1002/jcb.240590310.
- ^ а б в г Zhuo, S.; Dixon, J. E. (1997). „Effects of sulfhydryl regents on the activity of lambda Ser/Thr phosphoprotein phosphatase and inhibition of the enzyme by zinc ion”. Protein Eng. 10: 1445—1452. PMID 9543006.
- ^ а б в г д ђ Cha, J.; Pedersen, M. V.; Auld, D. S. (1996). „Metal and pH dependence of heptapeptide catalysis by human matrilysin”. Biochemistry. 35: 15831—13838. PMID 8961947. doi:10.1021/bi962085f.
- ^ а б в г Nocentini, G.; Barzi, A. (1997). „Antitumor activity of 2,2′-bipyridyl-6-carbothioamide: a ribonucleotide reductase inhibitor”. Gen. Pharmac. 29: 701—706. PMID 9347313. doi:10.1016/S0306-3623(97)00011-6.
- ^ а б Byrnes, R. W.; Mohan, M.; Antholine, W. E.; Xe, R. X.; Petering, D. H. (1990). „Oxidative stress induced by a copper-thiosemicarbazone complex”. Biochemistry. 29: 7046—7053. PMID 2171640. doi:10.1021/bi00482a014.
- ^ а б Hubbard, S. R.; Bishop, W. R.; Kirschmeier, P.; George, S. J.; Cramer, S. P.; Hendrickson, W. A. (1991). „Identification and characterization of zinc binding sites in protein kinase C”. Science. 254: 1776—1779. PMID 1763327. doi:10.1126/science.1763327.
- ^ а б в г V. Ashutosh Raocorresponding (10. 03. 2013). „Iron Chelators with Topoisomerase-Inhibitory Activity and Their Anticancer Applications”. Antioxid Redox Signal. 18 (8): 930—955. PMC 3557438
 . doi:10.1089/ars.2012.4877.
. doi:10.1089/ars.2012.4877.
- ^ а б Köpf-Maier, P.; Köpf, H. (1987). „Non-platinum group metal antitumor agents. History, current status, and perspectives”. Chem. Rev. 87: 1137—1152. doi:10.1021/cr00081a012.
- ^ а б в г Harding, M. M.; Prodigalidad, M.; Lynch, M. J. (1996). „Organometallic Anticancer Agents. 2. Aqueous Chemistry and Interaction of Niobocene Dichloride with Nucleic Acid Constituents and Amino Acids”. J. Med. Chem. 39: 5012—5016. PMID 8960562. doi:10.1021/jm9603678.
- ^ а б Harding, M. M.; Mokdsi, G.; Mackay, J. P.; Prodigalidad, M.; Lucas, C. W. (1998). „Interactions of the Antitumor Agent Molybdocene Dichloride with Oligonucleotides”. Inorg. Chem. 37: 2432—2437. doi:10.1021/ic971205k.
- ^ а б в Takahashi, A.; Alnemri, E. S.; Lazebnik, Y. A.; Fernandes-Alnemri, T.; Litwack, G.; Moir, R. D.; Goldman, R. D.; Poirier, G. G.; Kaufmann, S. G.; Earnshaw, W. C. (1996). „Cleavage of lamin A by Mch2 alpha but not CPP32: multiple interleukin 1 beta-converting enzyme-related proteases with distinct substrate recognition properties are active in apoptosis”. PNAS. 93: 8395—8400. PMID 38682.
- ^ а б Krynetskaya, N. F.; Kubareva, E. A.; Timchenko, M. A.; Belkov, V. M.; Shabarova, Z. A. (1998). „Transition-metal complexes as inhibitors of proteins recognizing double-stranded fragments of nucleic acids”. Biochemistry (Moscow). 63: 1068—1073. PMID 9795277.
- ^ а б Shao, H. S.; Meinken, G. E.; Srivastava, S. C.; Slosman, D.; Slacker, D. F.; Som, P.; Brill, A. B. (1986). „In-vitro and in-vivo characterization of ruthenium-bleomycin compared to cobalt- i copper-BLEOMYC” (PDF). J. Nucl. Med. 27: 1044—1045.
- ^ а б Scheich, L. A.; Gosling, P.; Brown, S. J.; Olmstead, M. M.; Mascharak, P. K. (1991). „Synthetic analog approach to metallobleomycins: possibility of coordination of the carboxamide group of the .beta.-aminoalaninamide moiety of bleomycin to copper in copper(II) bleomycin at physiological pH”. Inorg. Chem. 30: 1677—1680. doi:10.1021/ic00007a052.
- ^ а б в г Sacerdoti D, Escalante B, Abraham NG, McGiff JC, Levere RD, Schwartzman ML (1989). „Treatment with Tin Prevents the Development of Hypertension in Spontaneously Hypertensive Rats”. Science. 243: 388—90. PMID 2492116.
- ^ а б в г д Maines, M.; Trakshel, G. (1992). „Tin-protoporphyrin: a potent inhibitor of hemoprotein-dependent steroidogenesis in rat adrenals and testes”. J. Pharmacol. Exp. Ther. 260: 909—916. PMID 1371161.
- ^ а б в г д Trakshel, G.; Sluss, P.; Maines, M. (1992). „Comparative effects of tin- and zinc-protoporphyrin on steroidogenesis: tin-protoporphyrin is a potent inhibitor of cytochrome P-450-dependent activities in the rat adrenals”. Pediatr. Res. 31: 196—201. PMID 1542552. doi:10.1203/00006450-199202000-00022.
- ^ а б в Maines, M.; Trakshel, G. (1992). „Differential regulation of heme oxygenase isozymes by Sn- and Zn-protoporphyrins: possible relevance to suppression of hyperbilirubinemia”. Biochim. Biophys. Acta. 1131: 166—174. PMID 1610897. doi:10.1016/0167-4781(92)90072-8.
- ^ а б в Böni, R. E.; Boni, R. A.; Galbraith, R. A.; Drummond, G. S.; Kappas, A. (1993). „Tin-mesoporphyrin inhibits heme oxygenase activity and heme-iron absorption in the intestine”. Pharmacology. 47: 318—329. PMID 8265722.
- ^ а б в Robert A. Johnson; Manuel Lavesa; Bardia Askari; Nader G. Abraham; Alberto Nasjletti (1995). „A Heme Oxygenase Product, Presumably Carbon Monoxide, Mediates a Vasodepressor Function in Rats”. Hypertension. 25: 166—169. PMID 7843765. doi:10.1161/01.HYP.25.2.166.
- ^ а б в Russo, S.; Pepe, J.; Donohue, S.; Cable, E.; Lambrecht, R.; Bonkovsy, H. (1995). „Tissue distribution of zinc-mesoporphyrin in rats: relationship to inhibition of heme oxygenase”. J. Pharmacol. Exp. Ther. 272: 766—774. PMID 7853192.
- ^ а б в г Keino, H.; Banno, T.; Mimura, S.; Kashiwamata, S. (1993). „Cobalt-Mesoporphyrin Inhibits Heme Oxygenase Activity but It Does Not Induce Lipid Peroxidation in Rat Brain Membranes during Photoirradiation”. Biol. Neonate. 63: 285—289. PMID 8353156. doi:10.1159/000243943.
- ^ а б в г Vallier, H.; Rodgers, P.; Stevenson, D. (1993). „Inhibition of heme oxygenase after oral vs intraperitoneal administration of chromium porphyrins”. Life Sci. 52: PL79—PL84. PMID 8445977. doi:10.1016/0024-3205(93)90521-4.
- ^ а б в Drummond, G.; Rosenberg, D.; Kappas, A. (1992). „Intestinal heme oxygenase inhibition and increased biliary iron excretion by metalloporphyrins”. Gastroenterology. 102: 1170—1175. PMID 1551526. doi:10.1016/0016-5085(92)70011-Y.
- ^ а б в г Galbraith, R.; Drummond, G.; Kappas, A. (1992). „Suppression of Bilirubin Production in the Crigler-Najjar Type I Syndrome: Studies with the Heme Oxygenase Inhibitor Tin-Mesoporphyrin”. Pediatrics. 89: 175—182. PMID 1734381.
- ^ а б в Angelique Y. Louie; Thomas J. Meade (1999). „Metal Complexes as Enzyme Inhibitors”. Chemical Reviews. 99 (9): 2711—2734. doi:10.1021/cr9804285.
- ^ Cannon, J. B. (1993). „Pharmaceutics and drug delivery aspects of heme and porphyrin therapy”. J. Pharm. Sci. 82: 435—446. PMID 8360819. doi:10.1002/jps.2600820502.
- ^ а б Tsangaris, J. M.; Williams, D. R. (1992). „Tin in pharmacy and nutrition”. Appl. Organomet. Chem. 6: 3—18. PMID 11192741. doi:10.1002/aoc.590060103.
- ^ Marks, J. A.; Maines, M. D. (1992). „Tin-Protoporphyrin-Mediated Disruption In Vivo of Heme Oxygenase-2 Protein Integrity and Activity in Rat Brain” (PDF). Pediatr. Res. 32: 324—329. PMID 1408470. doi:10.1203/00006450-199209000-00016.
- ^ Hintz, S. R.; Vreman, H. J.; Stevenson, D. K. (1990). „Mortality of metalloporphyrin-treated neonatal rats after light exposure”. Dev. Pharmacol. 14: 187—192. PMID 2364856.
- ^ Cable, E.; Cable, J.; Bonkovsky, H. (1993). „Repression of hepatic δ-aminolevulinate synthase by heme and metalloporphyrins: Relationship to inhibition of heme oxygenase”. Hepatology. 18: 119—127. PMID 8325603. doi:10.1002/hep.1840180119.
- ^ Lathrop, J. T.; Timko, M. P. (1993). „Regulation by heme of mitochondrial protein transport through a conserved amino acid moti”. Science. 259: 522—525. PMID 8424176. doi:10.1126/science.8424176.
- ^ Bhasker, C. R.; Burgiel, G.; Neupert, B.; Emery-Goodman, A.; Kuhn, L. C.; May, B. K. (1993). „The Putative Iron-Responsive Element in the Human Erythroid 5-Aminolevulinate Synthase mRNA Mediates Translational Control” (PDF). JBC. 268: 12699—12705. PMID 8509404.
- ^ а б Serfass, L.; Burstyn, J. (1998). „Effect of heme oxygenase inhibitors on soluble guanylyl cyclase activity”. Arch. Biochem. Biophys. 359: 8—16. PMID 9799554. doi:10.1006/abbi.1998.0887.
- ^ а б Luo, D.; Vincent, S. (1994). „Metalloporphyrins inhibit nitric oxide-dependent cGMP formation in vivo”. Eur. J. Pharmacol.-Mol. Pharmacol. Sec. 267: 263—267. PMID 7522180. doi:10.1016/0922-4106(94)90149-X.
- ^ а б в г д Mariotto, S.; Cuzzolin, L.; Adami, A.; DelSoldato, P.; Suzuki, H.; Benoni, G. (1995). „Inhibition by sodium nitroprusside of the expression of inducible nitric oxide synthase in rat neutrophils”. Brit. J. Pharmacol. 114: 1105—1106. PMID 7542530. doi:10.1111/j.1476-5381.1995.tb13320.x.
- ^ а б Vickroy, T.; Malphurs, W. (1995). „Inhibition of nitric oxide synthase activity in cerebral cortical synaptosomes by nitric oxide donors: evidence for feedback autoregulation”. Neurochem. Res. 20: 299—304. PMID 7541898. doi:10.1007/BF00969546.
- ^ а б в Perry, J.; Marletta, M. (1998). „Effects of transition metals on nitric oxide synthase catalysis”. PNAS. 95: 11101—11106. PMID 9736696. doi:10.1073/pnas.95.19.11101.
- ^ а б Persechini A, McMillan K, Masters BS (1995). „Inhibition of Nitric Oxide Synthase Activity by Zn2+ Ion”. Biochemistry. 34: 15091—15095. PMID 7578122. doi:10.1021/bi00046a015.
- ^ а б Siegfried, G.; Amiel, C.; Friedlander, G. (1996). „Inhibition of Ecto-5′-nucleotidase by Nitric Oxide Donors”. J. Biol. Chem. 271: 4659—4664. PMID 8617729.
- ^ а б в Thomas, S.; Mohr, D.; Stocker, R. (1994). „Nitric oxide inhibits indoleamine 2,3-dioxygenase activity in interferon-gamma primed mononuclear phagocytes” (PDF). J. Biol. Chem. 269: 14457—14464. PMID 7514170.
- ^ а б в г Nicolaou, A.; Waterfield, C.; Kenyon, S.; Gibbons, W. (1997). „The Inactivation of Methionine Synthase in Isolated Rat Hepatocytes by Sodium Nitroprusside”. Eur. J. Biochem. 244: 8876—882. PMID 9108260. doi:10.1111/j.1432-1033.1997.00876.x.
- ^ а б Sato, T.; Kamata, Y.; Irifune, M.; Nishikawa, T. (1995). „Inhibition of purified (Na+,K+)-ATPase activity from porcine cerebral cortex by NO generating drugs”. Brain Res. 704: 117—120. PMID 8750971. doi:10.1016/0006-8993(95)01165-X.
- ^ Bredt, D. S.; Snyder, S. H. (1992). „Nitric oxide, a novel neuronal messenger”. Neuron. 8: 3—11. PMID 1370373. doi:10.1016/0896-6273(92)90104-L.
- ^ Jaffrey, S. R.; Snyder, S. H. (1996). „PIN: An associated protein inhibitor of neuronal nitric oxide synthase”. Science. 274: 774—777. PMID 8864115. doi:10.1126/science.274.5288.774.
- ^ а б Marletta, M. A. (1994). „Nitric oxide synthase: Aspects concerning structure and catalysis” (PDF). Cell. 78: 927—930. PMID 7522970. doi:10.1016/0092-8674(94)90268-2.
- ^ а б Moore, P. K.; Handy, R. L. C. (1997). „Selective inhibitors of neuronal nitric oxide synthase – is no NOS really good NOS for the nervous system?”. Trends Pharm. Sci. 18: 204— 211. PMID 9226999. doi:10.1016/S0165-6147(97)01064-X.
- ^ Bredt, D. S.; Snyder, S. H. (1990). „Isolation of nitric oxide synthetase, a calmodulin-requiring enzyme”. PNAS. 87: 682—685. PMID 1689048. doi:10.1073/pnas.87.2.682.
- ^ а б Weiss, G.; Lutton, J.; Fuchs, D.; Wernerfelmayer, G.; Bock, G.; Abraham, N.; Kappas, A.; Levere, R.; Wachter, H. (1993). „Comparative Effects of Heme and Metalloporphyrins on Interferon-γ-Mediated Pathways in Monocytic Cells (THP-1)”. Proc. Soc. Exp. Biol. Med. 202: 470—475. PMID 8456113. doi:10.3181/00379727-202-43561.
- ^ а б Meffert, M.; Haley, J.; Schulman, E.; Schulman, H.; Madison, D. (1994). „Inhibition of hippocampal heme oxygenase, nitric oxide synthase, and long-term potentiation by metalloporphyrins”. Neuron. 13: 1225—1233. PMID 7524564. doi:10.1016/0896-6273(94)90060-4.
- ^ а б Bing, O.; Grundemar, L.; Ny, L.; Moller, C.; Heilig, M. (1995). „Modulation of carbon monoxide production and enhanced spatial learning by tin protoporphyrin”. Neuroreport. 6: 1369—1372. PMID 7488726. doi:10.1097/00001756-199507100-00002.
- ^ а б в Pedregosa, J. C.; Casanova, J.; Alzuet, G.; Borras, J.; Garcia-Granda, S.; Diaz, M. R.; Guttierez-Rodriguez, A. (1995). „Metal complexes of 5-tertbutyloxycarbonylamido-1,3,4-thiadiazole-2-sulfonamide (B-H2ats), a carbonic anhydrase inhibitor. Synthesis and characterization of the copper(II) complex. Crystal structures of B-H2ats and the [Cu(B-ats)(NH3)2]2 dimer complex”. Inorg. Chim. Acta. 232: 117—124. doi:10.1016/0020-1693(94)04376-7.
- ^ а б Supuran, C. T.; Mincione, F.; Scozzafava, A.; Briganti, F.; Mincione, G.; Ilies, M. A. (1998). „Carbonic anhydrase inhibitors — Part 52. Metal complexes of heterocyclic sulfonamides: A new class of strong topical intraocular pressure-lowering agents in rabbits”. Eur. J. Med. Chem. 22: 247—254. doi:10.1016/S0223-5234(98)80059-7.
- ^ а б в Supuran CT, Scozzafava A, Saramet I, Banciu MD (1998). „Carbonic anhydrase inhibitors: inhibition of isozymes I, II and IV with heterocyclic mercaptans, sulfenamides, sulfonamides and their metal complexes”. J. Enzyme Inhib. 13: 177—194. PMID 9629536. doi:10.3109/14756369809028339.
- ^ а б Turkmen H, Durgun M, Yilmaztekin S, Emul M, Innocenti A, Vullo D, Scozzafava A, Supuran CT (1997). „Carbonic anhydrase inhibitors. Part 50. Interaction of isoenzymes I and II of carbonic anhydrase with Ge(IV) and Sb(III) derivatives”. Main Group Met. Chem. 20: 641—647. PMID 15603956. doi:10.1016/j.bmcl.2004.10.070.
- ^ а б Supuran, C. T. (1996). „Complexes with biologically active ligands. Part 3. Synthesis of coordination compounds of chlorothiazide with divalent metal ions”. Main Group Met. Chem. 19: 347—353. doi:10.1515/MGMC.1996.19.6.339.
- ^ а б Koppenho¨fer, A.; Hartmann, U.; Vahrenkamp, H. (1995). „Zinc Complexes of Drugs Containing Nitrogen Heterocycles”. Chem. Ber. 128: 779—785. doi:10.1002/cber.19951280807.
- ^ а б Gonzalez, E. B.; Farkas, E.; Soudi, A. A.; Tan, T.; Yanovsky, A. I.; Nolan, K. B. (1997). „Metal complexes of the angiotensin-converting enzyme inhibitor,lisinopril. Solution studies and the crystal and molecular structure ofa dimeric copper(II)-lisinopril complex”. J. Chem. Soc., Dalton Trans.: 2377—2379. doi:10.1039/A701500C.
- ^ а б Abrams MJ, Murrer BA (1993). „Metal compounds in therapy and diagnosis”. Science. 261: 725—730. PMID 8102010. doi:10.1126/science.8102010.
- ^ Sly WS, Hu PY (1995). „Human carbonic anhydrases and carbonic anhydrase deficiencies”. Annu. Rev. Biochem. 64: 375—401. PMID 7574487. doi:10.1146/annurev.bi.64.070195.002111.
- ^ Bergenhem, N. (1996). „Chromatographic and electrophoretic methods related to the carbonic anhydrase isozymes”. J. Chromatogr. B. 684: 289—305. PMID 8906478. doi:10.1016/0378-4347(95)00566-8.
- ^ Albert, D. M.; Jakobiec, F. M., ur. (1994). Principles and practice of ophthalmology. Philadelphia: W. B. Saunders. ISBN 978-0-7216-3416-6.
- ^ Heagerty, A. M. (1991). „Functional and structural effects of ACE inhibitors on the cardiovascular system”. Cardiology. 79: 3—9. PMID 1913721. doi:10.1159/000174899.
- ^ Kureya, P.; Beevers, D. G. (1991). „The mechanisms of hypertension and the role of ACE inhibitors”. J. Human Hypertension. 5: 3—8. PMID 1791616.
- ^ Pandurangi, R. S.; Katti, K. V.; Stillwell, L.; Barnes, C. L. (1998). „Retention of Inhibitory Potency of an ACE Inhibitor Conjugated with Rh(III) and Pd(II) (Iminophosphorano)phosphines. Synthesis and X-ray Structural Investigations”. J. Am. Chem Soc. 120: 11364—11373. doi:10.1021/ja9802403.
- ^ а б Bagger, S. (1993). „The binding of cobalt(III)-ligated amino acids and peptides to chymotrypsin and trypsin”. J. Inorg. Biochem. 52: 165—171. PMID 8254339.
- ^ а б в Bagger, S.; Wagner, K. J. (1998). „Molecular recognition of cobalt(III)-ligated peptides by serine proteases: the role of electrostatic effects”. Peptide Res. 52: 273—282. PMID 9832305. doi:10.1111/j.1399-3011.1998.tb01241.x.
- ^ а б Takeuchi, T.; Bottcher, A.; Quezada, C.; Simon, M.; Meade, T.; Gray, H. (1998). „Selective Inhibition of Human α-Thrombin by Cobalt(III) Schiff Base Complexes”. J. Am. Chem. Soc. 120: 8555—8556. doi:10.1021/ja981191x.
- ^ а б Böttcher, A.; Takeuchi, T.; Hardcastle, K.; Meade, T.; Gray, H.; Cwikel, D.; Kapon, M.; Dori, Z. (1997). „Spectroscopy and Electrochemistry of Cobalt(III) Schiff Base Complexes”. Inorg. Chem. 36: 2498—2504. doi:10.1021/ic961146v.
- ^ а б Takeuchi, T.; Böttcher, A.; Quezada, C. M.; Meade, T. J.; Gray, H. B. (1999). „Inhibition of thermolysin and human alpha-thrombin by cobalt(III) Schiff base complexes”. Bioorg. Med. Chem. 6: 1—5. PMID 10400334.
- ^ а б в Tsilikounas, E.; Kettner, C.; Bachovchin, W. (1992). „Identification of serine and histidine adducts in complexes of trypsin and trypsinogen with peptide and nonpeptide boronic acid inhibitors by proton NMR spectroscopy”. Biochemistry. 31: 12839—12846. PMID 1463754. doi:10.1021/bi00166a019.
- ^ а б в Tsilikounas, E.; Kettner, C.; Bachovchin, W. (1993). „Boron-11 NMR spectroscopy of peptide boronic acid inhibitor complexes of .alpha.-lytic protease. Direct evidence for tetrahedral boron in both boron-histidine and boron-serine adduct complexes”. Biochemistry. 32: 12651—12655. PMID 8251483. doi:10.1021/bi00210a013.
- ^ а б Suenaga, H.; Nakashima, K.; Shinkai, S. (1995). „Sugars intensify the inhibitory effect of phenylboronic acid on the hydrolytic activity of α-chymotrypsin”. J. Chem. Soc., Chem. Commun.: 29—30. doi:10.1039/C39950000029.
- ^ а б Katz, B.; Finermoore, J.; Mortezaei, R.; DH, R.; Stroud, R. (1995). „Episelection: Novel Ki .apprx. Nanomolar Inhibitors of Serine Proteases Selected by Binding or Chemistry on an Enzyme Surface”. Biochemistry. 34: 8264—8280. doi:10.1021/bi00026a008.
- ^ а б Geratz, J.; Tidwell, R.; Schwab, J.; Anderle, S.; Pryzwansky, K. (1990). „Sequential events in the pathogenesis of streptococcal cell wall-induced arthritis and their modulation by bis(5-amidino-2-benzimidazolyl)methane (BABIM)”. Am. J. Pathol. 136: 909—921. PMID 2327474.
- ^ а б в г Katz, B.; Clark, J.; Finer-Moore, J.; Jenkins, T.; Johnson, C.; Ross, M.; Luong, C.; Moore, W.; Stroud, R. (1998). „Design of potent selective zinc-mediated serine protease inhibitors”. Nature. 391: 608—612. PMID 9468142. doi:10.1038/35422.
- ^ а б Rice, K.; Tanaka, R.; Katz, B.; Numerof, R.; Moore, W. (1998). „Inhibitors of tryptase for the treatment of mast cell-mediated diseases”. Curr. Pharm. Des. 4: 381—396. PMID 10197050.
- ^ а б в Thorpe, H. H. (1998). „Bioinorganic chemistry and drug design: here comes zinc again”. Chem. Biol. 5: R125—R127. PMID 9653544. doi:10.1016/S1074-5521(98)90166-1.
- ^ а б в г Duffy, B.; Schwietert, C.; France, A.; Mann, N.; Culbertson, K.; Harmon, B.; McCue, J. P. (1998). „Transition metals as protease inhibitors”. Biol. Trace Element Res. 64: 197—213. PMID 9845474. doi:10.1007/BF02783336.
- ^ а б в г Thayer, J. S. (1984). Organometallic compounds and living organisms. New York: Academic Press. ISBN 978-0-12-686080-1.
- ^ а б в Babine, R. E.; Bender, S. L. (1997). „Molecular Recognition of Protein−Ligand Complexes: Applications to Drug Design”. Chem. Rev. 97: 1359—1472. PMID 11851455. doi:10.1021/cr960370z.
- ^ Bone, R.; Frank, D.; Kettner, C. A.; Agard, D. A. (1989). „Structural analysis of specificity: .alpha.-lytic protease complexes with analogs of reaction intermediates”. Biochemistry. 28: 7600—7609. PMID 2611204. doi:10.1021/bi00445a015.
- ^ Louie, A. Y.; Meade, T. J. (1998). „A cobalt complex that selectively disrupts the structure and function of zinc fingers”. PNAS. 95: 6663—6668. PMID 9618469. doi:10.1073/pnas.95.12.6663.
- ^ а б Mork, A. (1993). „Actions of Lithium on the Cyclic AMP Signalling System in Various Regions of the Brain - Possible Relations to its Psychotropic Actions -: A Study on the Adenylate Cyclase in Rat Cerebral Cortex, Corpus Striatum and Hippocampus”. Pharmacol. Toxicol. 71: 1—47. doi:10.1111/j.1600-0773.1993.tb01704.x.
- ^ а б в г Clauberg, M.; Joshi, J. G. (1993). „Regulation of serine protease activity by aluminum: implications for Alzheimer disease”. Proc. Natl. Acad. Sci. U.S.A. 90: 1009—1012. PMID 7679214.
- ^ а б Rao, K. S. J.; Rao, G. V. (1994). „Effect of aluminium (Al) on brain mitochondrial monoamine oxidase-A (MAO-A) activity--an in vitro kinetic study”. Mol. Cell. Biochem. 137: 57—60. PMID 7845378. doi:10.1007/BF00926039.
- ^ а б в г Nixon, R. A.; Clarke, J. F.; Logvinenko, K. B.; Tan, M. K. H.; Hoult, M.; Grynspan, F. (1990). „Aluminum inhibits calpain-mediated proteolysis and induces human neurofilament proteins to form protease-resistant high molecular weight complexes”. J. Neurochem. 55: 1950—1959. PMID 2121904. doi:10.1111/j.1471-4159.1990.tb05781.x.
- ^ а б в г д Joshi, J. G.; Dhar, M.; Clauberg, M.; Chauthaiwale, V. (1994). „Iron and aluminum homeostasis in neural disorders”. Environ. Health Perspect. 102: 207—213. PMID 7843099. doi:10.2307/3431788.
- ^ а б Lee, B. H.; Park, M. B.; Yu, B. S. (1998). „Inhibition of electric eel acetylcholinesterase by porphin compounds”. Bioinorg. Med. Chem. Lett. 8: 1467—1470. PMID 9873371. doi:10.1016/S0960-894X(98)00236-4.
- ^ а б Falkous, G.; Harris, J. B.; Mantle, D. (1995). „Effect of neurotoxic metal ions in vitro on proteolytic enzyme activities in human cerebral cortex”. Clin. Chim. Acta. 238: 125—135. PMID 7586572. doi:10.1016/0009-8981(95)06081-N.
- ^ а б в г Cuajungco, M. P.; Lees, G. K. (1997). „Zinc metabolism in the brain: relevance to human neurodegenerative disorders”. Neurobiol. Dis. 4: 137—169. PMID 9361293. doi:10.1006/nbdi.1997.0163.
- ^ Hay, R. W. (1984). Bio-inorganic Chemistry. New York: Ellis Horwood Limited. ISBN 978-0-85312-200-5.
- ^ а б в Atwood, C. S.; Moir, R. D.; Huang, X. D.; Scarpa, R. C.; Bacarra, N. M. E.; Romano, D. M.; Hartshorn, M. K.; Tanzi, R. E.; Bush, A. I. (1998). „Dramatic aggregation of Alzheimer abeta by Cu(II) is induced by conditions representing physiological acidosis”. J. Biol. Chem. 273: 12817—12826. PMID 9582309. doi:10.1074/jbc.273.21.12817.
- ^ а б в Fitzgerald, D. J.; Maggio, J. E.; Esler, W. P.; Stinson, E. R.; Jennings, J. M.; Ghilardi, J. R.; Mantyh, P. W.; Bush, A. I.; Moir, R. D.; Rosenkranz, K. M.; Tanzi, R. E. (1995). „Zinc and Alzheimer's disease”. Science. 268: 1920—1923. PMID 7604268.
- ^ Mantyh, P. W.; Ghilardi, J. R.; Rogers, S.; Demaster, E.; Allen, C. J.; Stimson, E. R.; Maggio, J. E. (1993). „Aluminum, iron, and zinc ions promote aggregation of physiological concentrations of beta-amyloid peptide”. J. Neurochem. 61: 1171—1174. PMID 8360682. doi:10.1111/j.1471-4159.1993.tb03639.x.
- ^ а б Huang, X. D.; Atwood, C. S.; Moir, R. D.; Hartshorn, M. A.; Vonsattel, J. P.; Tanzi, R. E.; Bush, A. I. (1997). „Zinc-induced Alzheimer's Abeta1-40 aggregation is mediated by conformational factors”. J. Biol. Chem. 272: 26464—26470. PMID 9334223. doi:10.1074/jbc.272.42.26464.
- ^ а б Bush, A. I.; Pettingell, W. H.; Multhaup, G.; Paradis, M. D.; Vonsattel, J. P.; Gusella, J. F.; Beyreuther, K.; Masters, C. L.; Tanzi, R. E. (1994). „Rapid induction of Alzheimer A beta amyloid formation by zinc”. Science. 265: 1464—1467. PMID 8073293.
- ^ Dyrks, T.; Dyrks, E.; Hartmann, T.; Masters, C.; Beyreuther, K. (1992). „Amyloidogenicity of beta A4 and beta A4-bearing amyloid protein precursor fragments by metal-catalyzed oxidation” (PDF). J. Biol. Chem. 267: 18210—18217. PMID 1517249.
- ^ Bondy, S. C.; Guo-Ross, S. X.; Truong, A. T. (1998). „Promotion of transition metal-induced reactive oxygen species formation by beta-amyloid”. Brain Res. 799: 91—96. PMID 9666089. doi:10.1016/S0006-8993(98)00461-2.
- ^ Cuajungco, M. P.; Lees, G. (1997). „Zinc and Alzheimer's disease: is there a direct link?”. J. Brain Res. Rev. 23: 219—236. PMID 9164672. doi:10.1016/S0165-0173(97)00002-7.
- ^ Sugumoto, H.; Iimura, Y.; Yamanishi, Y.; Yamatsu, K. (1995). „Synthesis and structure-activity relationships of acetylcholinesterase inhibitors: 1-benzyl-4-[(5,6-dimethoxy-1-oxoindan-2-yl)methyl]piperidine hydrochloride and related compounds”. J. Med. Chem. 38: 4821—4829. PMID 7490731. doi:10.1021/jm00024a009.
- ^ а б Danning, C. L.; Boumpas, D. T. (1998). „Commonly used disease-modifying antirheumatic drugs in the treatment of inflammatory arthritis: an update on mechanisms of action”. Clin. Exp. Rheumatol. 16: 595—604. PMID 9779311.
- ^ а б Hashimoto, K.; Whitehurst, C. E.; Matsubara, T.; Hirohata, K.; Lipsky, P. E. (1992). „Immunomodulatory effects of therapeutic gold compounds. Gold sodium thiomalate inhibits the activity of T cell protein kinase C”. J. Clin. Invest. 89: 1839—1848. PMID 1351061. doi:10.1172/JCI115788.
- ^ а б в Rajendran, K. G.; Sood, A.; Spielvogel, B. F.; Hall, I. H.; III, V. M. N.; Morse, K. W. (1995). „Anti-Osteoporotic activity of metal complexes of amine carboxyboranes”. Appl. Organomet. Chem. 9: 111—119. doi:10.1002/aoc.590090204.
- ^ Zhang, Z. Y.; Reardon, I. M.; Hui, J. O.; O’Connell, K. L.; Poorman, R. A.; Heinrikson, R. L. (1991). „Zinc inhibition of renin and the protease from human immunodeficiency virus type 1”. Biochemistry. 30: 8717—8721. PMID 1888732. doi:10.1021/bi00100a001.
- ^ а б в Hall, I. H.; Chen, S. Y.; Rajendran, K. G.; Sood, A.; Spielvogel, B. F.; Shih, J. (1994). „Hypolipidemic, anti-obesity, anti-inflammatory, anti-osteoporotic, and anti-neoplastic properties of amine carboxyboranes”. Environ. Health Perspect. 102: 21—30. PMID 7889876. doi:10.2307/3431958.
- ^ Pugh, M. C.; Pugh, C. B. (1987). „Current concepts in clinical therapeutics: disease-modifying drugs for rheumatoid arthritis”. Clin. Pharm. 6: 475—491. PMID 3319362.
- ^ Baker, D. G.; Rabinowitz, J. L. (1986). „Current concepts in the treatment of rheumatoid arthritis”. J. Clin. Pharmacol. 26: 2—21. PMID 3512617.
- ^ а б Sorenson, J. R. J. (1982). Sigel, H.; Marcel Dekker, ur. Metal ions in biological systems. 14. New York. ISBN 9780824715694.
- ^ Naughton, D. P.; Knappitt, J.; Fairburn, K.; Gaffney, K.; Blake, D. R.; Grootveld, M. (1995). „Detection and investigation of the molecular nature of low-molecular-mass copper ions in isolated rheumatoid knee-joint synovial fluid”. FEBS Lett. 362: 167—172. PMID 7698317. doi:10.1016/0014-5793(95)00165-6.
- ^ Miche, H.; Brumas, V.; Berthon, G. (1997). „Copper(II) interactions with nonsteroidal antiinflammatory agents. II. Anthranilic acid as a potential. OH-inactivating ligand”. J. Inorg. Biochem. 68: 27—38. PMID 9379178. doi:10.1016/S0162-0134(97)00005-6.
- ^ Menard, H. A.; Amine, M. E. (1996). „The calpain-calpastatin system in rheumatoid arthritis”. Immunol. Today. 17: 545—547. PMID 8991283. doi:10.1016/S0167-5699(96)30064-9.
- ^ Zhang, H.; Johnson, P. (1992). „Differential effects of aluminum ion on smooth muscle calpain I and calpain II activities”. Int. J. Biochem. 24: 1773—1778. PMID 1451912. doi:10.1016/0020-711X(92)90127-M.
- ^ Frolich, J. C. (1997). „A classification of NSAIDs according to the relative inhibition of cyclooxygenase isoenzymes”. Trends Pharm. Sci. 18: 30—34. PMID 9114728. doi:10.1016/S0165-6147(96)01017-6.
- ^ а б Moore, P.; Jones, C.; Mahmood, N.; Evans, I.; Goff, M.; Cooper, R.; Hay, A. (1995). „Anti-(human immunodeficiency virus) activity of polyoxotungstates and their inhibition of human immunodeficiency virus reverse transcriptase” (PDF). Biochem. J. 307: 129—134. PMID 7536411.
- ^ а б Casas, J.; Rodriguez-Arguelles, M.; Russo, U.; Sanchez, A.; Sordo, J.; Vazquez-Lopez, A.; Pinelli, S.; Lunghi, P.; Bonati, A.; Albertini, R. (1998). „Diorganotin(IV) complexes of pyridoxal thiosemicarbazone: synthesis, spectroscopic properties and biological activity”. J. Inorg. Biochem. 69: 283—292. PMID 9654752. doi:10.1016/S0162-0134(98)00004-X.
- ^ а б Chamorro, C.; Camarasa, M. J.; Perez-Perez, M. J.; Clercq, E. D.; Balzarini, J.; Felix, A. S. (1998). „An approach towards the synthesis of potential metal-chelating TSAO-T derivatives as bidentate inhibitors of human immunodeficiency virus type 1 reverse transcriptase”. Antiviral Chem. Chemother. 9: 413—423. PMID 9875394.
- ^ а б Nacsa, J.; Nagy, L.; Molnar, J.; Molnar, J. (1998). „Trifluoperazine and its metal complexes inhibit the Moloney leukemia virus reverse transcriptase”. Anticancer Res. 18: 1373—1376. PMID 9673343.
- ^ а б в г Woon, T.; Brinkworth, R.; Fairlie, D. (1992). „Inhibition of HIV-1 proteinase by metal ions”. Int. J. Biochem. 24: 911—914. PMID 1612181. doi:10.1016/0020-711X(92)90096-J.
- ^ а б Davis, D. A.; Branca, A. A.; Pallenberg, A. J.; Marschner, T. M.; Patt, L. M.; Chatlynne, L. G.; Humphrey, R. W.; Yarchoan, R.; Levine, R. L. (1995). „Inhibition of the human immunodeficiency virus-1 protease and human immunodeficiency virus-1 replication by bathocuproine disulfonic acid Cu1+”. Arch. Biochem. Biophys. 322: 127—134. PMID 7574666. doi:10.1006/abbi.1995.1444.
- ^ а б York, D. M.; Darden, T. A.; Pedersen, L. G.; Anderson, M. W. (1993). „Molecular modeling studies suggest that zinc ions inhibit HIV-1 protease by binding at catalytic aspartates”. Environ. Health Perspect. 101: 246—250. PMID 8404763.
- ^ а б Lebon, F.; deRosny, E.; Reboud-Ravauz, M.; Durant, F. (1998). „De novo drug design of a new copper chelate molecule acting as HIV-1 protease inhibitor”. Eur. J. Med. Chem. 33: 733—737. doi:10.1016/S0223-5234(98)80032-9.
- ^ а б Mazumder, A.; Gupta, M.; Perrin, D. M.; Sigman, C. S.; Ranbinovitz, M.; Pommier, Y. (1995). „Update on long-term symptomless HIV type 1 infection in recipients of blood products from a single donor”. AIDS Res. Hum. Retroviruses. 11: 1. PMID 7734182. doi:10.1089/aid.1995.11.1.
- ^ а б Farnet, C. M.; Wang, B.; Hansen, M.; Lipford, J. R.; Zalkow, L.; Robinson, W. E. J.; Siegel, J.; Bushman, F. (1998). „Human immunodeficiency virus type 1 cDNA integration: new aromatic hydroxylated inhibitors and studies of the inhibition mechanism”. Antimicrob. Agents Chemother. 42: 2245—2253. PMID 9736543.
- ^ Perrin, D. D.; Stunzi, H. (1982). Metal ions and chelating agents in antiviral chemotherapy. New York: Marcel Dekker.
- ^ а б LaFemina, R. L.; Schneider, C. L.; Robbins, H. L.; Callahan, P. L.; LeGrow, K.; Roth, E.; Schleif, W. A.; Emini, E. A. (1992). „Requirement of active human immunodeficiency virus type 1 integrase enzyme for productive infection of human T-lymphoid cells”. J. Virol. 66: 7414—7419. PMID 1433523.
- ^ Tarrago-Litvak, L.; Andreola, M.; Nevinsky, G. A.; Sarih-Cottin, L.; Litvak, S. (1994). „The reverse transcriptase of HIV-1: from enzymology to therapeutic intervention”. FASEB J. 18: 497—503. PMID 7514143.
- ^ Huang, H.; Chopra, R.; Verdine, G. L.; Harrison, S. C. (1998). „Structure of a covalently trapped catalytic complex of HIV-1 reverse transcriptase: implications for drug resistance”. Science. 282: 1669—1675. PMID 9831551. doi:10.1126/science.282.5394.1669.
- ^ Ferrari, M. B.; Fava, G. G.; Tarasconi, R.; Albertini, S.; Pinelli, R.; Starcich, J. (1994). „Synthesis, spectroscopic and structural characterization, and biological activity of aquachloro (pyridoxal thiosemicarbazone) copper(II) chloride”. J. Inorg. Biochem. 53: 13. PMID 8133248. doi:10.1016/0162-0134(94)80017-0.
- ^ Das K, Bauman JD, Rim AS, Dharia C, Clark AD Jr, Camarasa MJ, Balzarini J, Arnold E (28. 04. 2011). „Crystal structure of tert-butyldimethylsilyl-spiroaminooxathioledioxide-thymine (TSAO-T) in complex with HIV-1 reverse transcriptase (RT) redefines the elastic limits of the non-nucleoside inhibitor-binding pocket”. J Med Chem. 54 (8): 2727—37. PMID 21446702. doi:10.1021/jm101536x.
- ^ Spence, R. A.; Kati, W. M.; Anderson, K. S.; Johnson, K. A. (1995). „Mechanism of inhibition of HIV-1 reverse transcriptase by nonnucleoside inhibitors”. Science. 267: 988—993. PMID 7532321. doi:10.1038/nsb0495-303.
- ^ West, M. L.; Fairlie, D. P. (1995). „Targeting HIV-1 protease: a test of drug-design methodologies”. Trends Pharmacol. Sci. 16: 67—75. PMID 7762084. doi:10.1016/S0165-6147(00)88980-4.
- ^ а б Wisniewski, M. Z.; Surga, W. J.; Piekos, R. (1995). „Silver(I) compounds of some sulfonamides”. Polish J. Chem. 69: 987—991.
- ^ а б в Serra, M.; Pintar, A.; Casella, L.; Sabbioni, E. (1992). „Vanadium effect on the activity of horseradish peroxidase, catalase, glutathione peroxidase, and superoxide dismutase in vitro”. J. Inorg. Biochem. 46: 161—174. PMID 1325536. doi:10.1016/0162-0134(92)80027-S.
- ^ Karlstrom, A. R.; Levine, R. L. (1991). „Copper inhibits the protease from human immunodeficiency virus 1 by both cysteine-dependent and cysteine-independent mechanisms” (PDF). PNAS. 88: 5552—5556. PMC 51915
 .
.
- ^ Hazuda, D. J.; Felock, P. J.; Hastings, J. C.; Prmanik, B.; Wolfe, A. L. (1997). „Differential divalent cation requirements uncouple the assembly and catalytic reactions of human immunodeficiency virus type 1 integrase” (PDF). J. Virol. 71: 7005—7011. PMID 9261430.
- ^ а б DeZwart, M.; vanderGoot, H.; Timmerman, H. (1991). „Influence of Co(II), Ni(II), Cu(II), Zn(II) and Cd(II) on growth inhibition and enzyme activity of Mycoplasma gallisepticum in the absence or presence of a 2,2′-bipyridyl type ligand”. Eur. J. Med. Chem. 26: 101—108. doi:10.1016/0223-5234(91)90218-C.
- ^ а б Wells, T. N. C.; Scully, P.; Paravicini, G.; Proudfoot, A. E. I.; Payton, M. A. (1995). „Mechanism of irreversible inactivation of phosphomannose isomerases by silver ions and flamazine”. Biochemistry. 34: 7896—7903. PMID 7794901. doi:10.1021/bi00024a014.
- ^ а б Cunningham, M. L.; Zvelebil, M. J. J. M.; Fairlamb, A. H. (1994). „Mechanism of inhibition of trypanothione reductase and glutathione reductase by trivalent organic arsenicals”. Eur. J. Biochem. 221: 285—295. PMID 8168518. doi:10.1111/j.1432-1033.1994.tb18740.x.
- ^ а б Saha, A. K.; Crans, D. C.; Pope, M. T.; Simone, C. M.; Glew, R. H. (1991). „Inhibition of human seminal fluid and Leishmania donovani phosphatases by molybdate heteropolyanions” (PDF). J. Biol. Chem. 266: 3511—3517. PMID 1995614.
- ^ а б Yano, S.; Inoue, S.; Nouchi, R.; Mogami, K.; Shinohara, Y.; Yasuda, Y.; Kato, M.; Tanase, T.; Kakuchi, T.; Mikata, Y.; Suzuki, T.; Yamamoto, Y. (1998). „Antifungal nickel(II) complexes derived from amino sugars against pathogenic yeast, Candida albicans”. J. Inorg. Biochem. 69: 15—23. PMID 9606935.
- ^ а б Su, J. J.; Mansour, J. M.; Mansour, T. E. (1996). „Purification, kinetics and inhibition by antimonials of recombinant phosphofructokinase from Schistosoma mansoni”. Mol. Biochem. Parasitol. 81: 171—178. PMID 8898332. doi:10.1016/0166-6851(96)02702-8.
- ^ а б Saenz, R. E.; Rodriguez, C. C. D.; Johnson, C. M.; Berman, J. D. (1991). „Efficacy and toxicity of pentostam against Panamanian mucosal leishmaniasis”. Am. J. Trop. Med. 44: 394—398. PMID 1645930.
- ^ а б Meyer-Fernandes, J. R.; Dutra, P. M. L.; Rodrigues, C. O.; Saad-Nehme, J.; Lopes, A. H. C. S. (1997). „Mg-dependent ecto-ATPase activity in Leishmania tropica”. Arch. Biochem. Biophys. 341: 40—46. PMID 9143351.
- ^ а б Kendrick, M. J.; May, M. T.; Plishka, M. J.; Robinson, K. D. (1992). „Metals in Biological Systems”. New York: Ellis Horwood. ISBN 978-0-13-577727-5.
- ^ Bult, A. (1983). Sigel, H., ur. Metal ions in biological systems. 16. New York: Marcel Dekker. doi:10.1080/00945718208063132.
- ^ Garg, R. K.; Sharma, L. M. J. Indian Chem. Soc. (1995). „Binuclear transition metal complexes of some novel Schiff bases derived from dapsone (an antileprotic drug). Part II. Zinc(II) complexes”. 72: 231—234. ISSN 0019-4522.
- ^ Hueso-Urena, F.; Moreno-Carretero, M. N.; Romero-Molina, M. A.; Salas-Peregrin, J. M.; Sanchez-Sanchez, M. P.; Cienfuegos-Lopez, G. A. D.; Faure, R. J. (1993). „Transition metal complexes with monodeprotonated isoorotic and 2-thioisoorotic acids: Crystal structure, spectral and magnetic study, and antimicrobial activity”. Inorg. Biochem. 51: 613—632. doi:10.1016/0162-0134(93)85033-5.
- ^ Ibrahim, S. A.; El-Gyar, S. A.; El-Gahani, M. A. (1991). „Metal complexes of nitrogen-oxygen donor ligands as potential drugs”. Collect. Czech. Chem. Commun. 56: 1333—1339. doi:10.1135/cccc19911333.
- ^ Nagar, R.; Mohan, G. J. (1992). „Studies on mixed-ligand complexes of some transition metals of biological interest”. Therm. Anal. 38: 1415—1431.
- ^ Fairlamb, A. H.; Henderson, G. B.; Cerami, A. (1989). „Trypanothione is the primary target for arsenical drugs against African trypanosomes” (PDF). PNAS. 86: 2607—2611. PMID 2704738.
- ^ а б Tsai, H.; Dwarakanath, A.; Hart, C.; Milton, J.; Rhodes, J. (1995). „Increased faecal mucin sulphatase activity in ulcerative colitis: a potential target for treatment” (PDF). Gut. 36: 570—576. PMID 7737566.
- ^ а б Beil, W.; Birkholz, C.; Wagner, S.; Sewing, K. (1995). „Bismuth subcitrate and omeprazole inhibit Helicobacter pyloriF1-ATPase”. Pharmacology. 50: 333—337. PMID 7667394. doi:10.1159/000139299.
- ^ а б в г Schroeder, T.; Caspers, M. (1996). „Kinetics of aluminum-induced inhibition of delta-aminolevulinic acid dehydratase in vitro”. Biochem. Pharmacol. 52: 927—931. PMID 8781512. doi:10.1016/0006-2952(96)00449-2.
- ^ а б в г Exley, C.; Price, N.; Birchall, J. (1994). „Aluminum inhibition of hexokinase activity in vitro: a study in biological availability”. J. Inorg. Biochem. 54: 297—304. PMID 8014638. doi:10.1016/0162-0134(94)80035-9.
- ^ а б Canesi, L.; Ciacci, C.; Piccoli, G.; Stocchi, V.; Viarengo, A.; Gallo, G. (1998). „In vitro and in vivo effects of heavy metals on mussel digestive gland hexokinase activity: the role of glutathione”. Comp. Biochem. Physiol. C. 120 (2): 261—268. PMID 9827040. doi:10.1016/S0742-8413(98)10004-X.
- ^ а б в г Yoshino, M.; Murakami, K.; Kawano, K. (1998). „Interaction of aluminum ion with ATP. Mechanism of the aluminum inhibition of glycerol kinase and its reversal by spermine”. Biometals. 11: 63—67. doi:10.1023/A:1009213508942.
- ^ а б Hyppo¨nen, S.; Kohila, T.; Tahti, H. (1993). „The effects of cadmium, lead and aluminum on neural cell membrane adenosinetriphosphatase activity”. Neurosci. Res. Commun. 12: 77—84.
- ^ а б Yager, J. W.; Wiencke, J. K. (1997). „Inhibition of poly(ADP-ribose) polymerase by arsenite”. Mutat. Res. 386: 345—351. PMID 9219571. doi:10.1016/S1383-5742(97)00011-2.
- ^ а б в Hu, Y.; Su, L.; Snow, E. T. (1998). „Arsenic toxicity is enzyme specific and its affects on ligation are not caused by the direct inhibition of DNA repair enzymes”. Mutat. Res. 408: 203—218. PMID 9806419. doi:10.1016/S0921-8777(98)00035-4.
- ^ а б в Tsao, D.; Maki, A. (1991). „Optically detected magnetic resonance study of the interaction of an arsenic(III) derivative of cacodylic acid with EcoRI methyltransferase”. Biochemistry. 30: 4565—4572. PMID 2021649. doi:10.1021/bi00232a029.
- ^ а б Lam, W.; Tsao, D.; Maki, A.; Maegley, K.; Reich, N. (1992). „Spectroscopic studies of arsenic(III) binding to Escherichia coli RI methyltransferase and to two mutants, C223S and W183F”. Biochemistry. 31: 10438—10442. PMID 1420162. doi:10.1021/bi00158a004.
- ^ а б в Styblo, M.; Thomas, D. (1995). „In vitro inhibition of glutathione reductase by arsenotriglutathione”. Biochem. Pharmacol. 49: 971—977. PMID 7741769. doi:10.1016/0006-2952(95)00008-N.
- ^ а б Chawla, S.; Mutenda, E.; Dixon, H.; Freeman, S.; Smith, A. (1995). „Synthesis of 3-arsonopyruvate and its interaction with phosphoenolpyruvate mutase”. Biochem. J. 308: 931—935. PMID 8948453.
- ^ а б Snow, E.; Xu, L.; Kinney, P. (1993). „Effects of nickel ions on polymerase activity and fidelity during DNA replication in vitro”. Chem.-Biol. Interact. 88: 155—173. PMID 8403077. doi:10.1016/0009-2797(93)90089-H.
- ^ а б Yang, S. W.; Becker, F. F.; Chan, J. Y. H. (1996). „Inhibition of human DNA ligase I activity by zinc and cadmium and the fidelity of ligation”. Environ. Health Perspect. 28: 19—25. PMID 8698042. doi:10.1002/(SICI)1098-2280(1996)28:1<19::AID-EM5>3.0.CO;2-9.
- ^ а б в Hartwig, A. (1994). „Role of DNA repair inhibition in lead- and cadmium-induced genotoxicity: a review”. Environ. Health Perspect. 102: 45—50. PMID 7843136. doi:10.2307/3431762.
- ^ а б в Porter, D. W.; Nelson, V. C.; Fivash, M. J. J.; Kasprzak, K. S. (1996). „Mechanistic studies of the inhibition of MutT dGTPase by the carcinogenic metal Ni(II)”. Chem. Res. Toxicol. 9: 1375—1381. PMID 8951243. doi:10.1021/tx9600816.
- ^ а б в Wetmur, J. G. (1994). „Influence of the common human delta-aminolevulinate dehydratase polymorphism on lead body burden”. Environ. Health Perspect. 102: 215—219. PMID 7843101. doi:10.2307/3431789.
- ^ SI, Beale (1990). „Biosynthesis of the Tetrapyrrole Pigment Precursor, delta-Aminolevulinic Acid, from Glutamate”. Plant Physiol. 93 (4): 1273—9. PMC 1062668
 . PMID 16667613. doi:10.1104/pp.93.4.1273.
. PMID 16667613. doi:10.1104/pp.93.4.1273.
- ^ Willows, R.D. (2004). „Chlorophylls”. Ur.: Goodman, Robert M. Encyclopaedia of Plant and Crop Science. Marcel Dekker. str. 258—262. ISBN 978-0-8247-4268-3.
- ^ Thiele, D. J. (1992). „Metal-regulated transcription in eukaryotes” (PDF). Nuc. Acids Res. 20: 1183—1191. PMID 1561077.
- ^ O’Halloran, T. V. (1993). „Transition metals in control of gene expression”. Science. 261: 715—725. PMID 8342038. doi:10.1126/science.8342038.
Литература[уреди | уреди извор]
- Berg JM, Tymoczko JL, Stryer L (2002). Biochemistry (V izd.). New York, NY: W. H. Freeman. ISBN 978-0-7167-3051-4.
- Cornish-Bowden A, ur. (1997). New Beer in an Old Bottle: Eduard Buchner and the Growth of Biochemical Knowledge. Universitat de València. ISBN 978-84-370-3328-0.
- H, Suzuki (2015). How Enzymes Work: From Structure to Function. Boca Raton, FL: CRC Press. ISBN 978-981-4463-92-8.
- Cornish-Bowden A (2012). Fundamentals of Enzyme Kinetics (IV izd.). Weinheim: Wiley-VCH. ISBN 978-3527330744.
- Briggs, G. E.; J. B. S. Haldane (1925). „A note on the kinetics of enzyme action”. Biochem. J. 19: 339—339. PMC 1259181
 .
. - R.R. Dogonadze; V.G. Levich (1959). „Theory of Non-radiative Electronic Transitions between Ions in Solution”. Dokladi Akademii Nauk SSSR. Ser. Fizicheskoy Khimii. Moscow. 124: 123—126.
- R.R. Dogonadze (1960). „Rate of Electron Transfer Reactions in Solutions”. Dokladi Akademii Nauk SSSR. Ser. Fizicheskoy Khimii. Moscow. 133: 1368—1371.
- M, Nishimura; Chance B. (1963). „Studies on the electron-transfer systems in photosynthetic bacteria I. The light-induced absorption-spectrum changes and the effect of phenylmercuric acetate”. Biochim Biophys Acta. 66: 1—16. doi:10.1016/0006-3002(63)91162-4.
- V.G. Levich; R.R. Dogonadze; E.D. German; A.M. Kuznetsov; Yu.I. Kharkats (1970). „Theory of Homogeneous Reactions Involving Proton Transfer”. Electrochim.Acta. 15: 353—367.
- M.V. Volkenshtein; R.R. Dogonadze; A.K. Madumarov; Z.D. Urushadze; Yu. I. Kharkats (1972). „Theory of Enzyme Catalysis”. Molekuliarnaya Biologia: 431—439.
Спољашње везе[уреди | уреди извор]
- (језик: енглески) Веб-туторијал за ензимску инхибицију, приручник др Питера Берча са Универзитета у Пејслију који садржи веома јасне анимације
- (језик: енглески) Симболика и терминологија ензимске кинетике, препоруке Одбора за номенклатуру Међународне уније за биохемију (NC–IUB) око терминологије инхибиције ензима
- (језик: енглески) NCBI-јев PubChem, база података лекова и инхибитора ензима
- (језик: енглески) BRENDA Архивирано на сајту Wayback Machine (11. децембар 2008), база података ензима са списковима познатих инхибитора за сваки унос
- (језик: енглески) Ензими, кинетика и дијагностичка употреба Архивирано на сајту Wayback Machine (9. јул 2011), онлајн предавање др Мајкла V. Кинга из Медицинске школе Универзитета у Индијани с фокусом на медицинску примену инхибитора ензима
- (језик: енглески) BindingDB, javna baza podataka izmerenih afiniteta vezivanja proteina i liganda
- (jezik: engleski) Animirana vežba sa inhibicijom enzima, tutorijal + kvizovi
Hiperbilirubinemija je oboljenje koje uzrokuje prekomernu akumulaciju bilirubina u krvi i tkivima.[1] Bilirubin je produkt katabolizma hema, pri čemu se hem degradira posredstvom hem oksigenaze (HO) и формира се биливердин, који се затим редукује помоћу биливердин редуктазе до билирубина.[2] Након конјугације са глукуронском киселином, помоћу ензима билирубин глукуронид трансфераза, и формирања растворљивијег конјугата, билирубин се излучује. Прекомерно разлагање хема и недовољна активност трансферазе могу да доведу до акумулације билирубина. Ово накупљање је познато као неонатална жутица код беба са недовољно развијеном јетром и превремено рођене деце, која брзо разграђују хем (при прелазу са феталног на регуларни хемоглобин) али им недостају адекватне трансферазе. Хипербилирубинемија се такође јавља код генетичког Криглер—Најаровог синдрома, где долази до комплетног одсуства трансферазног дејства у јетри[3] и других болести као што су таласемија и конгениталне анемије.[2] Инхибиција разлагања хема у хем оксигеназном кораку је могући начин спречавања хипербилирубинемије.
Металопорфирини су екстензивно изучавани и добро познати инхибитори хем оксигеназе. Ови инхибитори се везују за каталитичко место, али нису ефективни супстрати. Знатан број металопорфирина има инхибиторно дејство, а има и оних који индукују хем оксигеназу. Најзначајнији инхибитори хем оксигеназе су калајни и цинкови порфирини. Неки од ових порфирина су нашли клиничку примену у сузбијању продукције билирубина.[3][4] Недавна истраживања су разјаснила природу инхибиције, утицај на друге биохемијске путеве, као и опсег биодистрибуције лекова.
Студије цинкових и калајних протопорфирина индицирају да је калајни протопорфирин (Sn-PP) исто тако ефективан инхибитор адреналне стероидогенезе, док цинков протопорфирин (Zn-PP) нема утицаја на тај пут.[5][6] Синтеза стероида је посредована бројним хемопротеинима, цитохромима P-450, те постоји комплексна међузависност између пута синтезе хема и стероидогенезе. Концентрација цитохрома је везана за промене у синтези и деградацији хема. У тестовима, користећи моделе на пацовима, утврђено је да Sn-PP знатно редукује активност стероидних биосинтетичких ензима митохондријске 11β-хидроксилазе и микрозомалне 21R-хидроксилазе; такође је уочено смањење садржаја микрозомалног цитохрома P-450.[5][6] У поменутој студији је исто тако запажено драстично смањење садржаја HO-2, неиндуцибилног изозима хем оксигеназе који је далеко превалентнији од индуцибилног HO-1, те се претпоставља да Sn-PP заправо уништава HO-2 уместо да га инхибира. Zn-PP, насупрот овога, инхибира активност HO али нема утицаја на ензиме стероидне биосинтезе.[5][6]
Даља истраживање поређењем дејства Zn-PP и Sn-PP са HO-1 и HO-2 показала су да су оба једнако инхибиторна за HO-1 без утицаја на интегритет протеина (што је утврђено вестерн блот анализом), као и да индукују повишење нивоа HO-1 транскрипије. Међутим, Sn-PP и Zn-PP се разликују у погледу своје активности спрам HO-2.[7] Мада оба инхибирају HO-2, разликују се у степену инхибиције. Степен инхибиције Zn-PP је исти за обе форме HO, док Sn-PP испољава знатнију инхибицију HO-2 него HO-1. Сматра се да Sn-PP поремећује интегритет HO-2 протеина (вестерн блот), док Zn-PP нема тај ефекат. Механизам који узрокује разлике активности Sn-PP и Zn-PP на HO формама није познат.
Утврђено је да разни порфирини инхибирају интестиналну хем оксигеназу и умањују преузимање гвожђа из црева, доводећи до повећаног излучивања овог метала. То може да буде корисно у третману случајева хемохроматозе.[8][9] Овај ефекат је уочен код свих парентерално администрираних порфирина, али су само Sn-MP, Sn-PP и Cr-MP били орално ефективни (на интестиналној HO; нису нађени на реналним, сплинским или хепатичим ткивима). Показано је да је Zn-MP ефективан у третману акутне порфирије (поремећаја изазваног дефицијенцијом хема), а студије дистрибуције у ткиву су показале да брзо бива уклоњен из плазме и да се првенствено задржава у јетри и слезини, где инхибира HO током периода од скоро недељу дана након једне инјекције.[10] Zn-MP не пролази кроз крвно-мождану баријеру, за разлику од Sn-PP за који је показано да штетно утиче на HO-2 интегритет и активност у мозгу пацова.[11] Металопорфирини делују као појачивачи фотосензитивности с варирајућим степенима[12] (они се такође користе у фотодинамичкој терапији). Познато је да Zn-PP у мањој мери подстиче фотосензитивност од Sn-PP, што је још једно својство које сугерише да су цинкове форме инхибитора вероватно подесније за клиничку примену.[13]
Co-MP и Cr-MP такође ефективно инхибирају HO.[14][15] Утврђено је да Co-MP не посредује липидну пероксидацију у можданим мембранама пацова након фотоирадијације (што је показано користећи малондиалдехидни тест); стога, он не подстиче фотосензитивност.[14] Cr-MP ефективно инхибира хепатичку HO након оралне администрације, док на сплинску HO нема утицаја.[15] Показано је да Zn-MP инхибира хепатичку 5-аминолевулинатну синтазу (ALAS), ензим који ограничава брзину пута биосинтезе хема. Овај ефекат се увећава кад се хем дода са порфирином.[16] Познато је да гвожђе и хем повратно регулишу ALAS путем инхибирања mРНК транскрипције/транспорта.[17] Уочено је да је ALAS транслација под контролом елемената респосивних на гвожђе.[18]
Употреба металопорфирина за третман хипербилирубинемије је узнапредовала даље у процесу развоја лекова у односу на антиканцерне агенсе описане у претходном одељку. Ови порфирини имају познат биолошки циљ, хем оксигеназу, те је њихова клиничка ефективност већ показана. Међутим, њихова главна биолошка мета је део комплексног пута, који је у великој мери повезан са другим процесима, као што је стероидна синтеза. Неопходно је праћење тих других процеса да би се спречили нежељени утицаји на њих.
- Трансдукција азот-моноксидног сигнала
| Трансдукција азот-моноксидног сигнала | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| PP | Zn | растворна гуанилатна циклаза (пречишћена)[19] | |
| PP, BG | Zn, Sn | растворна гуанилатна циклаза (пацови)[20] | |
| натријум нитропрусид (SNP) | Fe | азот-моноксид синтаза (неутрофили пацова)[21] | |
| SNP | Fe | NOS (церебрални кортикални синаптозоми)[22] | |
| јони | Cu, Zn, Co, Ni, Fe | NOS (пречишћена)[23] | |
| јон | Zn | NOS (пречишћени nNOS)[24] | |
| SNP | Fe | екто-5'-нуклеотидаза (ренално епителијална)[25] | |
| SNP | Fe | индоламин 2,3-диоксигеназа (мононуклеарни фагоцити)[26] | |
| SNP | Fe | метионин синтаза[27] | |
| SNP | Fe | (Na+/K+)-ATPаза[28] | |
Азот-моноксид (NO) игра улогу гласника у мноштву система. У имунском систему, NO posreduje respons belih krvnih zrnaca na patogene; u kardiovaskularnom sistemu, NO индукује релаксацију ћелија глатких мишића у крвним судовима; и у нервном систему, NO учествује у неуротрансмисији и неуромодулацији.[29][27][30] NO се формира из L-аргинина посредством азот-моноксидне синтазе (NOS), хем протеина који се јавља у више изоформи и за чије дејство је неопходан NADPH као донор електрона. Постоје три NOS изоформе: конститутивне изоформе присутне у мозгу (nNOS, тип I) и ендотелним ћелијама (eNOS, тип III) за чије дејство је неопходан калцијум/калмодулин, и цитокином индуковане форме (iNOS, тип II) за чије дејство није неопходан калцијум али које имају калмодулин као чврсто везану подјединицу.[31] Обе класе се јављају у облику хомодимера при чему свака подјединица садржи 1 еквивалент FAD, FMN, (6R)-5,6,7,8-тетрахидро-L-биоптерина (H4B) и протопорфирин IX хема.[23][32] Постоји дуга листа NOS инхибитора која обухвата селеноорганска једињења (која се везују за тиолне групе), Zn порфирине, те цинк (везује се за хем места).[32] У каскади преноса сигнала, познато је да NO стимулише гуанилатну циклазу и да индукује акумулацију секундарног гласника, cAMP. Многи аспекти NO сигнализације су испитани студирањем рамификација увођења NO донора у систем или путем NOS инхибирања NOS чиме се обуставља NO продукција.
NO је нашао широку примену као лиганд у гвожђе-хемним комплексима у неорганској хемији, и стога се намеће питање да ли NO може да буде ауторегулисан NOS инхибицијом (хемни је протеин).[31] Студије са NO донором, натријум нитропрусидом (SNP), Na2Fe(CN)5NO•2H2O, показују да NO може да инхибира NOS.[21][21] У студијама са неутрофилима пацова, липополисахарид се користи за индуковање активности NOS и ова индукција се инхибира помоћу SNP.[21] SNP испитивања користећи кортикалне синаптозоме пацова су указала на постојање концентрационо зависне NOS инхибиције NOS активности.[21] У овим студијама се NOS активност одређује праћењем формирања [3H]цитрулина из [3H]аргинина.[33] Познато је да прелазни метали инхибирају NOS,[23] као и да пречишћени Cu2+, Ni2+, Zn2+ и Co2+ делују као инхибитори индуцибилног NOS ензима, док нехемно гвожђе повећава каталитичку активност. За Cu2+ јон је утврђено да инхибира пречишћени неуронални NOS (други метали нису тестирани на nNOS). Из ових налаза произилази да нехемно гвожђе NOS ензима учествује у катализи, те да NOS вероватно садржи активно место за нехемно гвожђе/H4B.
Zn2+ реверзибилно инхибира активност nNOS (Ki = 30 μM).[24] Уочена је инхибиција NADPH-зависне редукције гвожђа хема и од калмодулина (CaM)-зависна редукција цитохрома c. Није уочена инхибиција CaM-независне редуктазе цитохром c редуктазе (мерено релативним бројем каталитичких циклуса цитохрома c). Међутим, чак и у одсуству Zn2+, CaM-независни пут има више него десет пута слабију активност од CaM-зависног пута. nNOS спектри разлика типа II демонстрирају смањење количине високоспинског гвожђа хема у присуству Zn2+. На основу ових резултата, закључено је да до инактивације ензима долази услед везивања Zn2+ за сулфхидриле у близини хем лиганда и накнадног поремећаја окружења око гвожђа хема.
SNP и NO продукција доприносе инхибицији низа других ензима. Индоламин 2,3-диоксигеназа (IDO) ензим је који садржи хем и који је део интерфероном γ (IFNγ) индукованог респонса мононуклеарних фагоцита на патогене.[26] IDO је ензим који ограничава брзину у путу деградације триптофана. Исцрпљивање триптофана, најмање доступне есенцијалне аминокиселине, може да допринесе антипатогеној активности мононуклеарних фагоцита. У студијама на изолованим IFNγ-третираним људским периферним крвним мононуклеарним ћелијама и из моноцита изведеним макрофагама, уочено је да SNP инхибира IDO активност.[26] Такође је показано да се IDO може инхибирати дејством Zn-MP.[34] Други ензими које инхибира SNP обухватају метионинску синтазу у хепатоцитима пацова,[27] (Na+/K+)-ATPазе[28] и екто-5'-нуклеотидазе у реналним епителијалним ћелијама.[25] Метионинска синтаза се састоји од метилкобаламина као кофактора, деривата витамина Б-12 који је у знатној мери сличан хемоглобину, а до инхибиције може доћи путем формирања NO-кобаламинског комплекса. Сматра се да до инхибиције екто ензима долази путем S-нитрозилације. Механизам инхибиције (N+/К+)-ATPазе није познат.
Постоје индикације да је угљен-моноксид (CO) физиолошки регулатор, који делује на сличан начин као и NO, укључујући способност стимулације гуанилил циклазе. CO се формира посредством HO, при конверзији хема до биливердина и CO. Многе студије улоге CO су извршене користећи HO инхибиторе, као што су Zn-PP и Sn-PP, да би се показало да супресија HO (и стога CO продукције) инхибира гуанилил циклазу. Међутим, недавне студије су показале да сами металопорфирини инхибирају гуанилил циклазу, те стога студије које користе те комплексе за испитивање утицаја CO вероватно треба преиспитати.[19][20] У другим студијама су коришћени порфирини за испитивање улоге CO у просторном учењу и дугорочној потенцијацији у хипокампусу.[35][36] Порфирини су коришћени под претпоставком да они искључиво делују као супресори CO продукције посредством HO; међутим, имајући у виду да је дејство порфирина вишестрано, тешко је претпоставити улогу CO искључиво на бази тих експеримената. Ове студије демонстрирају неке од проблема са којима се истраживачи суочавају кад специфичност инхибитора није апсолутна и илуструју неке од компликујућих фактора у анализи података кад се користе „индиректни” ефектори (нпр. инхибирање ензима који формира CO, уместо директног уклањања CO).
Хипертензивне примене[уреди | уреди извор]
| Хипертензивне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| сулфонамид | Cu | карбонатна анхидраза[37] | |
| хетероциклични сулфонамиди | Zn, Cu | карбонатна анхидраза[38] | |
| хетероциклични меркаптани, сулфенамиди, сулфонамиди | Zn, Cu | карбонатна анхидраза[39] | |
| разни сулфонамиди | Ge, Sb | карбонатна анхидраза[40] | |
| хлоротиазид | Hg, Pb | карбонатна анхидраза[41] | |
| каптоприл | Zn | ангиотензин конвертујући ензим[42] | |
| лисиноприл | Cu | ангиотензин конвертујући ензим[43] | |
Системи везани за хем који су разматрани у претходном одељку блиско су повезани са хипертензивним применама. Натријум нитропрусид је у широкој употреби као хипотензивни агенс,[27][44] а хем оксигеназа је имплицирана у одржавање крвног притиска.[45] Утврђено је да SnCl2 индукује HO-1 транскрипцију и стога инхибира дејство цитохром P450-арахидонска киселина ω/ω-1 хидроксилазе, што доводи до смањеног формирања ö/ö-1 хидроксилазних метаболита и нижег крвног притиска.[45] Хидроксилаза је хемни протеин чији су нивои контролисани доступношћу хема. Кад се индукује хем оксигеназа исцрпи се доступни хем; томе следи опадање нивоа ензима, а тиме и количине ензимских метаболита. Метаболити, односно 19[S]-хидроксиеикозатетраеноинска киселина (HETE) и 20-HETE, делују као прохипертензиви јер стимулишу Na+/K+-ATPазу и констрикцију крвних судова.
Још један од примарних ензимских циљева за хипертензију је карбонатна анхидраза (CAs). Она катализује хидрацију CO2 до бикарбоната и учествује у широком опсегу биолошких процеса, укључујући pH хомеостазу, продукцију окуларних и цереброваскуларних флуида, те секрецију електролита. У очима, на пример, карбонатна анхидраза игра критичну улогу у одржавању интраокуларног притиска. Познато је седам изоензима карбонатне анхидразе и неколико сродних протеина. Ови изоензими су присутни у цитосолу (CA I, II, III и VII), везани за ћелијске мембране (CA IV), у митохондријама (CA V) и у секреторној форми у пљувачки (CA VI).[46][47] Они имају различите улоге и веома различиту ткивну дистрибуцију, кинетичка својства и осетљивост на инхибиторе. CA ензими су металоензими, а многи инхибитори тих ензима су метал комплексирајући анјони који се директно координирају са цинком у активном месту ензима.
Карбонатне анхидразе, изузев CA III, такође инхибирају сулфонамиди који се везују за цинк путем супституције каталитички важног молекула воде.[39] Сулфонамиди су коришћени за третман глаукома дуги низ година јер снижавају интраокуларни притисак (IOP). Прецизни механизам снижавања притиска није познат, али се сматра да до тога долази услед редукције концентрације бикарбоната у постериорној комори ока, те да пратеће премештање бикарбонатних јона доводи до кретања флуида и смањења концентрације натријума.[48] Метални комплекси сулфонамида такође потентно инхибирају карбонатне анхидразе. Zn(II), Cu(II), Ni(II), Co(II), Fe(III) и Al-(III) комплекси адамантил сулфонамидних деривата имају инхибиторно дејство на три CA изозима (hCA I, hCA II и bCA IV) са nM Ki вредностима.[38] Zn(II) и Cu(II) комплекси, најјачи инхибитори у серији, топикално су били примењивани на зечји модел ока и утврђено је да снижавају IOP. Топикално примењени сулфонамид не снижава IOP, из чега следи да присуство металних јона критично мења својства инхибитора. Претпоставља се да метал мења растворљивост комплекса, чиме се повећава доступност лека. Hg(II) комплекси хлоротиазида, диуретика који се користи као антихипертензив, исто тако показују јаку инхибицију CA[41] као и Ge(IV) и Sb(III) комплекси арилсулфониламида[40] и Cu(II) комплекси ацетазоламидних деривата.[37] За металне комплексе се сматра да делују на CA на два начина: 1. инхибицијом са слободним сулфонамидом и 2. интеракцијом металних јона са хистидином у активном месту.[37]
Велики део литературе о хипертензивним агенсима је посвећен инхибиторима ангиотензин-конвертујућег ензима (ACE), компоненти ренин-ангиотензин система. Ренин-ангиотензин систем учествује у одржавању крвног притиска. ACE катализује конверзију ангиотензина I до ангиотензина II, вазоконстриктора који учествује у хипертензији. Ангиотензин I се формира конверзијом јетреног продукта посредством ренина, ензима који излучују бубрези.[49][50] Постоје рецепторска места на многим органима за ангиотензин II. Тај систем може да буде блокиран на више нивоа, познати β-блокатори блокирају отпуштање ренина, аналози ренин-супстрата и ренински инхибитори блокирају ренин, ангиотензин II рецепторе блокира саларзин, а ACE инхибитори блокирају ACE. Већина поменутих једињења не садржи метале, мада неки ACE инхибитори формирају металне комплексие ин виво. На пример, каптоприл је дизајниран да се надмеће са ангиотензином за јоне цинка у ензиму и да везује цинк путем тиолне групе.[42] Лисиноприл, још један ACE инхибитор, везује цинк путем аминокарбоксилатне гурпе.[43] Лисиноприл се конјугује са Rh(III) и Pd(II) (иминофосфорано)фосфинима, а конјугати имају нешто већу инхибиторну активност од родитељског једињења (долази до 18-струког смањења вредности IC50, наномоларни опсег).[51] Ова дериватизација у виду синтезе 105Rh и 109Pd радио-обележених једињења омогућава ин виво праћење дистрибуције лека.
Третмани за хипертензију су обично дугорочни и стога је стабилност интеракција коју пружа ковалентно везивање металних комплекса привлачна опција. Највећи део литературе у овој области се бави органским једињењима; међутим, знатан број тих једињења је зависан од интеракције са металима за испољавање свог дејства.
Серинскопротеазне примене[уреди | уреди извор]
| Серинскопротеазне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| аминокиселинске и пептидне лигације | Co | α-химотрипсин[52][53] | |
| Шифова база | Co | тромбин, термолизин[54][55][56] | |
| разне боронске киселине | B | трипсин[57] | |
| пептид | B | α-литичка протеаза[58] | |
| фенилборонска киселина | B | α-химотрипсин[59] | |
| трипептид | B | трипсин, α-литичка протеаза, трипсину сличне протеазе[60] | |
| BABIM | Zn | серинске протеазе[61][62][63][64] | |
| титанил сулфати | Ti | трипсин[65] | |
Серинске протеазе обухватају главну фамилију протеолитичких ензима са разноврсним опсегом функција. Серинске протеазе играју кључне улоге у каскади коагулације крви, у активацији комплемента, бактеријској патогенези, те фибринолизи.[57] Серинске протеазе су постале проминентни циљеви за дизајн лекова у антивирусним и антибактеријским истраживањима.[65] Велика класа инхибитора серинских протеаза су боронске киселине и пептид-боронске киселине.[66][39][67][68] Сматра се да боронил групе опонашању прелазно стање реакције, док пептидна порција усмерава специфичност на специфичне протеазе.
Серије 15N и 1H студија комплекса протеазних инхибитора дале су увид у интеракције између трипсина или α-литичких протеаза и разних боронскокиселинских инхибитора. У α-литичким протеазама и трипсину, супстратни аналози теже да формирају серинске адукте, док несупстратни аналози обично формирају хистидинске адукте,[57] мада и супстратни аналози могу понекад да формирају хистидинске адукте.[58][69] Даље, 11B NMR студије на хистидинским адуктима α-литичких протеаза и серинских адуката химотрипсина и α-литичких протеаза показале су да је атом бора тетраедралан у хистидинским и серинским адуктима.[58] Из рада са фенилборонском киселином произилази да адиција шећера (D-моносахарида) повећава инхибиторно дејство на α-химотрипсин.[59] Тај закључак је изведен на основу ацидификације атома бора путем самокомплексације са D-моносахаридима. Овај синергистички ефекат је pH зависан и није уочен изнад pH 9,5 (ензимска инхибиција дејством саме борне киселине такође није уочена). До јаке инхибиције ензима долази између pH 4 и pH 9 у присуству фенилборне киселине и фруктозе са највећим шећерно индукованим појачањем инхибиције на приближно неутралном pH. Разни трипептиди боронатних естара такође делују као инхибитори серинске протеазе.[60] Утврђено је да додатни пептидно-метални комплекси делују као серин протеазни инхибитори. Познато је да Co(III)-везане аминокиселине и дипептиди могу да инхибирају химотрипсин и трипсин.[52][53] Ове студије су провођене да би се испитали ефекти пентамин кобалта(III), који се користи као хидрофилна карбоксилна заштитна група у ензиматској пептидној синтези. Раније је примећено да присуство ове групе на аминокиселинама непосредно поред везе која је подложна ензимском дејству блокира каталитичку конверзију. Инхибиција пречишћеног химотрипсина и трипсина лигираним пептидима је компетитивна и реверзибилна. Накнадне студије ове хемијске групе сугеришу да се лигирани пептиди везују за ензим путем Кулонових интеракција.[53] Кобалт(III)-лигирани пептиди разних дужина су тестирани на трипсину, химотрипсину и протеинази K. На основу резултата моделовања химотрипсина, растојање између два негативно наелектрисана Asp остатка (Asp-35 и Asp-64) у S' везујућем и Ser-195 у активном месту одговара дужини инхибитора пептида оптималне дужине. Редослед инхибиционих ефикасности је металопептид > амид > слободни пептид, што се подудара са очекивањима имајући у виду постојање два негативно наелектрисана бочна ланца у месту везивања. У присуству повишених концентрација NaCl, инхибиција металопептидима је мање ефикасна, док се инхибиција слободних пептида побољшава. До промене инхибиције амида не долази. Ови резултати су конзистентни са електростатичким интеракцијама између инхибитора и активног места. Насупрот овоме, трипсин има два позитивно наелектрисана остатка (Lys-60 и Arg-62) у S' везујућем региону и сходно томе инхибиција слободним пептидима је ефективнија од позитивно наелектрисаних металопептида. Опсервације на протеинази K нису конзистентне са обрасцем ефикасности уоченим за друга два ензима, што сугерише да једно позитивно наелектрисање (Arg-218) у S' региону не одређује везивање. Те студије демонстрирају да адиција металног једињења може да промени афинитет везивања супстрата путем електростатичких ефеката.
У студијама комплекса Co(III) Шифове базе и пептидних конјугата тих комплекса показано је да ефективно инхибирају тромбин и термолизин.[54][55][56] Пептидни конјугат селективно инхибира тромбин у смеши са две друге серинске протеазе (Kи = μM). Селективност проистиче из интеракције пептидне компоненте, док је сама инхибиција последица кобалт(III) координације са хистидинима активног места. Алтернативно, кобалт се може координирати са хистидинима у близини али не и у самом активном месту, чиме се пептид закључава у месту везивања супстрата. Такође, показано је да ови комплекси имају способност везивања хистидина у модел систему пептида из цинковог прста HIV нуклеокапсидног протеина.[70] У овим студијама је помоћу 1H NMR спектроскопије демонстрирана директна интеракција између кобалтних комплекса и хистидина у цинковом прсту, што доводи до ремећења структуре цинковог прста. Из поменутих студија проистиче да ови комплекси могу да инхибирају цинкове металопротеазе.
Након што је класа инхибитора цинк-посредованих серинских протеаза окарактерисана,[61][62][63][64] у кристалографским студијама на трипсину је уочено да се ти инхибитори тетраедрално координирају са егзогеним јоном цинка између два хелирајућа атома азота инхибитора и два остатка активног места (His57 и Ser195).[62] Присуство цинка појачава инхибицију за скоро три реда величине, и у случају појединих инхибитора производи селективност. Ова класа инхибитора представља јединствен приступ у којем сам инхибитор није метални комплекс али је присуство прелазног метала од кључног значаја за инхибицију.
Серинске протеазе су имплициране у процесе бројних болести, а инхибиција ових ензима активно је поље изучавања.[62][64] Присуство хистидина у активном месту и афинитет јаких киселина за азот чини инхибицију серинских протеаза помоћу металних комплекса логичним избором. Нов приступ дизајну инхибитора, као што је описано изнад, везује органска једињења за активна места путем цинковог јона као „моста” (граничне Луисове киселине), што сугерише да цинк можда делује као регулаторни елемент. Ови мали молекули представљају потенцијални оквир за конструисање бројних других инхибитора, где инхибиторна порција молекула остаје непромењена, док се остатак молекула може прилагођавати да би се променила специфичност.
Неуролошке примене[уреди | уреди извор]
| Неуролошке примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| јон | Li | аденилатна циклаза, триптофанска хидроксилаза, Ca2+-ATPаза[71] | |
| јон | Al | серинске протеазе, α-химотрипсин[72] | |
| јон | Al | моноаминооксидаза А[73] | |
| јон | Al | калпаин[74] | |
| јон | Al | калпаин, хексокиназа, глукоза-6-фосфат дехидрогеназа[75] | |
| порфирини | Fe, Zn | ацетилхолинестераза[76] | |
| порфирини | Cr, Zn | хем оксигеназа, азот-моноксид синтаза[35] | |
| протопорфирин | Sn | хем оксигеназа[36] | |
| цисплатин, цоппер сулфате | Pt, Cu | моноаминооксидаза[77] | |
| јон | Cu, Cd, Pb, Mg, Zn | лизозомна, цитопласмична протеиназа, калпаин I и II[78] | |
| јон | Zn | матричне металопротеиназе, секретазе, цитохром c оксидаза, азот-моноксидна синтаза, ендонуклеаза[79] | |
Једна од најбоље познатих области примене металних инхибитора у неурологији је употреба литијума као третмана за биполарни поремећај (манично-депресивну болест). Литијумска терапија је уведена 1949. године, али прецизни механизам њеног терапеутског дејства није био познат. Последњих година су објављени извештаји који индицирају да литијум утиче на путеве инозитол фосфолипидне хидролизе (мада није јасно да ли је то услед инхибиције инозитол-1-фосфатазе) и да инхибира аденилатну циклазу.[71]
Улога алуминијума у Алцхајмеровој болести и детаљни механизам његовог учешћа у развоју болести нису потпуно разјашњени. Повезаност алуминијума са болешћу је имплицирана стицајем околности услед повишених нивоа алуминијума у мозгу пацијената са Алцхајмеровом болешћу и амиотрофичном латералном склерозом.[72][75][74] Алуминијумски садржај је висок у плаковима, неурофибриларним свежњевима и неуритским наслагама карактеристичним за поменута обољења. Алуминијум инхибира мождане хексокиназе[80] и некомпетитивно инхибира мождану митохондријску моноаминску оксидазу-A (MAO-A)[73] (као што је то случај са цревном MAO, у контексту канцера). Постоје индикације да алуминијум активира серинске протеазе, и да су тако активиране протеазе накнадно отпорне на дејство других инхибитора.[72][75] Серинске протеазе пресецају β-амилоидне прекурсорске протеине (APP) и формирају β-амилоидне пептиде. Предложен је модел по којем алуминијум супресује инхибиторски домен протеаза, чиме поспешује протеолитичко формирање пептида који се затим акумулирају и иницирају формирање плакова.[72]
Низ других метала је био имплициран у формирање амилоидних плакова. Примећено је да Zn2+, Fe2+ и Cu2+ (μM), као и Al2+ (mM), узрокују агрегацију при физиолошким концентрацијама β-амилоидних протеина.[81][82][79][83][84][85] Хистидински модификован људски A бета(1-40) не подлеже агрегацији посредством Zn2+, Fe2+ или Cu2+, из чега произилази да хистидини учествују у металом индукованој агрегацији.[81] Постоје индикације да метали делују путем различитих механизама. Fe2+-индукована агрегација је инхибирана присуством антиоксиданаса, док они немају утицаја на Zn2+-индуковану агрегацију. Овај несклад сугерише да Fe2+ узрокује агрегацију путем оксидативног механизма.[82] Познато је да оксидација може да индукује агрегацију,[86] те да β-амилоиди имају прооксидантна својства — посебице у присуству алуминијума.[87] Азот-моноксидни донори као што је SNP (који NO формирају услед оксидативног стреса) могу да посредују акумулацију цинка у хипокампалним ћелијама, те постоји могућност да су оксидативни ефекти повезани са цинковим ефектима.[79] За разлику од тога, механизам Zn2+-индуковане агрегације није зависан од оксидације, него се заснива на директним интеракцијама са пептидима.[81][82][84][85] Поред свог агрегационог дејства, Zn2+ инхибира бројне протеолитичке ензиме који учествују у трансформацијама амилоида, укључујући матрикс металопротеиназе (MMP) одговорне за деградацију амилоидних пептида, а вероватно и α-секретазе одговорне за пресецање амилоидног прекурсорског протеина.[79] Инхибиција протеолизе се остварује путем два различита вида дејства метала на супстрате: 1. APP има место везивања за Zn2+ и након везивања долази до инхибиције пресецања на α-секретазном месту, и 2. MMP ензими не пресецају агрегиране амилоиде. За бакар и кобалт (50 μM) утврђено је да инхибирају APP пресецање.[88] Директна интеракција са секретазама није потврђена у APP студијама.
Осим амилоидних плакова, Алцхајмерово мождано ткиво карактеришу неурофибриларни сплетови. Истражује се мноштво различитих фактора да би се утврдио узрок овог феномена, укључујући абнормални транспорт неурофиламената и абнормалну деградацију. Показано је да алуминијум инхибира калцијумом активирану неутралну протеиназу (калпаин II) која посредује разлагање неурофиламентних подјединица и цитоскелеталних протеина.[74] AlCl3 и алуминијум лактат инхибирају пречишћени калпаин II, из људског церебралног кортекса, са IC50 вредношћу од 200 μM и 400 μM, редом. Инхибиција дејства калпаина је последица директне интеракције са ензимом, пошто преинкубација супстрата [14C]метилазоказеина са алуминијумом нема ефекта на инхибиторну ефикасност. Алуминијумска инхибиција исто тако обухвата интеракцију са цитоскелеталним протеинима, и у неким случајевима (нпр. код неурофиламентних подјединица NF-H и NF-M) алуминијум индукује формирање нерастворних комплекса урее. Стога је инхибиција протеолизе алуминијумом вишеструки процес који обухвата директно везивање за ензим, везивање за супстрат чиме се омета протеолиза, те формирање супстратних комплекса који су отпорни на протеолизу. Алуминијум има висок афинитет за фосфате и сматра се да се везује за фосфорилисане групе на неурофиламентним протеинима.[74] Упркос овим интеракцијама, механизам инхибиције калпаинина није расветљен.
Такође је показано да алуминијум инхибира метаболичке ензиме у мозгу, чиме се производе метаболичке грешке. Могуће је да акумулација таквих метаболичких грешака доприноси неуролошким поремећајима као што је Алцхајмерова болест. Хексокиназа, Mg(II)-зависни ензим, катализује први корак у циклусу гликолизе, којим се глукоза разлаже уз ослобађање енергије. Инхибиција хексокиназе је посредована везивањем алуминијума за супстрат; ATP има 107 пута већи афинитет за Al(III) него Mg(II).[75] Док највећи део глукозе подлеже гликолизи, 15—20% се подвргава хексозомонофосфатном шанту. Један од кључних ензима у овом путу, глукоза-6-фосфат дехидрогеназа (G6PD), инхибира се посредством Al(III) (μM распон).[75] До тога долази услед директне интеракције са ензимом; Al(III)-везани ензим подлеже конформационој промени до насумичније уређене структуре (судећи по налазима циркуларне дихроизне спектроскопије).

Тренутно се органски ацетилхолинестеразни инхибитори користе у третману Алцхајмерове болести; међутим, порфирини цинка и гвожђа исто тако инхибирају ацетилхолинестеразу.[76] Број и позиције флуоринских група на порфиринском прстену имају огроман ефекат на инхибиторну активност.[89]
С обзиром да постоји евиденција да долази до акумулације металних јона у неколико болести централног нервног система (CNS), од знатног интереса је да се утврди да ли ова акумулација има улогу у патогенези болести, а ако је то случај и да се одреди биохемијска природа њиховог учешћа. У једној недавној студији, велики број лизозомалних и цитоплазмичних протеиназа које су присутне у церебралном кортексу тестиран је за инхибицију металним јонима.[78] Утврђено је да милимоларне концентрације Cu2+, Cd2+, Pb2+, Hg2+ и Zn2+ инхибирају све тестиране лизозомалне протеиназе. Ови јони исто тако инхибирају цитоплазмичне протеиназе у различитим мерама а у зависности од металног јона. Пролинска ендонуклеаза и леуцилна аминопептидаза се инхибирају 50% или више са Zn2+ и Cu2+, редом. Аланил-, леуцил- и трипептидиламинопептидазе су инхибитиране са 0,05 mM Fe2+. Пироглутамилна пептидаза се инхибира са 0,05 mM Cu2+, Cd2+, Mn2+, Hg2+ или Zn2+. Аланил- и рипептидиламинопептидазе, пролинска ендопептидаза, те пироглутамил аминопептидаза, инхибиране су у различим мерама са Co2+ и Mn2+. Cd2+, Hg2+, Mn2+, Zn2+ и Al3+ инхибирају калпаин I и II у различитим мерама при концентрацији 5 mM. Импликације ових налаза о металним јонама су предмент истраживања.
Из ових радова следи да је улога металних јона у неуролошким болестима комплексна и разнолика. Метални јони демонстрирају разноврстан асортиман ефеката, од кинетичких до структурних. Кинетички ефекти могу да буду инхибиторни или активирајући. Структурни ефекти могу да подстакну агрегацију или отежају везивање. Ови ефекти наговештавају да метални јони могу да буду интиматно укључени у процес ензимске регулације. Да би се спровела ин виво испитивања било би неопходно да се остваре милимоларне концентрације метала у ткивима, што је нормално случај под физиолошким условима. Другим речима, потребно је правити разлику између потенцијално регулаторних процеса и токсичних ефеката.
Артритисне примене[уреди | уреди извор]
| Артритисне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| Ауранофин, натријум тиомалат | Au | протеинска киназа C[90][91] | |
| триметиламински карбоксиборани | B, Cu, Fe | еластаза, колагеназа, липоксигеназа, катепсин, циклооксигеназа[92] | |
| јон | Al | калпаин I[93] | |
| амински карбоксиборанеи и њихови естри | B | инозин монофосфат, де ново регулаторни ензими у синтези липида[94] | |
Једињења злата, као што је ауранофин, екстензивно су коришћена за третман реуматоидног артритиса, мада механизам њиховог дејства још увек није утврђен. Многе студије су демонстрирале инхибицију лизозомалних ензима[95][96] и протеинске киназе C, што може да објасни имуносупресивно дејство соли злата.[90][91]
Комплекси бакра[97][98] и бакарни комплекси антиинфламаторних лекова[99] показали су се ефективним као антиинфламаторни агенси. Постоје индикације да ови комплекси утичу на више ензимских система, а могуће је и да сам бакар има улогу у патогенези болести. Оболели од артритиса имају повишене просечне серумске или плазмене концентрације бакра, што је у директној корелацији са јачином и активношћу болести.[97] Утврђено је да бакар инхибира глутатион-S-трансферазу, а умањена GST активност је симптоматична за хронични артритис. Познато је да су бројни од бакра зависни ензими неопходни за опоравак од упале ткива.
Ензими протеолитичког пута су фреквентно имплицирани у деструкцију хрскавице оболелих од артритиса. Они су металопротеиназе, серинске протеазе и цистеинске протеазе, генерално присутни у везаном облику са природним инхибиторима. Систем калпаин-калпастатина је значајан јер је калпастатин (инхибитор калпаина) аутоантиген код скоро 50% реуматоидних артритисних пацијената и постоји евиденција да је калпаин прекомерно изражен код артритисних болесника.[100] Калпаин је Ca(II)-зависна цистеинска протеаза која се јавља у виду две изоформе: 1. калпаин I, за чију активацију се неопходне ниске концентрације калцијума, и 2. калпаин II, коме су потребне високе концентрације. Јони алуминијума различито утичу на ове две изоформе у калцијум-зависном маниру.[101] У присуству милимоларне концентрације калцијума, Al инхибира калпаин II у концентрационо зависном маниру, док је калпаин I максимално инхибиран унутар уског концентрационог опсега (0,1—0,5 mM Al). У одсуству калцијума, алуминијум активира калпаин II (који је иначе неактиван).
Имајући у виду ефективност борана као серинскопротеазних инхибитора, али и улогу протеаза у артритису, није изненађујуће да је утврђено да су бројни амински карбоксиборани антиинфламаторни агенси. Комплекси бакра и гвожђа триметиламинских карбоксиборана инхибирају активност лизозомалних и протеолитичких ензима у макрофагама,[92] као и неки од самих аминских карбоксиборана.[94] Међу инхибираним ензимима су неутрални катепсин, трипсин, еластаза, колагеназе I и II, простагландинска синтаза, циклооксигеназа (индукована код инфламаторног артритиса)[102] и 5'-липоксигеназа. Сви су инхибирани при микромоларним концентрацијама.[92] Такође је утврђено да амински карбоксиборани имају мноштво других ефеката, укључујући инхибицију регулаторних ензима који учествују у де ново синтези липида, ДНК и РНК. Путем ин виво експеримената је исто тако утврђено да амински карбоксиборани врше различите утицаје, укључујући снижавање серумског холестерола, блокирање калцијумске ресорпције (што је проблематично код остеопорозе) и редуковање инфламација.[94] Даља истраживања су неопходна да би се утврдила специфичност ових агенаса и структурна својства која утичу на разна терапеутска својства. Артритис је добар пример болести у којој су метални комплекси екстензивно коришћени као терапија иако механизам дејства није познат.
Примена на инфекције[уреди | уреди извор]
Виралне примене[уреди | уреди извор]
| Виралне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| полиоксоволфрамати | W | HIV реверзна транскриптаза, РНК полимераза, ДНК полимераза[103] | |
| тиосемикарбазони | Sn | реверзна транскриптаза вируса леукемије[104] | |
| TSAO | Si | HIV реверзна транскриптаза[105] | |
| трифлуоперазин | V, Cu, Ni, Pd, Sn | реверзна транскриптаза вируса леукемије[106] | |
| стрептонигрин | Zn | топоизомераза, HIV реверзна транскриптаза[107] | |
| јони | Fe, U, V, Ti, Pb, Cu, Pd | протеиназа[108] | |
| батокупроинска дисулфонска киселина | Cu | протеаза, интеграза[109] | |
| јони | Zn | протеаза[110] | |
| јони | Zn | ренин, протеаза[108] | |
| инхибиторни хелат | Cu | протеаза[111] | |
| фенантролин, неокупроин, батокупроински комплекси | Cu | интеграза[112] | |
| ароматични полихидроксилати | Mn | интеграза, други ензими којима је потребан метал[113] | |
| порфирини | Fe, Co | хем оксигеназа[34] | |


Вируси користе релативно мали број, јединствених ензима за одржавање свог животног циклуса, што чини те ензиме атрактивним метама за антивирусне лекове.[114] На пример, геном вируса људске имунодефицијенције (HIV) кодира три критична ензима: 1. реверзну транскриптазу која конвертује инфекциону виралну ssРНК у dsДНК, 2. интегразу која умеће dsДНК у домаћинов геном, и 3. протеазу која пресеца вирусне генске продукте до њихових крајњих форми.[115] Вирусни ензими су генерално у већој мери конзервирани, а то је посебно случај са њиховим активним местима у односу на покровне протеине, још једну класу металекова; стога су мање склони развоју мутационе отпорности на лекове. Током последњих неколико декада огромни напори су уложени у истраживање начина спречавања пропагације HIV вируса, а један од главних терапијских циљева је била реверзна транскриптаза.
Реверзна транскриптаза (RT) проминентна је мета за инхибиторе јер је дистинктна у односу на нормалне полимеразе ћелија домаћина и физички одвојена од репликационе машинерије домаћина (вирална транскриптаза је цитоплазматична, а не једрена). Реверзна транскриптаза је мултифункционални ензим. Она делује као полимераза која формира плус и минус ланце ДНК и као рибонуклеаза Х која разлаже РНК порцију РНК-ДНК хибрида.[116] Инхибиција може да буде усмерена на било коју од тих функција или места везивања ензима, мада сви тренутно одобрени инхибитори утичу на полимеразну функцију.[117] Многи нуклеозидни аналози и ненуклеозидни инхибитори су развијени током последњих година, али релативно мали број тих инхибитора су метални комплекси.
Полиоксоволфрамати, а посебно серије силиковолфрамата из кегинске групе, класа су неорганских једињења за које је показано да имају антивирално дејство.[103] Ова једињења инхибирају виралну репликацију у HIV-ом инфектираним ћелијама и испољавају компетитивну и некомпетитивну инхибицију пречишћене или поли(етилен гликолом) преципитиране реверзне транскриптазе. Инхибиција РНК-зависне ДНК полимеразне функције се остварује на 3—6 пута нижој концентрацији него за ДНК-зависну ДНК полимеразну активност. Тестови на другим пречишћеним ДНК полимеразама индицирају да су силиковолфрамова једињења најсензитивнија против вируса леукемије мишева (IC50 = 0,0035 μM), мање ефективна против HIV-1 RT (IC50 = 3 μM) и релативно неефективна против људске ДНК полимеразе 1 (IC50 = 43 μM). Мада је ДНК полимераза α донекле сензитивнија на инхибицију од HIV-1 RT, тестови у култури су показали антивиралну активност без цитотоксичности; концентрације неопходне за производњу цитотоксичности су неколико редова величине више од концентрације неопходне за елиминацију вируса. Мада специфичност тих једињења против RT није установљена и тачно место инхибиције на RT није познато, њихово антивирално дејство у културама подстиче даља истраживања.
Тиосемикарбазони су већ дуже време познати као антивирални агенси. Диорганокалај(IV) комплекси пиридил тиосемикарбазона су недавно окарактерисани и утврђено је да инхибирају RT.[104] Комплекси бакра и кобалта истог лиганда (L) такође су испитани.[118] Sn(Bu)2(L) и Sn(Ph)2(L) комплекси су најефективнији против RT, али нису тестирани на другим полимеразама да би се утврдила специфичност инхибиције. Стога се на бази ових студија антивирално дејство једињења не може искључиво приписати њиховој инхибицији RT. Такође је познато да тиосемикарбазони инхибирају рибонуклеотидне редуктазе, РНК-зависну ДНК полимеразу, те дихидрофолатну редуктазу.[119]
Трифлуоперазини (TFP), деривати психотерапеутског лека фенотиазина, такође имају потврђено антивирално дејство. Метални комплекси TFP су тестирани на RT вируса леукемије мишева, и установљено је да метали поспешују инхибицију у редоследу VO(IV) > Ni(II) > Pd(II) > Cu(II) > Sn(IV) > слободни лиганд.[106] Ови комплекси су ефективни против реверзних транскриптаза више ретровируса. Стрептонигрин је антибиотик који је потенцијално могао да делује као антитуморски агенс за разне људске канцере; међутим, токсичне нуспојаве третмана стрептонигрином су довеле до прекида клиничких испитивања. Стрептонигрин такође селективно инхибира TT птичјег мијелобластозног вируса (AMV) и HIV без инхибирања ћелијских полимераза.[107] Механизам дејства стрептонигрина је испитан након прекида клиничких испитивања. Преглед резултата тих студија, укључујући детаљну структурну карактеризацију неколико металних комплекса лека, показао је да је метална јомплексација кључна за биолошку активност лека.[107] Међутим, прецизни механизам његовог терапеутског ефекта је још увек непознат.
Примена метал-хелирајућих деривата TSAO-T, а [2',5'-bis-O-(терт-бутилдиметилсилил)-β-дрибофуранозил]-3'-спиро-5-(4-амино-1,2-оксатиол-2,2-диоксид) нуклеозидног деривата тимина представља један другачији приступ побољшању инхибиције реверзне транскриптазе.[120] Родитељско једињење, TSAO, везује се за алостерно место лоцирано поред RT каталитичког места.[105] Ово место везивања инхибитора формира интеракције са оближњим Mg2+ местом везивања.[121] Нова класа једињења је дизајнирана са везаним инхибитором, TSAO-T, за металну хелирајућу групу, јер се сматрало да ће формирати бидентатни инхибитор са већим афинитетом за ензим. Неколико деривата је било синтетисано, а за оне са кратким алкилним ланцима је утврђено да су знатно ефективнији антивирални агенси. Неколико деривата који су једнако активни као родитељско једињење има знатно мању токсичност (10 пута мање концентрације резултују са 50% повећања ћелијске одрживости). Ова класа једињења је пример инхибитора који не садрже метал и инхибирају путем формирања металног комплекса.
HIV-1 протеаза је аспартилна протеаза која формира зреле протеине из продуката gag гена (групно специфичних гена) и pol гена (ДНК полимеразе). Отпорност на протеазне инхибиторе се теже остварује код вируса него отпорност на RT инхибиторе,[122] те су развијени многи пептидни инхибитори.[68] Утврђено је да бројни метални јони делују као инхибитори HIV-1 протеазе, а да су најефективнији тешки јони (Fe3+, UO22+, VO3−/VO43−, TiCp2Cl2, Pb2+), као и да су они углавном тетраедрално координирани.[108] Метали некомпетитивно инхибирају ензим, тако што симултано са супстратом заузимају активно место. Сматра се да се метали координирају са карбоксилатним бочним ланцима активних остатака Asp25 и Asp125, мада то није дефинитивно потврђено. Могуће је да ће ове обзервације подстаћи дизајн инхибитора HIV-1 протеаза који ће садржати метале који се везују за ензим јонским или ковалентним везама, те да ће стога бити знатно јаче везани од пептидних инхибитора.
Гореописана студија металних јона је наизглед у конфликту са резултатима једне раније студије која је показала да јони цинка и сребра некомпетитивно — а јони бакра компетитивно инхибирају протеазе и ренин из HIV-1.[108] Ranija studija je sprovedena na rekombinantnoj proteazi izolovanoj iz E. coli, док је каснија студија користила синтетичку SF2 секвенцу протеазе, у којој је аминобутирна киселина замењена цистеинским остатком.[22][68][123][124] Није сасвим јасно у којој мери синтетички ензим опонаша природни ензим. Исто тако, студије су изведене на различитим pH вредностима, раније студије на неутралном pH а касније на pH 5. Раније студије су заправо показале да је инхибиција цинком у великој мери зависна од pH. Процењује се долази до надметања цинка са протоном за групу са pKa = 7,0. Молекуларне динамичке симулације изведене на протеази у присуству цинка индицирају да се јони цинка везују за каталитички активно место на остацима Asp25 и Asp25' без поремећаја структуре ензима.[110]
Утврђено је да је CuCl2 ефективан инхибитор протеазе, али не и мутиране протеазе у којој су аланини супституисани цистеинима.[125] Мутирана протеаза може инхибирати CuCl2 у присуству бакарних хелатора. Утврђено је да је батокупроин сулфонска киселина Cu(I), BCSD-Cu(I), компетитивни инхибитор протеазе.[109] Сама BCSD не инхибира ензим, нити инхибиција комплекса може да буде блокирана помоћу EDTA. Из овога следи да је метални комплекс активни инхибитор, а не слободни лиганд нити слободни метал. Комплекс исто тако инхибира мутирану протеазу којој недостају цистени. Други бакарни хелати инхибрају HIV-1 протеазу. Утврђено је да је диаква[бис(2-пиридилкарбонил)амидо]бакар(II) нитрат дихидрат компетитивни инхибитор протеазе.[111] Ова студија такође сугерише да су молекули воде у активном месту који су присутни између Asp25 и Asp125 важни за структуру ензима. Ова чињеница може да утиче на дизајн инхибитора који не садрже хидроксилне супституенте.
Утврђено је да бакарни комплекси инхибирају HIV интегразу.[112] Долази до некомпетитивне инхибиције механизмом који се разликује од једноставног блокирања везивања супстрата или везивања ДНК. Инхибиција мутаната C- и N-терминалног брисања овим комплексима указује на чињеницу да се ови комплекси везују за сржни регион интегразе. Селективност комплекса за интегразе до сада није демонстрирана. Интегразе садрже мотиве цинковог прста у близини N-терминуса и конзервирани мотив аспартатних и глутаматних остатака који вероватно учествују у ДНК везивању или пресецању.[115] Они такође могу да представљају места потенцијалних интеракција са металним комплексима. За велики број антрахинона и сродних полихидроксилисаних фенолних молекула је показано да инхибирају интегразе при наномоларним концентрацијама.[113] Ова једињења реагују и са другим ензимима за чије дејство су неопходни метали (реверзне транскриптазе мишјег леукемијског вируса, MoMLV, и рестрикциони ензими Pvu II и EcoRI), али не и са ензимима којима нису потребни метали. Из ове чињенице произилази да метали учествују у инхибиторном механизму. За нека од тестираних једињења је познато да су метални хелатори. MoMLV инхибиција је ефикаснија у присуству Mn2+ него Mg2+ (до 26 пута мање вредности IC50 у зависности од једињења). Овај ефекат је уочен и код интегразе.[126] Познато је да каталитички домен интегразе везује метале, а инхибиција може да обухвати формирање терцијарног комплекса инхибитора, метала и ензима; међутим, то ово још увек није доказано.
Описани инхибитори виралних ензима углавном немају ексклузивну специфичност. Изузев деривата TSOA-T, инхибитори ове класе нису дизајнирани за интеракцију са специфичним местима. Многи инхибитори су идентификовани скринингом прво за инхибицију виралне репликације а затим за активност на пречишћеним ензимима.
Невиралне примене[уреди | уреди извор]
- Бактерије, глијвице и паразити
| Антимикробне примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| 1-амино-3-(2-пиридил)изохинолин, јони | Cu | NADH оксидаза, лактатна дехидрогеназа[127] | |
| сулфадиазин | Ag | фосфоманозна изомераза[128] | |
| тровалентна једињења арсена | As | трипанотионска редуктаза, глутатионска редуктаза[129] | |
| [XxMxOoHh]n- | Mo, V | киселинска фосфатаза[130] | |
| шећерни комплекси | Ni | хитиназа[131] | |
| тровалентна једињења амонијака | Sb | фосфофруктокиназа[132] | |
| пентостам | Sb | клинички демо[133] | |
| тиосемикарбазони | Cu | дихидрофолатна редуктаза[119] | |
| јон | V | ектокиселинска фосфатаза[134] | |
| титанил сулфати | Ti | серинске протеазе[65] | |
Неке од најранијих примена неорганских једињења у медицини су биле у виду антисептика и антимикробних агенаса.[44][67][135] Заправо, органоарсенична једињења су била прва једињења која су успешно примењена за третман сифилиса (она су касније замењена пеницилином), а коришћена су као адитиви сточне хране за спречавање бактеријских и паразитских инфекција.[67] Сулфаниламиди су велика класа једињења која испољава антибактеријску ефективност, а познато је и неколико металних јона који имају антимикробно дејство.[136] Органометална једињења се рутински тестирају за антимикробне ефекте ради идентификације могућих лекова. Осим агенаса који инхибирају ензиме, постоји мноштво агенаса чији механизам није познат.[137][138][139][140][123]
Једна недавна студија се бавила испитивањем инхибиције серинских протеаза код бактерија и гљивица ради развоја антимикробиних агенаса. Скрининг великог броја металних јона на трипсину из разних извора (пречишћених и у бактеријским лизатима) и говеђем панкреасном химотрипсинину показао је да само Ti(IV) у облику титанилног сулфата инхибира трипсин, док други метали или увећавају активност (Ca2+, Mn2+) или немају ефекта.[65] Ова инхибиција је компетитивна, што значи да се инхибитор везује за активно место. Инхибиција химотрипсина није уочена, те је предложено да се Ti(IV) везује за Asp-198 у супстратном месту везивања за остатак који није присутан код химотрипсина. Утврђено је да су титанилни алкохолни комплекси мање инхибиторни (25% инхибиторне активности) него сулфати. Петокоординатна геометрија Ti(IV) била је разматрана као могуће објашњење уочене активности Ti(IV) против бактерија у односу на друге металне јоне и геометрије.
Тривалентни арсенични лекови, као што је меларзопрол, још увек се рутински користе у третману трипанозомом посредованих болести, као што је афричка болест спавања. Механизам њиховог дејства није испитан, мада се сматра да је последица интеракције са протеинским дитиолима. Познато је да тривалентна једињења арсена формирају стабилне адукте са дитиол трипанотионом, те да се ти адукти ефективније надмећу за активно место трипанотион редуктазе.[141] Трипанотион, који је аналоган глутатиону код сисара, јединствен је за трипанозоме. Једна недавна студија је испитала утицај неколико једињења арсеника на трипанотионску и глутатионску редуктазу, два ензима која садрже каталитичке сулфидрилне групе.[129] Инхибиција оба ензима је знатно сензитивнија у присуству НАДПХ, што је индикација да цистеински сулфидрили морају да буду редуковани да би формирали интеракције са лековима. Трипанотионска редуктаза је сензитивнија на инхибицију од глутатионске редуктазе. Инхибицију обуставља дихидротрипанотион. Иако једињења арсена инхибирају ензим, пошто је дихидротрипанотион ин виво доступан у знатно вишим концентрацијама од трипанотионске редуктазе, мало је вероватно да би инхибиција овог ензима могла да има терапеутски учинак на трипанозомијазу.
Антимонијали су дуго коришћени као антипаразитици,[67][135] и још увек се користе у третману слузокожне лишманијазе.[133] Низ других метала се испитује за њихову активност против лишманијазе. Постоје индикације да киселинске фосфатазе (ACP) доприносе патогености трипаносома Leishmania. Те фосфатазе могу да инхибирају бројни прелазни метали и њихови комплекси, као што су арсенат и ванадат.[134] Студије у којима је коришћена тартратно сензитивна киселинска фосфатаза из људског семеног флуида и тартратно резистентна фосфатаза из протозое Leishmania donovani демонстрирале су да хетерополианјонски комплекси молибдена (са Ge, Fe, As, Ce, Th) селективно инхибирају ове ензиме.[130] Тестиране су четири класе комплекса, које садрже 4, 6—8, 12 или 18 атома Mo. Селективност је процењена на основу инхибиције поменутих ензима и одсуства ACP инхибиције из људске слезине. β-глукуронидазе и α-манозидазе из слезине су такође испољиле мало или нимало инхибиције услед дејства молибденат-хетерополианјона. Студије унакрсног надметања између ових инхибитора индицирају да се неки од комплекса везују за активно место, док се други везују за друго место које утиче на активно место. На пример, везивање ванадата и једног од комплекса Mo није било узајамно искључиво, а ванадат је појачавао инхибицију Mo комплекса.
Антимон се такође примењује као антишистозомијални агенс. Недавним истраживањима је утврђено да разни антимонијали инхибирају фосфофруктокиназу (PFK) из метиља Schistosoma mansoni.[132] Опстанак шистозома је зависан од велике брзине гликолизе, а PFK је кључни ензим у гликолитичком путу — садржи 20 цистеина. Упоређивањем шистозомалне и сисарске PFK је утврђено да антимонилтартарат калијум преферентно инхибира паразитов ензим. Механизам ове селективности није разјашњен.
Метални јони и метални комплекси су ефективни антифунгални агенси против патогеног квасца Candida albicans. Комплекси сребра инхибирају фосфоманозну изомеразу (PMI), кључни ензим у биосинтези квашчаних ћелијских зидова, са nM Ki.[128] PMI мутант код кога је Cys150 замењен са аланином понаша се на сличан начин као и природни ензим, али не бива инхибиран једињењима сребра и 1000 пута је мање сензитиван на живу. Из овога произилази да је Cys150 место интеракције инхибитора. Јони сребра инхибирају PMI са 210 пута вишом бимолекуларном константом брзине за људски ензим. Ова једињења редукују специфичност за људски ензим до 1,3 : 1. I док их ово не квалификује као инхибиторе који су селективни за паразите, може се претпоставити да је могуће развити лек путем модификација органских група. Комплекси никла инхибирају хитиназу, која такође учествује у биохемији ћелијског зида квасца-гљиве C. albicans.[131] Поменути комплекси садрже N-гликозиде изведене из аминошећера, који инхибирају у компетитивном маниру.
Микоплазми недостаје чврст ћелијски зид. Јонски бакар је ефективан инхибитор микоплазичне активности и показано је да инхибира ензиме у гликолитичком путу, NADH оксидазу и лактатну дехидрогеназу.[127] 2,2'-бипиридински тип лиганда олакшава транспорт бакра кроз микоплазмичну мембрану, па је антимикоплазмично дејство бакра знатно повећано у присуству ових лиганда — мада присуство лиганда умањује инхибиторни ефекат на пречишћеним, изолованим ензимима. Ова опажања потврђују да је јон бакра токсичан материјал, а да лиганд само служи као преносник.
- Третман чирева
| Третман чирева | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| јони | Bi | фекална слузокожна сулфатаза[142] | |
| јони | Bi | H. pylori ATPаза[143] | |
Бизмутове соли су коришћене у терапији чирева. Познато је да оне инхибирају аденозинтрифосфатазу из желучане бактерије H. pylori (која учествује у развићу пептичног чира),[143] као и фекалну слузокожну сулфатазу (чије је изражавање повишено код улцерозног колитиса).[142]
Токсичност примене[уреди | уреди извор]
| Токсичност примене | |||
|---|---|---|---|
| Комплекс | Метал | Инхибирани ензим | |
| ионс | Al | γ-аминолевулинска киселина[144] | |
| јони | Al | хексокиназа[145] | |
| јони | Cd, Cu, Hg, Zn, Pb | хексокиназа[146] | |
| јони | Al | глицеролна киназа[147] | |
| јони | Al, Cd, Pb | ATPаза[148] | |
| јони | As | поли-(ADP-рибоза) полимераза[149] | |
| јони | As | пируватна дехидрогеназа, ДНК лигаза[150] | |
| јони | As | метилтрансфераза[151] | |
| јони | As | метилтрансфераза[152] | |
| арсеноглутатион | As | глутатионска редуктаза[153] | |
| 3-арсонопируват | As | Фосфоенолпируватна мутаза[154] | |
| јон | Ni | ДНК полимераза[155] | |
| јон | Zn, Cd | ДНК лигаза[156] | |
| јон | Cd | О6-метилгуанин-ДНА метилтрансфераyа, ДНК полимераза β[157] | |
| cis-DDP | Pt | респираторни ензими[158] | |
| јони | V | пероксидаза рена, супероксид дисмутаза[124] | |
| јон | Ni | MutT-dGTPаза[159] | |
| јон | Pb | γ-аминолевулинатна дехидратаза[160] | |

Велика количина рада је уложена да би се одредио молекуларни механизам металне токсичности. Узрок смртности је комбинација више фактора. Разумевање путева на које метали утичу је пререквизит за спречавање токсичности, те пружа увид у потенцијалне примене у којима се токсичност искоришћава за производњу корисних ефеката. Алуминијумска токсичност индукује анемију, а сматра се да до овога долази услед пертурбације биосинтетичког пута хема.[144] Уочено је да алуминијум инхибира бројне ензиме ин витро, укључујући дехидратазу δ-аминолевулинске киселине (ака порфобилиногену синтазу),[144] хексокиназе,[145] глицеролне киназе[147] и ATPазу.[148] Механизам инхибиције се разликује од ензима до ензима. Дехидратаза δ аминолевулинске киселине која катализује други корак биосинтезе хема је металопротеин који везује осам јона цинка. Алуминијум некомпетитивно инхибира ове ензиме, из чега следи да се не везује за активно место, те да се вероватно надмеће са неким или свим јонима цинка.[144] Јонски пречник Al3+ је сличан пречнику Mg2+ или Fe3+, а могуће је да алуминијум инхибира Mg2+-зависне ензиме путем супституције за Mg2+ (на пример у хексокинази),[147] мада ово није било уочено у свим студијама.[145] За глицеролне киназе и хексокиназе је такође постулирано да се алуминијум надмеће са MgATP супстратом у облику алуминијум-ATP хелатног комплекса.[145][147] Кинетика инхибиције може да помогне у одређивању природе инхибиционог места, али су структурне студије неопходне за одређивање прецизног тока интеракције.
Друге студије су демонстрирале да Cd2+, Cu2+, Hg2+, Zn2+ и Pb2+ инхибирају хексокиназу (у ниском μM опсегу).[146] Cd2+ и Cu2+ су много ефективнији од других метала. Инхибиција помоћу Cu2+ доводи до пратећег снижења нивоа редукованог глутатиона (GSH). Преинкубација узорка са GSH заштићује ензим од Cu2+ инхибиције. Познато је да GSH формира GSH-Cu(I) комплексе, а заштитни ефекти GSH комплекса су вероватно последица једноставног уклањања Cu2+ из раствора. Предложени су бројни модели за релацију између хексокиназе, GSH и токсичности тешких метала ин виво.
Постоје индикације да је арсенична токсичност редокс зависна, тако да је пентавалентни As(V) знатно мање токсичан од тривалентне форме елемента, As(III).[153][151] Арсеник је карциноген, мада директно не оштећује ДНК. Најпроминентнија хипотеза за његов механизам деловања је инхибиција ензима путем везивања за сулфхидриле, те је знатан број студија био усредсређен на испитивање дејства арсеника на ензиме поправке и лигације ДНК. Утврђено је да As(III) инхибира ензим поли-(ADP-рибоза) полимеразу, који садржи два вицинална дитиола који посредују везивање ензима за прекиде ДНК ланаца.[149] Механизам инхибиције још увек није утврђен. Пируватну дехидрогеназу инхибира As(III) при микромоларним концентрацијама, али не и As(V). Неколико других ензима за ДНК поправку је тестирано и утврђено је да на њих As(III) нема утицаја, мада неки садрже SH групе од пресудног значаја за своју функцију.[150] Арсенит може да инхибира лигазну активност у култивисаним ћелијама али не и у нуклеарним екстрактима из тих ћелија, из чега следи да инхибиција лигаза није директна већ се јавља на неком другом нивоу поправке.[150] Спектроскопске студије As(III) инхибиције метилтрансферазе (ензима који учествује у модификацији и поправци неподударних ДНК сегмената) индицирају да се As(III) везује за Cys223, чиме индукује ефекат тешког атома (HAE) на оближњем Trp остатку. Ово је потврђено опсервацијом да се HAE не јавља код мутанта са Cys223 замењеним Ser223 остатком.[151][152] Појава HAE је заснована на налазима црвеног помака фосфоресцентног спектра и знатног скраћења животног века триплетног стања As(III)-пертурбираног триптофана. Ова интеракција не утиче на ензимску активност, тако да је инхибиција која је уочена у присуству вишка арсенита вероватно последица везивања за друге цистенске остатке ензима.
Инхибиција глутатионске редуктазе са As(III) конзистентна је са оксидацијом тиолних група у активном месту ензима.[153] Арсен формира арсеноглутатионске комплексе са глутатионом, и они делују као инхибитори мешовитог типа на глутатионској редуктази. Ензими који делују на форсфорним једињењима често препознају арсенске аналоге, нпр. аденилатна циклаза и РНК полимераза. Показано је да 3-арсонопируват компетитивно инхибира фосфоенолпируватну (PEP) мутазу са Ki = 27 μM.[154] PEP мутаза је главни ензим у биосинтетичком путу формирања C-P веза. Никл је попут арсена генотоксичан карциноген, мада прецизни механизам токсичности Ni није познат. Ni(II) служи као слаба замена за Mg(II) у неким полимеразама, док друге полимеразе бивају јако инхибиране.[155] Ефекат јона никла на инкорпорацију нуклеотида, процесивност и мисинкорпорацију проучаван је код седам различитих полимераза; изведен је закључак да је његов примарни ефекат инхибиција (микромоларни опсег). Међутим, ово зависи од бројних фактора чији значај варира од ензима до ензима. Дејство никла је комплексно, а прецизни механизам ометања полимеразне функције није установљен. Инхибиција репликације и поправке ДНК повезана је са мутагеношћу и карциногеношћу металних јона.[157] Уочено је да Ni(II) инхибира MutT-dGTPазу, која учествује у поправци 8-оксо-dGTP оштећења на ДНК (милимоларни Ki).[159] Ћелије изложене оксидативном стресу формирају 8-оксо-dGTP; присуство нуклеотида повишава мутациону фреквенцију A у C трансверзијама услед 8-оксо-dG-dA неспаривања. Инхибиција Mg(II)-зависног MutT ензима поправке може да доведе до повишене мутагенезе. Студије молекулским моделовањем указују да се Ni(II) не везује за место везивања Mg(II), него да индукује конформационе промене за које је предвиђени узрок везивање за хистидинске остатке.[159]
Уочено је да цинк и кадмијум такође инхибирају ензиме ДНК поправке.[157] Пречишћена ДНК лигаза се инхибира са 0,8 mM ZnCl2 и 0,04 mM CdCl2.[156] Оба метала инхибирају формирање интермедијера, трансферазно дејство и лигационо дејство, а немају ефекта на брзину мислигације. Другим речима, инхибиција једино утиче на ензимску активност док се тачност рада лизаге не мења. Лигазама је неопходан магнезијум као кофактор; Mg је неопходан за све три корака лигационе реакције која инхибира кадмијум и цинк. Јони Cd и Zn могу да делују путем супституисања јона Mg у месту везивања метала.
Један од метала с лошом репутацијом у очима јавности је олово. Тровање оловом заузима истакнуто место у јавној свести због мноштва инцидената узрокованих применом олова на радним местима, као и због тровања деце оловним бојама.[160] Један од механизама токсичности је инхибиција цинк металоензима, односно γ-аминолевулинатне дехидратазе (ALAD) која је такође некомпетитивно инхибирана алуминијумом. У случају олова, инхибиција се одвија путем супституције цинка оловом. Два алела ALAD ензима су идентификована код људи (ALAD1 и ALAD2) и они кодирају три дистинктна изозима. Тестирање великог броја деце (изложене ниским нивоима олова у животној средини) и радника из оловопрерађивачких фабрика показала су да ALAD2 позитивни имају повишене нивое олова у крви након сличних излагања и да су знатно сензитивнији на тровање оловом. Претпоставља се да ALAD2 јаче везује олово.[160]
Метална токсичност може да буде резултат оксидативних реакција. Ванадат учествује у мноштву таквих реакција, а недавно је објављена студија у којој је изучавано његово дејство на антиоксидантне ензиме.[124] Четири различита ензима су разматрана и утврђено је да ванадат инхибира пероксидазу рена. Ови налази додуше не дају јасну индикацију о релацији између антиоксидантске ензимске инхибиције и токсичности.
Знатан део литературе се бави једним другим механизмом инхибиције ензимске активности металним јонима: редукцијом количине ензима услед инхибирања транскрипције гена који кодирају ензим.[163][164] Највећим делом, резултати испитивања наглашавају да је токсичност узрокована металним јонима последица инхибиције која се јавља на многим нивоима у многим системима, те да је мало вероватно да било која појединачна промена може да буде самостално одговорна за токсичне ефекте.
Види још[уреди | уреди извор]
- Аналог прелазног стања
- Антиметаболит
- Фармакофор
- Инхибиција ензимских реакција
- Протеомика базирана на активности — грана протеомике која користи ковалентне инхибиторе ензима као индикаторе при изучавању ензимске активности
Референце[уреди | уреди извор]
- ^ Cannon, J. B. (1993). „Pharmaceutics and drug delivery aspects of heme and porphyrin therapy”. J. Pharm. Sci. 82: 435—446. PMID 8360819. doi:10.1002/jps.2600820502.
- ^ а б Tsangaris, J. M.; Williams, D. R. (1992). „Tin in pharmacy and nutrition”. Appl. Organomet. Chem. 6: 3—18. PMID 11192741. doi:10.1002/aoc.590060103.
- ^ а б Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid=1734381. - ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именом10.1021/cr9804285. - ^ а б в Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid=1371161. - ^ а б в Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid1542552. - ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid1610897. - ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid1551526. - ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid8265722. - ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid7853192. - ^ Marks, J. A.; Maines, M. D. (1992). „Tin-Protoporphyrin-Mediated Disruption In Vivo of Heme Oxygenase-2 Protein Integrity and Activity in Rat Brain” (PDF). Pediatr. Res. 32: 324—329. PMID 1408470. doi:10.1203/00006450-199209000-00016.
- ^ Hintz, S. R.; Vreman, H. J.; Stevenson, D. K. (1990). „Mortality of metalloporphyrin-treated neonatal rats after light exposure”. Dev. Pharmacol. 14: 187—192. PMID 2364856.
- ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid7843765. - ^ а б Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid8353156. - ^ а б Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid8445977. - ^ Cable, E.; Cable, J.; Bonkovsky, H. (1993). „Repression of hepatic δ-aminolevulinate synthase by heme and metalloporphyrins: Relationship to inhibition of heme oxygenase”. Hepatology. 18: 119—127. PMID 8325603. doi:10.1002/hep.1840180119.
- ^ Lathrop, J. T.; Timko, M. P. (1993). „Regulation by heme of mitochondrial protein transport through a conserved amino acid moti”. Science. 259: 522—525. PMID 8424176. doi:10.1126/science.8424176.
- ^ Bhasker, C. R.; Burgiel, G.; Neupert, B.; Emery-Goodman, A.; Kuhn, L. C.; May, B. K. (1993). „The Putative Iron-Responsive Element in the Human Erythroid 5-Aminolevulinate Synthase mRNA Mediates Translational Control” (PDF). JBC. 268: 12699—12705. PMID 8509404.
- ^ а б Serfass, L.; Burstyn, J. (1998). „Effect of heme oxygenase inhibitors on soluble guanylyl cyclase activity”. Arch. Biochem. Biophys. 359: 8—16. PMID 9799554. doi:10.1006/abbi.1998.0887.
- ^ а б Luo, D.; Vincent, S. (1994). „Metalloporphyrins inhibit nitric oxide-dependent cGMP formation in vivo”. Eur. J. Pharmacol.-Mol. Pharmacol. Sec. 267: 263—267. PMID 7522180. doi:10.1016/0922-4106(94)90149-X.
- ^ а б в г д Mariotto, S.; Cuzzolin, L.; Adami, A.; DelSoldato, P.; Suzuki, H.; Benoni, G. (1995). „Inhibition by sodium nitroprusside of the expression of inducible nitric oxide synthase in rat neutrophils”. Brit. J. Pharmacol. 114: 1105—1106. PMID 7542530. doi:10.1111/j.1476-5381.1995.tb13320.x.
- ^ а б Vickroy, T.; Malphurs, W. (1995). „Inhibition of nitric oxide synthase activity in cerebral cortical synaptosomes by nitric oxide donors: evidence for feedback autoregulation”. Neurochem. Res. 20: 299—304. PMID 7541898. doi:10.1007/BF00969546.
- ^ а б в Perry, J.; Marletta, M. (1998). „Effects of transition metals on nitric oxide synthase catalysis”. PNAS. 95: 11101—11106. PMID 9736696. doi:10.1073/pnas.95.19.11101.
- ^ а б Persechini A, McMillan K, Masters BS (1995). „Inhibition of Nitric Oxide Synthase Activity by Zn2+ Ion”. Biochemistry. 34: 15091—15095. PMID 7578122. doi:10.1021/bi00046a015.
- ^ а б Siegfried, G.; Amiel, C.; Friedlander, G. (1996). „Inhibition of Ecto-5′-nucleotidase by Nitric Oxide Donors”. J. Biol. Chem. 271: 4659—4664. PMID 8617729.
- ^ а б в Thomas, S.; Mohr, D.; Stocker, R. (1994). „Nitric oxide inhibits indoleamine 2,3-dioxygenase activity in interferon-gamma primed mononuclear phagocytes” (PDF). J. Biol. Chem. 269: 14457—14464. PMID 7514170.
- ^ а б в г Nicolaou, A.; Waterfield, C.; Kenyon, S.; Gibbons, W. (1997). „The Inactivation of Methionine Synthase in Isolated Rat Hepatocytes by Sodium Nitroprusside”. Eur. J. Biochem. 244: 8876—882. PMID 9108260. doi:10.1111/j.1432-1033.1997.00876.x.
- ^ а б Sato, T.; Kamata, Y.; Irifune, M.; Nishikawa, T. (1995). „Inhibition of purified (Na+,K+)-ATPase activity from porcine cerebral cortex by NO generating drugs”. Brain Res. 704: 117—120. PMID 8750971. doi:10.1016/0006-8993(95)01165-X.
- ^ Bredt, D. S.; Snyder, S. H. (1992). „Nitric oxide, a novel neuronal messenger”. Neuron. 8: 3—11. PMID 1370373. doi:10.1016/0896-6273(92)90104-L.
- ^ Jaffrey, S. R.; Snyder, S. H. (1996). „PIN: An associated protein inhibitor of neuronal nitric oxide synthase”. Science. 274: 774—777. PMID 8864115. doi:10.1126/science.274.5288.774.
- ^ а б Marletta, M. A. (1994). „Nitric oxide synthase: Aspects concerning structure and catalysis” (PDF). Cell. 78: 927—930. PMID 7522970. doi:10.1016/0092-8674(94)90268-2.
- ^ а б Moore, P. K.; Handy, R. L. C. (1997). „Selective inhibitors of neuronal nitric oxide synthase – is no NOS really good NOS for the nervous system?”. Trends Pharm. Sci. 18: 204— 211. PMID 9226999. doi:10.1016/S0165-6147(97)01064-X.
- ^ Bredt, D. S.; Snyder, S. H. (1990). „Isolation of nitric oxide synthetase, a calmodulin-requiring enzyme”. PNAS. 87: 682—685. PMID 1689048. doi:10.1073/pnas.87.2.682.
- ^ а б Weiss, G.; Lutton, J.; Fuchs, D.; Wernerfelmayer, G.; Bock, G.; Abraham, N.; Kappas, A.; Levere, R.; Wachter, H. (1993). „Comparative Effects of Heme and Metalloporphyrins on Interferon-γ-Mediated Pathways in Monocytic Cells (THP-1)”. Proc. Soc. Exp. Biol. Med. 202: 470—475. PMID 8456113. doi:10.3181/00379727-202-43561.
- ^ а б Meffert, M.; Haley, J.; Schulman, E.; Schulman, H.; Madison, D. (1994). „Inhibition of hippocampal heme oxygenase, nitric oxide synthase, and long-term potentiation by metalloporphyrins”. Neuron. 13: 1225—1233. PMID 7524564. doi:10.1016/0896-6273(94)90060-4.
- ^ а б Bing, O.; Grundemar, L.; Ny, L.; Moller, C.; Heilig, M. (1995). „Modulation of carbon monoxide production and enhanced spatial learning by tin protoporphyrin”. Neuroreport. 6: 1369—1372. PMID 7488726. doi:10.1097/00001756-199507100-00002.
- ^ а б в Pedregosa, J. C.; Casanova, J.; Alzuet, G.; Borras, J.; Garcia-Granda, S.; Diaz, M. R.; Guttierez-Rodriguez, A. (1995). „Metal complexes of 5-tertbutyloxycarbonylamido-1,3,4-thiadiazole-2-sulfonamide (B-H2ats), a carbonic anhydrase inhibitor. Synthesis and characterization of the copper(II) complex. Crystal structures of B-H2ats and the [Cu(B-ats)(NH3)2]2 dimer complex”. Inorg. Chim. Acta. 232: 117—124. doi:10.1016/0020-1693(94)04376-7.
- ^ а б Supuran, C. T.; Mincione, F.; Scozzafava, A.; Briganti, F.; Mincione, G.; Ilies, M. A. (1998). „Carbonic anhydrase inhibitors — Part 52. Metal complexes of heterocyclic sulfonamides: A new class of strong topical intraocular pressure-lowering agents in rabbits”. Eur. J. Med. Chem. 22: 247—254. doi:10.1016/S0223-5234(98)80059-7.
- ^ а б в Supuran CT, Scozzafava A, Saramet I, Banciu MD (1998). „Carbonic anhydrase inhibitors: inhibition of isozymes I, II and IV with heterocyclic mercaptans, sulfenamides, sulfonamides and their metal complexes”. J. Enzyme Inhib. 13: 177—194. PMID 9629536. doi:10.3109/14756369809028339.
- ^ а б Turkmen H, Durgun M, Yilmaztekin S, Emul M, Innocenti A, Vullo D, Scozzafava A, Supuran CT (1997). „Carbonic anhydrase inhibitors. Part 50. Interaction of isoenzymes I and II of carbonic anhydrase with Ge(IV) and Sb(III) derivatives”. Main Group Met. Chem. 20: 641—647. PMID 15603956. doi:10.1016/j.bmcl.2004.10.070.
- ^ а б Supuran, C. T. (1996). „Complexes with biologically active ligands. Part 3. Synthesis of coordination compounds of chlorothiazide with divalent metal ions”. Main Group Met. Chem. 19: 347—353. doi:10.1515/MGMC.1996.19.6.339.
- ^ а б Koppenho¨fer, A.; Hartmann, U.; Vahrenkamp, H. (1995). „Zinc Complexes of Drugs Containing Nitrogen Heterocycles”. Chem. Ber. 128: 779—785. doi:10.1002/cber.19951280807.
- ^ а б Gonzalez, E. B.; Farkas, E.; Soudi, A. A.; Tan, T.; Yanovsky, A. I.; Nolan, K. B. (1997). „Metal complexes of the angiotensin-converting enzyme inhibitor,lisinopril. Solution studies and the crystal and molecular structure ofa dimeric copper(II)-lisinopril complex”. J. Chem. Soc., Dalton Trans.: 2377—2379. doi:10.1039/A701500C.
- ^ а б Abrams MJ, Murrer BA (1993). „Metal compounds in therapy and diagnosis”. Science. 261: 725—730. PMID 8102010. doi:10.1126/science.8102010.
- ^ а б Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid2492116. - ^ Sly WS, Hu PY (1995). „Human carbonic anhydrases and carbonic anhydrase deficiencies”. Annu. Rev. Biochem. 64: 375—401. PMID 7574487. doi:10.1146/annurev.bi.64.070195.002111.
- ^ Bergenhem, N. (1996). „Chromatographic and electrophoretic methods related to the carbonic anhydrase isozymes”. J. Chromatogr. B. 684: 289—305. PMID 8906478. doi:10.1016/0378-4347(95)00566-8.
- ^ Albert, D. M.; Jakobiec, F. M., ur. (1994). Principles and practice of ophthalmology. Philadelphia: W. B. Saunders. ISBN 978-0-7216-3416-6.
- ^ Heagerty, A. M. (1991). „Functional and structural effects of ACE inhibitors on the cardiovascular system”. Cardiology. 79: 3—9. PMID 1913721. doi:10.1159/000174899.
- ^ Kureya, P.; Beevers, D. G. (1991). „The mechanisms of hypertension and the role of ACE inhibitors”. J. Human Hypertension. 5: 3—8. PMID 1791616.
- ^ Pandurangi, R. S.; Katti, K. V.; Stillwell, L.; Barnes, C. L. (1998). „Retention of Inhibitory Potency of an ACE Inhibitor Conjugated with Rh(III) and Pd(II) (Iminophosphorano)phosphines. Synthesis and X-ray Structural Investigations”. J. Am. Chem Soc. 120: 11364—11373. doi:10.1021/ja9802403.
- ^ а б Bagger, S. (1993). „The binding of cobalt(III)-ligated amino acids and peptides to chymotrypsin and trypsin”. J. Inorg. Biochem. 52: 165—171. PMID 8254339.
- ^ а б в Bagger, S.; Wagner, K. J. (1998). „Molecular recognition of cobalt(III)-ligated peptides by serine proteases: the role of electrostatic effects”. Peptide Res. 52: 273—282. PMID 9832305. doi:10.1111/j.1399-3011.1998.tb01241.x.
- ^ а б Takeuchi, T.; Bottcher, A.; Quezada, C.; Simon, M.; Meade, T.; Gray, H. (1998). „Selective Inhibition of Human α-Thrombin by Cobalt(III) Schiff Base Complexes”. J. Am. Chem. Soc. 120: 8555—8556. doi:10.1021/ja981191x.
- ^ а б Böttcher, A.; Takeuchi, T.; Hardcastle, K.; Meade, T.; Gray, H.; Cwikel, D.; Kapon, M.; Dori, Z. (1997). „Spectroscopy and Electrochemistry of Cobalt(III) Schiff Base Complexes”. Inorg. Chem. 36: 2498—2504. doi:10.1021/ic961146v.
- ^ а б Takeuchi, T.; Böttcher, A.; Quezada, C. M.; Meade, T. J.; Gray, H. B. (1999). „Inhibition of thermolysin and human alpha-thrombin by cobalt(III) Schiff base complexes”. Bioorg. Med. Chem. 6: 1—5. PMID 10400334.
- ^ а б в Tsilikounas, E.; Kettner, C.; Bachovchin, W. (1992). „Identification of serine and histidine adducts in complexes of trypsin and trypsinogen with peptide and nonpeptide boronic acid inhibitors by proton NMR spectroscopy”. Biochemistry. 31: 12839—12846. PMID 1463754. doi:10.1021/bi00166a019.
- ^ а б в Tsilikounas, E.; Kettner, C.; Bachovchin, W. (1993). „Boron-11 NMR spectroscopy of peptide boronic acid inhibitor complexes of .alpha.-lytic protease. Direct evidence for tetrahedral boron in both boron-histidine and boron-serine adduct complexes”. Biochemistry. 32: 12651—12655. PMID 8251483. doi:10.1021/bi00210a013.
- ^ а б Suenaga, H.; Nakashima, K.; Shinkai, S. (1995). „Sugars intensify the inhibitory effect of phenylboronic acid on the hydrolytic activity of α-chymotrypsin”. J. Chem. Soc., Chem. Commun.: 29—30. doi:10.1039/C39950000029.
- ^ а б Katz, B.; Finermoore, J.; Mortezaei, R.; DH, R.; Stroud, R. (1995). „Episelection: Novel Ki .apprx. Nanomolar Inhibitors of Serine Proteases Selected by Binding or Chemistry on an Enzyme Surface”. Biochemistry. 34: 8264—8280. doi:10.1021/bi00026a008.
- ^ а б Geratz, J.; Tidwell, R.; Schwab, J.; Anderle, S.; Pryzwansky, K. (1990). „Sequential events in the pathogenesis of streptococcal cell wall-induced arthritis and their modulation by bis(5-amidino-2-benzimidazolyl)methane (BABIM)”. Am. J. Pathol. 136: 909—921. PMID 2327474.
- ^ а б в г Katz, B.; Clark, J.; Finer-Moore, J.; Jenkins, T.; Johnson, C.; Ross, M.; Luong, C.; Moore, W.; Stroud, R. (1998). „Design of potent selective zinc-mediated serine protease inhibitors”. Nature. 391: 608—612. PMID 9468142. doi:10.1038/35422.
- ^ а б Rice, K.; Tanaka, R.; Katz, B.; Numerof, R.; Moore, W. (1998). „Inhibitors of tryptase for the treatment of mast cell-mediated diseases”. Curr. Pharm. Des. 4: 381—396. PMID 10197050.
- ^ а б в Thorpe, H. H. (1998). „Bioinorganic chemistry and drug design: here comes zinc again”. Chem. Biol. 5: R125—R127. PMID 9653544. doi:10.1016/S1074-5521(98)90166-1.
- ^ а б в г Duffy, B.; Schwietert, C.; France, A.; Mann, N.; Culbertson, K.; Harmon, B.; McCue, J. P. (1998). „Transition metals as protease inhibitors”. Biol. Trace Element Res. 64: 197—213. PMID 9845474. doi:10.1007/BF02783336.
- ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid38682. - ^ а б в г Thayer, J. S. (1984). Organometallic compounds and living organisms. New York: Academic Press. ISBN 978-0-12-686080-1.
- ^ а б в Babine, R. E.; Bender, S. L. (1997). „Molecular Recognition of Protein−Ligand Complexes: Applications to Drug Design”. Chem. Rev. 97: 1359—1472. PMID 11851455. doi:10.1021/cr960370z.
- ^ Bone, R.; Frank, D.; Kettner, C. A.; Agard, D. A. (1989). „Structural analysis of specificity: .alpha.-lytic protease complexes with analogs of reaction intermediates”. Biochemistry. 28: 7600—7609. PMID 2611204. doi:10.1021/bi00445a015.
- ^ Louie, A. Y.; Meade, T. J. (1998). „A cobalt complex that selectively disrupts the structure and function of zinc fingers”. PNAS. 95: 6663—6668. PMID 9618469. doi:10.1073/pnas.95.12.6663.
- ^ а б Mork, A. (1993). „Actions of Lithium on the Cyclic AMP Signalling System in Various Regions of the Brain - Possible Relations to its Psychotropic Actions -: A Study on the Adenylate Cyclase in Rat Cerebral Cortex, Corpus Striatum and Hippocampus”. Pharmacol. Toxicol. 71: 1—47. doi:10.1111/j.1600-0773.1993.tb01704.x.
- ^ а б в г Clauberg, M.; Joshi, J. G. (1993). „Regulation of serine protease activity by aluminum: implications for Alzheimer disease”. Proc. Natl. Acad. Sci. U.S.A. 90: 1009—1012. PMID 7679214.
- ^ а б Rao, K. S. J.; Rao, G. V. (1994). „Effect of aluminium (Al) on brain mitochondrial monoamine oxidase-A (MAO-A) activity--an in vitro kinetic study”. Mol. Cell. Biochem. 137: 57—60. PMID 7845378. doi:10.1007/BF00926039.
- ^ а б в г Nixon, R. A.; Clarke, J. F.; Logvinenko, K. B.; Tan, M. K. H.; Hoult, M.; Grynspan, F. (1990). „Aluminum inhibits calpain-mediated proteolysis and induces human neurofilament proteins to form protease-resistant high molecular weight complexes”. J. Neurochem. 55: 1950—1959. PMID 2121904. doi:10.1111/j.1471-4159.1990.tb05781.x.
- ^ а б в г д Joshi, J. G.; Dhar, M.; Clauberg, M.; Chauthaiwale, V. (1994). „Iron and aluminum homeostasis in neural disorders”. Environ. Health Perspect. 102: 207—213. PMID 7843099. doi:10.2307/3431788.
- ^ а б Lee, B. H.; Park, M. B.; Yu, B. S. (1998). „Inhibition of electric eel acetylcholinesterase by porphin compounds”. Bioinorg. Med. Chem. Lett. 8: 1467—1470. PMID 9873371. doi:10.1016/S0960-894X(98)00236-4.
- ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомISSN 0168-8561. - ^ а б Falkous, G.; Harris, J. B.; Mantle, D. (1995). „Effect of neurotoxic metal ions in vitro on proteolytic enzyme activities in human cerebral cortex”. Clin. Chim. Acta. 238: 125—135. PMID 7586572. doi:10.1016/0009-8981(95)06081-N.
- ^ а б в г Cuajungco, M. P.; Lees, G. K. (1997). „Zinc metabolism in the brain: relevance to human neurodegenerative disorders”. Neurobiol. Dis. 4: 137—169. PMID 9361293. doi:10.1006/nbdi.1997.0163.
- ^ Hay, R. W. (1984). Bio-inorganic Chemistry. New York: Ellis Horwood Limited. ISBN 978-0-85312-200-5.
- ^ а б в Atwood, C. S.; Moir, R. D.; Huang, X. D.; Scarpa, R. C.; Bacarra, N. M. E.; Romano, D. M.; Hartshorn, M. K.; Tanzi, R. E.; Bush, A. I. (1998). „Dramatic aggregation of Alzheimer abeta by Cu(II) is induced by conditions representing physiological acidosis”. J. Biol. Chem. 273: 12817—12826. PMID 9582309. doi:10.1074/jbc.273.21.12817.
- ^ а б в Fitzgerald, D. J.; Maggio, J. E.; Esler, W. P.; Stinson, E. R.; Jennings, J. M.; Ghilardi, J. R.; Mantyh, P. W.; Bush, A. I.; Moir, R. D.; Rosenkranz, K. M.; Tanzi, R. E. (1995). „Zinc and Alzheimer's disease”. Science. 268: 1920—1923. PMID 7604268.
- ^ Mantyh, P. W.; Ghilardi, J. R.; Rogers, S.; Demaster, E.; Allen, C. J.; Stimson, E. R.; Maggio, J. E. (1993). „Aluminum, iron, and zinc ions promote aggregation of physiological concentrations of beta-amyloid peptide”. J. Neurochem. 61: 1171—1174. PMID 8360682. doi:10.1111/j.1471-4159.1993.tb03639.x.
- ^ а б Huang, X. D.; Atwood, C. S.; Moir, R. D.; Hartshorn, M. A.; Vonsattel, J. P.; Tanzi, R. E.; Bush, A. I. (1997). „Zinc-induced Alzheimer's Abeta1-40 aggregation is mediated by conformational factors”. J. Biol. Chem. 272: 26464—26470. PMID 9334223. doi:10.1074/jbc.272.42.26464.
- ^ а б Bush, A. I.; Pettingell, W. H.; Multhaup, G.; Paradis, M. D.; Vonsattel, J. P.; Gusella, J. F.; Beyreuther, K.; Masters, C. L.; Tanzi, R. E. (1994). „Rapid induction of Alzheimer A beta amyloid formation by zinc”. Science. 265: 1464—1467. PMID 8073293.
- ^ Dyrks, T.; Dyrks, E.; Hartmann, T.; Masters, C.; Beyreuther, K. (1992). „Amyloidogenicity of beta A4 and beta A4-bearing amyloid protein precursor fragments by metal-catalyzed oxidation” (PDF). J. Biol. Chem. 267: 18210—18217. PMID 1517249.
- ^ Bondy, S. C.; Guo-Ross, S. X.; Truong, A. T. (1998). „Promotion of transition metal-induced reactive oxygen species formation by beta-amyloid”. Brain Res. 799: 91—96. PMID 9666089. doi:10.1016/S0006-8993(98)00461-2.
- ^ Cuajungco, M. P.; Lees, G. (1997). „Zinc and Alzheimer's disease: is there a direct link?”. J. Brain Res. Rev. 23: 219—236. PMID 9164672. doi:10.1016/S0165-0173(97)00002-7.
- ^ Sugumoto, H.; Iimura, Y.; Yamanishi, Y.; Yamatsu, K. (1995). „Synthesis and structure-activity relationships of acetylcholinesterase inhibitors: 1-benzyl-4-[(5,6-dimethoxy-1-oxoindan-2-yl)methyl]piperidine hydrochloride and related compounds”. J. Med. Chem. 38: 4821—4829. PMID 7490731. doi:10.1021/jm00024a009.
- ^ а б Danning, C. L.; Boumpas, D. T. (1998). „Commonly used disease-modifying antirheumatic drugs in the treatment of inflammatory arthritis: an update on mechanisms of action”. Clin. Exp. Rheumatol. 16: 595—604. PMID 9779311.
- ^ а б Hashimoto, K.; Whitehurst, C. E.; Matsubara, T.; Hirohata, K.; Lipsky, P. E. (1992). „Immunomodulatory effects of therapeutic gold compounds. Gold sodium thiomalate inhibits the activity of T cell protein kinase C”. J. Clin. Invest. 89: 1839—1848. PMID 1351061. doi:10.1172/JCI115788.
- ^ а б в Rajendran, K. G.; Sood, A.; Spielvogel, B. F.; Hall, I. H.; III, V. M. N.; Morse, K. W. (1995). „Anti-Osteoporotic activity of metal complexes of amine carboxyboranes”. Appl. Organomet. Chem. 9: 111—119. doi:10.1002/aoc.590090204.
- ^ Zhang, Z. Y.; Reardon, I. M.; Hui, J. O.; O’Connell, K. L.; Poorman, R. A.; Heinrikson, R. L. (1991). „Zinc inhibition of renin and the protease from human immunodeficiency virus type 1”. Biochemistry. 30: 8717—8721. PMID 1888732. doi:10.1021/bi00100a001.
- ^ а б в Hall, I. H.; Chen, S. Y.; Rajendran, K. G.; Sood, A.; Spielvogel, B. F.; Shih, J. (1994). „Hypolipidemic, anti-obesity, anti-inflammatory, anti-osteoporotic, and anti-neoplastic properties of amine carboxyboranes”. Environ. Health Perspect. 102: 21—30. PMID 7889876. doi:10.2307/3431958.
- ^ Pugh, M. C.; Pugh, C. B. (1987). „Current concepts in clinical therapeutics: disease-modifying drugs for rheumatoid arthritis”. Clin. Pharm. 6: 475—491. PMID 3319362.
- ^ Baker, D. G.; Rabinowitz, J. L. (1986). „Current concepts in the treatment of rheumatoid arthritis”. J. Clin. Pharmacol. 26: 2—21. PMID 3512617.
- ^ а б Sorenson, J. R. J. (1982). Sigel, H.; Marcel Dekker, ur. Metal ions in biological systems. 14. New York. ISBN 9780824715694.
- ^ Naughton, D. P.; Knappitt, J.; Fairburn, K.; Gaffney, K.; Blake, D. R.; Grootveld, M. (1995). „Detection and investigation of the molecular nature of low-molecular-mass copper ions in isolated rheumatoid knee-joint synovial fluid”. FEBS Lett. 362: 167—172. PMID 7698317. doi:10.1016/0014-5793(95)00165-6.
- ^ Miche, H.; Brumas, V.; Berthon, G. (1997). „Copper(II) interactions with nonsteroidal antiinflammatory agents. II. Anthranilic acid as a potential. OH-inactivating ligand”. J. Inorg. Biochem. 68: 27—38. PMID 9379178. doi:10.1016/S0162-0134(97)00005-6.
- ^ Menard, H. A.; Amine, M. E. (1996). „The calpain-calpastatin system in rheumatoid arthritis”. Immunol. Today. 17: 545—547. PMID 8991283. doi:10.1016/S0167-5699(96)30064-9.
- ^ Zhang, H.; Johnson, P. (1992). „Differential effects of aluminum ion on smooth muscle calpain I and calpain II activities”. Int. J. Biochem. 24: 1773—1778. PMID 1451912. doi:10.1016/0020-711X(92)90127-M.
- ^ Frolich, J. C. (1997). „A classification of NSAIDs according to the relative inhibition of cyclooxygenase isoenzymes”. Trends Pharm. Sci. 18: 30—34. PMID 9114728. doi:10.1016/S0165-6147(96)01017-6.
- ^ а б Moore, P.; Jones, C.; Mahmood, N.; Evans, I.; Goff, M.; Cooper, R.; Hay, A. (1995). „Anti-(human immunodeficiency virus) activity of polyoxotungstates and their inhibition of human immunodeficiency virus reverse transcriptase” (PDF). Biochem. J. 307: 129—134. PMID 7536411.
- ^ а б Casas, J.; Rodriguez-Arguelles, M.; Russo, U.; Sanchez, A.; Sordo, J.; Vazquez-Lopez, A.; Pinelli, S.; Lunghi, P.; Bonati, A.; Albertini, R. (1998). „Diorganotin(IV) complexes of pyridoxal thiosemicarbazone: synthesis, spectroscopic properties and biological activity”. J. Inorg. Biochem. 69: 283—292. PMID 9654752. doi:10.1016/S0162-0134(98)00004-X.
- ^ а б Chamorro, C.; Camarasa, M. J.; Perez-Perez, M. J.; Clercq, E. D.; Balzarini, J.; Felix, A. S. (1998). „An approach towards the synthesis of potential metal-chelating TSAO-T derivatives as bidentate inhibitors of human immunodeficiency virus type 1 reverse transcriptase”. Antiviral Chem. Chemother. 9: 413—423. PMID 9875394.
- ^ а б Nacsa, J.; Nagy, L.; Molnar, J.; Molnar, J. (1998). „Trifluoperazine and its metal complexes inhibit the Moloney leukemia virus reverse transcriptase”. Anticancer Res. 18: 1373—1376. PMID 9673343.
- ^ а б в Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid8230091. - ^ а б в г Woon, T.; Brinkworth, R.; Fairlie, D. (1992). „Inhibition of HIV-1 proteinase by metal ions”. Int. J. Biochem. 24: 911—914. PMID 1612181. doi:10.1016/0020-711X(92)90096-J.
- ^ а б Davis, D. A.; Branca, A. A.; Pallenberg, A. J.; Marschner, T. M.; Patt, L. M.; Chatlynne, L. G.; Humphrey, R. W.; Yarchoan, R.; Levine, R. L. (1995). „Inhibition of the human immunodeficiency virus-1 protease and human immunodeficiency virus-1 replication by bathocuproine disulfonic acid Cu1+”. Arch. Biochem. Biophys. 322: 127—134. PMID 7574666. doi:10.1006/abbi.1995.1444.
- ^ а б York, D. M.; Darden, T. A.; Pedersen, L. G.; Anderson, M. W. (1993). „Molecular modeling studies suggest that zinc ions inhibit HIV-1 protease by binding at catalytic aspartates”. Environ. Health Perspect. 101: 246—250. PMID 8404763.
- ^ а б Lebon, F.; deRosny, E.; Reboud-Ravauz, M.; Durant, F. (1998). „De novo drug design of a new copper chelate molecule acting as HIV-1 protease inhibitor”. Eur. J. Med. Chem. 33: 733—737. doi:10.1016/S0223-5234(98)80032-9.
- ^ а б Mazumder, A.; Gupta, M.; Perrin, D. M.; Sigman, C. S.; Ranbinovitz, M.; Pommier, Y. (1995). „Update on long-term symptomless HIV type 1 infection in recipients of blood products from a single donor”. AIDS Res. Hum. Retroviruses. 11: 1. PMID 7734182. doi:10.1089/aid.1995.11.1.
- ^ а б Farnet, C. M.; Wang, B.; Hansen, M.; Lipford, J. R.; Zalkow, L.; Robinson, W. E. J.; Siegel, J.; Bushman, F. (1998). „Human immunodeficiency virus type 1 cDNA integration: new aromatic hydroxylated inhibitors and studies of the inhibition mechanism”. Antimicrob. Agents Chemother. 42: 2245—2253. PMID 9736543.
- ^ Perrin, D. D.; Stunzi, H. (1982). Metal ions and chelating agents in antiviral chemotherapy. New York: Marcel Dekker.
- ^ а б LaFemina, R. L.; Schneider, C. L.; Robbins, H. L.; Callahan, P. L.; LeGrow, K.; Roth, E.; Schleif, W. A.; Emini, E. A. (1992). „Requirement of active human immunodeficiency virus type 1 integrase enzyme for productive infection of human T-lymphoid cells”. J. Virol. 66: 7414—7419. PMID 1433523.
- ^ Tarrago-Litvak, L.; Andreola, M.; Nevinsky, G. A.; Sarih-Cottin, L.; Litvak, S. (1994). „The reverse transcriptase of HIV-1: from enzymology to therapeutic intervention”. FASEB J. 18: 497—503. PMID 7514143.
- ^ Huang, H.; Chopra, R.; Verdine, G. L.; Harrison, S. C. (1998). „Structure of a covalently trapped catalytic complex of HIV-1 reverse transcriptase: implications for drug resistance”. Science. 282: 1669—1675. PMID 9831551. doi:10.1126/science.282.5394.1669.
- ^ Ferrari, M. B.; Fava, G. G.; Tarasconi, R.; Albertini, S.; Pinelli, R.; Starcich, J. (1994). „Synthesis, spectroscopic and structural characterization, and biological activity of aquachloro (pyridoxal thiosemicarbazone) copper(II) chloride”. J. Inorg. Biochem. 53: 13. PMID 8133248. doi:10.1016/0162-0134(94)80017-0.
- ^ а б Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmid8098234. - ^ Das K, Bauman JD, Rim AS, Dharia C, Clark AD Jr, Camarasa MJ, Balzarini J, Arnold E (28. 04. 2011). „Crystal structure of tert-butyldimethylsilyl-spiroaminooxathioledioxide-thymine (TSAO-T) in complex with HIV-1 reverse transcriptase (RT) redefines the elastic limits of the non-nucleoside inhibitor-binding pocket”. J Med Chem. 54 (8): 2727—37. PMID 21446702. doi:10.1021/jm101536x.
- ^ Spence, R. A.; Kati, W. M.; Anderson, K. S.; Johnson, K. A. (1995). „Mechanism of inhibition of HIV-1 reverse transcriptase by nonnucleoside inhibitors”. Science. 267: 988—993. PMID 7532321. doi:10.1038/nsb0495-303.
- ^ West, M. L.; Fairlie, D. P. (1995). „Targeting HIV-1 protease: a test of drug-design methodologies”. Trends Pharmacol. Sci. 16: 67—75. PMID 7762084. doi:10.1016/S0165-6147(00)88980-4.
- ^ а б Wisniewski, M. Z.; Surga, W. J.; Piekos, R. (1995). „Silver(I) compounds of some sulfonamides”. Polish J. Chem. 69: 987—991.
- ^ а б в Serra, M.; Pintar, A.; Casella, L.; Sabbioni, E. (1992). „Vanadium effect on the activity of horseradish peroxidase, catalase, glutathione peroxidase, and superoxide dismutase in vitro”. J. Inorg. Biochem. 46: 161—174. PMID 1325536. doi:10.1016/0162-0134(92)80027-S.
- ^ Karlstrom, A. R.; Levine, R. L. (1991). „Copper inhibits the protease from human immunodeficiency virus 1 by both cysteine-dependent and cysteine-independent mechanisms” (PDF). PNAS. 88: 5552—5556. PMC 51915
 .
.
- ^ Hazuda, D. J.; Felock, P. J.; Hastings, J. C.; Prmanik, B.; Wolfe, A. L. (1997). „Differential divalent cation requirements uncouple the assembly and catalytic reactions of human immunodeficiency virus type 1 integrase” (PDF). J. Virol. 71: 7005—7011. PMID 9261430.
- ^ а б DeZwart, M.; vanderGoot, H.; Timmerman, H. (1991). „Influence of Co(II), Ni(II), Cu(II), Zn(II) and Cd(II) on growth inhibition and enzyme activity of Mycoplasma gallisepticum in the absence or presence of a 2,2′-bipyridyl type ligand”. Eur. J. Med. Chem. 26: 101—108. doi:10.1016/0223-5234(91)90218-C.
- ^ а б Wells, T. N. C.; Scully, P.; Paravicini, G.; Proudfoot, A. E. I.; Payton, M. A. (1995). „Mechanism of irreversible inactivation of phosphomannose isomerases by silver ions and flamazine”. Biochemistry. 34: 7896—7903. PMID 7794901. doi:10.1021/bi00024a014.
- ^ а б Cunningham, M. L.; Zvelebil, M. J. J. M.; Fairlamb, A. H. (1994). „Mechanism of inhibition of trypanothione reductase and glutathione reductase by trivalent organic arsenicals”. Eur. J. Biochem. 221: 285—295. PMID 8168518. doi:10.1111/j.1432-1033.1994.tb18740.x.
- ^ а б Saha, A. K.; Crans, D. C.; Pope, M. T.; Simone, C. M.; Glew, R. H. (1991). „Inhibition of human seminal fluid and Leishmania donovani phosphatases by molybdate heteropolyanions” (PDF). J. Biol. Chem. 266: 3511—3517. PMID 1995614.
- ^ а б Yano, S.; Inoue, S.; Nouchi, R.; Mogami, K.; Shinohara, Y.; Yasuda, Y.; Kato, M.; Tanase, T.; Kakuchi, T.; Mikata, Y.; Suzuki, T.; Yamamoto, Y. (1998). „Antifungal nickel(II) complexes derived from amino sugars against pathogenic yeast, Candida albicans”. J. Inorg. Biochem. 69: 15—23. PMID 9606935.
- ^ а б Su, J. J.; Mansour, J. M.; Mansour, T. E. (1996). „Purification, kinetics and inhibition by antimonials of recombinant phosphofructokinase from Schistosoma mansoni”. Mol. Biochem. Parasitol. 81: 171—178. PMID 8898332. doi:10.1016/0166-6851(96)02702-8.
- ^ а б Saenz, R. E.; Rodriguez, C. C. D.; Johnson, C. M.; Berman, J. D. (1991). „Efficacy and toxicity of pentostam against Panamanian mucosal leishmaniasis”. Am. J. Trop. Med. 44: 394—398. PMID 1645930.
- ^ а б Meyer-Fernandes, J. R.; Dutra, P. M. L.; Rodrigues, C. O.; Saad-Nehme, J.; Lopes, A. H. C. S. (1997). „Mg-dependent ecto-ATPase activity in Leishmania tropica”. Arch. Biochem. Biophys. 341: 40—46. PMID 9143351.
- ^ а б Kendrick, M. J.; May, M. T.; Plishka, M. J.; Robinson, K. D. (1992). „Metals in Biological Systems”. New York: Ellis Horwood. ISBN 978-0-13-577727-5.
- ^ Bult, A. (1983). Sigel, H., ur. Metal ions in biological systems. 16. New York: Marcel Dekker. doi:10.1080/00945718208063132.
- ^ Garg, R. K.; Sharma, L. M. J. Indian Chem. Soc. (1995). „Binuclear transition metal complexes of some novel Schiff bases derived from dapsone (an antileprotic drug). Part II. Zinc(II) complexes”. 72: 231—234. ISSN 0019-4522.
- ^ Hueso-Urena, F.; Moreno-Carretero, M. N.; Romero-Molina, M. A.; Salas-Peregrin, J. M.; Sanchez-Sanchez, M. P.; Cienfuegos-Lopez, G. A. D.; Faure, R. J. (1993). „Transition metal complexes with monodeprotonated isoorotic and 2-thioisoorotic acids: Crystal structure, spectral and magnetic study, and antimicrobial activity”. Inorg. Biochem. 51: 613—632. doi:10.1016/0162-0134(93)85033-5.
- ^ Ibrahim, S. A.; El-Gyar, S. A.; El-Gahani, M. A. (1991). „Metal complexes of nitrogen-oxygen donor ligands as potential drugs”. Collect. Czech. Chem. Commun. 56: 1333—1339. doi:10.1135/cccc19911333.
- ^ Nagar, R.; Mohan, G. J. (1992). „Studies on mixed-ligand complexes of some transition metals of biological interest”. Therm. Anal. 38: 1415—1431.
- ^ Fairlamb, A. H.; Henderson, G. B.; Cerami, A. (1989). „Trypanothione is the primary target for arsenical drugs against African trypanosomes” (PDF). PNAS. 86: 2607—2611. PMID 2704738.
- ^ а б Tsai, H.; Dwarakanath, A.; Hart, C.; Milton, J.; Rhodes, J. (1995). „Increased faecal mucin sulphatase activity in ulcerative colitis: a potential target for treatment” (PDF). Gut. 36: 570—576. PMID 7737566.
- ^ а б Beil, W.; Birkholz, C.; Wagner, S.; Sewing, K. (1995). „Bismuth subcitrate and omeprazole inhibit Helicobacter pyloriF1-ATPase”. Pharmacology. 50: 333—337. PMID 7667394. doi:10.1159/000139299.
- ^ а б в г Schroeder, T.; Caspers, M. (1996). „Kinetics of aluminum-induced inhibition of delta-aminolevulinic acid dehydratase in vitro”. Biochem. Pharmacol. 52: 927—931. PMID 8781512. doi:10.1016/0006-2952(96)00449-2.
- ^ а б в г Exley, C.; Price, N.; Birchall, J. (1994). „Aluminum inhibition of hexokinase activity in vitro: a study in biological availability”. J. Inorg. Biochem. 54: 297—304. PMID 8014638. doi:10.1016/0162-0134(94)80035-9.
- ^ а б Canesi, L.; Ciacci, C.; Piccoli, G.; Stocchi, V.; Viarengo, A.; Gallo, G. (1998). „In vitro and in vivo effects of heavy metals on mussel digestive gland hexokinase activity: the role of glutathione”. Comp. Biochem. Physiol. C. 120 (2): 261—268. PMID 9827040. doi:10.1016/S0742-8413(98)10004-X.
- ^ а б в г Yoshino, M.; Murakami, K.; Kawano, K. (1998). „Interaction of aluminum ion with ATP. Mechanism of the aluminum inhibition of glycerol kinase and its reversal by spermine”. Biometals. 11: 63—67. doi:10.1023/A:1009213508942.
- ^ а б Hyppo¨nen, S.; Kohila, T.; Tahti, H. (1993). „The effects of cadmium, lead and aluminum on neural cell membrane adenosinetriphosphatase activity”. Neurosci. Res. Commun. 12: 77—84.
- ^ а б Yager, J. W.; Wiencke, J. K. (1997). „Inhibition of poly(ADP-ribose) polymerase by arsenite”. Mutat. Res. 386: 345—351. PMID 9219571. doi:10.1016/S1383-5742(97)00011-2.
- ^ а б в Hu, Y.; Su, L.; Snow, E. T. (1998). „Arsenic toxicity is enzyme specific and its affects on ligation are not caused by the direct inhibition of DNA repair enzymes”. Mutat. Res. 408: 203—218. PMID 9806419. doi:10.1016/S0921-8777(98)00035-4.
- ^ а б в Tsao, D.; Maki, A. (1991). „Optically detected magnetic resonance study of the interaction of an arsenic(III) derivative of cacodylic acid with EcoRI methyltransferase”. Biochemistry. 30: 4565—4572. PMID 2021649. doi:10.1021/bi00232a029.
- ^ а б Lam, W.; Tsao, D.; Maki, A.; Maegley, K.; Reich, N. (1992). „Spectroscopic studies of arsenic(III) binding to Escherichia coli RI methyltransferase and to two mutants, C223S and W183F”. Biochemistry. 31: 10438—10442. PMID 1420162. doi:10.1021/bi00158a004.
- ^ а б в Styblo, M.; Thomas, D. (1995). „In vitro inhibition of glutathione reductase by arsenotriglutathione”. Biochem. Pharmacol. 49: 971—977. PMID 7741769. doi:10.1016/0006-2952(95)00008-N.
- ^ а б Chawla, S.; Mutenda, E.; Dixon, H.; Freeman, S.; Smith, A. (1995). „Synthesis of 3-arsonopyruvate and its interaction with phosphoenolpyruvate mutase”. Biochem. J. 308: 931—935. PMID 8948453.
- ^ а б Snow, E.; Xu, L.; Kinney, P. (1993). „Effects of nickel ions on polymerase activity and fidelity during DNA replication in vitro”. Chem.-Biol. Interact. 88: 155—173. PMID 8403077. doi:10.1016/0009-2797(93)90089-H.
- ^ а б Yang, S. W.; Becker, F. F.; Chan, J. Y. H. (1996). „Inhibition of human DNA ligase I activity by zinc and cadmium and the fidelity of ligation”. Environ. Health Perspect. 28: 19—25. PMID 8698042. doi:10.1002/(SICI)1098-2280(1996)28:1<19::AID-EM5>3.0.CO;2-9.
- ^ а б в Hartwig, A. (1994). „Role of DNA repair inhibition in lead- and cadmium-induced genotoxicity: a review”. Environ. Health Perspect. 102: 45—50. PMID 7843136. doi:10.2307/3431762.
- ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомpmc2002465. - ^ а б в Porter, D. W.; Nelson, V. C.; Fivash, M. J. J.; Kasprzak, K. S. (1996). „Mechanistic studies of the inhibition of MutT dGTPase by the carcinogenic metal Ni(II)”. Chem. Res. Toxicol. 9: 1375—1381. PMID 8951243. doi:10.1021/tx9600816.
- ^ а б в Wetmur, J. G. (1994). „Influence of the common human delta-aminolevulinate dehydratase polymorphism on lead body burden”. Environ. Health Perspect. 102: 215—219. PMID 7843101. doi:10.2307/3431789.
- ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомNizvan_97-20230321214409. - ^ Грешка код цитирања: Неважећа ознака
<ref>; нема текста за референце под именомNizvan_98-20230321214409. - ^ Thiele, D. J. (1992). „Metal-regulated transcription in eukaryotes” (PDF). Nuc. Acids Res. 20: 1183—1191. PMID 1561077.
- ^ O’Halloran, T. V. (1993). „Transition metals in control of gene expression”. Science. 261: 715—725. PMID 8342038. doi:10.1126/science.8342038.
Литература[уреди | уреди извор]
- Berg JM, Tymoczko JL, Stryer L (2002). Biochemistry (V izd.). New York, NY: W. H. Freeman. ISBN 978-0-7167-3051-4.
- Cornish-Bowden A, ur. (1997). New Beer in an Old Bottle: Eduard Buchner and the Growth of Biochemical Knowledge. Universitat de València. ISBN 978-84-370-3328-0.
- H, Suzuki (2015). How Enzymes Work: From Structure to Function. Boca Raton, FL: CRC Press. ISBN 978-981-4463-92-8.
- Cornish-Bowden A (2012). Fundamentals of Enzyme Kinetics (IV izd.). Weinheim: Wiley-VCH. ISBN 978-3527330744.
- Briggs, G. E.; J. B. S. Haldane (1925). „A note on the kinetics of enzyme action”. Biochem. J. 19: 339—339. PMC 1259181
 .
. - R.R. Dogonadze; V.G. Levich (1959). „Theory of Non-radiative Electronic Transitions between Ions in Solution”. Dokladi Akademii Nauk SSSR. Ser. Fizicheskoy Khimii. Moscow. 124: 123—126.
- R.R. Dogonadze (1960). „Rate of Electron Transfer Reactions in Solutions”. Dokladi Akademii Nauk SSSR. Ser. Fizicheskoy Khimii. Moscow. 133: 1368—1371.
- M, Nishimura; Chance B. (1963). „Studies on the electron-transfer systems in photosynthetic bacteria I. The light-induced absorption-spectrum changes and the effect of phenylmercuric acetate”. Biochim Biophys Acta. 66: 1—16. doi:10.1016/0006-3002(63)91162-4.
- V.G. Levich; R.R. Dogonadze; E.D. German; A.M. Kuznetsov; Yu.I. Kharkats (1970). „Theory of Homogeneous Reactions Involving Proton Transfer”. Electrochim.Acta. 15: 353—367.
- M.V. Volkenshtein; R.R. Dogonadze; A.K. Madumarov; Z.D. Urushadze; Yu. I. Kharkats (1972). „Theory of Enzyme Catalysis”. Molekuliarnaya Biologia: 431—439.
Спољашње везе[уреди | уреди извор]
- (језик: енглески) Веб-туторијал за ензимску инхибицију, приручник др Питера Берча са Универзитета у Пејслију који садржи веома јасне анимације
- (језик: енглески) Симболика и терминологија ензимске кинетике, препоруке Одбора за номенклатуру Међународне уније за биохемију (NC–IUB) око терминологије инхибиције ензима
- (језик: енглески) NCBI-јев PubChem, база података лекова и инхибитора ензима
- (језик: енглески) BRENDA Архивирано на сајту Wayback Machine (11. децембар 2008), база података ензима са списковима познатих инхибитора за сваки унос
- (језик: енглески) Ензими, кинетика и дијагностичка употреба Архивирано на сајту Wayback Machine (9. јул 2011), онлајн предавање др Мајкла V. Кинга из Медицинске школе Универзитета у Индијани с фокусом на медицинску примену инхибитора ензима
- (језик: енглески) BindingDB, javna baza podataka izmerenih afiniteta vezivanja proteina i liganda
- (jezik: engleski) Animirana vežba sa inhibicijom enzima, tutorijal + kvizovi


![{\displaystyle V={\frac {V_{max}[S]}{\alpha K_{m}+\alpha ^{\prime }[S]}}={\frac {(1/\alpha ^{\prime })V_{max}[S]}{(\alpha /\alpha ^{\prime })K_{m}+[S]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4a8f0a9dda1d308de7f090f99c2833f944f11a09)
![{\displaystyle \alpha =1+{\frac {[I]}{K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/57fcf54938a9784f9313437681b220079ff43ee5)
![{\displaystyle \alpha ^{\prime }=1+{\frac {[I]}{K_{i}^{\prime }}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8b7d75a61e059ecea4053a1c7afb91f9cf39a2ab)
![{\displaystyle {\cfrac {V_{\max }}{1+{\cfrac {\ce {[I]}}{K_{i}}}}}={\cfrac {V_{\max }}{\cfrac {[{\ce {I}}]+K_{i}}{K_{i}}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/974bf2132f8729fe17e42bcf5e6835fd9bf541fc)
![{\displaystyle {\cfrac {V_{\max }}{\cfrac {[{\ce {I}}]+K_{i}}{[{\ce {I}}]+K_{i}-[{\ce {I}}]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ea1e5957a1680cbbd38b9a6157e59859632c37ba)
![{\displaystyle {\cfrac {V_{\max }}{\cfrac {1}{1-{\cfrac {\ce {[I]}}{[{\ce {I}}]+K_{i}}}}}}=V_{\max }-V_{\max }{\cfrac {\ce {[I]}}{[{\ce {I}}]+K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1dd17bc78dc831a088b059c70ea9b734c99f15a5)
![{\displaystyle {\cfrac {\ce {[S]}}{[{\ce {S}}]+K_{m}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/eb08dd139085a394e6e7370f47ebfa255f1ad685)
![{\displaystyle {\cfrac {\ce {[I]}}{[{\ce {I}}]+K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9ed50a1f7a5f2c52f406b52263916ab48b268e07)
![{\displaystyle V_{\max }-\Delta V_{\max }{\cfrac {\ce {[I]}}{[{\ce {I}}]+K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7dff424ec79284c3a1cea14f0f82b0eaace53c69)
![{\displaystyle V_{\max 1}-(V_{\max 1}-V_{\max 2}){\cfrac {\ce {[I]}}{[{\ce {I}}]+K_{i}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/f3874623edd9524ba2741fe448927bf5cf0ab257)
![{\displaystyle V_{\max 1}-(V_{\max 1}-V_{\max 2}){\cfrac {\ce {[X]}}{[{\ce {X}}]+K_{x}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/306d44733a89308883053e3b8372a8cf9ce0239b)
![{\displaystyle K_{m1}-(K_{m1}-K_{m2}){\cfrac {\ce {[X]}}{[{\ce {X}}]+K_{x}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/cb4e0de216e1e625bb803ee725bf85c9989a15f5)








