Натализумаб
 | |
| Моноклонално антитело | |
|---|---|
| Тип | цело антитело |
| Извор | Хуманизовано (од миша) |
| Мета | алфа-4 интегрин |
| Клинички подаци | |
| Подаци о лиценци |
|
| Категорија трудноће | |
| Начин примене | IV |
| Правни статус | |
| Правни статус |
|
| Фармакокинетички подаци | |
| Биорасположивост | н/а |
| Полувреме елиминације | 11 ± 4 дана |
| Идентификатори | |
| CAS број | 189261-10-7 |
| ATC код | L04AA23 (WHO) |
| DrugBank | BTD00083 |
| Хемијски подаци | |
| Моларна маса | 149 кДа |
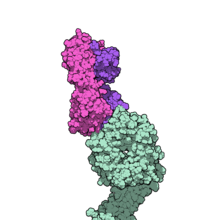
Натализумаб је хуманизовано моноклонално антитело против целуларног адхезионог молекула α4-интегрина. Натализумаб се користи у третману мултипле склерозе и Кронове болести. Овај лек заједнички продају компаније Biogen Idec и Élan као Tysabri, а раније бе био познат под именом Антегрен. Натализумаб се администрира интравенозном инфузијом сваких 28 дана. За овај лек се мисли да дејствује путем редуковања способности инфламаторних имуних ћелија да се вежу за и прођу кроз ћелијске слојеве дуж интестиналне и крвно-мождане баријере. Ефективност натализумаба у третирању симптома обе болести, спречавању релапса, губитка вида, губљења когнитивних способности и значајног побољшања квалитета живота људи са мултиплом склерозом, као и превенције релапса Кронове болести.
Натализумаб је био одобрен 2004. од стране ФДА. Он је накнадно био повучен са тржишта након успостављања везе са три случаја ретког неуролошког стања прогресивна мултифокална леукоенцефалопатија (ПМЛ) кад је администриран у комбинацији са интерфероном бета-1а, још једним имуносупресивним леком често коришћеним у третману мултипле склерозе. Након разматрања безбедносних информација, и пошто није било других смртних случајева, овај лек је враћен на тржиште у САДу 2006. године са посебним ограничењима за издавање рецепата. Јуна 2009, десет ПМЛ случајева је било познато. Међутим, двадесет четири ПМЛ случаја су пријављена откако је лек поново уведен октобра 2009. године. Овакво нагло повећане броја фаталних случаја је подстакло разматрање услова за примену овог лека од стране Европске медицинске агенције.[1][2][3] До јануара 2010. број ПМЛ случаја приписаних натализумабу је био 31. ФДА није донела одлуку да се овај лек повуче са тржишта зато што његова клиничка користност надмашује ризике везане за његову употребу.[4] У Европској унији, овај лек је био одобрен за људску употребу само у третману мултипле склерозе, и само као монотерапија због иницијалних ПМЛ случајеве. За касније фаталне случајеве, произвођачи лека тврде да су везани за употребу ранијих медикација од стране преминулих корисника.
Biogen Idec је најавио почетак клиничког испитивања за Tysabri као потенцијалног први-у-класи третмана за рак у септембру 2008.[5]
Индикације[уреди | уреди извор]
Натализумаб је одобрен од стране ФДА за третман мултипле склерозе и Кронове болести. Овај лек је одобрен је за третман мултипле склерозе у Европи, али је тренутно под разматрањем од стране ЕМЕА.[6][7]
Мултипла склероза[уреди | уреди извор]
Натализумаб је евалуиран у два рандомизована, дупло-слепа, плацебо-контролисана испитивања код људи са мултиплом склерозом. Обе студије су обухватале индивидуе са МС које су прошле кроз бар један клинички релапс у току претходне године и које су имале Куртцкеову ЕДСС вредност између 0 и 5. У тим испитивањима за натализумаб је показано да редукује релапсе код индивидуа са МС за 68% у поређењу са плацебом, маргина која је далеко већа него код других одобрених МС терапија.[8] Натализумаб је такође успорио прогресију онеспособљености код пацијената са релапсном МС.[8][9] У комбинацији са интерфероном бета-1а (ИБ1А), релапсирање и развој инвалидности су редуковани више него само са ИБ1А.[10] Додатна корист употребе натализумаба за пацијенте са релапсном МС је умањење губитка вида,[11] значајно повећање пропорције индивидуа бе даљих манифестација болести,[12] знатно побољшање квалитета живота код релапсирајућих индивидуа,[13][14] редукција губитка когнитивних способности,[15] редукција хоспитализације и употребе стероида,[16] и превенција формирања нових лезија.[8][17] За око 6% оф индивидуа које су примале натализумаб је нађено да развијају трајна антитела за овај лек, што умањује његову ефикасност[10][18][19] и производи реакције током инфузије лека, као и хиперсензитивност.[10] Натализумаб је одобрен у САДу и Европској унији. Он је индициран као монотерапија (не комбинује се са другим лековима) за третман високо активне релапсно ремитујуће МС упркос претходних третмана.[20] Натализумаб даје ограничено побољшање ефикасноти у поређењу са другим третманима за МС, али због недостатка информација о његовој дуготрајној употреби, као и потенцијално фаталних исхода, резервисаност је изражена у погледу употребе овог лека изван опсега компаративног истраживања са постојећим медикацијама.[10]
Кронова болест[уреди | уреди извор]
Неколико рандомизованих контролисаних испитивања су демонстрирала да је натализумаб ефективан у повећању стопе ремисије[21] и одржавања без-симптомског стања[22] код пацијената са Кроновом болести. Натализумаб је можда подесан за пацијенте који нису реаговали на медикације које блокирају ТНФ-алфа као што је инфликсимаб.[23] Постоје подаци који подржавају идеју да комбиновани третман Кронове болести са натализумабом и инфликсимабом може бити користан у индуцирању ремисије.[24] Третман адолесцентних пацијената са натализумабом је демонстрирао ефективност сличну оној што је запажена код одраслих пацијената.[25]
Јануара 2008, ФДА је одобрила натализумаб за индукције ремисије и одржавања ремисије за умерено до јаке Кронове болести.[26] Овај лек није одобрен за овакву употребу у Европској унији због забринутости да ризик/корист однос није довољно повољан.[27]
Непожељни ефекти[уреди | уреди извор]
Уобичајени непожељни ефекти обухватају исцрпљеност и алергијске реакције са ниским ризиком од анафилаксије,[28] главобољу, мучнину, прехладу и погоршање Кронове болести код малог дела пацијената.[24] Адолесценти оболели од Кровом болести доживљавају главобоље, грозницу и погоршање болести.[25] Натализумаб је контраиндициран за људе са познатом хиперсензитивношћу на лек или његове компоненте, и код пацијената са ПМЛ историјом.
Пост-продајни надзор је 2008. је показао да 0.1% пацијената који користе натализумаб доживљавају клинички значајна оштећења јетре, што је навело ФДА, ЕМЕА и произвођаче да препоруче да се употреба лека обустави код пацијената са жутицом или другом евиденцијом значајног оштећења јетре.[29][30][31] Ова стопа упоредива са другим имуносупресивним лековима.[32] Евиденција хепатотоксичности у облику повећаних нивоа билирубина и трансаминазе у крви се може јавити већ након шест дана након иницијалне дозе; реакције су непредвидиве и могу се јавити чак и ако пацијент не реагује на претходни третман.[33]
Натализумаб је такође био повезан са меланомом, мада ова асоцијација није јасна.[34] Дугорочни ефекти лека су непознати[35] и била је изражена забринутост у вези ризика од инфекције и рака.[10]
Прогресивна мултифокална леукоенцефалопатија, једна опортунистичка инфекција узрокована ЈЦ вирусом, која се типично јавља код пацијената који су имуно-компромитовани, се развила код седам пацијената који су користили натализумаб [36]; три случаја су примећена у клиничким испитивањима 2006[37] што је довело до привременог повлачења лека са тржишта; два случаја су пријављене ФДАу августа 2008 [38]; и два случаја су објављена децембра 2008 [36]. Недавна прелиминарна студија сугестира да пацијенти који користе овај лек дуже од 12 месеци имају једанаест пута већи ПМЛ ризик.[39]
Механизам акције[уреди | уреди извор]

Натализумаб је хуманизовано моноклонално антитело против алфа-4 (α4) интегрина. Ово је први лек у класи селективних инхибитора адхезионих молекула. Интегрин α4 је неопходан за омугућавање улаза белих крвних зрнаца у органе. Механизам акције натализумаба се верује да је инхибиција преласка тих имуних ћелија из крвних судова.[40]
Мултипла склероза[уреди | уреди извор]
Симптом-узрокујуће лезије мултипле склерозе се верује да настају кад инфламаторне ћелије као што су Т-лимфоцити прођу кроз крвно-мождану баријеру путем интеракције са рецепторима на ендотелним ћелијама. Натализумаб изгледа да умањује пренос имуних ћелија у централни нервни систем путем интеракције са α4β1-интегрин рецептор молекулима на ћелијској површини. Овај ефекат изгледа да се јавља на ендотелним ћелијама које изражавају ВЦАМ-1 ген, и паренхимал ћелијама које изражавају остеопонтин ген. Код животиња које се користе у МС моделима, поновљено дозирање натализумаба је редуцирало миграцију леукоцита у мождане паренхиме, и дошло је до умањења лезија, мада је неизвесно да ли је то клинички значајно код људи.[41]
Индивидуе обелеле од [[мултипла склероза|мултипле склерозеђђ које су дозиране са натализумабом су демонстрирале повећање броја ЦД34-изражавајућих ћелија, са пиком експресије након 72 сата.[42]
Кронова болест[уреди | уреди извор]
Интеракција α4β7 интегрина и адресин (исто познатих као МАДЦАМ1) ендотелних ћелијских рецептора се верује да доприноси хроничној инфламацији црева која узрокује Кронову болест. Адресин је првенствено изражен у ендотелним венулама у танким цревима и он је критичан у вођењу Т-лимфоцита и лимфатичним ткивима. Места активне инфламације црева код оболелих од Кронове болести имају повишено изражавање адресина, што сугерише да можда постоји веза између инфламације и овој рецептора. Натализумаб може да блокира интеракцију између α4β7 интегрина и адресина на местима инфламације. Животињски модели су утврдили повишене нивое VCAM-1 експресије код мишева са иритабилним цревним синдромом (IBS) и VCAM-1 ген може исто тако да игра улогу у Кроновој болести мада његова улога још увек није разјашњена.[41]
Види још[уреди | уреди извор]
Литература[уреди | уреди извор]
- ^ „Еуропеан Медицинес Агенцy, Пресс Оффице, Цоммиттее фор Медицинал Продуцтс фор Хуман Усе” (ПДФ). Архивирано из оригинала (ПДФ) 27. 12. 2009. г. Приступљено 22. 10. 2009.
- ^ „РЕУТЕРС ЕУ агенцy репортс 24тх цасе оф Тyсабри инфецтион”.
- ^ Цларке, Тони wитх Стеве Орлофскy анд Лиса Вон Ахн (29. 6. 2009). „Биоген репортс 10тх цасе оф ПМЛ браин инфецтион”. Реутерс.
- ^ „МС Друг Тyсабри Тиед то Браин Инфецтион. WебМД.цом Аугуст 1, 2008.”.
- ^ „Биоген Идец тестинг Тyсабри ас а цанцер треатмент”. 5. 9. 2008. Приступљено 5. 9. 2008.
- ^ „Тyсабри сафетy фаллс ундер ЕМЕА сцрутинy”. Архивирано из оригинала 03. 03. 2016. г. Приступљено 26. 06. 2010.
- ^ „Пресс релеасе - Еуропеан Медицинес Агенцy: Цоммиттее фор Медицинал Продуцтс фор Хуман Усе 24-27 Април 2006” (ПДФ). Еуропеан Медицинес Агенцy. 28. 4. 2006. Архивирано из оригинала (ПДФ) 10. 7. 2007. г. Приступљено 2. 4. 2008.
- ^ а б в Полман ЦХ, О'Цоннор ПW, Хаврдова Е, et al. (2006). „А рандомизед, плацебо-цонтроллед триал оф натализумаб фор релапсинг формс оф мултипле сцлеросис”. Н. Енгл. Ј. Мед. 354 (9): 899—910. ПМИД 16510744. дои:10.1056/НЕЈМоа044397.
- ^ „ТYСАБРИ: АННЕX I – СУММАРY ОФ ПРОДУЦТ ЦХАРАЦТЕРИСТИЦС” (ПДФ). Еуропеан Медицинес Агенцy. Архивирано из оригинала (ПДФ) 20. 8. 2007. г. Приступљено 9. 3. 2008.
- ^ а б в г д „Натализумаб: неw друг. Мултипле сцлеросис: рискy маркет аппровал”. Пресцрире Инт. 17 (93): 7—10. 2008. ПМИД 18354844.
- ^ Балцер Љ, Галетта СЛ, Цалабреси ПА, et al. (2007). „Натализумаб редуцес висуал лосс ин патиентс wитх релапсинг мултипле сцлеросис”. Неурологy. 68 (16): 1299—304. ПМИД 17438220. дои:10.1212/01.wнл.0000259521.14704.а8.
- ^ Галетта, С; et al. (18. 4. 2008). „Натализумаб Инцреасес тхе Пропортион оф Патиентс Фрее оф Цлиницал ор МРИ Дисеасе Ацтивитy ин Релапсинг Мултипле Сцлеросис”. унпублисхед/унпресентед цонференце постер. Архивирано из оригинала 21. 03. 2008. г. Приступљено 11. 3. 2008.; индустрy публицатион - „Неw ТYСАБРИ Дата то Бе Пресентед ат тхе Еуропеан Цоммиттее фор Треатмент анд Ресеарцх ин Мултипле Сцлеросис”. Éлан. 11. 10. 2007. Приступљено 9. 3. 2008.
- ^ Рудицк РА, Миллер ДМ (2008). „Хеалтх-релатед qуалитy оф лифе ин мултипле сцлеросис : цуррент евиденце, меасуремент анд еффецтс оф дисеасе северитy анд треатмент”. ЦНС другс. 22 (10): 827—39. ПМИД 18788835. дои:10.2165/00023210-200822100-00004.
- ^ Рудицк РА, Миллер D, Хасс С, et al. (2007). „Хеалтх-релатед qуалитy оф лифе ин мултипле сцлеросис: еффецтс оф натализумаб”. Анн. Неурол. 62 (4): 335—46. ПМИД 17696126. дои:10.1002/ана.21163.
- ^ „Неw Дата он Натализумаб Демонстрате Сигнифицант Импровемент ин Цогнитиве Фунцтион ин Патиентс Wитх Мултипле Сцлеросис”. Доцтор'с Гуиде. 28. 9. 2006. Архивирано из оригинала 11. 2. 2008. г. Приступљено 9. 3. 2008.
- ^ „Неw Пхармацоецономиц Дата Он ТYСАБРИ Демонстрате Сигнифицант Редуцтион Ин Стероид Усе Анд Хоспитализатионс Ин Патиентс Wитх Мултипле Сцлеросис”. wебwире. 6. 10. 2006. Приступљено 9. 3. 2008.
- ^ Миллер ДХ, Соон D, Фернандо КТ, et al. (2007). „МРИ оутцомес ин а плацебо-цонтроллед триал оф натализумаб ин релапсинг МС”. Неурологy. 68 (17): 1390—401. ПМИД 17452584. дои:10.1212/01.wнл.0000260064.77700.фд.
- ^ Хутцхинсон, M. (2007). „Натализумаб: А неw треатмент фор релапсинг ремиттинг мултипле сцлеросис”. Тхер Цлин Риск Манаг. 3 (2): 259—268. ПМЦ 1936307
 . ПМИД 18360634. дои:10.2147/тцрм.2007.3.2.259. Приступљено 22. 4. 2008.
. ПМИД 18360634. дои:10.2147/тцрм.2007.3.2.259. Приступљено 22. 4. 2008.
- ^ Цалабреси ПА, Гиованнони Г, Цонфавреуx C, et al. (2007). „Тхе инциденце анд сигнифицанце оф анти-натализумаб антибодиес: ресултс фром АФФИРМ анд СЕНТИНЕЛ”. Неурологy. 69 (14): 1391—403. ПМИД 17761550. дои:10.1212/01.wнл.0000277457.17420.б5.
- ^ „Аннеx: Цондитионс ор рестрицтионс wитх регард то тхе сафе анд еффецтиве усе оф тхе медицинал продуцт то бе имплементед бy тхе мембер статес” (ПДФ). Еуропеан Медицинес Агенцy. Архивирано из оригинала (ПДФ) 20. 8. 2007. г. Приступљено 9. 3. 2008.
- ^ Гхосх С, Голдин Е, Гордон Ф, Малцхоw Х, Раск-Мадсен Ј, Рутгеертс П, Вyхнáлек П, Зáдоровá З, Палмер Т, Доногхуе С (2003). „Натализумаб фор ацтиве Црохн'с дисеасе”. Н. Енгл. Ј. Мед. 348 (1): 24—32. ПМИД 12510039. дои:10.1056/НЕЈМоа020732.
- ^ Феаган БГ, Сандборн WЈ, Хасс С, Ниецко Т, Wхите Ј (2007). „Хеалтх-релатед qуалитy оф лифе дуринг натализумаб маинтенанце тхерапy фор Црохн'с дисеасе”. Ам. Ј. Гастроентерол. 102 (12): 2737—46. ПМИД 18042106. дои:10.1111/ј.1572-0241.2007.01508.x.
- ^ Мицхетти, П.; Моттет C; Јуиллерат П; et al. (2007). „Севере анд стероид-ресистант Црохн'с дисеасе”. Дигестион. 76 (2): 99—108. ПМИД 18239400. дои:10.1159/000111023.
- ^ а б Сандс, Б. Е.; Козарек Р; Спаинхоур Ј; et al. (2007). „Сафетy анд толерабилитy оф цонцуррент натализумаб треатмент фор патиентс wитх Црохн'с дисеасе нот ин ремиссион wхиле рецеивинг инфлиxимаб”. Инфламм. Боwел Дис. 13 (1): 2—11. ПМИД 17206633. дои:10.1002/ибд.20014.
- ^ а б Хyамс, Ј. С.; Wилсон DC; Тхомас А; et al. (2007). „Натализумаб тхерапy фор модерате то севере Црохн дисеасе ин адолесцентс”. Ј. Педиатр. Гастроентерол. Нутр. 44 (2): 185—91. ПМИД 17255829. дои:10.1097/01.мпг.0000252191.05170.е7.
- ^ „ФДА Аппровес Тyсабри то Треат Модерате-то-Севере Црохн'с Дисеасе”. Фоод анд Друг Администратион. 14. 1. 2008. Приступљено 9. 3. 2008.
- ^ „Рефусал ЦХМП ассессмент репорт фор натализумаб” (ПДФ). Еуропеан Медицинес Агенцy. 15. 11. 2007. Приступљено 2. 4. 2008.[мртва веза] лаy-суммарy Архивирано на сајту Wayback Machine (18. јул 2009)
- ^ Horga A, Horga de la Parte JF (2007). „[Natalizumab in the treatment of multiple sclerosis]”. Rev Neurol (на језику: Spanish; Castilian). 45 (5): 293—303. PMID 17876741.
- ^ „FDA MedWatch - 2008 Safety Information Alerts”. Food and Drug Administration. 28. 2. 2008. Приступљено 5. 4. 2008.
- ^ „EMEA concludes new advice to doctors and patients for Tysabri (natalizumab) needed” (PDF) (на језику: енглески). European Medicines Agency. 20. 3. 2008. Архивирано из оригинала (PDF) 18. 7. 2009. г. Приступљено 5. 4. 2008.
- ^ „Questions and answers on Tysabri and liver injury” (PDF). European Medicines Agency. 20. 3. 2008. Приступљено 14. 4. 2008.[мртва веза]; lay-summary Архивирано на сајту Wayback Machine (11. јун 2008), сецонд суммарy
- ^ Кеннетх Гросс, M.D. (3. 3. 2008). „Мултипле Сцлеросис - Натализумаб (Тyсабри) Цан Рарелy Цаусе Ливер Проблемс”. Приступљено 5. 4. 2008.
- ^ Панзара, M; Францис V (1. 2. 2008). „Импортант сафетy информатион: Деар Хеалтхцаре Працтитионер леттер” (ПДФ). Биоген Идец анд Éлан. Приступљено 11. 4. 2008.; лаy суммарy Архивирано на сајту Wayback Machine (11. јун 2008)
- ^ Mullen JT, Vartanian TK, Atkins MB (2008). „Melanoma complicating treatment with natalizumab for multiple sclerosis”. N. Engl. J. Med. 358 (6): 647—8. PMID 18256405. doi:10.1056/NEJMc0706103.
- ^ van Bronswijk H, Dubois EA, van Gerven JM, Cohen AF (2008). „[New drugs; natalizumab]”. Ned Tijdschr Geneeskd (на језику: Dutch; Flemish). 152 (9): 499—500. PMID 18389881.
- ^ а б Greene, Robert T. (15. 12. 2008). „Biogen, Elan Report Brain Illness in Tysabri Patient” (на језику: енглески). Bloomberg.com. Приступљено 21. 12. 2008.
- ^ G, Van Assche; M, Van Ranst; Sciot R; et al. (2005). „Прогрессиве мултифоцал леукоенцепхалопатхy афтер натализумаб тхерапy фор Црохн'с дисеасе”. Н. Енгл. Ј. Мед. 353 (4): 362—8. ПМИД 15947080. дои:10.1056/НЕЈМоа051586.
- ^ У.С. Фоод анд Друг Администратион (2008). „Натализумаб Ињецтион фор Интравенеоус [''sic''] Усе (маркетед ас Тyсабри)”. Приступљено 22. 12. 2008.
- ^ Цхен, Y.; et al. (2009). „Асyмптоматиц реацтиватион оф ЈЦ вирус ин патиентс треатед wитх натализумаб”. Н Енгл Ј Мед. 361: 1067.
- ^ Рице ГП, Хартунг ХП, Цалабреси ПА (2005). „Анти-алпха4 интегрин тхерапy фор мултипле сцлеросис: мецханисмс анд ратионале”. Неурологy. 64 (8): 1336—42. ПМИД 15851719. дои:10.1212/01.WНЛ.0000158329.30470.Д0.
- ^ а б „Финал ТYСАБРИ ПИ” (ПДФ). Архивирано из оригинала (ПДФ) 22. 8. 2007. г. Приступљено 13. 3. 2008.
- ^ Зохрен Ф, Тоутзарис D, Кларнер V, Хартунг ХП, Киесеиер Б, Хаас Р (2008). „Тхе моноцлонал анти-ВЛА4 антибодy натализумаб мобилизес ЦД34+ хематопоиетиц прогенитор целлс ин хуманс”. Блоод. 111 (7): 3893. ПМИД 18235044. дои:10.1182/блоод-2007-10-120329.[мртва веза]
Спољашње везе[уреди | уреди извор]
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
