Полифосфат
Полифосфати су соли или естри полимерних оксиањона који су формирани од тетраедарског ПО4 фосфата, структурне јединице која је везана за заједнички атом кисеоника. Полифосфати могу имати линеарну или прстенасту структуру. У биолошким процесима и супстанцама, полифосфатни естри аденозин-дифосфат (АДП) и АТП укључени су у складиштење енергије. Мноштво полифосфата има примену у минералним секвестрацијама комуналних вода, углавном у количинама 1 до 5 ппм.[1] ГТП, ЦТП и УТП су такође важни нуклеотиди у синтези протеина и липида, као и метаболизму угљених хидрата.
Структура[уреди | уреди извор]
-
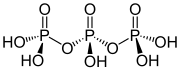
Структура трифосфорне киселине
-
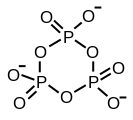
Циклични триметафосфат
-
Аденозин-дифосфат (АДП)
Структура триполифосфорне киселине илуструје начела која дефинишу структуре полифосфата. Састоји се од три тетраедарне ПО4 јединице повезане заједничким кисеоничним центрима. За линеарне ланце, фосфорна група на крају има један заједнички оксид, а остали фосфори у центрима деле два оксидна центра. Одговарајући фосфати се претварају у киселине губитком киселих протона. У случају цикличних тримера, сваки тетраедар дели два чвора са сусједним тетраедром.
Постоје три заједничка могуча угла. Овај мотив представља умрежавање линеарног полимера. Умрежени полифосфати имају листасте структуре филосиликата, али такве структуре јављају се само у екстремним условима.
Формирање и синтеза[уреди | уреди извор]
Полифосфати настају полимеризацијом деривата фосфорне киселине. Процес почиње са две фосфатне јединице које улазе у заједничку кондензацијску реакцију:
- 2 ХПО42− П2О74− + Х2О
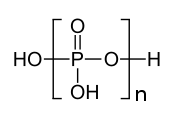
Кондензација је приказана као равнотежна зато што је такође могућа повратна реакција, хидролиза. Процес се може наставити постепено: у сваком кораку, на ланац се додаје наредна јединица ПО3, као што је означено у заградама у илустрацији полифосфорне киселине. П4О10 се види као крајњи производ кондензацијских реакција, где сваки тетраедар има три заједничка угла са осталима. Насупрот томе, сложена мешавина полимера настаје када се фосфор-пентоксиду додаје мала количина воде.
Киселинско-базна и комплексацијска својства[уреди | уреди извор]
Полифосфати су слабе базе. Усамљени пар електрона на атому кисеоника може бити дониран јону водоника (протону) или металном јону путем типичних интеракција Луисових киселина и база. То има дубоко значење у биологији. На пример, око 25% аденозин-трифосфата је протонисано у воденом раствору при пХ 7.[2]
- АТП4− + Х+ АТПХ3−, пКа 6.6
Даље протонације јављају се на нижим пХ вредностима.
„Високоенегетска“ фосфатна веза[уреди | уреди извор]
АТП формира хелатне комплексе са металним јонима. Константа стабилности за равнотежу
- АТП4− + Мг2+ МгАТП2−, лог β 4
посебно је велика.[3] Формирање комплекса магнезијума је кључни елемент у процесу хидролизе АТП, јер слаби везу између терминалне фосфатне групе и остатка молекула.[2][4]
По биолошким стандардима, отпуштена енергија у хидролизи АТП,
- АТП4− + Х2О → АДП3− + Пи−
ΔГ –36,8 кЈ мол−1 је велика. Пи је ланац неорганских фосфата, који је протонисан при биолошком пХ вредностима. Међутим, по неорганским стандардима та енергија није велика. Термин „високоенергетски“ се односи на чињеницу да је релативно висока за количине енергије ослобађене у органско хемијским реакцијама које се одвијају у живим системима.
Високополимерни неоргански полифосфати[уреди | уреди извор]
Добро су познати полифосфати са високом молекулском масом.[5] Један такав дериват је стакласта (и.е. аморфна) Грахамова со. Кристални полифосфати високе молекуларне тежине укључују Куролову и Мадрелову со. Ти молекули имају формулу [НаПО3]н[НаПО3(ОХ)]2, где н може бити веће од 2000. У погледу њихове структуре, ови полимери се састоје од ПО3– „мономера“, са ланцима који се завршавају протонизираним фосфатима.[6]
Природни полифосфати[уреди | уреди извор]
L. Либерман је 1890. додине пронашао високо-полимерне неорганске полифосфате у живим организмима. Ова једињења су линеарни полимери који садрже од неколико до више стотина ортофосфорних остатака повезаних енергетски богатим фосфоанхидридним везама.
Раније су ова једињења сматрана „молекуларним фосилима“ или као само фосфор и извор енергије за опстанак микроорганизама под екстремним условиима. За њих се сада зна да имају и регулаторне улоге и да се налазе у представницима свих царстава живих организама, где учествују у метаболичким корекцијама и контроли на генетичким и ензиматским нивоима. Полифосфати су директно учествују у пребацивању из генетичког програма који карактерише експоненцијална фазе раста бактерија у програм ћелијског опстанка под стационарним условима, "живота у спорој линији". Они учествују у многим регулаторним механизама бактерија:
- Учествују у индукцији рпоС, РНК-полимеразне подјединице која је одговорна за изражавање велике групе гена који учествују у корекцијама стационарне фазе раста и многих стресних агенаса.
- Важни су за мобилну покретљивост, формирање биофилма и вируленције.
- Полифосфати и ексополифосфатаза учествују у регулацији нивоа оскудног респонсног фактора, гванозин 5'-дифосфат 3'-дифосфата (ппГпп), који је секундарни гласник у бактеријским ћелијама.
- Полифосфати учествују у формирању канала кроз живе ћелијске мембране. Ти канали које формирају полифосфат и поли-Б-хидроксибутират са Ца2+ учествују у транспортним процесима у различитим организмима.
- Важна функција полифосфата у микроорганизмима (прокариотима) и нижим еукариотама је прилагођавање на промене услова животне средине пружајући фосфате и енергетске резерве. Полифосфати су присутни у животињским ћелијама, и доступна је знатна количина података о њиховом учешћу у регулаторним процесима током развића и ћелијској пролиферацији и диференцијацији; а посебно у коштаним ткивима и мозгу.
Код људи је показано да полифосфати играју кључну улогу у коагулацији крви. Након што их произведу и ослободе тромбоцити[7] они активирају фактор XII који је есенцијалан за формирање крвних угрушака. Осим тога, полифосфати изведени из тромбоцита активирају фактора XII (Хагеманов фактор) згрушавања крви који иницира формирање фибрина и стварање једног од проинфламаторних посредника, брадикинина, који доприноси цурењу из крвних судова и тромбози.[8][9]
Неоргански полифосфати имају кључну улогу у толеранцији ћелија квасца на токсичност тешких металних катјона.[10]
Види још[уреди | уреди извор]
Референце[уреди | уреди извор]
- ^ „Архивирана копија” (ПДФ). Архивирано из оригинала (ПДФ) 19. 04. 2011. г. Приступљено 30. 01. 2017.
- ^ а б Сторер А; Цорнисх-Боwден А (1976). „Цонцентратион оф МгАТП2- анд отхер ионс ин солутион. Цалцулатион оф тхе труе цонцентратионс оф специес пресент ин миxтурес оф ассоциатинг ионс”. Биоцхем Ј. 159 (1): 1—5. ПМЦ 1164030
 . ПМИД 11772.
. ПМИД 11772.
- ^ Wилсон Ј, Цхин А (1991). „Цхелатион оф дивалент цатионс бy АТП, студиед бy титратион цалориметрy”. Анал Биоцхем. 193 (1): 16—9. ПМИД 1645933. дои:10.1016/0003-2697(91)90036-С.
- ^ Гарфинкел L, Алтсцхулд Р, Гарфинкел D (1986). „Магнесиум ин цардиац енергy метаболисм”. Ј Мол Целл Цардиол. 18 (10): 1003—13. ПМИД 3537318. дои:10.1016/С0022-2828(86)80289-9.
- ^ Греенwоод, Норман Н.; Еарнсхаw, Алан (1997). Цхемистрy оф тхе Елементс (II изд.). Оxфорд: Буттерwортх-Хеинеманн. ИСБН 0080379419.
- ^ Клаус Сцхрöдтер, Герхард Беттерманн, Тхомас Стаффел, Фриедрицх Wахл, Тхомас Клеин, Тхомас Хофманн "Пхоспхориц Ацид анд Пхоспхатес" ин Уллманн’с Енцyцлопедиа оф Индустриал Цхемистрy 2008, Wилеy-ВЦХ, Wеинхеим. . дои:10.1002/14356007.а19_465.пуб3. Недостаје или је празан параметар
|титле=(помоћ) - ^ Руиз ФА, Леа ЦР, Олдфиелд Е, Доцампо Р (2004). „Хуман плателет денсе гранулес цонтаин полyпхоспхате анд аре симилар то ацидоцалцисомес оф бацтериа анд уницеллулар еукарyотес”. Ј Биол Цхем. 279 (43): 44250—7. ПМИД 15308650. дои:10.1074/јбц.М406261200.
- ^ Мüллер Ф, Мутцх Њ, Сцхенк WА, Смитх СА, Естерл L, Спронк ХМ, Сцхмидбауер С, Гахл WА, Морриссеy ЈХ, Реннé Т (2009). „Плателет полyпхоспхатес аре проинфламматорy анд процоагулант медиаторс ин виво”. Целл. 139 (6): 1143—56. ПМЦ 2796262
 . ПМИД 20005807. дои:10.1016/ј.целл.2009.11.001.
. ПМИД 20005807. дои:10.1016/ј.целл.2009.11.001.
- ^ „Неwлy дисцоверед мецханисм бy wхицх блоод цлотс форм”. пхyсорг.цом. 10. 12. 2009. Приступљено 13. 12. 2009.
- ^ Андреева Н, Рyазанова L, Дмитриев V, Кулаковскаyа Т, Кулаев I (2013). „Адаптатион оф Саццхаромyцес церевисиае то тоxиц манганесе цонцентратион триггерс цхангес ин инорганиц полyпхоспхатес.”. ФЕМС Yеаст Рес. 13 (5): 463—470. ПМИД 23663411. дои:10.1111/1567-1364.12049.
Спољашње везе[уреди | уреди извор]
- Павлов Е, Гримблy C, Диао ЦТ, Френцх РЈ (2005). „А хигх-цондуцтанце моде оф а полy-3-хyдроxyбутyрате/цалциум/полyпхоспхате цханнел исолатед фром цомпетент Есцхерицхиа цоли целлс”. ФЕБС Летт. 579 (23): 5187—92. ПМИД 16150446. дои:10.1016/ј.фебслет.2005.08.032.
- Кулаев I, Вагабов V, Кулаковскаyа Т (1999). „Неw аспецтс оф инорганиц полyпхоспхате метаболисм анд фунцтион”. Ј. Биосци. Биоенг. 88 (2): 111—29. ПМИД 16232585. дои:10.1016/С1389-1723(99)80189-3.
- Кулаев I, Кулаковскаyа Т (2000). „Полyпхоспхате анд пхоспхате пумп”. Анну. Рев. Мицробиол. 54: 709—34. ПМИД 11018142. дои:10.1146/аннурев.мицро.54.1.709.[мртва веза]