Benzofuran
| |||
| |||
| Nazivi | |||
|---|---|---|---|
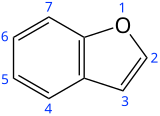
| IUPAC naziv
1-Benzofuran
| |||
| Drugi nazivi
Kumaron, benzo[b]furan
| |||
| Identifikacija | |||
3D model (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.439 | ||
| KEGG[1] | |||
| UNII | |||
| |||
| Svojstva | |||
| C8H6O | |||
| Molarna masa | 118,14 g·mol−1 | ||
| Tačka topljenja | −18 °C (0 °F; 255 K) | ||
| Tačka ključanja | 173 °C (343 °F; 446 K) | ||
| Opasnosti | |||
| Letalna doza ili koncentracija (LD, LC): | |||
LD50 (LD50)
|
500 mg/kg (mice).[4] | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |||
| Reference infokutije | |||
Benzofuran je heterociklično jedinjenje koji se sastoji od kondenzovanih prstena benzena i furana. Ova bezbojna tečnost je komponenta katrana. Benzofuran je osnova mnogih srodnih jedinjenja sa kompleksnijim strukturama. Na primer, psoralen je derivat benzofurana koji se javlja u nekoliko biljki.
Produkcija[uredi | uredi izvor]
Benzofuran se može ekstrahovati iz katrana. On se takođe dobija dehidrogenacijom 2-etilfenola.[4]
Laboratorijski metodi[uredi | uredi izvor]
Benzofuran se može pripremiti putem O-alkilacije salicilaldehida sa hlorosirćetnom kiselinom i naknadnom dehidratacijom nastalog etra.[5] U drugom metodu zvanom Perkinovo preuređenje[6][7][8] kumarin reaguje sa hidroksidom:
Srodna jedinjenja[uredi | uredi izvor]
Reference[uredi | uredi izvor]
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б Collin, G.; Höke, H. (2007). „Benzofurans”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.l03_l01.
- ^ Burgstahler, A. W.; Worden, L. R. (1966). „Coumarone” (PDF). Org. Synth. 46: 28.; Coll. Vol., 5, стр. 251
- ^ Perkin, W. H. (1870). „XXIX. On some New Bromine Derivatives of Coumarin”. Journal of the Chemical Society. 23: 368—371. doi:10.1039/JS8702300368.
- ^ Perkin, W. H. (1871). „IV. On some New Derivatives of Coumarin”. Journal of the Chemical Society. 24: 37—55. doi:10.1039/JS8712400037.
- ^ Bowden, K.; Battah, S. (1998). „Reactions of Carbonyl Compounds in Basic Solutions. Part 32. The Perkin Rearrangement”. Journal of the Chemical Society, Perkin Transactions 2. 1998 (7): 1603—1606. doi:10.1039/a801538d.