Клаузијус–Клапејронов однос
| Термодинамика |
|---|
 |
Клаузијус–Клапејронов однос, назван по Рудолфу Клаузијусу[1] и Емилу Клаперону[2], је начин карактеризације неконтинуираног фазног прелаза између две фазе материје једног саставног дела.
Дефиниција[уреди | уреди извор]
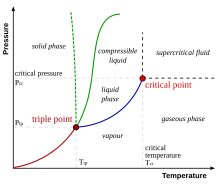
На дијаграму притисак - температура (П – Т), линија која раздваја две фазе позната је као крива коегзистенције. Однос Клаусиус-Клаперон даје нагиб тангенте на ову криву Математички.
Где је:
- је нагиб тангенте до кривуље суживота у било којој тачки,
- је специфична латентна топлота,
- је температура,
- је промена специфичног волумена фазног прелаза, и Деривације
- је специфична ентропијска промена фазног прелаза.
Деривација[уреди | уреди извор]
Извођење из државног постулата[уреди | уреди извор]
Помоћу државног постулата[а] узмите одређену ентропију , да хомогена супстанца буде функција специфичне запремине и температуре [5].
Однос Клаузије-Клаперон карактерише понашање затвореног система током фазне промене , током које су температура и притисак константни по дефиницији. Дакле, [6].
Коришћењем одговарајућег Маквеловог односа даје се[7]
где је притисак. Пошто су притисак и температура константни, дериват притиска у односу на температуру се не мења[8][9]:57, 62 & 671 Стога се делимични дериват специфичне ентропије може променити у укупни дериват
и укупни дериват притиска у односу на температуру може се узети у обзир при интегрисању из почетне фазе до завршне фазе ,[10] да се добије
где су и промена специфичне ентропије и специфичне запремине. С обзиром да је промена фазе интерно реверзибилни процес и да је наш систем затворен, први закон термодинамике се држи
где је унутрашња енергија система. С обзиром на константан притисак и температуру (током фазне промене) и дефиницију специфичне енталпије , ми добијамо
С обзиром на константан притисак и температуру (током фазне промене), добијамо[11]
Замјена дефиниције специфичне латентне даје
Замјена овог резултата горњим дериватом притиска (), добијамо[12][13]
Овај резултат (познат и као Kлаперонова једначина ) изједначава нагиб тангенте према кривуљи суживота, у било којој тачки на кривуљи, функције специфичне латентне топлоте , температура , и промена специфичне запремине.
Деривација из односа Гибс-Духем[уреди | уреди извор]
Претпоставимо две фазе, и , су у контакту и у равнотежи једни са другима. Њихови хемијски потенцијали су повезани
Даље, дуж криве суживота,
Због тога може се користити Џибс-Духем однос
где је:
- специфична ентропија
- специфична запремина
- моларна маса
да би се добила
Преуређење даје
из којег се наставља извођење Kлаперонове једнчине као у претходном одељку.
Идеална апроксимација гаса на ниским температурама[уреди | уреди извор]
Када је фазни прелаз неке супстанце између гасне фазе и кондензоване фазе ( течне или чврсте ) и догоди се на температурама много нижим од критичне температуре те материје, специфичан волумен гасне фазе увелико прелази фазу кондензоване фазе . Стога се може приближити
на ниским температурама aко је притисак низак, гас се може апроксимирати и законом идеалног гаса, тако да
где је притисак, је специфична константа гаса и је температура. Замена у Клапеиронову једначину
можемо добити Клаузијус – Клапеирон једначину [14]
за ниске температуре и притиске [15], где је је специфична латентна топлота материје. Дозволити и бити било које две тачке дуж кривуље суживота између две фазе и Генерално варира између било које две такве тачке, у зависности од температуре. Али ако је константа,
Последње једначине су корисне јер односе равнотежни притисак паре или притисак засићења паре и температуру са латентном топлотом промене фазе, без тражења посебних података о запремини.
Апликације[уреди | уреди извор]
Хемија и хемијско инжењерство[уреди | уреди извор]
За прелазе између гасне и кондензоване фазе са горе описаним апроксимацијама, израз се може преписати као
где је константа. За прелаз течни гас је специфична латентна топлота (или специфична енталпија ) испаравања ; за прелаз чврстог гаса, је специфична латентна топлота сублимације . Ако је позната латентна топлота, тада познавање једне тачке на кривуљи суживота одређује остатак кривуље. Супротно томе, однос између and је линеарна, па се линеарна регресија користи за процену латентне топлоте.
Метеорологија и климатологија[уреди | уреди извор]
Атмосферска водена пара покреће многе важне Метеорологија метеоролошке појаве (нарочито падавине), мотивишући интерес за њену Динамички систем динамику. Клаузијус-Клапеирон једначина за водену пару у типичним атмосферским условима (близу Стандардни услови за температуру и притисак стандардне температуре и притиска ) је
где:
- је притисак засићења паре
- је температура
- је специфична латентна топлота за испаравање воде
- је константа гаса водене паре
Температурна зависност латентне топлоте (и притиска засићене паре ) не може се занемарити у овој апликацији. Срећом, формула Август-Рош-Магнус даје врло добру апроксимацију:
У горњем изразу, је у Паскалима и је у Целзијусу , док је свуда другде на овој страници, је апсолутна температура (нпр. у Келвину). (То се такође понекад назива апроксимација Магнуса или Магнуса – Тетена , мада је ова атрибуција историјски нетачна.)[20]. Али, погледајте и ову расправу о тачности различитих приближних формула за притисак засићења пара водом .
У типичним атмосферским условима је именитељ експонента слабо зависи од тога (за коју је јединица целзијус). Стога једначина Август-Рош-Магнус имплицира да се притисак засићене водене паре приближно експоненцијално мења са температуром у типичним атмосферским условима, те се стога капацитет задржавања воде у атмосфери повећава за око 7% за сваки пораст температуре од 1°C [21].
Пример[уреди | уреди извор]
Једна од употреба ове једначине је одредити да ли ће се у датој ситуацији догодити фазни прелаз. Размотримо питање колики је притисак потребан да се растопи лед на температури испод 0°C. Имајте на уму да је вода необична по томе што је промена запремине након топљења негативна. Можемо претпоставити
и замена са
- (латентна топлота фузије за воду),
- K (апсолутна температура) и
- (промена специфичне запремине из чврсте у течне),
добијамо
Да бисте пружили груби пример колики је ово притиска, да бисте растопили лед на –7°C, потребно је уравнотежити мали аутомобил (маса = 1000 кг[22]) на напрстку (површина = 1 цм²).
Други дериват[уреди | уреди извор]
Иако однос Клаусиус-Клаперон даје нагиб кривуље коегзистенције, он не даје никакве информације о његовој закривљености или другој деривацији. Други дериват криве суживота фаза 1 и 2 дат је[23]
где претплате 1 и 2 означавају различите фазе, је специфични топлотни капацитет при константном притиску, је термални коефицијент ширења и је изотермна стишљивост.
Напомене[уреди | уреди извор]
- ^ Стање постулат је термин који се користи у термодинамике који дефинише одређени број својстава на термодинамички систем у стању равнотеже. Понекад се назива и државним принципом[3].. Државни постулат омогућава одређивање коначног броја својстава како би се у потпуности описало стање термодинамичке равнотеже. Једном када се постулати стања дају остала неодређена својства морају попримати одређене вриједности.
- Државни постулат каже: Стање једноставног стисљивог система у потпуности одређују два независна, интензивна својства[4]
Референце[уреди | уреди извор]
- ^ Clausius, R. (1850). „Ueber die bewegende Kraft der Wärme und die Gesetze, welche sich daraus für die Wärmelehre selbst ableiten lassen” [On the motive power of heat and the laws which can be deduced therefrom regarding the theory of heat]. Annalen der Physik (на језику: German). 155 (4): 500—524. Bibcode:1850AnP...155..500C. doi:10.1002/andp.18501550403. hdl:2027/uc1.$b242250
 .
.
- ^ Clapeyron, M. C. (1834). „Mémoire sur la puissance motrice de la chaleur”. fr (на језику: French). 23: 153—190. ark:/12148/bpt6k4336791/f157.
- ^ Moran, Michael J., author. Fundamentals of engineering thermodynamics. ISBN 9781119391388. OCLC 992798629.
- ^ Cengel, Yunus A.; Boles, Michael A. (2008). Thermodynamics: an engineering approach.
 . New York, NY: McGraw-Hill. ISBN 0-07-238332-1.
. New York, NY: McGraw-Hill. ISBN 0-07-238332-1.
- ^ Wark, Kenneth (1988) [1966]. „Generalized Thermodynamic Relationships”. Thermodynamics (5th изд.). New York, NY: McGraw-Hill, Inc. стр. 508. ISBN 978-0-07-068286-3.
- ^ Wark 1988, стр. 508 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Wark 1988, стр. 508 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Çengel, Yunus A.; Boles, Michael A. (1998) [1989]. Thermodynamics – An Engineering Approach. McGraw-Hill Series in Mechanical Engineering (3rd изд.). Boston, MA.: McGraw-Hill. ISBN 978-0-07-011927-7.
- ^ Wark 1988, стр. 508 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Wark 1988, стр. 508 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Wark 1988, стр. 508 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Salzman, William R. (21. 8. 2001). „Clapeyron and Clausius–Clapeyron Equations”. Chemical Thermodynamics. University of Arizona. Архивирано из оригинала 7. 6. 2007. г. Приступљено 11. 10. 2007.
- ^ Wark 1988, стр. 509 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Wark 1988, стр. 509 harvnb грешка: више циљева (2×): CITEREFWark1988 (help)
- ^ Cengel 1998, стр. 672
- ^ Masterton, William L.; Hurley, Cecile N. (2008). Chemistry : principles and reactions (6th изд.). Cengage Learning. стр. 230. ISBN 9780495126713. Приступљено 3. 4. 2020.
- ^ Alduchov, Oleg; Eskridge, Robert (1. 11. 1997), Improved Magnus' Form Approximation of Saturation Vapor Pressure, NOAA, doi:10.2172/548871 — Equation 25 provides these coefficients.
- ^ Alduchov, Oleg A.; Eskridge, Robert E. (1996). „Improved Magnus Form Approximation of Saturation Vapor Pressure”. Journal of Applied Meteorology. 35 (4): 601—9. Bibcode:1996JApMe..35..601A. doi:10.1175/1520-0450(1996)035<0601:IMFAOS>2.0.CO;2. Equation 21 provides these coefficients.
- ^ Lawrence, M. G. (2005). „The Relationship between Relative Humidity and the Dewpoint Temperature in Moist Air: A Simple Conversion and Applications” (PDF). Bulletin of the American Meteorological Society. 86 (2): 225—233. Bibcode:2005BAMS...86..225L. doi:10.1175/BAMS-86-2-225.
- ^ IPCC, Climate Change 2007: Working Group I: The Physical Science Basis, "FAQ 3.2 How is Precipitation Changing ?", URL http://www.ipcc.ch/publications_and_data/ar4/wg1/en/faq-3-2.html Архивирано 2018-11-02 на сајту Wayback Machine
- ^ Zorina, Yana (2000). „Mass of a Car”. The Physics Factbook.
- ^ Krafcik, Matthew; Sánchez Velasco, Eduardo (2014). „Beyond Clausius–Clapeyron: Determining the second derivative of a first-order phase transition line”. American Journal of Physics. 82 (4): 301—305. Bibcode:2014AmJPh..82..301K. doi:10.1119/1.4858403.
Литература[уреди | уреди извор]
- Masterton, William L.; Hurley, Cecile N. (2008). Chemistry : principles and reactions (6th изд.). Cengage Learning. стр. 230. ISBN 9780495126713. Приступљено 3. 4. 2020.
- Çengel, Yunus A.; Boles, Michael A. (1998) [1989]. Thermodynamics – An Engineering Approach. McGraw-Hill Series in Mechanical Engineering (3rd изд.). Boston, MA.: McGraw-Hill. ISBN 978-0-07-011927-7.
- Cengel, Yunus A.; Boles, Michael A. (2008). Thermodynamics: an engineering approach.
 . New York, NY: McGraw-Hill. ISBN 0-07-238332-1.
. New York, NY: McGraw-Hill. ISBN 0-07-238332-1. - Wark, Kenneth (1988) [1966]. „Generalized Thermodynamic Relationships”. Thermodynamics (5th изд.). New York, NY: McGraw-Hill, Inc. ISBN 978-0-07-068286-3.
- Yau, M.K.; Rogers, R.R. (1989). Short Course in Cloud Physics (3rd изд.). Butterworth–Heinemann. ISBN 978-0-7506-3215-7.
- Iribarne, J.V.; Godson, W.L. (2013). „4. Water-Air systems § 4.8 Clausius–Clapeyron Equation”. Atmospheric Thermodynamics. Springer. стр. 60—. ISBN 978-94-010-2642-0.
- Callen, H.B. (1985). Thermodynamics and an Introduction to Thermostatistics. Wiley. ISBN 978-0-471-86256-7.

















































































![{\displaystyle {\begin{aligned}{\frac {\mathrm {d} ^{2}P}{\mathrm {d} T^{2}}}={\frac {1}{v_{2}-v_{1}}}\left[{\frac {c_{p2}-c_{p1}}{T}}-2(v_{2}\alpha _{2}-v_{1}\alpha _{1}){\frac {\mathrm {d} P}{\mathrm {d} T}}\right]+{}\\{\frac {1}{v_{2}-v_{1}}}\left[(v_{2}\kappa _{T2}-v_{1}\kappa _{T1})\left({\frac {\mathrm {d} P}{\mathrm {d} T}}\right)^{2}\right],\end{aligned}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6b1f9040b083bf122ad453b25f90fd71f4504034)


