Titanijum tetrajodid

| |
| |
| Nazivi | |
|---|---|
| IUPAC naziv
Titanijum(IV) jodid
| |
| Drugi nazivi
Titanijum tetrajodid
| |
| Identifikacija | |
| ECHA InfoCard | 100.028.868 |
| Svojstva | |
| TiI4 | |
| Molarna masa | 555,485 g/mol |
| Agregatno stanje | crveno-smeđi kristali |
| Gustina | 4,3 g/cm3 |
| Tačka topljenja | 150 °C |
| Tačka ključanja | 377 °C |
| hidrolizuje se | |
| Rastvorljivost u drugi rastvarači | rastvoran u CH2Cl2 CHCl3 CS2 |
| Struktura | |
| Kristalna rešetka/struktura | kubna (a = 12.21 Å) |
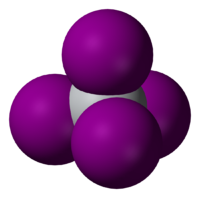
| Geometrija molekula | tetraedralna |
| Dipolni moment | 0 D |
| Opasnosti | |
| Opasnost u toku rada | silovita hidroliza korozivan |
| R-oznake | 34-37 |
| S-oznake | 26-36/37/39-45 |
| Srodna jedinjenja | |
Srodne materije
|
titanijum tetrahlorid, titanijum tetrabromid, ugljen tetrajodid, I2, Ta2I10 |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Titanijum tetrajodid je neorgansko jedinjenje sa formulom TiI4. On je redak binarni metalni jodid, koji se sastoji od izolovanih molekula sa tetraedralnim Ti(IV) centrima.[3] Usled njegovog molekulskog karaktera, TiI4 se može destilovati bez razlaganja u atmosferi. Ova osobina je osnova Van Arkelovog procesa za prečišćavanje titanijum. Razlike u tačkama topljenja između TiCl4 (-24 °C) i TiI4 (150 °C) su uporedive sa razlikama tački topljenja CCl4 (-23 °C) i CI4 (168 °C), što je posledica jačeg međumolekulskog van der Valsovog vezivanja u jodidima.
Proizvodnja[уреди | уреди извор]
Tri metoda su poznata: Iz elementa, tipično koristeći peć na 425 °C:[4]
- Ti + 2 I2 → TiI4
This reaction can be reversed to produce highly pure films of Ti metal.[5]
Reakcija razmene titanijum tetrahlorida i HI.
- TiCl4 + 4 HI → TiI4 + 4 HCl
Oksido-jodna razmena sa aluminijum jodidom.
- 3 TiO2 + 4 AlI3 → 3 TiI4 + 2 Al2O3
Reakcije[уреди | уреди извор]
Poput TiCl4 i TiBr4, TiI4 formira adukte sa Luisovim bazama. On se isto tako može redukovati. Kad se redukcija izvodi u prisustvu Ti metala, dobijaju se polimerni Ti(III) i Ti(II) derivati kao što su CsTi2I7 i lanac CsTiI3, respektivno.[6] U rastvoru CH2Cl2, TiI4 manifestuje reaktivnost ka alkenima i alkinima, te proizvodi organojodne derivate.[7]
Reference[уреди | уреди извор]
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Tornqvist, Erik G. M.; Libby, Willard F. (1979). „Crystal structure, solubility, and electronic spectrum of titanium tetraiodide”. Inorganic Chemistry. 18 (7): 1792—1796. doi:10.1021/ic50197a013.
- ^ Lowery, R. N.; Fay, R. C. "Titanium(IV) Iodide" Inorganic Syntheses 1967, volume X, pages 1-6.
- ^ Blumenthal, Warren B.; Smith, Howard (1950). „Titanium tetraiodide, Preparation and Refining”. Industrial and Engenieering Chemistry. 42 (2): 249—251. doi:10.1021/ie50482a016.
- ^ Jongen, L.; Gloger, T.; Beekhuizen, J.; Meyer, G. "Divalent Titanium: The Halides ATiX3 (A = K, Rb, Cs; X = Cl, Br, I)" Zeitschrift fur Anorganische und Allgemeine Chemie 2005, volume 631, pages 582-586.
- ^ Shimizu, Makoto; Toyoda, Tadahiro; Baba, Toru. An Intriguing Hydroiodination of Alkenes and Alkynes with Titanium Tetraiodide. Synlett 2005, volume 16, pages 2516-2518.
