Voltametrija


Voltametrija je klasa elektroanalitičkih metoda koja se koristi u analitičkoj hemiji i raznim industrijskim procesima. U voltametriji se informacija o analitu dobija merenjem struje dok se potencijal varira.[1][2]
Tri elektrodni sistem[уреди | уреди извор]
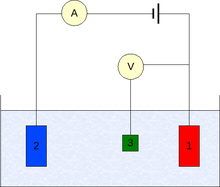
Voltametrijski eksperimenti ispituje polu ćelijsku reaktivnost analita. Voltametrija je studija struje u funkciji primenjenog potencijala.
Krive I = f(E) se nazivaju voltamogrami. Potencijal se arbitrarno varira bilo stepen po stepen ili kontinuirano, i vrednost struje se meri kao zavisna promenljiva. Suprotan pristup, tzv. amperometrija, je takođe moguć ali nije uobičajen.
Oblik krivih zavisi od brzine varijacije potencijala (priroda pokretačka snaga) i od toga da li se rastvor meša ili je u mirovanju (maseni transfer).
Većina eksperimenta kontroliše potencijal (volt) elektrode u kontaktu sa analitom, dok se meri rezultujuća struja (amper).[3]
Za izvođenje eksperimenta potrebne su najmanje dve elektrode. Na radnu elektrodu koja dolazi u kontakt sa analitom se mora primeniti željeni potencijal na kontrolisani način da bi se omogućio prenos naelektrisanja na i sa analita. Druga elektroda je drugi deo ćelije. Ona mora da ima poznat potencijal kojim se podešava potencijal radne elektrode. Ona isto tako balansira naelektrisanje dodato ili uklonjeno sa radne elektrode. Iako je ovo održiva postava, ona ima niz nedostataka. Najznačajniji od njih je da je veoma teško da se održi konstantni potencijal elektrode.
Da bi se rešio ovaj problem, uloge snabdevanja elektronima i referentnog potencijal su podeljene između dve zasebne elektrode. Referentna elektroda je polovina ćelije sa poznatim redukcionim potencijalom. Njena jedina uloga je da deluje kao referenca u merenju i kontroli potencijala radne elektrode. On ne sprovodi struju. Pomoćna elektroda sprovodi struju neophodnu za balansiranje struje radne elektrode. Da bi se to ostvarilo, pomoćna elektroda će ćesto poprimiti ekstremne potencijala na granicama opsega rastvarača, gde ona oksidiše ili redukuje rastvarač ili podržavajući elektrolit. Ove elektrode, radna, referentna i pomoćna sačinjavaju moderne tri elektrodne sisteme.
Vidi još[уреди | уреди извор]
Reference[уреди | уреди извор]
- ^ Kissinger, Peter; Heineman, William R. (23. 1. 1996). Laboratory Techniques in Electroanalytical Chemistry, Second Edition, Revised and Expanded (2 изд.). CRC. ISBN 978-0-8247-9445-3.
- ^ Zoski, Cynthia G. (7. 2. 2007). Handbook of Electrochemistry. Elsevier Science. ISBN 978-0-444-51958-0.
- ^ Bard, Allen J.; Faulkner, Larry R. (18. 12. 2000). Electrochemical Methods: Fundamentals and Applications (2 изд.). Wiley. ISBN 978-0-471-04372-0.
Literatura[уреди | уреди извор]
- Reinmuth, W. H. (1. 11. 1961). „Theory of Stationary Electrode Polarography”. Analytical Chemistry. 33 (12): 1793—1794. doi:10.1021/ac60180a004.
- Skoog, Douglas A.; West, Donald M.; F. James Holler (1995). Fundamentals of Analytical Chemistry (7th изд.). Harcourt Brace College Publishers. ISBN 978-0-03-005938-4.
- Zanello, P. (2003). Inorganic Electrochemistry: Theory, Practice, and Application (1 изд.). Royal Society of Chemistry. ISBN 978-0-85404-661-4.
