Citrat — разлика између измена
Садржај обрисан Садржај додат
м r2.6.4) (Робот додаје: sh:Citrati |
м додана категорија Карбоксилатни анјони помоћу геџета HotCat |
||
| Ред 14: | Ред 14: | ||
[[Категорија:Цитрати]] |
[[Категорија:Цитрати]] |
||
[[Категорија:Карбоксилатни анјони]] |
|||
[[su:Sitrat]] |
[[su:Sitrat]] |
||
Верзија на датум 25. јануар 2012. у 12:21
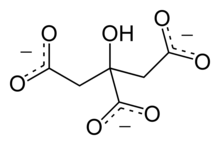

Citrati su soli limunske kiseline.[1][2][3]
Važniji citrati
- Gvožđe(II) citrat - upotrebljava se kao lek protiv malokrvnosti. Dobija se otapanjem gvožđa u limunskoj kiselini.
- Natrijum citrat - upotrebljava se kao zamena za kuhinjsku so. Dobija se otapanjem natrijuma u limunskoj kiselini ili reakcijom sode bikarbone i limunske kiseline.
- Kalijum citrat- Nastaje otapanjem kalijuma u limunskoj kiselini ili neutralizacijom kalijum hidroksida sa limunskom kiselinom.
- Kalcijum citrat nastaje otapanjem kalcijuma u limunskoj kiselini ili neutralizacijom kalcijum hidroksida sa limunskom kiselinom.
Literatura
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ McMurry John E. (1992). Fundamentals of Organic Chemistry (3rd изд.). Belmont: Wadsworth. ISBN 0-534-16218-5.
- ^ Morrison Robert Thornton; Boyd Robert Neilson (2006). Organic chemistry. Engelwood Cliffs, New Jersey: Prentice Hall. ISBN 8120307658.
