Солватација — разлика између измена
м Робот додаје {{Commonscat|Solvation}} |
|||
| Ред 19: | Ред 19: | ||
{{-}} |
{{-}} |
||
{{Аналитичка хемија}} |
{{Аналитичка хемија}} |
||
{{Commonscat|Solvation}} |
|||
[[Категорија:Хемијске реакције]] |
[[Категорија:Хемијске реакције]] |
||
Верзија на датум 25. фебруар 2012. у 05:28
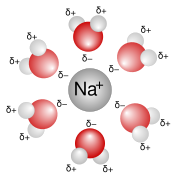
Солватација је процес окруживања честице растворка честицама растварача. При томе су честице растварача најчешће молекули док честице растворка могу бити молекули, атоми или јони.
Хидратација (од грч. hydor - вода) - нагомилавање молекула воде око растворка. Хидратација је специјални случај солватације.
Солватација је универзална појава али је најизразитија код веома поларних растварача, где и растворак има изражене поларне особине или поседује јонску везу. Молекули поларног растварача тада граде доста постојани омот (солватациону сферу, а када је расртварач вода, хидратациону сферу) дебљине до 4-5 молекула растварача око честице растворка. Код бројних хемијских реакција јона у воденим растворима хидратациона сфера представља препреку која успорава реакцију.
Солватација је основни узрок електролитичке дисоцијације код раствора.
Приликом солватације одигравају се промене у енергетском садржају система (енталпије) као и промене уређености система (ентропије). Пре него што је могуће да дође до интеракције честица растворка и растварача, потребно је да дође до раскидања међумолекулских веза између истих. Овај процес је ендотерман али се уравнотежује са стварањем нових интермолекулских веза између растворка и растварача, што је егзотерман процес. Нето промена енергије је у општем случају мала (мада има екстремних изузетака) и може да има како ендо- тако и егзотерман карактер. Ендотермне спонтане солватације објашњавају се проманама ентропије. Наиме, повећање неуређености система фаворизује растварање.
