2-Бутанол

| |
| Називи | |
|---|---|
| IUPAC назив
Butan-2-ol[1]
| |
| Други називи
сец-Бутанол
сец-Бутил алкохол 2-Бутанол 2-Бутил алкохол | |
| Идентификација | |
| |
3Д модел (Jmol)
|
|
| Бајлштајн | 773649 1718764 (R) |
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.001.053 |
| EC број | 201-158-5 |
| Гмелин Референца | 1686 396584 (R) |
| МеСХ | 2-бутанол |
| RTECS | ЕО1750000 |
| УН број | 1120 |
| |
| Својства | |
| C4H10O | |
| Моларна маса | 74,12 g·mol−1 |
| Густина | 0,808 g cm−3 |
| Тачка топљења | −115 °C; −175 °F; 158 K |
| 290 g dm−3[4] | |
| log P | 0.683 |
| Напон паре | 1,67 kPa (на 20 °C) |
| Индекс рефракције (nD) | 1,3978 (на 20 °C) |
| Термохемија | |
| Специфични топлотни капацитет, C | 197,1 J K−1 mol−1 |
| Стандардна моларна ентропија S |
213,1 J K-1 mol−1 |
Стд енталпија
формирања (ΔfH⦵298) |
−343,3–−342,1 kJ mol-1 |
| Стд енталпија сагоревања ΔcH |
−2,6611–−2,6601 MJ mol−1 |
| Opasnosti | |
| Bezbednost prilikom rukovanja | inchem.org |
| GHS grafikoni |  
|
| GHS signalna reč | Upozorenje |
| H226, H319, H335, H336 | |
| P261, P305+351+338 | |
EU klasifikacija (DSD)
|
|
| R-oznake | R10, R36/37, R67 |
| S-oznake | (S2), S7/9, S13, S24/25, S26, S46 |
| NFPA 704 | |
| Tačka paljenja | 22 to 27 °C (72 to 81 °F; 295 to 300 K) |
| 405 °C (761 °F; 678 K) | |
| Eksplozivni limiti | 1.7–9.8% |
| Letalna doza ili koncentracija (LD, LC): | |
LCLo (LCLo)
|
16,000 ppm (pacov, 4 hr) 10,670 ppm (miš, 3.75 hr) 16,000 ppm (miš, 2.67 hr)[5] |
| SAD zdravstvene granice izlaganja (NIOSH): | |
PEL (dozvoljivo)
|
TWA 150 ppm (450 mg/m3)[5] |
REL (preporučeno)
|
TWA 100 ppm (305 mg/m3) ST 150 ppm (455 mg/m3)[5] |
IDLH (neposredna opasnost)
|
2000 ppm[5] |
| Srodna jedinjenja | |
Srodne butanoli
|
n-Butanol Izobutanol tert-Butanol |
Srodna jedinjenja
|
Butanon |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
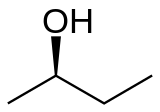
2-Бутанол (сец-бутанол) је органско једињење са формулом CH3CH(OH)CH2CH3. Овај секундарни алкохол је запаљива, безбојна течност, која је растворна у 12 делова воде и комплетно се меша са поларним органским растварачима, као што су етри и други алкохоли. Он се производи у великим размерама, првенствено као прекурзор индустријског растварача метил етил кетона. 2-Бутанол је хиралан, те постоје два стереоизомера, који се означавају као (R)-(−)-2-бутанол и (S)-(+)-2-бутанол. Он се нормално налази као смеша два стереоизомера – рацемска смеша.
 |

|
 |

|
Производња и примене[уреди | уреди извор]
2-Бутанол се индустријски производи хидратацијом 1-бутена или 2-бутена:
Сумпорна киселина се користи као катализатор овер конверзије.[6]
Мада се део произведеног 2-бутанола користи као растварач, он се углавном конвертује до бутанона ("МЕК"), који је важан индустријски растварач и присутан је у средствима за чишћење и уклањање фарбе. Испарљиви естри 2-бутанола имају пријатне ароме, те се у малим количинама користе у парфемима и вештачким зачинима.
Референце[уреди | уреди извор]
- ^ „2-бутанол - Цомпоунд Суммарy”. ПубЦхем Цомпоунд. УСА: Натионал Центер фор Биотецхнологy Информатион. 26. 3. 2005. Идентифицатион анд Релатед Рецордс. Приступљено 12. 10. 2011.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Alger, Donald B. (1991). „The water solubility of 2-butanol: A widespread error”. Journal of Chemical Education. USA: ACS Publications. 68 (11): 939. doi:10.1021/ed068p939.1. Приступљено 12. 10. 2011.
- ^ а б в г NIOSH Џепни водич хемијских хазарда 0077
- ^ Уллманн’с Енцyцлопедиа оф Индустриал Цхемистрy. Wеинхеим: Wилеy-ВЦХ. 2005.


