Хемиосмоза
Хемиосмоза је кретање јона кроз полупропусну мембрану, низ њен електрохемијски градијент. Пример тога је формирање аденозин трифосфата (АТП) кретањем водоничних јона кроз мембрану током ћелијске респирације или фотосинтезе.
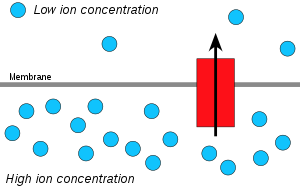
Водонични јони, или протони, дифузијом се померају из области високе протонске концентрације у област ниске протонске концентрације, и електрохемијски концентрациони градијент протона кроз мембрану се може користити за формирање АТП молекула. Овај процес је сродан са осмозом, дифузијом воде кроз мембрану, и стога се назива „хемиосмозом”.
АТП синтаза је ензим који формира АТП путем хемиосмозе. Он омогућава протонима да прођу кроз мембрану и користи слободну енергију разлике за фосфорилацију аденозин дифосфата (АДП), чиме се формира АТП. Генерисање АТП путем хемиосмозе се јавља у митохондријама и хлоропластима, као и у већини бактерија и археја, ланац електронског транспорта пумпа јоне у тилакоидне просторе кроз тилакоидне мембране.
Хемиосмотска теорија[уреди | уреди извор]
Питер Мичел је предложио хемиосмотску хипотезу 1961. године.[1] Та теорија есенцијално постулира да се већински део аденозин трифосфата (АТП) који се синтетише при ћелијском дисању настаје услед електрохемијског градијента кроз унутрашње мембране митохондрија користећи енергију НАДХ и ФАДХ2 формираних разлагањем енергетски богатих молекула, као што је глукоза.
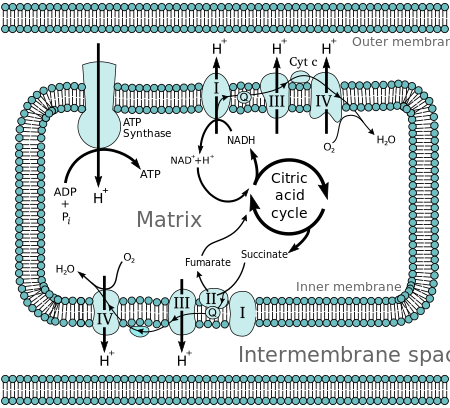
Молекули као што је глукоза бивају метаболизовани ради продукције ацетил КоА као енергетски богатог интермедијера. Оксидација ацетил коензима А (ацетил-КоА) у митохондријском матриксу је спрегнута са редукцијом преносних молекула као што су никотинамид аденин динуклеотид (НАД) и флавин аденин динуклеотид (ФАД).[2] Преносници достављају електроне у ланац транспорта електрона (ЕТЦ) у унутрашњој митохондријској мембрани, и они затим бивају пренети на друге протеине ланца. Доступна енергија електрона се користи за пумпање протона из матрикса кроз строму, чиме се чува енергија у виду трансмембранског елецтрохемијског градијента. Протони се враћају кроз унутрашњу мембрану кроз ензим АТП синтаза. Проток протона назад у митохондријски матрикс кроз АТП синтазу пружа довољно енергије да се АДП комбинује са неорганским фосфатом и да се формира АТП. Електроне и протоне у задњој пумпи ланца преузима кисеоник и формира се вода.
То је својевремено био радикалан предлог, и није био добро призваћен. Превалентно гледиште је било да је енергија електронског трансфера ускладиштена као стабилни интермедијер високог потенцијала, што је хемијски конзервативнији концепт. Проблем с том старијом парадигмом је да високо енергетски интермедијер никад није био пронађен, и евиденција за пумпање протона путем комплекса ланца електронског трансфера је постала сувише велика да би се игнорисала. На крају је тежина доказа почела да фаворизује хемиосмотску хипотезу, и 1978. године, Питер Мичел је награђен Нобеловом наградом за хемију.[3]
Хемиосмотско спрезање је важно за АТП продукцију у митохондријама, хлоропластима[4] и многим бактеријама и архејама.[5]
Референце[уреди | уреди извор]
- ^ Митцхелл, Петер (1961). „Цоуплинг оф пхоспхорyлатион то елецтрон анд хyдроген трансфер бy а цхеми-осмотиц тyпе оф мецханисм”. Натуре. 191 (4784): 144–148. Бибцоде:1961Натур.191..144М. ПМИД 13771349. дои:10.1038/191144а0.
- ^ Албертс, Бруце; Јохнсон, Алеxандер; Јулиан Леwис; Рафф, Мартин; Кеитх Робертс; Wалтер, Петер (2002). „Протон Градиентс Продуце Мост оф тхе Целл'с АТП”. Молецулар Биологy оф тхе Целл. Гарланд. ISBN 978-0-8153-4072-0.
- ^ The Nobel Prize Архивирано на сајту Wayback Machine (4. децембар 2008) ин Цхемистрy 1978.
- ^ Цоопер, Геоффреy M. (2000). „Фигуре 10.22: Елецтрон транспорт анд АТП сyнтхесис дуринг пхотосyнтхесис”. Тхе Целл: А Молецулар Аппроацх (2нд изд.). Синауер Ассоциатес, Инц. ISBN 978-0-87893-119-4.
- ^ Албертс, Бруце; Јохнсон, Алеxандер; Јулиан Леwис; Рафф, Мартин; Кеитх Робертс; Wалтер, Петер (2002). „Фигуре 14-32: Тхе импортанце оф Х+-дривен транспорт ин бацтериа”. Молецулар Биологy оф тхе Целл. Гарланд. ISBN 978-0-8153-4072-0.
Литература[уреди | уреди извор]
- Албертс, Бруце; Јохнсон, Алеxандер; Јулиан Леwис; Рафф, Мартин; Кеитх Робертс; Wалтер, Петер (2002). „Протон Градиентс Продуце Мост оф тхе Целл'с АТП”. Молецулар Биологy оф тхе Целл. Гарланд. ISBN 978-0-8153-4072-0.
- Биоцхемистрy теxтбоок референце, фром тхе НЦБИ бооксхелф – Јеремy M. Берг; Јохн L. Тyмоцзко; Луберт Стрyер (ур.). „18.4. А Протон Градиент Поwерс тхе Сyнтхесис оф АТП”. Биоцхемистрy (5тх изд.). W. Х. Фрееман.
- Тецхницал референце релатинг оне сет оф еxпериментс аиминг то тест соме тенетс оф тхе цхемиосмотиц тхеорy – Сеији Огаwа & Тсо Минг Лее (1984). „Тхе Релатион бетwеен тхе Интернал Пхоспхорyлатион Потентиал анд тхе Протон Мотиве Форце ин Митоцхондриа дуринг АТП Сyнтхесис анд Хyдролyсис”. Јоурнал оф Биологицал Цхемистрy. 259 (16): 10004–10011. ПМИД 6469951.

