Trovanje morskim plodovima
| Trovanje morskim plodovima | |
|---|---|
 | |
| Morski plodovi, iako primarno uključuje ribe i školjke, su bilo koji oblik morskog života koji ljudi smatraju hranom. | |
| Specijalnosti | urgentna medicina, toksikologija |
Trovanje morskim plodovima, trovanje morskom hranom ili bolest koja se prenosi morskim plodovima nastaje kao rezultat ljudske konzumacije hrane iz mora. Ovo trovanje uključuje, ali nije ograničeno samo na ribu i školjke, već i na druge plodove mora. Oboleleli sa bolestima koje se prenose morskim plodovima često su dijagnostički izazov, jer mogu imati različite znakove i simptome, različiti stepene ozbiljnosti trovanja, kao i nejasne vremenske okvire u vezi sa ingestijom.[1]
Obim bolesti koje se prenose morskim plodovima je ogroman, a sa povećanim putovanjima i širenjem trgovine morskom hranom, povećava se verovatnoća da će se zdravstveni radnici susresti sve više sa bolestima koju prenosi morska hrana.[1][2][3]
Godišnji izveštaj Nacionalne agencije za trovanje Američkog udruženja i centara za kontrolu trovanja u 2019. godini dokumentovao je 808 pojedinačnih izloženosti ihtiosarkotoksinima (ciguatera trovanje koje nastaje nakon konzumacije toksina koji se mogu naći u jestivim ribama sa područja koralnih grebena tropskih mora, trovanje paralitičkim školjkama, skombroidnim i drugim vrstama riba, i drugih trovanja morskim plodovima), pri čemu se u izveštaju na navode smrtni slučajevi.[4]
Ciguatera[uredi | uredi izvor]

Ciguatera je klinički sindrom uzrokovan jedenjem mesa otrovne ribe ulovljene u oblisti tropskih koralnih grebena i oko ostrva u tropskim morima. Veruje se da toksin potiče od mikroskopske dinoflagelatne alge Gambierdiscus toxicus koji raste na grebenima[5]. Međutim, umešane su i druge bentoske alge. Ribe koje jedu alge postaju toksične, a efekat se povećava kroz lanac ishrane tako da velike ribe grabljivice postaju najotrovnije. Pojava toksičnih riba ima tendenciju da bude lokalizovana, ali lokalizacija nije konzistentna i toksična riba se može sporadično pojaviti bilo gde na grebenu ili bilo kojoj lokaciji oko ostrva.[6] Više od 400 vrsta je umešano u trovanje ciguaterom,[7] ali najčešće umešane ribe uključuju amberjack, snapper, grouper, škarpinu, barakudu, kozu i grebensku ribu koja pripada poorodici Carrangidae.
U Sjedinjenim Američkim Državama, ciguatera se uglavnom javlja na Havajima, Portoriku, Devičanskim ostrvima, Guamu i Floridi.[8] Posebno visoka incidenca prijavljena je sa Guama,[9] a nekoliko slučajeva je prijavljeno je i u drugim državama uzrokovanih ribom dopremljenom sa Floride. Slučajevi su često povezani sa putovanjem u endemska područja ciguatere kao što su Havaji i Devičanska ostrva, a postoji zabrinutost da lekari u kontinentalnom delu SAD nisu u stanju da uvek prepoznaju mnoge slučajeve.
Bolest pogađa istovremeno gastrointestinalni i neurološki sistem.[10][11]
- Simptomi od strane gastrointestinalni simptomi, uključujući dijareju, mučninu, povraćanje i bol u stomaku, pojavljuju se 3-5 sati nakon uzimanja ribe i kratko traju.
- Neurološki simptomi počinju 12-18 sati nakon konzumiranja i mogu biti umereni do teški; obično traju 1-82 dana, ali mogu da traju i nekoliko meseci. U retkim slučajevima, simptomi mogu da traju godinama, sa egzacerbacijom povezanim sa konzumiranjem ribe ili eventualno alkohola.[12]
- Simptomi obično uključuju inverziju toplo-hladno (vruća kafa ima hladan ukus, sladoled vruć); bolovi u mišićima; peckanje i utrnulost usana, jezika i perioralne regije; metalni ukus; suvoća usta; anksioznost; prostration; vrtoglavica; jeza; znojenje; proširene oči, zamagljen vid, i privremeno slepilo.
- U retkim ekstremnih slučajeva može doći do paralize i smrti.
- Simptomi mogu biti izuzetno iscrpljujući, što rezultira produženim periodima invaliditeta.
Intravenski manitol može ublažiti akutne simptome,[13] pod uslovom da se da u roku od nekoliko sati od konzumacije, sa amitriptilinom,[14] ili tokainidom,[15] kod hronične manifestacije.
Utvrđena je značajna individualnost u odgovoru pacijenata,[16] posebno onih sa hroničnim manifestacijama.[16]
Paralitičko trovanje školjkama[uredi | uredi izvor]


Paralitičko trovanje školjkama (akronim PSP - eng. Paralytic shellfish poisoning) se dešava širom sveta, ali je najčešće u umerenim vodama, posebno na obalama Pacifika i Atlantika Severne Amerike, uključujući Aljasku. Slučajevi su takođe prijavljeni i u zemaljama kao što su Filipini, Kina, Čile, Škotska, Irska, Novi Zeland i Australija.[17] [18][19] Paralitičko trovanje školjkama nije samo najčešći oblik trovanja školjkama, već je i najsmrtonosniji, sa stopom smrtnosti od 6% širom sveta (smrtnost je veća u zemljama u razvoju).[20][21]
Uzročnik je saksitoksin, koji proizvode dinoflagelati (mikroalge) koje unose školjke (npr ostrige, dagnje, školjke) koje se hrane filtratom (npr. ostrige, dagnje, školjke) koje koncentrišu toksin i potom ih konzumiraju grabežljivci, uključujući i ljude.
Saksitoksin je jedan od najjačih poznatih neurotoksina. Procenjuje se da 0,5-1 mg može biti fatalno za ljude.[22][23] Deluje slično kao TTKS po tome što blokira natrijumove kanale osetljive na napon, što, zauzvrat, remeti nervnu provodljivost i rezultuje motoričkim i senzornim neurološkim abnormalnostima.
Paralitičko trovanje školjkama se obično javlja u epidemijama i najčešće se primećuje kod rekreativnih sakupljača školjki.[24]
Simptomi se javljaju u roku od 15 minuta do 3 sata i uključuju parestezije usta, lica i udova sa mučninom, povraćanjem i dijarejom. Često se opisuje osećaj plutanja. Disfonija, ataksija, slabost i paraliza skeletnih mišića (koje dovode do respiratorne insuficijencije) mogu se javiti u roku od 2-12 sati kod teškog trovanja i mogu trajati do 72 časa do nedelju dana. Smrt od paralitičkog trovanje školjkama nastaje kao posledica paralize mišića disanja.[25]
Osnova lečenja paralitičkog trovanja školjkama je pomoćna nega slična onoj kod trovanja ribom puhačem (trovanje TTKS). Mehanička ventilacija je indikovana u slučaju nedovoljne respiratorne funkcije.[25]
Neurotoksično trovanje školjkama[uredi | uredi izvor]



Neurotoksično trovanje školjkama (akronim NSP od eng.Neurotoxic shellfish poisoning) prijavljeno je sa:
- jugoistočne obale Sjedinjenih Američkih Država,
- obale Meksičkog zaliva,
- obala Kariba,
- obala Novog Zelanda.
Neurotoksično trovanje školjkama izazivaju brevetoksini, koje proizvode dinoflagelati (mikroalge) koje unose školjke (npr ostrige, dagnje, školjke) u kojima se koncentrišu toksin koje kasnije konzumiraju grabežljivci, uključujući i ljude.
Prijavljene su respiratorne tegobe i iritacija oka zbog izlaganja aerosolima talasa dok se razbijaju u blizini plaže.[traži se izvor] Ovaj sindrom je sličan trovanju ciguaterom, ali bez paralitičke komponente, i može trajati od nekoliko sati do nekoliko dana.
Kao i mnogi morski toksini, brevetoksini su bez ukusa, mirisa i toplotno stabilni. Oni su slični ciguatoksinima po tome što su otvarači natrijumovih kanala koji izazivaju neuroekscitatorne efekte.
Iako se brevetoksini mogu akumulirati u mišićima i iznutricama riba, ne postoje dokumentovani slučajevi neurotoksično trovanje školjkama nakon konzumiranja riba kod ljudi, tako da se NSP i CFP mogu međusobno razlikovati sa kompletnom istorijom konzumiranja morskih plodova.[26]
Bolest koja se javlja kod neurotoksično trovanje školjkamaje je blaža forma od od one kod paralitičkog trovanja školjkama.
Početak simptoma kreće se od 15 minuta do 18 sati nakon uzimanja, a trajanje toksičnosti kreće se od 1-72 časa (obično < 24 časa). Simptomi koji se manifestuju uključuju:
- gastroenteritis;
- rektalno žarenje;
- parestezije lica, trupa i udova;
- mijalgije;
- ataksiju;
- vrtoglavicz;
- smenjivanje osećaja toplog i hladnog.
- druge manje uobičajene karakteristike (tremor, disfagiju, bradikardiju, smanjene reflekse i midrijazu)
Lečenje je simptomatsko.
Trovanja školjkama sa dijarejom[uredi | uredi izvor]
Većina slučajeva trovanja školjkama sa dijarejom (akronim DSP od eng. Diarrheal shellfish poisoning) je rezultat jedenja toksičnih školjkaša kao što su školjke i kapice. Ova vrsta trovanja je prijavljene u Evropi, Aziji, Severnoj Americi, Južnoj Africi, Australiji i Novom Zelandu.[27]
Trovanja školjkama sa dijarejom je blago trovanje. Čini se da je glavni uzročnik okadaična kiselina (iako su umešani i drugi), koju proizvode dinoflagelati (mikroalge) koje unose školjke koje se hrane filtratom (npr ostrige, dagnje, školjke) koje koncentrišu toksin i potom se konzumiraju.
Simptomi su uglavnom blagi i sastoje se od mučnine, povraćanja, dijareje i bolova u stomaku. Vreme do početka od konzumiranja školjki je u roku od 30 minuta do nekoliko sati, a potpuni oporavak u roku od 3 dana.
Lečenje je simptomatsko i podržavajuće. Nisu prijavljeni slučajevi smrti kod trovanja školjkama sa dijarejom.
Azaspiracidi u školjkama[uredi | uredi izvor]
Azaspiracidi (AZA) su grupa visoko toksičnih otrova koji se nalaze u školjkama .i proizvodima od školjki.[28] Oni pripadaju strukturi policikličnih etara.
Prvi slučaj trovanja azaspiracidom otkriven je u Holandiji 1995. godine, tako da ova vrsta trovanja spada u jedno je od nedavno otkrivenih trovanja morskim plodovima. Trovanje je identifikovano kod nekioliko slučajeva teške gastrointestinalne bolesti usled konzumiranja kontaminiranih dagnji iz Irske. Kontaminacija je naknadno potvrđena širom zapadne obale Evrope. Poznato je da azaspiracidi izazivaju trovanja širom sveta, a na Dalekom istoku, između ostalih, dagnje se prvo nude domaćim životinjama kako bi se utvrdila njihova potencijalna toksičnost.
Mešavima toksina, azaspiracida, akumuliraju se u školjkašima koje se hrane toksičnim mikroalgama. Toksikološke studije su pokazale da azaspiracidi mogu izazvati široko rasprostranjeno oštećenje organa kod miševa i da su verovatno opasniji od prethodno poznatih klasa toksina školjki.[29][30]
Struktura azaspiracida-1 (AZA1) je prvi put prijavljena 1998. godine kada je uspešno izolovan iz dagnji (Mytilus edulis). Strukture koje pripadaju azaspiracidima do sada su identifikovane u više od 30 jedinjenja.
Amnezičko trovanje školjkama (trovanje domoičnom kiselinom)[uredi | uredi izvor]
Amnezičko trovanje školjkama (akronim ASP od eng. Amnesic shellfish poisoning ) je potencijalno ozbiljno trovanje koje je prijavljeno iz Kanade, Škotske, Irske, Francuske, Belgije, Španije, Portugala, Novog Zelanda, Australije i Čilea. Otrovne školjke, kapice, školjke i rakovi bili su odgovorni za te epidemije.[31]
Dijatomeje proizvode domoinsku kiseline (DA), koja ulazi u lanac ishrane preko kontaminiranih mekušaca. DA je glutamatni agonist, i, dok simptomi ASP uključuju mučninu, povraćanje, dijareju, ono što ga razlikuje od drugih trovanja školjkama je njegovo duboko dejstvo na centralni nervni sistem.[32]
Na severozapadu Pacifika, u zalivu Chesapeake Bay i duž obala zapadne Evrope i istočne Azije, vršni godišnji nivoi DA u školjkama mogu premašiti regulatornu granicu, što dovodi do povremenih ograničenja za žetvu školjki.[33]
Prvo prijavljeno izbijanje ASP kod ljudi dogodilo se 1987. godine u kanadskoj istočnoj provinciji Ostrvo Princa Edvarda i pogodilo je više od 100 ljudi. Približno 50% pacijenata imalo je jaku glavobolju; neki su pretrpeli konfuziju, napade i komu. Dvadeset pet odsto pacijenata imalo je kratkoročni gubitak pamćenja, koji je za mnoge postao trajan. Od više od 100 obolelih, 4 pacijenta su umrla.[34]
Lečenje je suportivna nega, uz preporučeno neurološko praćenje.
Trovanje naduvanom ribom[uredi | uredi izvor]

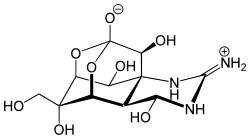
Trovanje naduvanom ribom, naduvačom ili četvorozubke (lat. Tetraodontidae) iz porodica morskih i priobalnih riba reda, nastaje kao rezultat gutanja mesa određenih vrsta riba iz ovog roda.[12] Toksin odgovoran za trovanje je tetrodotoksin i prvobitno se verovalo da je pravi ihtiosarkotoksin koji proizvodi sama riba. Toksičnost otrovnih naduvanih riba uveliko varira.[35] Nedavna zapažanja da je uzgojena naduvena riba atoksična ukazuje na to da je poreklo toksina iz lanca ishrane a ne iz organizma ribe, ali to još nije sasvim potvrđeno.[36] Međutim, nedavno je pokazano da određeni uobičajeni morski vibrioni mogu proizvesti ovaj oblik toksina,[37] a pošto se vibrioni javljaju kao deo mikroflore naduvane ribe, mogu biti umešani u razvoj njene toksičnosti.[38]
Trovanje naduvanom ribom nije prijavljeno u kontinentalnom delu Sjedinjenih Američkih Država poslednjih godina, ali su incidenti prijavljeni u prošlosti. Na Floridi je prijavljeno sedam slučajeva između 1951. i 1974. godine, uključujući i tri smrtna slučaja.[39] Izgleda da su ova trovanja uzrokovana konzumiranjem lokalno ulovljenih vrsta lat. Sphoeroides.
Obična naduvana riba, lat. Arothron hispidus, umešana je u najmanje sedam smrtnih slučajeva na Havajima.[40]
Svake godine u Japanu ima 20-100 smrtnih slučajeva od trovanja naduvanom ribom, u mestima gde se razne vrste naduvene ribe jedu kao poslastica; ovo se dešava uprkos veoma strogim kontrolama koje su japanske vlasti nametnule na marketing i pripremu jela u restoranima.[41]
Simptomi trovanja naduvanom ribom su slični onima opisanim za paralitičko trovanje školjkama, uključujući:
- mučninu i povraćanje koji su uobičajeni rani simptomi,
- početno peckanje i utrnulost usana, jezika i prstiju
- paralize ekstremiteta;
- ataksija;
- teškoće u govoru;
- smrt usled gušenja izazvanog respiratornom paralizom.
Sličnost simptoma nije iznenađujuća jer tetrodotoksin, iako se hemijski razlikuje od saksitoksina, takođe blokira natrijumove kanale. Nije identifikovan antidot za tetrodotoksin i lečenje je podržavajuće. Toksičnost tetrodotoksina je slična onoj kod saksitoksina, a 1-4 mg predstavlja smrtonosnu dozu za ljude.
Postoji neslaganje oko toksičnosti američke atlantske naduvane ribe. Nedavno Nacionalna administracija za okeane i atmosferu,[42] opisuje severnu naduvanu ribu (lat. Sphoeroides maculatuss) kao netoksičnu i napominje da je riba prodavana duž atlantske obale kao „morska riba“ tokom Drugog svetskog rata. Međutim,[39] Hemmert, C.D. je u dokazao da su iznutrice, koža i nešto mesa lat. S. maculatus uhvaćene u Atlantiku bili toksični,[43][44][45] su takođe izvestili da je S. maculatus toksičan. Sa Zapadne obale SAD, su dva istraživača izvestila,[46] da je pacifička vrsta lat. S. annulatus često toksična, dok je vrsta lat. Arothron hispidus odgovorna za najmanje sedam smrtnih slučajeva na Havajima.

Veleprodaja, priprema i prodaja naduvane ribe kao hrane u Japanu je pod najstrožim uslovima za javno zdravlje, i može da bude pripremana samo od strane obučenih i sertifikovanih kuvara za naduvanu ribu. Međutim i pored toga nije sasvim eliminisala opasnost od jedenja ove ribe, pa tako je naduvana riba i dalje glavni uzrok smrtonosne intoksikacije hranom u Japanu. Ukratko, jedenje otrovnih pufera je u najboljem slučaju igra ruskog ruleta.
Sve američke naduvane ribe mogu biti potencijalno toksične. Kako postoji previše varijabli u poslovanju sa naduvanom ribom, njihova prodaja bi trebalo da bude zabranjena u Sjedinjenim Američkim Državama. Ovu temu je dokumentovao i opširno raspravljao Halstead, B.W..[12][35]
Imajući u vidu ove izveštaje, činilo bi se mudrim isključiti naduvanu ribu, bilo domaću ili uvezenu, iz komercijalnih kanala u SAD barem dok se ne izvrši odgovarajuća procena stepena rizika koji oni mogu predstavljati. FDA je nedavno odobrila uvoz japanske naduvene ribe za potrebe restorane u Sjedinjenim Američkim Državama. Iako su nametnuti veoma strogi zahtevi u pokušaju da se osigura da riba nije toksična, kontinuirano japansko iskustvo bi trebalo da pokrene pitanja u vezi sa bezbednošću ovog procesa u američkoj javnosti.[47]
Drugi toksini[uredi | uredi izvor]
Postoje sporadični izveštaji o drugim intoksikacijama morskim plodovima s vremena na vreme,[48][49] ali oni nisu dovoljno istraženi da bi se identifikovao toksični agensa. Kao što je ranije navedeno, donekle promenljivi simptomi definisani kao ciguatera i prijavljena povezanost polietarskih supstanci i palitoksina,[50][51] kod riba umešanih u takve slučajeve postavljaju pitanja o toksičnosti povezanih sa grebenskim ribama.
Jedan dobro definisan sindrom koji se javlja na Havajima je „halucinogeno trovanje ribom“. Ova bolest prati konzumaciju cipala i većeg broja grebenskih riba i javlja se sezonski, obično tokom letnjih meseci. Halucinacije, nesanica, intenzivno sanjanje, slabost i peckanje u grlu su uobičajeni ubrzo nakon jedenja ribe.[52] Prijavljene su zastrašujuće noćne more i javljaju se konstriktivni bolovi u grudima. Stanje je kratkotrajno i rešava se samo od sebe.[48]. Čini se da ne postoji nikakav analitički test za ovaj toksin.
Vidi još[uredi | uredi izvor]
Izvori[uredi | uredi izvor]
- ^ a b Prester L. Seafood Allergy, Toxicity, and Intolerance: A Review. J Am Coll Nutr. 2015 Aug 7. 1-13. [Medline].
- ^ Vandermeersch G, Lourenço HM, Alvarez-Muñoz D, Cunha S, Diogène J, Cano-Sancho G, et al. Environmental contaminants of emerging concern in seafood - European database on contaminant levels. Environ Res. 2015 Nov. 143 (Pt B):29-45. [Medline].
- ^ Cano-Sancho G, Sioen I, Vandermeersch G, Jacobs S, Robbens J, Nadal M, et al. Integrated risk index for seafood contaminants (IRISC): Pilot study in five European countries. Environ Res. 2015 Nov. 143 (Pt B):109-15. [Medline].
- ^ Gummin DD, Mowry JB, Beuhler MC, Spyker DA, Brooks DE, Dibert KW, et al. 2019 Annual Report of the American Association of Poison Control Centers' National Poison Data System (NPDS): 37th Annual Report. Clin Toxicol (Phila). 2020 Dec. 58 (12):1360-1541.
- ^ Bagnis, R., S. Chanteau, E. Chungue, J.M. Hurtel, T. Yasumoto, and A. Inoue. 1980. Origins of ciguatera fish poisoning: A new dinoflagellate Gambierdiscus toxicus Adachi and Fukuyo, definitely involved as a causal agent. Toxicon 18:199-208. [PubMed]
- ^ Engleberg, N.C., J.G. Morris, Jr., J. Lewis, J.P. McMillan, R.A. Pollard, and P.A. Blake. 1983. Ciguatera fish poisoning: A major common source outbreak in the U.S. Virgin Islands. Ann. Intern. Med. 98:336-337.
- ^ Randall, J.E. 1980. A survey of ciguatera at Eniwetok and Bikini Marshall Islands, with notes on the systematics and food habits of ciguatoxic fish. Fish Bull. 78:201-249.
- ^ CDC (Centers for Disease Control). 1989. Annual Summary of Foodborne Disease, unpublished dates from 1983 to 1986. U.S. Department of Health and Human Services, Atlanta, Ga. 1989.
- ^ Haddock, R.L. 1989. Letter report on food-borne disease incidence, dated September 8, 1989, from Dr. Robert L. Haddock, Territorial Epidemiologist, Department of Public Health and Social Services, Government of Guam to Dr. Farid E. Ahmed, Project Director, Committee on Evaluation of the Safety of Fishery Products, Institute of Medicine, National Academy of Sciences, Washington, D.C.
- ^ Bagnis, R., T. Kuberski, and S. Laugier. 1979. Clinical observations on 3009 cases of ciguatera (fish poisoning) in the South Pacific. Am. J. Trop. Med. Hyg. 28:1067-1073. [PubMed]
- ^ Morris, J.G., Jr., P. Lewin, N.T. Hargrett, C.W. Smith, P.A. Blake, and R. Schneider. 1982. a. Clinical features of ciguatera fish poisoning: A study of the disease in the U.S. Virgin Islands. Arch. Intern. Med. 142:1090-1092.
- ^ a b v Halstead, B.W. 1967. Poisonous and Venomous Marine Animals of the World, Vol. I, pp. 83-87 ; Vol. II, pp. 679-844. U.S. Government Printing Office, Washington, D.C.
- ^ Palafox, N.A., L.G. Jain, A.Z. Pinano, T.M. Gulick, R.K. Williams, and I.J. Schatz. 1988. Successful treatment of ciguatera fish poisoning with intravenous mannitol. J. Am. Med. Assoc. 259:2740-2742. [PubMed]
- ^ Bowman, P.B. 1984. Amitriptyline and ciguatera. Med. J. Australia 140:802. [PubMed]
- ^ Lange, W.R., S.D. Kreider, M. Hattwick, and J. Hobbs. 1988. Potential benefit of tocainide in the treatment of ciguatera: Report of three cases. Am. J. Med. 84:1087-1088. [PubMed]
- ^ a b Engleberg, N.C., J.G. Morris, Jr., J. Lewis, J.P. McMillan, R.A. Pollard, and P.A. Blake. 1983. Ciguatera fish poisoning: A major common source outbreak in the U.S. Virgin Islands. Ann. Intern. Med. 98:336-337. [PubMed]
- ^ Taylor, F. J. R.; Fukuyo, Y.; Larsen, J.; Hallegraeff, G. M. (2003). "Taxonomy of harmful dinoflagellates". In Hallegraeff, G.M.; Anderson, D.M.; Cembella, A.D. (eds.). Manual on Harmful Marine Microalgae. ISBN 92-3-103948-2. str. 389–432..
- ^ Cembella, A. D. (1998). "Ecophysiology and Metabolism of Paralytic Shellfish Toxins in Marine Microalgae". In Anderson, D. M.; Cembella, A. D.; Hallegraeff, G. M. (eds.). Physiological Ecology of Harmful Algal Blooms. NATO ASI. Berlin: Springer. ISBN 978-3-662-03584-9. str. 381–403..
- ^ Balech, Enrique (1985). „The genus Alexandrium or Gonyaulax of the Tamarensis Group”. Ur.: Anderson, Donald M.; White, Alan W.; Baden, Daniel G. Toxic Dinoflagellates. New York: Elsevier. str. 33—8. ISBN 978-0-444-01030-8..
- ^ Lehane L. Paralytic shellfish poisoning: a potential public health problem. Med J Aust. 2001 Jul 2. 175(1):29-31. [Medline].
- ^ Isbister GK, Kiernan MC. Neurotoxic marine poisoning. Lancet Neurol. 2005 Apr. 4(4):219-28.
- ^ Clark RF, Williams SR, Nordt SP, Manoguerra AS. A review of selected seafood poisonings. Undersea Hyperb Med. 1999. 26(3):175-84. [Medline].
- ^ James KJ, Carey B, O'Halloran J, van Pelt FN, Skrabáková Z. Shellfish toxicity: human health implications of marine algal toxins. Epidemiol Infect. 2010 Jul. 138(7):927-40. [Medline].
- ^ CDC. Paralytic shellfish poisoning --- southeast Alaska, May--June 2011. MMWR Morb Mortal Wkly Rep. 2011 Nov 18. 60(45):1554-6. [Medline].
- ^ a b Jeremy Sobel, John Painter. Illnesses Caused by Marine Toxins. Clinical Infectious Diseases. 1 Nov 2005. Volume 41, issue 9:1290-1296. [Full Text].
- ^ Friedman MA, Fernandez M, Backer LC, et al. An Updated Review of Ciguatera Fish Poisoning: Clinical, Epidemiological, Environmental, and Public Health Management. Mar Drugs. 2017 Mar 14. 15 (3):[Medline].
- ^ Lee TC, Fong FL, Ho KC, Lee FW. The Mechanism of Diarrhetic Shellfish Poisoning Toxin Production in Prorocentrum spp.: Physiological and Molecular Perspectives. Toxins (Basel). 2016 Sep 22. 8 (10):[Medline]. [Full Text].
- ^ „SRPS EN 16204:2013”. iss.rs/sr. Pristupljeno 24. 11. 2021.
- ^ James KJ, Fidalgo Sáez MJ, Furey A, Lehane M. Azaspiracid poisoning, the food-borne illness associated with shellfish consumption. Food Addit Contam. 2004 Sep. 21(9):879-92.
- ^ Furey A, O'Doherty S, O'Callaghan K, Lehane M, James KJ. Azaspiracid poisoning (AZP) toxins in shellfish: toxicological and health considerations. Toxicon. 2010 Aug 15. 56(2):173-90. [Medline].
- ^ Ansdell, VE. Food Poisoning from Marine Toxins. Gary W. Brunette, Editor in Chief. CDC Yellow Book 2018: Health Information for International Travelers. New York: Oxford University Press; May 31, 2017. 77-80. [Full Text].
- ^ Isbister GK, Kiernan MC. Neurotoxic marine poisoning. Lancet Neurol. 2005 Apr. 4(4):219-28. [Medline].
- ^ Zuloaga DG, Lahvis GP, Mills B, Pearce HL, Turner J, Raber J. Fetal domoic acid exposure affects lateral amygdala neurons, diminishes social investigation and alters sensory-motor gating. Neurotoxicology. 2016 Mar. 53:132-140.
- ^ Perl TM, Bedard L, Kosatsky T, Hockin JC, Todd EC, Remis RS. An outbreak of toxic encephalopathy caused by eating mussels contaminated with domoic acid. N Engl J Med. 1990 Jun 21. 322(25):1775-80. [Medline].
- ^ a b Halstead, B.W. 1988. Poisonous and Venomous Marine Animals of the World, 2nd rev. ed. Darwin Press, Princeton, N.J. 1168 pp.
- ^ Mosher, H., and F.A. Fuhrman. 1984. Occurrence and origin of tetrodotoxin. Pp. 333-334 in E.P. Ragelis, editor. , ed. Seafood Toxins. American Chemical Society, Washington, D.C.
- ^ Narita, H., S. Matsubara, N. Miwa, S. Akahane, M. Murakami, T. Goto, M. Nara, T. Noguchi, T. Shida, and K. Hashimoto. 1987. Vibrio alginolyticus a TTX-producing bacterium isolated from the starfish Astropecten polyacanthus . Nippon Suisan Gakk. 53:617-621.
- ^ Sugita, H., J. Iwata, C. Miyajima, T. Kubo, T. Noguchi, K. Hashimoto, and Y. Deguchi. 1989. Changes in microflora of a puffer fish Fugu niphobles with different water temperatures. Marine Biology 101:299-304
- ^ a b Hemmert, C.D. 1974. Tetraodon (puffer fish) poisoning. Memorandum of Florida Department of Health, Tallahassee, Fla.
- ^ HDH (Hawaii Department of Health). 1988. Fish Poisoning in Hawaii. Advisory Leaflet. Honolulu, Hawaii.
- ^ Ogura, Y. 1971. Fugu (puffer fish) poisoning and the pharmacology of crystalline tetrodotoxin in poisoning. Pp. 139-159 in L.L. Simpson, editor. , ed. Neuropoisons, Vol. I. Plenum Press, New York.
- ^ NOAA (National Oceanic and Atmospheric Administration). 1988. Japan's "Fugu" (Puffer Fish) Market Advisory. Doc/NOAA/NMFS, Washington, D.C. 1 p.
- ^ Lalone, R.C., E.D. DeVillez, and E. Larson. 1963. An assay of the toxicity of the Atlantic puffer fish Sphoeroides maculatus . Toxicon 1:159-164.
- ^ Larson, E., L.R. Rivas, R.C. Lalone, and S. Coward. 1959. Toxicology of the Western Atlantic Puffer Fish of the Genus Sphoeroides . The Pharmacologists 1:70 (Abstract)
- ^ Larson, E., R.C. Lalone, and L. Rivas. 1960. Comparative toxicity of the Atlantic pufferfishes of the genera Sphoeroides, Lactophrys, Lagocelhalus and Chilomycterus . Fed. Proc. 19:388 (Abstract).
- ^ Goe, D.R., and B.R. Halstead. 1953. A preliminary report of the toxicity of the Gulf puffer, Sphoeroides annulatus. Calif. Fish and Game 39:229-232.
- ^ Halstead, B.W. 1988. Poisonous and Venomous Marine Animals of the World, 2nd rev. ed. Darwin Press, Princeton, N.J. 1168 pp.
- ^ a b Halstead, B.W. 1988. Poisonous and Venomous Marine Animals of the World, 2nd rev. ed. Darwin Press, Princeton, N.J. 1168 pp.
- ^ Wekell, J., and J. Liston. 1982. Pp. 111-155 in P. Newberne, editor. , ed. Seafood Biotoxicants in Trace Substances and Health: A Handbook Part II. Marcel Dekker, New York.
- ^ Hokama, Y., S.A.A. Honda, A.Y. Asahina, J.M.L. Fong, C.M. Matsumoto, and T.S. Gallacher. 1989. a. Cross-reactivity of ciguatoxin, okadaic acid, and polyethers with monoclonal antibodies. Food Agric. Immunol. 1:29-35
- ^ Kodama, A.M., Y. Hokama, T. Yasumoto, M. Fukui, S.J. Manea, and N. Sutherland. 1989. Clinical and laboratory findings implicating palytoxin as cause of ciguatera poisoning due to Decapterus macrosoma (mackerel). Toxicon 27:1051-1053. [PubMed]
- ^ Halstead, B.W., and E.J. Schantz. 1984. Paralytic shellfish poisoning. WHO Offset Publication No. 79:1-60. Geneva, Switzerland. [PubMed]
Literatura[uredi | uredi izvor]
- Chan TY. Ciguatera fish poisoning in East Asia and Southeast Asia. Mar Drugs. 2015 Jun 2;13(6):3466–78.
- Friedman MA, Fleming LE, Fernandez M et al. Ciguatera fish poisoning: treatment, prevention and management. Mar Drugs. 2008;6:456–79.
- Hungerford JM. Scombroid poisoning: a review. Toxicon. 2010 Aug 15;56(2):231–43.
- Isbister GK, Kiernan MC. Neurotoxic marine poisoning. Lancet Neurol. 2005 Apr;4(4):219–28.
- Palafox NA, Buenoconsejo-Lum LE. Ciguatera fish poisoning: review of clinical manifestations. J Toxicol Toxin Rev. 2001 May;20(2):141–60.
- Schnorf H, Taurarii M, Cundy T. Ciguatera fish poisoning: a double-blind randomized trial of mannitol therapy. Neurology. 2002 Mar 26;58(6):873–80.
- Sobel J, Painter J. Illnesses caused by marine toxins. Clin Infect Dis. 2005 Nov 1;41(9):1290–6.
Spoljašnje veze[uredi | uredi izvor]
- Vernon E. Ansdell Food Poisoning from Marine Toxins - wwwnc.cdc.gov
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
