Желудачноцревни рак — разлика између измена
мНема описа измене |
|||
| Ред 40: | Ред 40: | ||
== Опште информације == |
== Опште информације == |
||
Иако су разјашњене у многим аспектима, молекуларне и генетске основе развоја и прогресије гастроинтестиналног рак оне још увек нису у потпуности схваћене. Сада знамо да је гастроинтестинални рак узрокован различитим мутацијама које погађају одређене гене. Јединствени образац акумулираних мутација у људском геному формира специфичне молекуларне облике рака. Сходно томе, рак гастроинтестиналног тракта се данас не доживљава као једна болест, већ скуп болести са специфичним хетерогеним генетским профилима. Генетска основа рака је, без сумње, застрашујућа јер кодира молекуларне промене својствене мноштву есенцијалних ћелијских процеса. Молекуларни играчи који управљају пролиферацијом, апоптозом, диференцијацијом, ангиогенезом, ћелијском способношћу кретања, као и имуним одговором, сви могу бити циљани на специфичне карциноме који показују јединствене мутационе обрасце.<ref>Somarelli, J. A., Gardner, H., Cannataro, V. L., Gunady, E. F., Boddy, A. M., Johnson, N. A., et al. (2020). Molecular biology and evolution of cancer: from discovery to action. ''Mol. Biol. Evol''. 37, 320–326. doi |
Иако су разјашњене у многим аспектима, молекуларне и генетске основе развоја и прогресије гастроинтестиналног рак оне још увек нису у потпуности схваћене. Сада знамо да је гастроинтестинални рак узрокован различитим мутацијама које погађају одређене гене. Јединствени образац акумулираних мутација у људском геному формира специфичне молекуларне облике рака. Сходно томе, рак гастроинтестиналног тракта се данас не доживљава као једна болест, већ скуп болести са специфичним хетерогеним генетским профилима. Генетска основа рака је, без сумње, застрашујућа јер кодира молекуларне промене својствене мноштву есенцијалних ћелијских процеса. Молекуларни играчи који управљају пролиферацијом, апоптозом, диференцијацијом, ангиогенезом, ћелијском способношћу кретања, као и имуним одговором, сви могу бити циљани на специфичне карциноме који показују јединствене мутационе обрасце.<ref>Somarelli, J. A., Gardner, H., Cannataro, V. L., Gunady, E. F., Boddy, A. M., Johnson, N. A., et al. (2020). Molecular biology and evolution of cancer: from discovery to action. ''Mol. Biol. Evol''. 37, 320–326. {{doi|10.1093/molbev/msz242}}</ref> Штавише, неисправност многих сигналних путева је одговорна за иницијацију и еволуцију гастроинтестиналног рака. Колекција уочених генетских промена често се назива „пејзажи генома рака“.<ref>Vogelstein, B., Papadopoulos, N., Velculescu, V. E., Zhou, S., Diaz, L. A. Jr., and Kinzler, K. W. (2013). Cancer genome landscapes. ''Science'' 339, 1546–1558. {{doi|10.1126/science.1235122}}</ref> Наше знање о геномици рака се тренутно повећава скоро експоненцијално са крајњим циљем да се разуме његова биологија, побољшање дијагностичких и прогностичких алата и развој нових терапијских стратегија које се могу прилагодити потребама појединачних пацијената. Међутим, када се описују есенцијални ћелијски процеси укључени у рак, не смемо заборавити на процесе поправке ДНК чији су поремећени механизми такође веома често укључени у етиологију рака. |
||
== Епидемиологија == |
== Епидемиологија == |
||
| Ред 83: | Ред 83: | ||
=== Рак желуца === |
=== Рак желуца === |
||
[[Датотека:Adenocarcinoma, stomach, gross pathology IMG0037a lores.jpg|мини|Аденокарцином желуца]] |
[[Датотека:Adenocarcinoma, stomach, gross pathology IMG0037a lores.jpg|мини|Аденокарцином желуца]] |
||
[[Рак желуца]] четврти је најчешћи тип рака и други највећи узрок смрти од рака у свету.<ref name=":0" /> Источна Азија (Кина, Јапан, Кореја, Монголија) је подручје високог ризика за рак желуца, а Северна Америка, Аустралија, Нови Зеланд и западна и северна Африка су области са ниским ризиком.<ref>Bennett, C; Wang, Y; Pan, T (Oct 7, 2009). "Endoscopic mucosal resection for early gastric cancer". ''The Cochrane Database of Systematic Reviews'' (4): CD004276. doi |
[[Рак желуца]] четврти је најчешћи тип рака и други највећи узрок смрти од рака у свету.<ref name=":0" /> Источна Азија (Кина, Јапан, Кореја, Монголија) је подручје високог ризика за рак желуца, а Северна Америка, Аустралија, Нови Зеланд и западна и северна Африка су области са ниским ризиком.<ref>Bennett, C; Wang, Y; Pan, T (Oct 7, 2009). "Endoscopic mucosal resection for early gastric cancer". ''The Cochrane Database of Systematic Reviews'' (4): CD004276. {{doi|10.1002/14651858.CD004276.pub3}}. PMC 7199372. <nowiki>PMID 19821324</nowiki>.</ref> Најчешћи тип рака желуца је аденокарцином, који узрокује око 750.000 смртних случајева сваке године.<ref name=":2">O'Connor, A; McNamara, D; O'Moráin, CA (Sep 23, 2013). "Surveillance of gastric intestinal metaplasia for the prevention of gastric cancer". ''The Cochrane Database of Systematic Reviews''. '''9''' (9): CD009322.</ref> |
||
Важни фактори који могу допринети развоју рака желуца су исхрана, пушење и конзумирање алкохола, генетска предиспозиција (укључујући низ наследних синдрома) и инфекције (на пример, ''[[Helicobacter pylori]]'' и ''[[Epštajn-Barov virus|Епштајн-Бар вирус]]'') и пернициозна анемија.<ref name=":0" /><ref name=":2" /> Иако хемотерапија побољшава преживљавање у поређењу са најбољом супортивном негом, оптимални режим је нејасан.<ref>Wagner, Anna Dorothea; Syn, Nicholas LX; Moehler, Markus; Grothe, Wilfried; Yong, Wei Peng; Tai, Bee-Choo; Ho, Jingshan; Unverzagt, Susanne (2017-08-29). "Cochrane Database of Systematic Reviews" (PDF). ''Cochrane Database of Systematic Reviews''. '''8''': CD004064. doi |
Важни фактори који могу допринети развоју рака желуца су исхрана, пушење и конзумирање алкохола, генетска предиспозиција (укључујући низ наследних синдрома) и инфекције (на пример, ''[[Helicobacter pylori]]'' и ''[[Epštajn-Barov virus|Епштајн-Бар вирус]]'') и пернициозна анемија.<ref name=":0" /><ref name=":2" /> Иако хемотерапија побољшава преживљавање у поређењу са најбољом супортивном негом, оптимални режим је нејасан.<ref>Wagner, Anna Dorothea; Syn, Nicholas LX; Moehler, Markus; Grothe, Wilfried; Yong, Wei Peng; Tai, Bee-Choo; Ho, Jingshan; Unverzagt, Susanne (2017-08-29). "Cochrane Database of Systematic Reviews" (PDF). ''Cochrane Database of Systematic Reviews''. '''8''': CD004064. {{doi|10.1002/14651858.cd004064.pub4}}. PMC 6483552. <nowiki>PMID 28850174</nowiki>.</ref> |
||
=== Рак танког црева === |
=== Рак танког црева === |
||
=== Рак дебелог црева === |
=== Рак дебелог црева === |
||
[[Датотека:Blausen 0246 ColorectalCancer.png|мини|Рак дебелог црева и ректума]] |
[[Датотека:Blausen 0246 ColorectalCancer.png|мини|Рак дебелог црева и ректума]] |
||
{{види још|Рак дебелог црева}} |
{{види још|Рак дебелог црева}} |
||
Рак дебелог црева је један од најчешћих карцинома савременог човека,са инциденцијом која је висока у у Европи и свету. У Србији се годишње региструје више од 4.500 нових случајева рака дебелог црева, а годишње од њега умре око 3.000 људи. Рак дебелог црева је први или други на листи малигних тумора дигестивног тракта, у зависности од географског окружења.<ref>Bibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (jun 2016). „Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA. 315 (23): 2564—2575. PMID 27304597. doi |
Рак дебелог црева је један од најчешћих карцинома савременог човека,са инциденцијом која је висока у у Европи и свету. У Србији се годишње региструје више од 4.500 нових случајева рака дебелог црева, а годишње од њега умре око 3.000 људи. Рак дебелог црева је први или други на листи малигних тумора дигестивног тракта, у зависности од географског окружења.<ref>Bibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (jun 2016). „Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA. 315 (23): 2564—2575. PMID 27304597. {{doi|10.1001/jama.2016.5989}}.</ref> |
||
Тачан узрок рака дебелог црева није у потпуности познат. За сада знамо да настаје као последица утицаја наследних и фактора средине, исхране и начина живота. |
Тачан узрок рака дебелог црева није у потпуности познат. За сада знамо да настаје као последица утицаја наследних и фактора средине, исхране и начина живота. |
||
| Ред 132: | Ред 132: | ||
=== Рак гуштераче === |
=== Рак гуштераче === |
||
[[Датотека:Ultrasonography of pancreatic cancer.jpg|мини|Ултрасонографија рака гуштераче]] |
[[Датотека:Ultrasonography of pancreatic cancer.jpg|мини|Ултрасонографија рака гуштераче]] |
||
Рак гуштераче или панкреаса је пети најчешћи узрок смрти од рака у Сједињеним Америчким Државама,[8] и седми најчешћи у Европи.<ref name=":5">Moss, AC; Morris, E; Mac Mathuna, P (Apr 19, 2006). "Palliative biliary stents for obstructing pancreatic carcinoma". ''The Cochrane Database of Systematic Reviews'' (2): CD004200. doi |
Рак гуштераче или панкреаса је пети најчешћи узрок смрти од рака у Сједињеним Америчким Државама,[8] и седми најчешћи у Европи.<ref name=":5">Moss, AC; Morris, E; Mac Mathuna, P (Apr 19, 2006). "Palliative biliary stents for obstructing pancreatic carcinoma". ''The Cochrane Database of Systematic Reviews'' (2): CD004200. {{doi|10.1002/14651858.CD004200.pub4}}. PMC 6769023. <nowiki>PMID 16625598</nowiki>.</ref> У 2008. години, глобално је пријављено 280.000 нових случајева рака панкреаса и 265.000 смртних случајева.<ref name=":6">Gurusamy, Kurinchi Selvan; Kumar, Senthil; Davidson, Brian R; Fusai, Giuseppe; Gurusamy, Kurinchi Selvan (2012). "Resection versus other treatments for locally advanced pancreatic cancer". ''Cochrane Database of Systematic Reviews''. {{doi|10.1002/14651858.CD010244}}.</ref> |
||
Ови карциноми су класификовани као ендокрини или неендокрини тумори. Најчешћи је дуктални аденокарцином.<ref name=":0" /> Најзначајнији фактори ризика за рак панкреаса су поодмакле године (преко 60 година) и пушење дувана.<ref name=":7">Arcidiacono, PG; Calori, G; Carrara, S; McNicol, ED; Testoni, PA (Mar 16, 2011). "Celiac plexus block for pancreatic cancer pain in adults". ''The Cochrane Database of Systematic Reviews'' (3): CD007519. doi |
Ови карциноми су класификовани као ендокрини или неендокрини тумори. Најчешћи је дуктални аденокарцином.<ref name=":0" /> Најзначајнији фактори ризика за рак панкреаса су поодмакле године (преко 60 година) и пушење дувана.<ref name=":7">Arcidiacono, PG; Calori, G; Carrara, S; McNicol, ED; Testoni, PA (Mar 16, 2011). "Celiac plexus block for pancreatic cancer pain in adults". ''The Cochrane Database of Systematic Reviews'' (3): CD007519. {{doi|10.1002/14651858.CD007519.pub2}}. PMC 6464722. <nowiki>PMID 21412903</nowiki></ref> Хронични панкреатитис, дијабетес или друга стања такође могу бити укључени у њихов развој.<ref name=":4" /> Рани карцином гуштераче нема тенденцију да доведе до било каквог симптома, али када тумор узнапредује, пацијент може да осети јак бол у горњем делу стомака, који се може ширити у леђа.<ref name=":7" /> Други симптом може бити жутица, жута боја коже и беоњача очију.<ref name=":5" /> |
||
Рак гуштераче има лошу прогнозу,<ref name=":4" /> са петогодишњом стопом преживљавања мањом од 5%. У време када се канцер дијагностикује, он је обично у узнапредовалом, неоперабилном стадијуму.<ref name=":5" />Само један од петнаест до двадесет пацијената је покушао куративни хируршки захват. Рак гуштераче има тенденцију да буде агресиван и отпоран је на радиотерапију и хемотерапију.<ref name=":6" /> |
Рак гуштераче има лошу прогнозу,<ref name=":4" /> са петогодишњом стопом преживљавања мањом од 5%. У време када се канцер дијагностикује, он је обично у узнапредовалом, неоперабилном стадијуму.<ref name=":5" />Само један од петнаест до двадесет пацијената је покушао куративни хируршки захват. Рак гуштераче има тенденцију да буде агресиван и отпоран је на радиотерапију и хемотерапију.<ref name=":6" /> |
||
Верзија на датум 22. јануар 2023. у 06:17
| Гастроинтестинални рак | |
|---|---|
| Синоними | Gastrointestinal cancer |
| Специјалности | гастроентерологија, онкологија |
| Симптоми | горњи део хематемеза мелена доњи део повраћање хематохезија |
Гастроинтестинални рак укључује све врсте рака у органима дигестивног тракта, који почиње од једњака (цеви која води храну од уста до желуца) и завршава се у анусу (где отпад излази из тела). Одговоран је на глобалном нивоу за највећи број карцинома и велики број смрти од рака једњака желудца, дванаестопалачног, дебело и танког црева, панкреаса, јетре, билијарног система ректума и ануса, у односу на било који други систем у телу,[1][2] Ова врта рака има значајне географске варијације у стопама и врстама.[1]
Симптоми се односе на захваћени орган и могу укључивати опструкцију (која доводи до потешкоћа при гутању или дефекацији), абнормално крварење или друге повезане проблеме.
Дијагноза често захтева ендоскопију, након чега следи биопсија сумњивог ткива.
Лечење зависи од локације тумора, као и од врсте ћелије рака и од тога да ли је рак захватио друга ткива или се проширио (метастазирао) негде другде. Ови фактори такође одређују прогнозу.
| Систем органа за варење код човека | |
|---|---|
 Пробавни систем човека.
1. Усна шупљина; 2.Непце; 3. Ждрело; 4. Језик; 6. Пљувачне жлезде; 7. Подјезична; 8. Подвилична; 9. Доушна жлезда; 11. Једњак; 12. Јетра; 13. Жучни мехур; 14. Жучни водови; 15. Желудац; 16. Панкреас; 17. Панкреасни каналић; 19. Дуоденум; 21. Илеум; 22. Црвуљак; 23. Дебело црево; 24. Colon transversum; 25. Colon ascendens; 26. Слепо црево; 27. Colon descendens; 29. Ректум; 30. Анус | |
| Детаљи | |
| Идентификатори | |
| Латински | Systema digestorium |
| Анатомска терминологија | |
Опште информације
Иако су разјашњене у многим аспектима, молекуларне и генетске основе развоја и прогресије гастроинтестиналног рак оне још увек нису у потпуности схваћене. Сада знамо да је гастроинтестинални рак узрокован различитим мутацијама које погађају одређене гене. Јединствени образац акумулираних мутација у људском геному формира специфичне молекуларне облике рака. Сходно томе, рак гастроинтестиналног тракта се данас не доживљава као једна болест, већ скуп болести са специфичним хетерогеним генетским профилима. Генетска основа рака је, без сумње, застрашујућа јер кодира молекуларне промене својствене мноштву есенцијалних ћелијских процеса. Молекуларни играчи који управљају пролиферацијом, апоптозом, диференцијацијом, ангиогенезом, ћелијском способношћу кретања, као и имуним одговором, сви могу бити циљани на специфичне карциноме који показују јединствене мутационе обрасце.[3] Штавише, неисправност многих сигналних путева је одговорна за иницијацију и еволуцију гастроинтестиналног рака. Колекција уочених генетских промена често се назива „пејзажи генома рака“.[4] Наше знање о геномици рака се тренутно повећава скоро експоненцијално са крајњим циљем да се разуме његова биологија, побољшање дијагностичких и прогностичких алата и развој нових терапијских стратегија које се могу прилагодити потребама појединачних пацијената. Међутим, када се описују есенцијални ћелијски процеси укључени у рак, не смемо заборавити на процесе поправке ДНК чији су поремећени механизми такође веома често укључени у етиологију рака.
Епидемиологија
Упркос значајним напрецима у разумевању молекуларне патогенезе канцера, гастроинтестинални малигнитет (желудац, колоректални, панкреасни и јетрени) и даље је међу водећим узроцима смртности и морбидитета од рака широм света.[5]
Етиологија
Гастроинтестинални рак почиње када ћелије које облажу један или више органа у дигестивном тракту мутирају и почну да расту, производећи туморе, који се понекад шире на лимфне чворове и друге органе.
Још увек се у потпуности незна узрок гастроинтестиналног рака. Ипак, сматра се да оштећење ћелија гастроинтестиналног система повећавају шансу да се појаве абнормалности, а то може бити последица инфекција, гојазности, пушења дувана и неких фактора ризика из животне средине.
Карциномима гастроинтестиналног тракта обично претходе доброћудни (бенигни) диспластични интермедијери, који настају директно из нормалних ткива. Ове диспластичне лезије се могу морфолошки разликовати и класификовати на основу специфичних патолошких критеријума. У дебелом цреву, секвенца аденом-карцинома описује ову прогресију од нормалне слузокоже преко диспластичних интермедијера до инвазивног карцинома , и добро је подржана од стране многих патолошких, епидемиолошких и студија на животињама. Најранија изразита лезија у овој секвенци је аберантна жаришта крипте (АЖК) (микроскопске лезије, које су први пут идентификоване у дебелом цреву обојеном метиленском плавом бојом код мишева третираних азоксиметаном) као крипте које су изгледале веће и дебље, са повећаним луминалним пречником и отвором који је често био у облику прореза или назубљен. Већина људских АЖК је хиперпластична (65–95%); међутим, значајан део је диспластичан и на много начина сличан аденоматозним полипима. Најинтригантније је да је генетска анализа АЖК идентификовала мутације гена које се обично примећују код аденоматозних полипа.[6]
Иако почетни покретач и узрок могу бити различити, једна од заједничких карактеристика свих карцинома гастроинтестиналног тракта је повећан морталитет и морбидитет због откривања у касној фази и лошег преживљавања након метастаза.[5] Постоји општи консензус да се већина карцинома гастроинтестиналног тракта развија током дужег временског периода, што представља атрактивну прилику за интервенцију и превенцију ако се болест рано дијагностикује.[5]
Фактори ризика
Фактори ризика варирају за сваки тип рак. Међутим, фактори као што су начина живота могу играти улогу у многим од њих. То укључује гојазност, невежбање, пушење, лошу исхрану и тешку употребу алкохола. Породична историја такође може повећати вероватноћу за појаву болести. Остали фактори ризика укључују:
- Инфекција хепатитисом А или Б (рак јетре)
- Инфекција Хеликобактером пилори (рак желуца)
- Пушење
- Гастритис
- Конзумирање алкохола
- Прекомерна тежина или гојазност
- Претходну дијагноза гастроинтестиналнох рака или другог карцинома
- Претходна операција на једном или више органа дигестивног система
- Породична историја гастроинтестиналног рака
- Претходни полипи који расту у дебелом цреву или желуцу
Генетика
Гастроинтестинални карциноми су углавном повезани са факторима животне средине који изазивају соматске мутације у туморима. Међутим, скроман проценат карцинома гастроинтестиналног тракта (не више од 5%) може бити повезан са мутацијама заметне линије у различитим генима, укључујући ген супресор тумора (ген АПЦ, који узрокује доминантни облик породичне аденоматозне полипозе, или ФАП) и гени за поправку ДНК (гени за поправку неусклађености ДНК који изазивају Линчев синдром и ген за поправку ексцизије базе MUTYH, који узрокује рецесивни облик ФАП-а).[7]
Постоји неколико препознатљивих породичних синдрома који су повезани са хамартоматозним полипима гастроинтестиналног тракта и повећаним ризиком од карцинома, укључујућиPeutz–Jeghers syndrome (STK11/LKB1 ген), синдром јувенилне полипозе (повезан са СМАД4, БМРПР1А и ЕНГ), Кауденов синдром и Bannayan–Riley–Ruvalcaba syndrome - познат као синдром тумора ПТЕН хамартома (повезан са ПТЕН, а такође и КЛЛН), и други. ЦДХ1 ген је повезан са наследним дифузним карциномом желуца (ХДГЦ), а више гена је повезано са повећаним ризиком од рака панкреаса, од којих већина производи фенотипски препознатљиву болест, укључујући породични панкреатитис (ПРСС1), породични атипични вишеструки младеж. /меланомски синдром, ФАМММ (п16), Peutz–Jeghers-ов синдром, наследни рак дојке и јајника (БРЦА2 и БРЦА1), Линчев синдром (такође познат као наследни неполипозни колоректални карцином) и ФАП.[7]
Врсте
Гастроинтестинални рак утиче на све органе дигестивног тракта, и укључује ове врсте:
Рак једњака

Рак једњака је злоћудни тумор горњих партија гастроинтестиналног система, који због тенденције ка давању удаљених метастаза има веома лошу прогнозу, без обзира на до сада доступне начине лечења. Најчешћи и најзначајнији облици малигних тумора једњака (мишићне цеви чија је улога транспорт хране од уста до желуца) су планоцелуларни карцином и аденокарцином.
Карцином једњака, на глобалном нивоу седми је по реду узрок смрти у свету. Јавља се код отприлике 3-6 особе на 100.000 становника, и у сталном је благом порасту, посебно у ендемским областима које имају и већу стопу по глави становника. Стопа петогодишњег преживљавања болесника, у раздобљу од 2001. до 2007. године, била је 19%.[8]
Рак желуца

Рак желуца четврти је најчешћи тип рака и други највећи узрок смрти од рака у свету.[1] Источна Азија (Кина, Јапан, Кореја, Монголија) је подручје високог ризика за рак желуца, а Северна Америка, Аустралија, Нови Зеланд и западна и северна Африка су области са ниским ризиком.[9] Најчешћи тип рака желуца је аденокарцином, који узрокује око 750.000 смртних случајева сваке године.[10]
Важни фактори који могу допринети развоју рака желуца су исхрана, пушење и конзумирање алкохола, генетска предиспозиција (укључујући низ наследних синдрома) и инфекције (на пример, Helicobacter pylori и Епштајн-Бар вирус) и пернициозна анемија.[1][10] Иако хемотерапија побољшава преживљавање у поређењу са најбољом супортивном негом, оптимални режим је нејасан.[11]
Рак танког црева
Рак дебелог црева
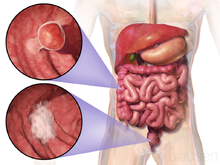
Рак дебелог црева је један од најчешћих карцинома савременог човека,са инциденцијом која је висока у у Европи и свету. У Србији се годишње региструје више од 4.500 нових случајева рака дебелог црева, а годишње од њега умре око 3.000 људи. Рак дебелог црева је први или други на листи малигних тумора дигестивног тракта, у зависности од географског окружења.[12]
Тачан узрок рака дебелог црева није у потпуности познат. За сада знамо да настаје као последица утицаја наследних и фактора средине, исхране и начина живота.
Рак ректума
Рак ануса

Рак ануса настаје када ћелије ануса почну ненормално да расту. Већина случајева овог ретког рака изазвано је хуманим папилома вирусом (ХПВ), уобичајеном инфекцијом која се шири сексуалним контактом. Примена ХПВ вакцине може смањити ризик од развоја аналног рака.
Описане су две врсте аналног рака у односу на то где се налазе канцерогене ћелије.[13]
Рак аналне маргине или ивице, који је видљив на кожи изван ануса, који не треба мешати са меланомом ануса. Ова врста рака се обично лечи на исти начин као и рак коже - хируршким изрезивањем лезије (израслина), али не и самог ануса.[14]
Рак аналног канала, обично открива дигиталним ректалним прегледом или проктоскопијом, јер споља није видљив. Обично се лечи комбинацијом хемотерапије и радиотерапије. Хируршка интервенција је ретко потребна.[14]
Рак јетре

Рак јетре (који се такође назива хепатоцелуларни карцином, ХЦК или хепатом) обично настаје након продужене инфекције хепатитисом Б или Ц или као резултат цирозе јетре изазване хроничним алкохолизмом. Рак јетре може изазвати жутило коже и очију (жутица), свраб (пруритус) или узроковати накупљање течности у трбушној дупљи (асцитес). Особа може осетити повећање масе, или се рак може открити абнормалним тестовима функције јетре.[15]
Ови карциноми се обично лече у складу са њиховим ТНМ стадијумом и да ли или није присутна цироза. Опције укључују хируршку ресекцију, емболизацију, аблацију или трансплантацију јетре.[16]
Рак жучне кесе

Карциноми жучне кесе су типично аденокарциноми и чести су код старијих жена. Рак жучне кесе је снажно повезан са жучним камењем, изгледом порцеланске жучне кесе на ултразвуку и присуством полипа унутар жучне кесе.
Рак жучне кесе може се манифестовати губитком телесне тежине, жутицом и болом у горњем десном углу трбуха. Обично се дијагностикује ултразвуком и компјутеризованом томографијом. Прогноза за рак жучне кесе је лоша.[16]
Рак жучних канала
Рак жучних канала или холангиокарцином је врста рака која се формира у жучним каналима, ( разгранатим танким цевима) које транспортују жуч уз помоћ којих се масти из хране варе. Жучни канали повезују јетру са жучном кесом и танким цревом. Углавном се јавља код људи старијих од 50 година, иако се може развити у било ком узрасту.[17]
Холангиокарцином се развија када ћелије у жучним каналима развију промене у својој ДНК. Ове промене говоре ћелијама да се умножавају ван контроле и формирају масу ћелија, односно тумор који може да нападне и уништи здраво телесно ткиво. Међутим, још увек није јасно шта тачно изазива промене које доводе до холангиокарцинома.
Рак жучних канала јавља се као један од три типа рака, на основу тога где се рак јавља у жучним каналима:[17]
- Интрахепатични холангиокарцином, који се јавља у деловима жучних канала унутар јетре и понекад се класификује као врста рака јетре.
- Хиларни холангиокарцином, који настаје у жучним каналима непосредно изван јетре. Овај тип се такође назива перихиларни холангиокарцином.
- Дистални холангиокарцином, који се развија у делу жучног канала који је најближи танком цреву. Овај тип се такође назива екстрахепатични холангиокарцином.
Како се рак жучних канала често дијагностикује када је узнапредовао, то отежава његово лечење.
Рак гуштераче

Рак гуштераче или панкреаса је пети најчешћи узрок смрти од рака у Сједињеним Америчким Државама,[8] и седми најчешћи у Европи.[18] У 2008. години, глобално је пријављено 280.000 нових случајева рака панкреаса и 265.000 смртних случајева.[19]
Ови карциноми су класификовани као ендокрини или неендокрини тумори. Најчешћи је дуктални аденокарцином.[1] Најзначајнији фактори ризика за рак панкреаса су поодмакле године (преко 60 година) и пушење дувана.[20] Хронични панкреатитис, дијабетес или друга стања такође могу бити укључени у њихов развој.[2] Рани карцином гуштераче нема тенденцију да доведе до било каквог симптома, али када тумор узнапредује, пацијент може да осети јак бол у горњем делу стомака, који се може ширити у леђа.[20] Други симптом може бити жутица, жута боја коже и беоњача очију.[18]
Рак гуштераче има лошу прогнозу,[2] са петогодишњом стопом преживљавања мањом од 5%. У време када се канцер дијагностикује, он је обично у узнапредовалом, неоперабилном стадијуму.[18]Само један од петнаест до двадесет пацијената је покушао куративни хируршки захват. Рак гуштераче има тенденцију да буде агресиван и отпоран је на радиотерапију и хемотерапију.[19]
Клиничка слика
У раним стадијумима рака гастроинтестиналног тракта, могу изостати симптоми. Такође скоро је немогуће осетити туморе гастроинтестиналног тракта док се они развијају.
Као резултат тога, гастроинтестинални рак се често идентификују у скрининзима пре него што се појаве било какви симптоми, или се дијагностикује након што су узнапредовали до те мере да изазивају симптоме у озбиљнијој фази болести.
Када је гастроинтестинални рак довољно узнапредовао да изазове симптоме и знаке болест, они могу укључивати:
- грчеви или бол у стомаку
- крвава или веома тамна столица
- промене у раду црева, као што су дијареја, затвор или промене у конзистенцији или сужавању столице
- потешкоће при гутању
- проблеми са варењем
- жутица (жутило очију и коже)
- мучнина и повраћање
- оток у трбуху или абдомену
- умор, слабост, губитак тежине или губитак апетита
Дијагноза
Рак дигестивног система се обично дијагностикују помоћу једног или више дијагностичких тестова:
- Колоноскопија, у којој се танка цев са камером на њој убацује у дебело црево да би се потражили и уклонили канцерогени или преканцерозни полипи
- Ендоскопија, у којој се ендоскоп убацује у једњак (грло) и користи се за преглед једњака, желуца и танког црева
- Лапароскопија, у којој се лапароскоп (мала камера) убацује кроз мали рез
- Тестови снимања као што су рендгенски зраци (са или без контраста баријума), МРИ, ПЕТ скенирање, ЦТ скенирање и ултразвук
- Биопсија сумњивих подручја раста рака
- Детаљан физички преглед, преглед ваше историје и дискусија о свим недоумицама
- Тестови крви за тражење повишених ензима и знакова рака који могу бити присутни у крви
Терапија
Данас су доступне различите врсте третмана за пацијенте са раком. Неки третмани су стандардни (тренутно коришћени третман), а неки се тестирају у клиничким испитивањима . Клиничко испитивање лечења је истраживачка студија намењена побољшању постојећих третмана или добијању информација о новим третманима за пацијенте са раком . Када клиничка испитивања покажу да је нови третман бољи од стандардног лечења, нови третман може постати стандардни третман. При томе требало би имати у виду да врста лечења зависи од специфичног типа рака.
Оперативно лечење
Операција је стандардни третман за већину карцинома ГИ; уклањање целог или дела дебелог црева, желуца, жучне кесе и других органа за варење може бити најефикаснији начин за уклањање ћелија рака из тела болесника.
Уклањање тумора може бити лековито ако је рак у раној фази. Уобичајена операција је исецање захваћеног дела органа. Понекад се уклања цео орган. Понекад се то ради лапароскопски. Чак и ако је рак узнапредовао и излечење није могуће, неке хируршке технике могу и даље да ублажеза симптоме. На пример, блокада у пасажи хране може се ублажити уклањањем дела желуца, ласерском операцијом или бајпасом.
Хемотерапија
Хемотерапија је лечење рака коришћењем лекова против рака који убијају ћелије рака или спречавају њихово размножавање. Када се хемотерапија користи као додатак операцији, позната је као адјувантна хемотерапија. На пример, после операције може се дати хемотерапије. Ово има за циљ да убије све ћелије рака које су се можда прошириле даље од примарног тумора. Понекад се хемотерапија даје пре операције, како би се смањио велики тумор тако да је операција лакша - ово је познато као неоадјувантна хемотерапија.
Радиотерапија
Радиотерапија дејством зрачења које убија ћелија рака и смањује тумор. Радиотерапија је третман који користи високоенергетске зраке који су фокусирани на канцерогено ткиво. Она убија ћелије рака, или зауставља ћелије рака да се размножавају. Радиотерапија се обично не користи за лечење рака желуца. Понекад се користи и за смањење величине одређеног дела рака који изазива симптоме.
Хеморадиотерапија
У неким случајевима се нуди комбинација хемотерапије и радиотерапије – често као додатак операцији.
Циљана терапија
Циљна терапаија уништава челије рака коришћењем маркера присутних само на ћелијама рака.
Имунотерапија
Имунотерапија се заснива на чињеници да а ова врста рака показују хетерогеност у осетљивости на блокаду имунолошке контролне тачке . Анти-ПД-1 терапија ниволумабом или пембролизумабом ће вероватно постати стандардна терапија за хеморефракторни гастроеофагеални карцином након објављивања резултата регистрационих испитивања. Хепатоцелуларни карцином такође показује осетљивост на имунотерапију , а ниволумаб је опција за пацијенте са хепатоцелуларним карциномом који је напредовао након прве линије лечења. Насупрот томе, колоректални карцином и рак панкреаса изгледа да не реагују на прву генерацију нових имунотерапија као појединачни агенси.[21]
Прогноза
Без лечења, рак ће вероватно постати већи и проширити се на друге делове тела. Ако се дијагностикује и лечи у раној фази (пре него што израсте кроз зид гастроинтестиналних органа или се прошири на лимфне чворове или друге делове тела), онда постоје добре шансе за излечење операцијом. Нажалост, већина случајева се не дијагностикује у раној фази.
Ако се рак дијагностикује када је урастао у зид органа или се проширио на друге делове тела, излечење је мање вероватно. Међутим, лечење често може успорити напредовање канцера, коришћењем лекова за хемотерапију.
Лечење рака је област медицине у развоју. Нови третмани се и даље развијају, а информације о изгледима (прогнози) су веома често опште.
Превенција
Један од кључних клиничких изазова у ефикасном смањењу оптерећења болести повезаног са гастроинтестиналном неоплазијом произилази из касне дијагнозе, наглашавајући потребу за раним откривањем, проценом ризика и интервенцијом. Тренутно доступни приступи скринингу су неадекватни, а развој тачних неинвазивних молекуларних биомаркера је веома потребан. У будућности је вероватно да ће миРНА биомаркери револуционисати персонализовану медицину и ублажити оптерећење болести повезано са раком гастроинтестиналног тракта.[5]
Извори
- ^ а б в г д Yamada T, Alpers DH, et al. (2009). Textbook of gastroenterology (5th ed.). Chichester, West Sussex: Blackwell Pub. pp. 603, 1028.
- ^ а б в Bjelakovic, G; Nikolova, D; Simonetti, RG; Gluud, C (Jul 16, 2008). "Antioxidant supplements for preventing gastrointestinal cancers". The Cochrane Database of Systematic Reviews (3): CD004183.
- ^ Somarelli, J. A., Gardner, H., Cannataro, V. L., Gunady, E. F., Boddy, A. M., Johnson, N. A., et al. (2020). Molecular biology and evolution of cancer: from discovery to action. Mol. Biol. Evol. 37, 320–326. doi:10.1093/molbev/msz242
- ^ Vogelstein, B., Papadopoulos, N., Velculescu, V. E., Zhou, S., Diaz, L. A. Jr., and Kinzler, K. W. (2013). Cancer genome landscapes. Science 339, 1546–1558. doi:10.1126/science.1235122
- ^ а б в г Link, Alexander; Goel, Ajay (2013-01-01), Makowski, Gregory S., ур., Chapter Six - microRNA in Gastrointestinal Cancer: A Step Closer to Reality (на језику: енглески), 62, Elsevier, стр. 221—268, Приступљено 2023-01-21
- ^ „Physiology of the Gastrointestinal Tract”. ScienceDirect (на језику: енглески). Приступљено 2023-01-21.
- ^ а б C.R. Boland, ... J.M. Carethers, Cancer of the Colon and Gastrointestinal Tract, in Reference Module in Biomedical Sciences, 2014
- ^ Whittemore, edited by David Schottenfeld, Joseph F. Fraumeni Jr.; associate editors, Graham A. Colditz, Jonathan M. Samet, Alice S. (2006). Cancer epidemiology and prevention (3rd ed.). Oxford: Oxford University Press. p. 697.
- ^ Bennett, C; Wang, Y; Pan, T (Oct 7, 2009). "Endoscopic mucosal resection for early gastric cancer". The Cochrane Database of Systematic Reviews (4): CD004276. doi:10.1002/14651858.CD004276.pub3. PMC 7199372. PMID 19821324.
- ^ а б O'Connor, A; McNamara, D; O'Moráin, CA (Sep 23, 2013). "Surveillance of gastric intestinal metaplasia for the prevention of gastric cancer". The Cochrane Database of Systematic Reviews. 9 (9): CD009322.
- ^ Wagner, Anna Dorothea; Syn, Nicholas LX; Moehler, Markus; Grothe, Wilfried; Yong, Wei Peng; Tai, Bee-Choo; Ho, Jingshan; Unverzagt, Susanne (2017-08-29). "Cochrane Database of Systematic Reviews" (PDF). Cochrane Database of Systematic Reviews. 8: CD004064. doi:10.1002/14651858.cd004064.pub4. PMC 6483552. PMID 28850174.
- ^ Bibbins-Domingo K, Grossman DC, Curry SJ, Davidson KW, Epling JW, García FA, Gillman MW, Harper DM, Kemper AR, Krist AH, Kurth AE, Landefeld CS, Mangione CM, Owens DK, Phillips WR, Phipps MG, Pignone MP, Siu AL (jun 2016). „Screening for Colorectal Cancer: US Preventive Services Task Force Recommendation Statement”. JAMA. 315 (23): 2564—2575. PMID 27304597. doi:10.1001/jama.2016.5989.
- ^ „Types of Anal Cancer”. www.pennmedicine.org. Приступљено 2023-01-20.
- ^ а б „Anal Cancer Treatment”. www.pennmedicine.org. Приступљено 2023-01-20.
- ^ Vinay Kumar; et al., eds. (2007). Robbins basic pathology (8th ed.). Philadelphia: Saunders/Elsevier. ISBN 978-1-4160-2973-1. OCLC 804094752.
- ^ а б Nicki R. Colledge; Brian R. Walker; Stuart H. Ralston, eds. (2010). Davidson's principles and practice of medicine. Illustrated by Robert Britton (21st ed.). Edinburgh: Churchill Livingstone/Elsevier. ISBN 978-0-7020-3085-7. OCLC 455157186.
- ^ а б „What is bile duct cancer”. nhs.uk (на језику: енглески). 2017-10-20. Приступљено 2023-01-21.
- ^ а б в Moss, AC; Morris, E; Mac Mathuna, P (Apr 19, 2006). "Palliative biliary stents for obstructing pancreatic carcinoma". The Cochrane Database of Systematic Reviews (2): CD004200. doi:10.1002/14651858.CD004200.pub4. PMC 6769023. PMID 16625598.
- ^ а б Gurusamy, Kurinchi Selvan; Kumar, Senthil; Davidson, Brian R; Fusai, Giuseppe; Gurusamy, Kurinchi Selvan (2012). "Resection versus other treatments for locally advanced pancreatic cancer". Cochrane Database of Systematic Reviews. doi:10.1002/14651858.CD010244.
- ^ а б Arcidiacono, PG; Calori, G; Carrara, S; McNicol, ED; Testoni, PA (Mar 16, 2011). "Celiac plexus block for pancreatic cancer pain in adults". The Cochrane Database of Systematic Reviews (3): CD007519. doi:10.1002/14651858.CD007519.pub2. PMC 6464722. PMID 21412903
- ^ Vasiliki Michalarea, Elizabeth C. Smyth, Rationale for Immunotherapy in Gastrointestinal Malignancies in Oncogenomics, 2019
Спољашње везе
| Класификација |
|---|
![]() Медији везани за чланак Желудачноцревни рак на Викимедијиној остави
Медији везани за чланак Желудачноцревни рак на Викимедијиној остави
