Биоеквивалентност
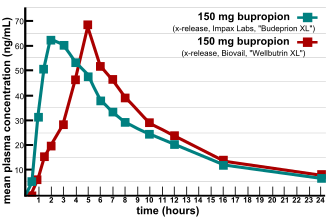
Биоеквивалентност је фармакокинетички термин који се користи за поређење очекиване биолошке ин виво еквиваленције лекова различитих проивођача. Ако су производи биоеквивалентни они морају да буду идентични у сваком погледу.
Биркет је 2003. дефинисао биоеквиваленцију на следећи начин, „два фармацеутска производа су биоеквивалентна ако су фармацеутски еквивалентна и њихове биорасположивости (брзине и степени доступности) након администрације у истој моларној дози су сличне у тој мери да се може очекивати да је њихово дејство, у погледу ефикасности и безбедности, есенцијално исто. Фармацеутска еквиваленција подразумева исту количину исте активне супстанце у датом облику дозирања, при истом начину администрације и задовољавања истих или упоредивих стандарда.“[1]
ФДА дефинише биоеквиваленцију као, „одсуство знатних разлика у брзини и мери у којој активни ингредијент или активни састојак у фармацеутским еквивалентима или фармацеутским алтернативама постаје доступан на месту дејства лека кад се администира у истој моларној дози под сличним условима у подесно дизајнираној студији.“[2]
Референце[уреди | уреди извор]
- ^ Биркетт ДЈ (2003). „Генерицс - еqуал ор нот?” (ПДФ). Ауст Пресцр. 26: 85—7. Архивирано из оригинала (ПДФ) 26. 06. 2012. г. Приступљено 21. 10. 2013.
- ^ Центер фор Друг Евалуатион анд Ресеарцх (2003). „Гуиданце фор Индустрy: Биоаваилабилитy анд Биоеqуиваленце Студиес фор Ораллy Администеред Друг Продуцтс — Генерал Цонсидератионс” (ПДФ). Унитед Статес Фоод анд Друг Администратион.
Литература[уреди | уреди извор]
- Hussain AS, et al. The Biopharmaceutics Classification System: Highlights of the FDA's Draft Guidance Office of Pharmaceutical Science, Center for Drug Evaluation and Research, Food and Drug Administration.
- Mills D (2005). Regulatory Agencies Do Not Require Clinical Trials To Be Expensive International Biopharmaceutical Association: IBPA Publications.
- FDA CDER Office of Generic Drugs - further U.S. information on bioequivalence testing and generic drugs
