Алтернативно сплајсовање

Алтернативно сплајсовање (или диференцијално сплајсовање) је процес којим се РНК ексони произведени транскрипцијом гена (примарни генски транскрипт или пре-иРНК) поновно спајају на више начина током РНК сплајсовања. Резултујући различити иРНК молекули могу бити транслирани у различите протеинске изоформе; тим путем један ген може да кодира више протеина[1].
Алтернативно сплајсовање се јавља као нормална појава код еукариота, где то знатно повећава разноврсност протеина који могу бити кодирани геномом[1]. Код људи преко 80% гена су алтернативно сплајсовани[2]. Бројни модови алтернативног сплајсовања су уочени, од којих најчешћи је прескакање ексона. У том моду, поједини ексон може бити укључен у иРНК под неким условима или у појединим ткивима, и изостављен из иРНК у другим[1].
Производња алтернативно сплајсованих иРНК молекула је регулисана системом транс-делујућих протеина који се везују за цис-делујућа места на самим пре-иРНК молекулима. Такви протеини обухватају сплајсне активаторе који подстичу употребу одређеног сплајсног места, и сплајсне репресоре који умањују употребу појединих места. Механизми алтернативног сплајсовања су високо варијабилни, и нови примери се константно налазе, посебно употребом високопроточних техника. Истраживачи се надају да ће временом регулаторни систем сплајсовања бити потпуно испитан, тако да ће постати могуће да се предвиде производи алтернативног сплајсовања гена под датим условима употребом „сплајсног кода“[2][3].
Абнормалне варијације у сплајсовању су могући узрок многих болести. Велики део људских наследних болести је последица неадекватних сплајсних варијанти[2]. За абнормалне сплајсне варијанте се такође сматра да доприносе развоју рака[4][5][6][7].
Откриће[уреди | уреди извор]
Алтернативно сплајсовање је први пут запажено 1977.[8][9] Аденовируси производе два различита примарна транскрипта, један рано у животном циклусу и један касније, након ДНК репликације. Утврђено је да је примарни РНК транскрипт произведен аденовирусом тип 2 у касној фази сплајсован на различите начине, што доводи до иРНК молекула који кодирају различите виралне протеине. Оба, 5’ и 3’, сплајсна места су варирала, и додатно, транскрипт је садржао вишеструка места полиаденилације, што је давало различите 3’ крајеве обрађеним иРНК молекулима[10][11][12]
Први пример алтернативног сплајсовања у транскриптима нормалних, ендогених гена је карактерисан 1981. године[10]. За ген који кодира тиреоидни хормон калцитонин је нађено да је алтернативно сплајсован у ћелијама сисара. Пре-иРНК овог гена садржи 6 ексона; иРНК калцитонина садржи ексоне 1-4, и завршава се након полиаденилационог места у ексону 4. Други иРНК молекул је произведен овом пре-иРНК прескачући ексон 4, и садржи ексоне 1-3, 5, и 6. Он кодира протеин познат као CGRP (калцитонинском гену сродан пептид)[13][14]. Примери алтернативног сплајсовања транскрипата гена имуноглобина код сисара су такође примећени током раних 1980-тих[10][15].
Од тог времена, за алтернативно сплајсовање је утврђено да је свеприсутно код еукариота[1]. „Рекордер“ у алтернативном сплајсовању је D. melanogaster ген под именом Dscam, који потенцијално може да има 38,016 сплајсних варијанти[16].
Модови[уреди | уреди извор]
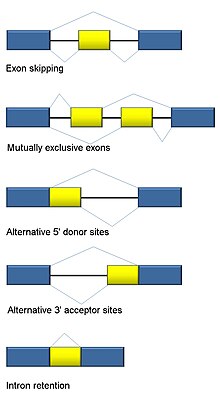
Постоји пет основних начина алтернативног сплајсовања.[1][2][17]
- Прескакање ексона или касета ексона: у овом случају, ексон може бити изостављен из примарног транскрипта или задржан. Ово је најчешћи мод код сисарске пре-иРНК[17].
- Међусобно искључиви ексони: Један од два ексона се задржава у иРНК након спајања, али не оба.
- Алтернативно донорско место: Алтернативни 5' спој (донорско место) се користи, чиме се мења 3' граница низводног ексона.
- Алтернативно акцепторско место: Алтернативни 3' спој (акцепторско место) се користи, чиме се мења 5' граница низводног ексона.
- Задржавање интрона: Део секвенца може може бити изостављен као интрон или једноставно задржан. Овај мод се разликује од прескакања ексона по томе што задржана секвенца није оивичена интронима. Ако је задржани интрон кодирајући регион, он мора да кодира аминокиселине између суседних ексона, јер стоп кодон или померање оквира читања би вероватно произвело протеин без функције. Ово је најређи мод код сисара[17].
Поред ових примарних модова алтернативног сплајсовања, постоје два друга механизма којима се различити иРНК молекули стварају из истог гена: вишеструки промотери и вишеструка места полиаденилације. Употреба више промотера је пре механизам транскрипционе регулације него алтернативног сплајсовања. Почињући транскрипцију у различитим тачкама, транскрипти са различитим 5'-крајњим ексонима могу бити формирани. С друге стране, вишеструка места полиаденилације омогућавају различите 3' крајње тачке. Оба ова механизма су нађена у комбинацији са алтернативним сплајсовањем и производе додатну варијабилност иРНК молекула изведених из датог гена[1][2].
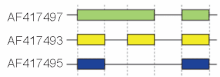
Ови модови описује основне сплајсне механизме. Постоји могућност да су они нису адекватни за описивање комплексних сплајсних догађаја. Слика са десне стране показује три сплајсне форме мишјег гена хијалуронидазе. Поређење структуре на првој линији (зелено) са структуром на другој линији (жуто) показује задржавање интрона, док поређење друге и треће линије (жуто вс. плаво) је пример прескакања. Номенклатура модела која јединствено одређује све могуће узорке спајања је недавно била предложена[17].
Литература[уреди | уреди извор]
- ^ а б в г д ђ Блацк, Доуглас L. (2003). „Мецханисмс оф алтернативе пре-мессенгер РНА сплицинг”. Аннуал Ревиеwс оф Биоцхемистрy. 72 (1): 291—336. ПМИД 12626338. дои:10.1146/аннурев.биоцхем.72.121801.161720.
- ^ а б в г д Матлин, АЈ; Цларк Ф; Смитх, ЦWЈ (2005). „Ундерстандинг алтернативе сплицинг: тоwардс а целлулар цоде”. Натуре Ревиеwс. 6 (5): 386—398. ПМИД 15956978. дои:10.1038/нрм1645.
- ^ Давид ЦЈ, Манлеy ЈЛ (2008). „Тхе сеарцх фор алтернативе сплицинг регулаторс: неw аппроацхес оффер а патх то а сплицинг цоде”. Генес & Девелопмент. 22 (3): 279—85. ПМЦ 2731647
 . ПМИД 18245441. дои:10.1101/гад.1643108.
. ПМИД 18245441. дои:10.1101/гад.1643108.
- ^ Скотхеим анд Неес (2007). „Алтернативе сплицинг ин цанцер: ноисе, фунцтионал, ор сyстематиц?”.
- ^ Хе C, Зхоу Ф, Зуо З, Цхенг Х, Зхоу Р (2009). „А глобал виеw оф цанцер-специфиц трансцрипт вариантс бy субтрацтиве трансцриптоме-wиде аналyсис”. Плос Оне. 4 (3): е4732. ПМЦ 2648985
 . ПМИД 19266097. дои:10.1371/јоурнал.поне.0004732.
. ПМИД 19266097. дои:10.1371/јоурнал.поне.0004732.
- ^ Фацкентхал, Јд; Годлеy, Ла (2008). „Аберрант РНА сплицинг анд итс фунцтионал цонсеqуенцес ин цанцер целлс”. Дисеасе моделс & мецханисмс. 1 (1): 37—42. ИССН 1754-8403. ПМЦ 2561970
 . ПМИД 19048051. дои:10.1242/дмм.000331. Архивирано из оригинала (Фрее фулл теxт) 13. 03. 2021. г. Приступљено 21. 12. 2010.
. ПМИД 19048051. дои:10.1242/дмм.000331. Архивирано из оригинала (Фрее фулл теxт) 13. 03. 2021. г. Приступљено 21. 12. 2010.
- ^ Валлетти А, Анселмо А, Мангиулли M, Бориа I, Мигноне Ф, Мерла Г, D'Ангело V, Тулло А, Сбисà Е, D'Ерцхиа АМ, Песоле Г (2010). „Идентифицатион оф тумор-ассоциатед цассетте еxонс ин хуман цанцер тхроугх ЕСТ-басед цомпутатионал предицтион анд еxпериментал валидатион”. Молецулар Цанцер. 9: 230. ПМЦ 2941758
 . ПМИД 20813049. дои:10.1186/1476-4598-9-230.
. ПМИД 20813049. дои:10.1186/1476-4598-9-230.
- ^ Цхоw ЛТ, Гелинас РЕ, Брокер ТР, Робертс РЈ (1977). „Ан амазинг сеqуенце аррангемент ат тхе 5' ендс оф аденовирус 2 мессенгер РНА”. Целл. 12 (1): 1—8. ПМИД 902310. дои:10.1016/0092-8674(77)90180-5.
- ^ Бергет СМ, Мооре C, Схарп ПА (1977). „Сплицед сегментс ат тхе 5' терминус оф аденовирус 2 лате мРНА”. Проц. Натл. Ацад. Сци. У.С.А. 74 (8): 3171—5. ПМЦ 431482
 . ПМИД 269380. дои:10.1073/пнас.74.8.3171.
. ПМИД 269380. дои:10.1073/пнас.74.8.3171.
- ^ а б в Лефф СЕ, Росенфелд МГ, Еванс РМ (1986). „Цомплеx трансцриптионал унитс: диверситy ин гене еxпрессион бy алтернативе РНА процессинг”. Анну. Рев. Биоцхем. 55: 1091—117. ПМИД 3017190. дои:10.1146/аннурев.би.55.070186.005303.
- ^ Цхоw ЛТ, Брокер ТР (1978). „Тхе сплицед струцтурес оф аденовирус 2 фибер мессаге анд тхе отхер лате мРНАс”. Целл. 15 (2): 497—510. ПМИД 719751. дои:10.1016/0092-8674(78)90019-3.
- ^ Невинс ЈР, Дарнелл ЈЕ (1978). „Степс ин тхе процессинг оф Ад2 мРНА: полy(А)+ нуцлеар сеqуенцес аре цонсервед анд полy(А) аддитион прецедес сплицинг”. Целл. 15 (4): 1477—93. ПМИД 729004. дои:10.1016/0092-8674(78)90071-5.
- ^ Росенфелд МГ, Амара СГ, Роос БА, Онг ЕС, Еванс РМ (1981). „Алтеред еxпрессион оф тхе цалцитонин гене ассоциатед wитх РНА полyморпхисм”. Натуре. 290 (5801): 63—5. ПМИД 7207587. дои:10.1038/290063а0.
- ^ Росенфелд МГ; Лин ЦР; Амара СГ (1982). „Цалцитонин мРНА полyморпхисм: пептиде сwитцхинг ассоциатед wитх алтернативе РНА сплицинг евентс”. Проц. Натл. Ацад. Сци. У.С.А. 79 (6): 1717—21. ПМЦ 346051
 . ПМИД 6952224. дои:10.1073/пнас.79.6.1717.
. ПМИД 6952224. дои:10.1073/пнас.79.6.1717.
- ^ Маки Р; Роедер W; Траунецкер А (1981). „Тхе роле оф ДНА реаррангемент анд алтернативе РНА процессинг ин тхе еxпрессион оф иммуноглобулин делта генес”. Целл. 24 (2): 353—65. ПМИД 6786756. дои:10.1016/0092-8674(81)90325-1.
- ^ Сцхмуцкер D, Цлеменс ЈЦ, Сху Х, Wорбy ЦА, Xиао Ј, Муда M, Диxон ЈЕ, Зипурскy СЛ (2000). „Дросопхила Дсцам ис ан аxон гуиданце рецептор еxхибитинг еxтраординарy молецулар диверситy”. Целл. 101 (6): 671—84. ПМИД 10892653. дои:10.1016/С0092-8674(00)80878-8.
- ^ а б в г Мицхаел Самметх; Сyлваин Фоиссац; Родериц Гуигó (8. 8. 2008). „А генерал дефинитион анд номенцлатуре фор алтернативе сплицинг евентс”. ПЛоС Цомпут Биол. 4 (8): е1000147. ПМЦ 2467475
 . ПМИД 18688268. дои:10.1371/јоурнал.пцби.1000147.
. ПМИД 18688268. дои:10.1371/јоурнал.пцби.1000147.
