Фибрински лепак
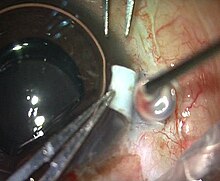 Примена ФЛ у операцији интраокуларног сочива | |
| Комбинација | |
|---|---|
| Фибриноген | Гликопротеин |
| Тромбин | Фактори коагулације |
| Клинички подаци | |
| Продајно име | Артисс, Евицел, Тиссеел, отхерс |
| Drugs.com | |
| Подаци о лиценци | |
| Категорија трудноће | |
| Начин примене | На телесним површинама |
| Правни статус | |
| Правни статус | |
| Идентификатори | |
| CAS број | 9001-32-5 9002-04-4 |
| ATC код | B02BC30 (WHO) |
| DrugBank | DB09222 DB11571 |
| UNII | N94833051K 6K15ABL77G |
Фибрински лепак (акроним ФЛ) је биолошко терапијско средство које потпомаже успостављање локалне хемостазе и омогућава атрауматско повезивање и/или покривање (затварање) оштећене ткивне површине (својим ткивно-адхезивним и „заптивним” дејством), што је временом допринело постизању већег терапијског учинка.[8][9][10][11]
Чињеница да ФЛ представља двокомпонентни биолошки систем, са локалним хемостазним, адхезивним, заптивним и другим ефектима, и да спада у терапијски агенс чије се дејство базира на биолошким и физиолошким принципима, довела је до његове широке примене у свим гранама хирургије. Фибрински лепак који данас има широку примену у савременој хируршкој пракси је хемостатско-адхезивна супстанција. С обзиром на то да се ради о продукту природног, а највећим делом и хуманог порекла, он није ткивно-токсичан, биодеградабилан је, а појава хетеро или алоантитела по примени ФЛ је ретка.[12]
Називи
[уреди | уреди извор]Фибрински лепак — фибрин глуе — фибрин сеалант — фибрин тиссуе адхесиве — фибрин сутуре
Историја
[уреди | уреди извор]Историјат и савремена клиничка примена фибрина у клиничкој пракси забележена је с почетка 20.века, када је Бергел, 1909. године уочио хемостатски ефекат пулверизованог фибрина.[13] Међутим кључни моменат за употребу фибринске емулзије за стимулацију зарастања рана настао је 1970-их, захваљујући напретку трансфузиолошких техника. Те деценије су прво Матрас и сар., 1972. године успешна експериментална применили криопреципитат плазме и говеђег тромбина за бешавну анастомозу периферног нерва (зечији модел),[14] а затим Кудема и Матрас, 1975. године, успешно су клинички применили ФЛ за бешавну анастомозу повређеног периферног нерва.[15]
У производњи и клиничкој примени ФЛ прво су предњачиле европске земље, док је у Сједињеним Америчким Државама, због ризика вирусне инфекције, индустријска производња фибриногена из крвне плазме забрањена 1978. године и први комерцијални препарат ФЛ (Тиссеел) регистрован од стране Фоод анд Друг Администратион (ФДА) тек 1998. године.[10]
Основне информације
[уреди | уреди извор]Фибрински лепак настаје из биолошки активне супстанце – фибрина – као крајњег производа завршне фазе коагулације крви.160, а фибрински коагулум уједно представља супстрат почетне фазе зарастања ране.[16][17]
Састав
[уреди | уреди извор]Конвенционални фибрински лепак је, начелно, двокомпонентни производ комерцијално доступан у лиофилизованом облику или у виду замрзнутог раствора:
- Компонента 1
Главни састојци компоненте 1 су фибриноген, концентрован (40–127 мг/мл, зависно од производа) из криопреципитата крвне плазме једног или више давалаца или самог пацијента; фибронектин (2–9 мг/мл); и фактор коагулације XIII (10–80 У).
- Компонента 2
Друга компонента ФЛ садржи тромбин (4–1000 ИУ/мл), бовиног („прва генерација” препарата ФЛ) или хуманог порекла (унапређена, „друга генерација”), који се пре употребе реконституише у раствору калцијум-хлорида (40 ммол ЦаЦл2/л).
- Остали састојци
Поред наведених компоненти 1 и 2,поједини препарати ФЛ садрже и антифибринолитик (бовини апротинин [1000–3000 КИУ/мл], аминокапроинска или транексаминска киселина).[10]
Брзина образовања фибринског коагулума
[уреди | уреди извор]На брзину образовања фибринског коагулума пресудно утиче концентрација тромбина, док су биофизичка и биохемијска својства ФЛ детерминисана првенствено садржајем фибриногена.[18][19]
Индикације за примену ФЛ
[уреди | уреди извор]У индикације за примену ФЛ у клиничкој пракси спадају:
- Прихваћене индикације
- Контрола крварења (локални хемостатик) као комплементарна и адјувантна мера, посебно код дифузног, нехируршког крварења и у присуству урођене/стечене коагулопатије.
- Заптивање ткивних површина (тиссуе сеалинг)
- Ткивна адхезија (тиссуе глуинг)
- Шире индикације
- Стимулација зарастања ране (ФЛ ± тромбоцити)
- Медијум за фармаколошки активне супстанце и ћелије — антибиотици (гентамицин, бацитрацин/неомицин, цефазолин, ванкомицин, и др.), фактори раста, цитостатици, лидокаин, хепарин; ендотелне, матичне ћелије.
- Супстрат за „ткивни инжењеринг”
Нежељени ефекти
[уреди | уреди извор]Као могући нежељени ефекти након примене ФЛ, који зависе од састава и порекла компоненти, могу се јавити:
- Пренос вирусне инфекције (теоретски ризик, без документованих случајева преноса ХИВ, ХБВ и ХЦВ у досадашњој пракси)
- Имунолошка реакција на бовини тромбин.
- Преосетљивост на апротинин (ткђ. протеин говеђег порекла)
- Неуротоксичност транексаминске киселине (конвулзије)
- Ваздушна/тромбоемболија, дисеминована интраваска коагулација (код акциденталне интраваскуларне апликације)
- Патолошка локална реакција ткива (некроза, фиброза, и др.)
Данас, у односу на прву генерацију ФЛ друге генерације су безбеднији (јер су без састојака животињског порекла), а најбезбеднији су аутологни ФЛ.
Извори
[уреди | уреди извор]- ^ а б „ВераСеал”. Тхерапеутиц Гоодс Администратион (ТГА). 12. 11. 2021. Приступљено 28. 12. 2021.
- ^ „Упдатес то тхе Пресцрибинг Медицинес ин Прегнанцy датабасе”. Тхерапеутиц Гоодс Администратион (ТГА). 12. 5. 2022. Приступљено 13. 5. 2022.
- ^ „АусПАР: Хуман Фибриноген / Хуман Тхромбин”. Тхерапеутиц Гоодс Администратион (ТГА). 29. 6. 2022. Приступљено 17. 7. 2022.
- ^ „Хеалтх продуцт хигхлигхтс 2021: Аннеxес оф продуцтс аппровед ин 2021”. Хеалтх Цанада. 3. 8. 2022. Приступљено 25. 3. 2024.
- ^ „ТацхоСил сеалант матриx - Суммарy оф Продуцт Цхарацтеристицс (СмПЦ)”. (емц). 31. 1. 2020. Архивирано из оригинала 10. 7. 2020. г. Приступљено 10. 7. 2020.
- ^ „Тиссеел Реадy то усе Солутионс фор Сеалант - Суммарy оф Продуцт Цхарацтеристицс (СмПЦ)”. (емц). 30. 12. 2019. Приступљено 10. 7. 2020.
- ^ „Артисс Солутионс фор Сеалант - Суммарy оф Продуцт Цхарацтеристицс (СмПЦ)”. (емц). 29. 1. 2019. Приступљено 10. 7. 2020.
- ^ Станојковић З, Балинт БЈ, Игњатовић D, Балинт L, Остојић Г (2004). „Фибрински лепак - као ефикасан локални хемостатик и адхезивни-заптивни агенс”. Анестезија реанимација трансфузија. 32 (1-2): 69—74..
- ^ Албала MD (2003). „Фибрин сеалантс ин цлиницал працтице”. Цардиовасц Сург. 11 (1): 5—11..
- ^ а б в Јацксон, M. Р. (2001). „Фибрин сеалантс ин сургицал працтице: ан овервиеw”. Ам Ј Сург. 182 (2): 1—7..
- ^ Спотнитз WД (2014). „Фибрин сеалант: Тхе онлy аппровед хемостат, сеалант, анд адхесиве – а лабораторy анд цлиницал перспецтиве”. ИСРН Сург. 2014: 203943..
- ^ Гиббле ЈW, Несс ПМ. Фибрин глуе: тхе перфецт оперативе сеалант? Трансфусион. 30 (8): 741–7.
- ^ 170. Бергел С. Üбер Wиркунген дес Фибринс. Дтсцх Мед Wсцхр. 35 663–5.
- ^ Матрас Х, Дингес ХП, Лассманн Х, Мамоли Б. Зур нахтлосен интерфасзикулäрен Нервентрансплантатион им Тиереxперимент. Wиен Мед Wсцхр. 122 (37):::517–23.
- ^ Кудерна Х, Матрас Х. Дие клинисцхе Анwендунг дер Клебунг вон Нервенанастомосен мит Гериннунгссубстанзен беи дер Реконструктион верлетзтер перипхерер Нервен. Wиен Клин Wсцхр. 87 495–8.
- ^ Цларк, Р. А. (2001). „Фибрин анд wоунд хеалинг”. Анн Н Y Ацад Сци. 936: 355—67..
- ^ Лауренс Н, Коолwијк П, де Маат МП (2006). „Ј Фибрин струцтуре анд wоунд хеалинг”. Тхромб Хаемост. 4 (5): 932—9.
- ^ Wозниак, Г. (2003). „Фибрин сеалантс ин суппортинг сургицал тецхниqуес: тхе импортанце оф индивидуал цомпонентс”. Цардиовасц Сург. 11 (1): 17—21..
- ^ Буцхта C, Хедрицх ХЦ, Мацхер M, Хöцкер П, Редл Х. Биоцхемицал цхарацтеризатион оф аутологоус фибрин сеалантс продуцед бy ЦрyоСеал анд Вивостат ин цомпарисон то тхе хомологоус фибрин сеалант продуцт Тиссуцол/Тиссеел. Биоматериалс. 26 (31): 6233–41.
Литература
[уреди | уреди извор]- Моника Бартхелс, Марио вон Депка: Дас Гериннунгскомпендиум. Сцхнеллориентиерунг, Бефундинтерпретатион, клинисцхе Консеqуензен. Тхиеме, Стуттгарт у. а. 2002. ISBN 3-13-131751-5..
- Г. Дицкнеите, Х. Ј. Метзнер, M. Кроез, Б. Хеин, У. Ницолаy: Тхе импортанце оф фацтор XIII ас а цомпонент оф фибрин сеалантс. Ин: Јоурнал оф Сургицал Ресеарцх. 107, 2, Оцт. 2002, С. 186–195.
Спољашње везе
[уреди | уреди извор] | Молимо Вас, обратите пажњу на важно упозорење у вези са темама из области медицине (здравља). |
