Веза угљеник-угљеник
Веза угљеник-угљеник је ковалентна веза између два атома угљеника.[1] Најчешћи облик је једнострука веза: веза састављена од два електрона, по један из сваког од два атома. Једнострука веза угљеник-угљеник је сигма веза и формира се између једне хибридизоване орбитале из сваког атома угљеника. У етану, орбитале су сп3-хибридизоване орбитале, али се јављају једноструке везе формиране између атома угљеника са другим хибридизацијама (нпр. сп2 са сп2). Заправо, атоми угљеника у једнострукој вези не морају бити исте хибридизације. Атоми угљеника такође могу да формирају двоструке везе у једињењима која се називају алкени или троструке везе у једињењима која се зову алкини. Двострука веза се формира са сп2-хибридизованом орбиталом и п-орбиталом која није укључена у хибридизацију. Трострука веза се формира са сп-хибридизованом орбиталом и две п-орбитале из сваког атома. Употреба п-орбитала формира пи везу.[2]
Ланци и гранање
[уреди | уреди извор]Угљеник је један од ретких елемената који могу да формирају дугачке ланце сопствених атома, својство које се зове катенација. Ово заједно са [бонд стренгтх[|јачином]] везе угљеник-угљеник доводи до огромног броја молекуларних облика, од којих су многи важни структурни елементи живота, тако да једињења угљеника имају своје поље проучавања: органску хемију.
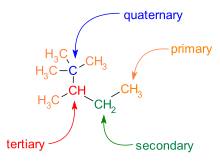
Гранање је такође уобичајено у C-C скелетима. Атоми угљеника у молекулу су категорисани према броју суседа угљеника које имају:
- Примарни угљеник има један суседни угљеник.
- Секундарни угљеник има два суседна угљеника.
- Терцијарни угљеник има три суседна угљеника.
- Кватернарни угљеник има четири суседна угљеника.
У „структурно сложеним органским молекулима“, облик молекула диктира тродимензионална оријентација веза угљеник–угљеник на кватернарним локусима.[3] Даље, квартенарни локуси се налазе у многим биолошки активним малим молекулима, као што су кортизон и морфијум.[3]
Референце
[уреди | уреди извор]- ^ Дембицки, Харрy (2016-10-06). Працтицал Петролеум Геоцхемистрy фор Еxплоратион анд Продуцтион (на језику: енглески). Елсевиер. стр. 7. ИСБН 9780128033517.
- ^ Смитх, Мицхаел Б.; Марцх, Јеррy (2007). Адванцед Органиц Цхемистрy: Реацтионс, Мецханисмс, анд Струцтуре (6тх изд.). Неw Yорк: Wилеy-Интерсциенце. ИСБН 0-471-72091-7.
- ^ а б Qуасдорф, Кyле W.; Оверман, Ларрy Е. (2014). „Ревиеw: Цаталyтиц енантиоселецтиве сyнтхесис оф qуатернарy царбон стереоцентрес”. Натуре (папер). 516 (7530): 181—191. Бибцоде:2014Натур.516..181Q. ПМЦ 4697831
 . ПМИД 25503231. дои:10.1038/натуре14007.
. ПМИД 25503231. дои:10.1038/натуре14007.
