DPPH

| |
| Nazivi | |
|---|---|
| IUPAC naziv
ди(фенил)-(2,4,6-тринитрофенил)иминоазанијум
| |
| Drugi nazivi
2,2-дифенил-1-пикрилхидразил
1,1-дифенил-2-пикрилхидразил радикал 2,2-дифенил-1-(2,4,6-тринитрофенил)хидразил Дифенилпикрилхидразил | |
| Identifikacija | |
3D model (Jmol)
|
|
| Abrevijacija | DPPH |
| ChemSpider | |
| ECHA InfoCard | 100.015.993 |
| |
| Svojstva | |
| C18H12N5O6 | |
| Molarna masa | 394,32 g/mol |
| Agregatno stanje | Прах нијанси од црне до зелене, љубичасти раствор |
| Gustina | 1,4 g/cm3 |
| Tačka topljenja | 135 °C (275 °F; 408 K) |
| нерастворљив | |
| Opasnosti | |
| NFPA 704 | |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
DPPH је честа скраћеница за органско једињење 2,2-дифенил-1-пикрилхидразил. Представља тамни кристаласти прах кога чине стабилни слободни радикали. DPPH има две битне примене: праћење хемијских реакција слободних радикала и стандард позиције и интензитета ЕСР сигнала.
Својства и примена
[уреди | уреди извор]DPPH има неколико кристалних форми које се разликују по симетрији кристалне решетке и по тачки топљења. Комерцијални прах је мешавина фаза која се топи на око 130 °C. DPPH-I (т. т. 106 °C) је орторомбичан, DPPH-II (т. т. 137 °C) је аморфан и DPPH-III (т. т. 128–129 °C) је триклиничан.[3]
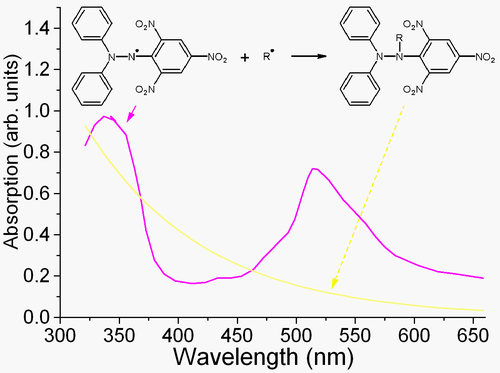
DPPH је позната замка ("хватач", scavenger) за друге радикале. Стога, брзина редукције при хемијској реакцији у којој учествује DPPH представља меру радикалске природе те реакције. Због оштрог пика апсорпције на 520 nm, DPPH радикал има тамно-љубичасту боју у раствору, а постаје безбојан или жут када се редукује (неутрализује). Ово својство омогућава визуелно праћење реакције, а број радикала на почетку може се утврдити по промени апсорбанце на 520 nm или по ЕСР сигналу DPPH радикала.[4]
Зато што је хватач радикала, он је јак инхибитор полимеризације слободнорадикалског механизма.[5]

Као стабилан и добро карактеризован чврст извор радикала, DPPH је традиционалан и можда најпопуларнији стандард (g-фактор) за позицију и интензитет ЕСР сигнала - број радикала у свеже припремљеном узорку може се одредити мерењем тежине и ЕСР фактор цепања за DPPH калибрисан на g = 2.0036. DPPH сигнал је погодан јер је обично концентрисан само у једној линији, чији интензитет се повећава линеарно са квадратним кореном микроталасне снаге у ширем опсегу. Разређена природа DPPH радикала (један неспарен електрон на 41 атом) даје релативно малу ширину спектралне линије (1.5–4.7 Гауса). Међутим, ширина линије се повећава ако молекули растварача остану у кристалу и ако су мерења рађена на високим фреквенцијама (~200 GHz), где мала g-анизотропија DPPH радикала постаје приметна.[6][7]
Иако је DPPH при нормалним условима парамагнетична чврста супстанца, прелази у антиферомагнетично стање при хлађењу на изузетно ниске температуре реда 0.3 K. Овај феномен је први пут уочио Александар Михајлович Прохоров 1963. године.[8][9][10][11]
Референце
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Kiers C. T.; De Boer J. L.; Olthof R.; Spek A. L. (1976). „The crystal structure of a 2,2-diphenyl-1-picrylhydrazyl (DPPH) modification”. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. 32: 2297. doi:10.1107/S0567740876007632.
- ^ Mark S. M. Alger (1997). Polymer science dictionary. Springer. стр. 152. ISBN 978-0-412-60870-4.
- ^ Cowie J. M. G.; Arrighi Valeria (2008). Polymers: Chemistry and Physics of Modern Materials (3rd изд.). Scotland: CRC Press. ISBN 978-0-8493-9813-1.
- ^ M.J. Davies (2000). Electron Paramagnetic Resonance. Royal Society of Chemistry. стр. 178. ISBN 978-0-85404-310-1.
- ^ Poole, Charles P. (1996). Electron spin resonance: a comprehensive treatise on experimental techniques. Courier Dover Publications. стр. 443. ISBN 978-0-486-69444-3.
- ^ A. M. Prokhorov and V.B. Fedorov, Soviet Phys. JETP 16 (1963) 1489.
- ^ Teruaki Fujito (1981). „Magnetic Interaction in Solvent-free DPPH and DPPH–Solvent Complexes”. Bulletin of the Chemical Society of Japan. 54 (10): 3110.[мртва веза]
- ^ Stig Lundqvist (1998). „A. M. Prokhorov”. Nobel lectures in physics, 1963-1970. World Scientific. стр. 118. ISBN 978-981-02-3404-1.
- ^ Aleksandr M. Prokhorov, The Nobel Prize in Physics 1964
Литература
[уреди | уреди извор]- Poole, Charles P. (1996). Electron spin resonance: a comprehensive treatise on experimental techniques. Courier Dover Publications. стр. 443. ISBN 978-0-486-69444-3.
- Stig Lundqvist (1998). „A. M. Prokhorov”. Nobel lectures in physics, 1963-1970. World Scientific. стр. 118. ISBN 978-981-02-3404-1.
- M.J. Davies (2000). Electron Paramagnetic Resonance. Royal Society of Chemistry. стр. 178. ISBN 978-0-85404-310-1.
- Cowie J. M. G.; Arrighi Valeria (2008). Polymers: Chemistry and Physics of Modern Materials (3rd изд.). Scotland: CRC Press. ISBN 978-0-8493-9813-1.
- Mark S. M. Alger (1997). Polymer science dictionary. Springer. стр. 152. ISBN 978-0-412-60870-4.