Neovaskularizacija
| Neovaskularizacija | |
|---|---|
 | |
| Klasifikacija i spoljašnji resursi | |
| eMedicine | oph/414 oph/415 |
| MeSH | D003930 |
Neovaskularizacija je proces formiranje mikrovaskularnih mreže novih krvnih sudova, u odraslih osoba, njihovim razgranavanjem i produžavanjem, iz već postojećih, prethodnom vaskulogenezom formiranih krvnih sudova.[1][2] Neovaskularizacija se razlikuje od angiogeneze u tome što angiogenezu uglavnom karakteriše nastank novih krvnih sudova iz izdanaka kapilarnih pupoljaka i klica već postojećih krvnih sudova. U oftalmologiji, horoidalna neovaskularizacija je formiranje novostvorene mikrovaskulaturne mreže, kao reakcija u pokušaju sanacije bolešću izazvane ishemije u unutrašnjem sloju horoideje ili sudovnjače, anatomskog sloja oka bogatog mikrovaskularnom mrežom krvnih sudova. Uobičajenih uzroci neovaskularizacije na mrežnjači (retini) ili u blizini optičkog diska oka su, šećerna bolest, okluzija retinalne vene, i zračenje. Neovaskularizacija može da bude i prateća pojava, nakon operativnih zahvata (npr na krvnim sudovima udova),[3] patoloških stanja kod hronične upale, uključujući psorijazu, reumatoidni artritis i granulomatozna oboljenja.[4]
Osnove postavke[uredi | uredi izvor]
Tri različita procesa mogu doprineti rastu novih krvnih sudova: vaskulogeneza, arteriogeneza i angiogeneza.[5][6]
Vaskulogeneza[uredi | uredi izvor]
Vaskulogeneza, je primarni proces odgovoran za rast novih krvnih sudova tokom embrionalnog razvoja [7] i ima još uvek nedefinisanu ulogu u zrelem odraslim tkivima.[8][9] Odlikuje se diferencijacijom pluripotentnih endotelnih ćelija prekursora (hemangioblasta ili sličnih ćelija) u endotelne ćelije koje utiču na formiranje primitivnih krvinih sudova. Naknadnim angažovanjem drugih tipova vaskularnih ćelija završava se proces formiranja krvnog suda.[7]
Arteriogeneza[uredi | uredi izvor]
Arteriogeneza se odnosi na pojavu novih arterija koje poseduju u potpunosti razvijenu tuniku mediju.[10] Proces može da podrazumeva sazrevanje postojećih kolaterala ili se može odraziti na formiranje novih zrelih krvnih sudova. Primeri uključuju arteriogenezom formirane, angiografski vidljive kolaterala kod pacijenata sa naprednim opstruktivnim koronarnim ili perifernim bolestima krvnih sudova. U ovaj proces uključeni su svi vaskularni tipovi ćelija, uključujući i glatke mišićne ćelije i pericite.
Angiogeneza[uredi | uredi izvor]
Angiogeneze je proces odgovoran za formiranje novih krvnih sudova u kojima nedostaje razvijena medija.[5] Primeri angiogeneze su kapilarna proliferacija u zarastanju rana ili duž granice srčanog mišića (miokarda).
Niže navedena tabela daje pregled bioloških efekata ova 3 procesa;
| - | Vaskulogeneza | Arteriogeneza | Angiogeneza |
|---|---|---|---|
| Tip ćelija uključen u proces | |||
| Primarni podsticaj | |||
| Krajnji rezultat | |||
| Javlja se kod zrelih tkiva | |||
| Doprinos efikasnoj perfuziji | |||
| Faktora rasta koji su uključeni |
Mehanizmi neovaskularizacije[uredi | uredi izvor]
Istovremena pojava angiogeneze i arteriogeneze nedvosmisleno je dokazana na različitim životinjskim modelima,[11][12] kao i kod pacijenata sa koronarnom bolešću.[13] [14]
Pojava vaskulogeneze u zrelim organizmima ostaje nerešeno pitanje. Prema dosadašnjim istraživanjima smatra se da je malo verovatno da ovaj proces značajnije doprinosi da se novi krvni sudovi razvijaju ako se taj proces javlja spontano, kao odgovor na ishemiju ili zapaljenja[15] ili kao odgovor na stimulišuće faktore. Tkiva ishemije po sebi ne može biti ključni podsticaj pokretanja angiogenetskog odgovor. Nekoliko pacijenata pokazalo je tu mogućnost u toku hronične ishemije miokarda, ali ne i većina pacijenata sa difuznim mnogostrukim bolestima krvnih sudova kod kojih se ne razvija ishemija na nivou tkiva u odsustvu provokacije. Upala i stres može biti mnogo izraženiji nadražaj,[16][17] i zato se jako mali broj angiogeneze odvija u odsustvo upale.[15] Suzbijanje inflamatornih odgovora, zbog genetskih abnormalnosti, patofiziološkim procesima, ili lekova, može negativno uticati na sposobnost tkiva da se u njima izazove rast novih krvnih sudova.[15][18]
Postavlja se još jedno značajno pitanje je da li će neishemični miokard odgovoriti na stimulaciju faktorima rasta? Značajan broj podataka iz literature ukazuje da neishemična tkiva u velikoj meri reaguju na angiogenične stimulanse. To može da dovede ne tako često do nedostatka endogenog faktora rasta, ili da se promeni u ekstracelularnom matriksu, prisustvo inhibitora endogena, kao što su angiopoetin–2, i odsustvo ekspresije receptora faktora rasta i drugih signalizirajućih molekula koji su uključeni u angiogenetsku signalizaciju.[15]
Značaj prožetosti tkiva neovaskularizacijom[uredi | uredi izvor]
U većini tkiva ugrađen je mehanizam koji održava prožetost tkiva krvnim sudovima, na tačno onom nivou koja je potrebna da se zadovoljivi metabolička potreba tkiva.
| „ | Kao opšte pravilo u fiziologiji vlada da je prožetost krvnim sudovima većine tkiva u organizmu direktno srazmerna lokalnom metabolizmu.[19] | ” |
Kada god se ova konstanta proporcionalno promeni dugoročno će lokalni regulacioni mehanizmi, tokom kraćeg ili dužeg vremena, pokušati da automatski podese nivo prožetosti krvnim sudovima. Kod mladih osoba ova podešavanja su veoma tačna, dok su kod starijih ljudi ona samo delimična, a u pojedinim bolestima nepoželjna.[19]
Poseban značaj neovaskularizacija ima u patološkim stanjima, kao što je to npr. kod šećerna bolesi. Kontinuirano i dugotrajno trajanje i neprestano uvećanje ishemije mrežnjače u šećernoj bolesti pokreće proizvodnju vazoproliferativnih faktora koji stimulišu formiranje (neoangiogenezu) novih krvnih sudova. Ekstracelularni matriks krvnih sudova prvo razara proteaza, a novi kapilari koji proizilaze uglavnom iz venula mrežnjače, prodiru u njenu unutrašnju membranu i formiraju kapilarnu mrežu između unutrašnje površine mrežnjače i njenog zadnjeg hijaloidnog dela.[20]
Najnovijim istraživanjima utvrđeno je da kod bolesnika sa proliferativnom dijabetesnom retinopatijom (PDR), noćna, intermitentna hipoksija/reoksigenacija, koja nastaje u snu zbog poremećaja disanja može biti jedan od faktor rizika za dužičnu i/ili ugaonu neovaskularizaciju.[21]
Neovaskularizacija je najizraženija na granici perfuzije i neperfuzije mrežnjače najčešće se javlja duž vaskularnog luka i na glavnom optičkom nervu. Novostvoreni krvni sudovi probijaju i rastu duž površine mrežnjače u skleru i zadnji hijaloidni deo. Sami po sebi, ovi krvni sudovi retko izazvaju vidne ispade, ali su zbog krhkosti veoma popustljivi i lako se mogu prekinuti u staklastom telu, što može dovesti do krvarenja u šupljinu staklastog tela ili preretinalni prostor.[22]
Neovaskularizacijom stvoreni novi i umnoženi krvni sudovi u početku su povezani malom količinom fibroglijalne supstance u formiranom fibroblastnom tkivu. Međutim, kako se gustina neovaskularizovanog dela povećava, tako raste i nivo vlaknastog oblikovanja tkiva.[23]
U kasnijim fazama šećerne bolesti, umnožavanje (neovaskularizacija) krvnih sudova mrežnjače može nazadovati, ostavljajući za sobom samo mrežu fibrovaskularnog tkiva u slojevima mrežnjače i zadnjem hijaloidnom sloju. U staklastom telu ovo novostvoreno fibroblastno tkivo može da vrši, trakcionim silama, povlačenje mrežnjače preko fibroglijalnih veza. Proklizavanje može izazvati edem mrežnjače, heterotropiju mrežnjače i obostrano trakciono odignuće (odlubljivanje) mrežnjače od pigmentnog epiteta.[24]
Izvori[uredi | uredi izvor]
- ^ a b M, Simons; Bonow RO; NA, Chronos (12. 9. 2000). „Clinical trials in coronary angiogenesis: issues, problems, consensus: An expert panel summary”. Circulation. 102 (11): E73—86. PMID 10982554. Arhivirano iz originala 10. 07. 2012. g. Pristupljeno 18. 6. 2009.
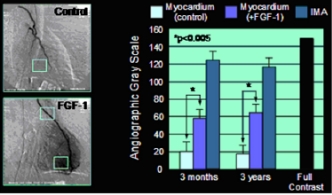
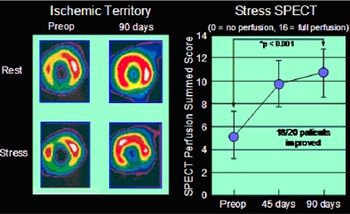
- ^ Stegmann, T.J., Hoppert, T., Schneider, A., Popp, M., Strupp, G., Ibing, R.O., Hertel, A.: Therapeutic angiogenesis: intramyocardial growth factor delivery of FGF-1 as sole therapy in patients with chronic coronary artery disease. CVR. 2000; 1: 259-267.
- ^ Myreel Maren Marklewitz (2011). Neovascularisation After Surgery for Recurrent Saphenofemoral Incompetence: Does Surgical Dissection Technique Matter? : a Randomised Controlled Trial.
- ^ Karen S. Moulton, Khashayar Vakili§, David Zurakowski, Mohsin Soliman, Catherine Butterfield, Erik Sylvin, Kin-Ming Lo, Inhibition of plaque neovascularization reduces macrophage accumulation and progression of advanced atherosclerosis pp. 4736–4741, PNAS April 15, (2003) vol. 100, no.8 [1] Arhivirano na sajtu Wayback Machine (24. septembar 2015) Pristupljeno 15.1.2014.
- ^ a b Ware JA, Simons M. Angiogenesis in ischemic heart disease. Nat Med. 1997;3:158 –164.
- ^ Ferrara N, Alitalo K. Clinical applications of angiogenic growth factors and their inhibitors. Nat Med. 1999;5:1359 –1364.
- ^ a b Beck L Jr, D’Amor e PA. Vascul ardeve lopment: cellular and molecular regulation. FASEB J. 1997;11:365–373.
- ^ Asahara T, Masuda H, Takahashi T, et al. Bone marrow origin of endothelial progenitor cells responsible for postnatal vasculogenesis in physiological and pathological neovascularization. Circ Res. 1999; 85:221–228.
- ^ Asahara T, Takahashi T, Masuda H, et al. VEGF contributes to postnatal neovascularization by mobilizing bone marrow-derived endothelial progenitor cells. EMBO J. 1999;18.
- ^ Buschmann I, Schaper W. The pathophysiology of the collateral circulation (arteriogenesis). J Pathol. 2000;190:338 –342.
- ^ White F, Carroll S, Magnet A, et al. Coronary collateral development in swine after coronary arteryocclusion. Circ Res. 1992;71: 1490 –1500.
- ^ Wolf C, Cai WJ, Vosschulte R, et al. Vascular remodeling and altered protein expression during growth of coronary collateral arteries. J Mol Cell Cardiol. 1998;30:2291–2305
- ^ Gibson CM, Ryan K, Sparano A, et al. Angiographic methods to assess human coronary angiogenesis. Am Heart J. 1999;137:169 –179.
- ^ Sasayama S, Fujita M. Recent insights into coronary collateral circulation. Circulation. 1992;85:1197–1204.
- ^ a b v g Seed & Walsh 2008, str. 90
- ^ Ito W, Arras M, Scholz D, et al. Angiogenesis but not collateral growth is associated with ischemia after femoral artery occlusion. Am J Physiol. 1997;273:H1255–H1265.
- ^ Li J, Post M, Volk R, et al. PR39, a peptide regulator of angiogenesis. Nat Med. 2000;6:49 –55.
- ^ Jones MK, Wang H, Peskar BM, et al. Inhibition of angiogenesis by nonsteroidal anti-inflammatory drugs: insight into mechanisms and implications for cancer growth and ulcer healing [see comments]. Nat Med. 1999;5:1418 –1423
- ^ a b Arnall Patz, Studies on retinal neovascularization, Friedenwald Lecture, Invest. Ophthalmol. Vis. Sci. September 1980 [2] Pristupljeno 15.1.2014.
- ^ Barchetta I, Riccieri V, Vasile M, et al. High prevalence of capillary abnormalities in patients with diabetes and association with retinopathy. Diabet Med. Sep 2011;28(9):1039-44. [Medline].
- ^ Shiba T, Takahashi M, Hori Y, Saishin Y, Sato Y, Maeno T. Relationship between sleep-disordered breathing and iris and/or angle neovascularization in proliferative diabetic retinopathy cases. Am J Ophthalmol. Apr 2011;151(4):604-9. [Medline].
- ^ Andou N. Clinical feature of central-type diabetic retinopathy and its management. Rinshou Ganka. 1988;42:763–766
- ^ Henkind P. Microcirculation of the peripapillary retina. Trans Am Acad Ophthalmol Otolaryngol. 1969;73:890–897
- ^ Valsania P, Warram JH, Rand LI, Krolewski AS. Different determinants of neovascularization on the optic disc and on the retina in patients with severe nonproliferative diabetic retinopathy. Arch Ophthalmol. 1993;111:203–206
Literatura[uredi | uredi izvor]
- Myreel Maren Marklewitz (2011). Neovascularisation After Surgery for Recurrent Saphenofemoral Incompetence: Does Surgical Dissection Technique Matter? : a Randomised Controlled Trial.
- Joyce Tombran-Tink; Barnstable, Colin J. (2007). Ocular Angiogenesis: Diseases, Mechanisms, and Therapeutics. Springer. ISBN 978-1-59745-047-8.
- Reddy U, Krzystolik M (2006). Antiangiogenic therapy with interferon alfa for neovascular age-related macular degeneration. Cochrane Database Syst Rev (1): CD005138.
Spoljašnje veze[uredi | uredi izvor]
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |