Трансестерификација
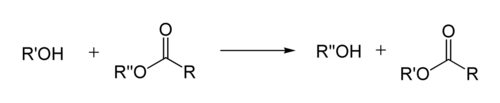
У органској хемији, трансестерификација је процес замене органске групе естра R са органском групом алкохола R′. Ове реакције су често катализоване додавањем киселине или базног катализатора. Реакција се такође може постићи уз помоћ ензима (биокатализатори), посебно липазе.
Механизам
[уреди | уреди извор]Механизам трансестерификације почиње тиме што кисеоник из алкил групе, нападне водоник из друге супстанце сложене структуре. Реакција је повратна, па се може десити да ће се супстанца вратити на претходни корак или настати супстанца која садржи парцијално позитиван угљеник и позитивно наелектрисан OH+ јон. То је врло неповољно и нестабилно стање, па се алкохол, додаје како би кисеоник из алкохола напао угљеник. Ово је такође повратна реакција и како би се повећала вероватноћа судара угљеника са кисеоником, потребно је ставити размеру са већим уделом кисеоника, односно алкохола и управо зато се алкохол тада ставља у вишку. Након тога настаје структура са једном OH групом, две алкил групе, и једним позитивно наелектрисаним алкохолом, са наелектрисањем на кисеонику. Како би постигао стабилност, одузима се H+ јон и настаје нова релативно нестабилна структура. Постигла се стабилност OH јона, поред тога је стабилна и једна алкил група, док су нестабилни алкокси и метокси групе нестабилне.

С обзиром да се цео процес трансестерификације одиграва у киселој средини, један водоник се веже за алкокси групу, која се хомолитичко формира у алкохол. С друге стране, угљеник који је био парцијално наелектрисан, постаје потпуно наелектрисан са три везе, што је за њега врло неповољно, па се наелектрисање пребацује на OH јон који тада постаје позитино наелектрисан. Како би он постигао стабилност, кисеоник отпушта водоник и настаје двострука веза. Коначан производ трансестерификације је естар.
