Алкохол


У хемији, алкохол је органско једињење у коме је хидроксилна функционална група (-O H) везана за засићени атом угљеника.[2][3] Општа формула алкохола је R-O H, дакле хидроксилна група O H, везана на алкан тј. ланац угљоводоници. Сличну структуру имају карбоксилне киселине које се добијају оксидацијом алкохола. Хидроксилна група (функциона група) се састоји од једног атома водоника и једног атома кисеоника, према томе је једновалентна. Зато и ланац на који се група везује мора да буде једновалентан. Тако ће нпр. сажета структурна формула етанола да буде CH3-CH2-OH. Термин алкохол се првобитно односио на примарни алкохол етил алкохол (етанол), који је преовлађујући алкохол у алкохолним пићима.
Суфикс -ол се јавља у IUPAC хемијским именима[4] свих супстанци у којима је хидроксилна група функционална група са највишим приоритетом; у супстанцама где је присутна група вишег приоритета користи се префикс хидрокси- у IUPAC именима. Суфикс -ол у несистематским именима (као што је парацетамол[5][6] или холестерол[7]) такође типично указује на присуство хидроксилне групе у супстанци, и оне се стога могу назвати алкохолима. Међутим многе супстанце, посебно шећери (на пример глукоза[8] и сахароза[9]) садрже хидроксилне функционалне групе, а суфикс се не користи. Једна важна класа алкохола, чији најједноставнији чланови су метанол и етанол, су алкохоли са засићеним неразгранатим ланцом. Њихова општа формула је CnH2n+1OH.
Подела алкохола[уреди | уреди извор]
- Према броју OH група
- Монохидроксилни (1 OH група)
- Двохидроксилни (2 OH групе)
- Полихидроксилни (3 или више OH група)
- Према начину везивања угљеникових атома
- Алифатичне R-OH алкил група
- Ароматични AR-CN2OH арил група
- Према положају алкил групе
- Примарни CH3-CH2-OH (10)
- Секундарни CH3-CH-CH3 (20)
- Терцијарни
Особине[уреди | уреди извор]
У хомологном низу примарних алкохола нижи су чланови (прва четири) течности, средњи (до 11 угљикових атома), уљасте течности, а виши су чврсте материје.
Нижи алкохоли се мешају се с водом, виши се у води уопште не растварају. С киселинама дају естре, с алкалијским растворима алкоксиде, а оксидацијом прелазе у алдехиде, кетоне и органске киселине. Алкохоли који у својој структури имају већи број C атома су нерастворни у води јер имају дужи део молекулске неполарне грађе.
Алкохоли имају врло сличну структуру као вода. Тачка кључања етанола и воде је виша него што одговара њиховој релативној молекулској маси.
Неутралне течности, могу реаговати с алкалним металима, натријумом или калијумом. У тој реакцији настају алкосиди. Реакција алкохола с халогеноводичном киселином настају алкил-халогениди.
Алкохоли се с обзиром на положај OH групе деле на примарне, секундарне и терцијарне алкохоле. Примарни алкохоли су алкохоли чија је -OH група везана за примарни атом угљеника, тј. онај који је у структури везан са само једним другим атомом угљеника. Оксидацијом примарних алкохола добијају се алдехиди, а оксидацијом секундарних алкохола настају кетони.
Најпознатији алкохол који се користи у медицини и пићу је обични алкохол. Хемијска реакција за добијање етанола је алкохолно врење (ферментација). То је природни процес којим се шећер уз помоћ деловања квашчевих гљивица (ензима који делују као катализатори) претвара у етанол и CO2.
Номенклатура алкохола[уреди | уреди извор]
Алкохоли се именују тако да се уз име алкана дода наставак -ол. Тако ће нпр. алкохол с три угљеникова атома да буде пропанол, јер се уз име алкана пропана додао ол од алкохола.
Уколико неки алкохол има две или више хидроксилних група, онда се испред наставка 'ол' додаје ди, три итд. Нпр. пропандиол, пропантриол.
Напомена: У ситуацијама када алкохол има већи број угљеникових атома, мора се напоменути на ком се угљениковом атому налази хидроксилна група. Нпр. 2-бутанол, 3-пентанол итд.

Систематска имена[уреди | уреди извор]
IUPAC номенклатура се користи у научним публикацијама и кад год је прецизна идентификација супстанце важна, посебно у случајевима где релативна комплексност молекула не чини таква систематска имена непрактичним. У IUPAC систему, при именовању једноставних алкохола се на име алканског ланца додаје „ол“, нпр., као код имена „метанол“ и „етанол“.[10] Кад је то неопходно, позиција хидроксилне групе се обележава бројем између имена алкана и „ол“: пропан-1-ол за CH3CH2CH2OH, пропан-2-ол за CH3CH(OH)CH3. Ако је присутна група вишег приоритета (као што је алдехидна, кетонска, или карбоксилна), користи се префикс „хидрокси“,[10] нпр., као у 1-хидрокси-2-пропанон (CH3C(O)CH2OH).[11]
Несистематска имена[уреди | уреди извор]
У другим мање формалним контекстима, алкохол се обично назива именом које кореспондира алкил групи чему следи реч „алцохол“, нпр., метил алкохол, етил алкохол. Пропил алкохол може да буде н-пропил алкохол или изопропил алкохол, у зависности од тога да ли је хидроксилна група везана на крају или у средини линијског пропанског ланца. Као што је то описано у секцији о систематским именима, ако друга група у молекулу има приоритет, алкохолна група се обично означава префиксом „хидрокси“-.
| Хемијска формула | IUPAC име | Несистемско име |
|---|---|---|
| Monohidroksilni alkoholi | ||
| CH3OH | Метанол | Дрвни алкохол |
| C2H5OH | Етанол | Алкохол |
| C3H7OH | Изопропил алкохол | Дезинфекциони алкохол |
| C4H9OH | Бутил алкохол | Бутанол |
| C5H11OH | Пентанол | Амил алкохол |
| C16H33OH | Хексадекан-1-ол | Цетил алкохол |
| Полихидроксилни алкохоли | ||
| C2H4(OH)2 | Етан-1,2-диол | Етилен гликол |
| C3H6(OH)2 | Пропан-1,2-диол | Пропилен гликол |
| C3H5(OH)3 | Пропан-1,2,3-триол | Глицерол |
| C4H6(OH)4 | Бутан-1,2,3,4-етраол | Еритритол, Треитол |
| C5H7(OH)5 | Пентан-1,2,3,4,5-пентол | Ксилитол |
| C6H8(OH)6 | Heksan-1,2,3,4,5,6-heksol | Manitol, Sorbitol |
| C7H9(OH)7 | Хептан-1,2,3,4,5,6,7-хептол | Волемитол |
| Незасичени алифатични алкохоли | ||
| C3H5OH | Проп-2-ен-1-ол | Алил алкохол |
| C10H17OH | 3,7-Диметилокта-2,6-диен-1-ол | Гераниол |
| C3H3OH | Проп-2-ин-1-ол | Пропаргил алкохол |
| Алициклични алкохоли | ||
| C6H6(OH)6 | Циклохексан-1,2,3,4,5,6-хексол | Инозитол |
| C10H19OH | 2 - (2-пропил)-5-метил-циклохексан-1-ол | Ментол |
Алкохоли се групишу у примарне, секундарне (sec-, s-), и терцијарне (tert-, t-), по броју атома угљеника везаних за атом угљеника који носи хидроксилну функционалну групу. (Одговарајуће нумеричке скраћенице 1°, 2°, и 3° се такође користе у неформалним ситуацијама.[12]) Примарни алкохоли имају опште формуле RCH2OH; метанол (CH3OH је најједноставнији примарни алкохол (R=H), и након њега долази етанол (R=CH3). Секундарни алкохоли се могу скраћено описати формулом RR'CHOH; 2-пропанол је најједноставнији пример (R=R'=CH3). Терцијарни алкохоли се могу описати скраћеницом RR'R"COH; terc-бутанол (2-метилпропан-2-ол) је најједноставнији пример (R=R'=R"=CH3). У тим скраћеним записима, R, R', и R" представљају супституенте, алкилне или друге везане, генерално органске групе.
Варијације алкил ланца у алкохолима[уреди | уреди извор]
Кратколанчани алкохоли имају алкил ланце са 1-3 угљеника. Алкохоли средњих дужина ланца имају алкил групе са 4-7 угљеника. Дуголанчани алкохоли (такође познати као масни алкохоли) имају алкил ланце са 8-21 угљеника, и алкохоли са веома дугим ланцима имају алкил групе са 22 или више угљеника.[13]
Једноставни алкохоли[уреди | уреди извор]
Термин "једноставни алкохоли" нема једнозначну дефиницију. Имена једноставних алкохола се обично формирају додавањем речи „алкохол“ на име одговарајуће алкил групе. На пример, ланац који садржи један угљеник (метил групу, CH3) са OH групом везаном за угљеник се назива „метил алкохол“, док се ланац са два уљеника (етил групом, CH2CH3) са OH групом везаном за CH2 назива „етил алкохол“. За комплексније алкохоле је неопходно користити IUPAC номенклатуру.[14]
Једноставни алкохоли, а посебно етанол и метанол, поседују денатурациона и дезинфекциона својства, те се користе као анти-микробни агенси у медицини, фармацији, и индустрији.
Виши алкохоли[уреди | уреди извор]
Енциклопедија Британница износи, „Виши алкохоли - они који садрже 4 до 10 атома угљеника – су умерено вискозни, или уљасти, и имају воћне мирисе. Неки од високо разгранатих алкохола и многи алкохоли који садрже више од 12 атома угљеника су чврсте материје на собној температури.“[15]
Попут етанола, бутанол се може произвести путем процеса ферментације. Познато је да квасац Saccharomyces производи више алкохоле на температурама изнад 24 °C. Бактерија Clostridium acetobutylicum може да се храни целулозом и да производи бутанол у индустријским размерама.
Вино и ферментација[уреди | уреди извор]

Виноградарство је грана пољопривреде која постоји од давнина, а култура производње вина одржала се вековима. Процес производње вина је следећи: Убрано грожђе из винограда се прво гази тако да се исцеди сок а доцније се љуска дели од течности (Љуска може да се искористи за прављење ракије или сл.). Течност - "мошт" (која је већим постотком шећер) се оставља у буради где на одређеној температури уз дејствовање квашчевих гљивица ферментује (догађа се алкохолно врење или ферментација). Тако се шећер претвара у алкохол и течност постаје вино. Напомена: Неколико седмица пре процеса траје период каренце. У том се периоду грожђе не сме да се прска отровима јер би на тај начин доспели у вино.
Продукција[уреди | уреди извор]
Циглеров и оксо процеси[уреди | уреди извор]
У Циглеровом процесу, линеарни алкохоли се производе из етилена и триетилалуминијума, чему следе оксидација и хидролиза.[16] Идеализована синтеза 1-октанола је:
- Al(C2H5)3 + 9 °Csub>2H4 → Al(C8H17)3
- Al(C8H17)3 + 3 O + 3 H2O → 3 HOC8H17 + Al(OH)3
Процес генерише опсег алкохола који се раздвајају дестилацијом.
Многи виши алкохоли се производе путем хидроформилације алкена, чему следи хидрогенација. Кад се процес примени на терминалне алкене, као што је то најчешће случај, типично се добија линеарни алкохол:[16]
- RCH=CH2 + H2 + CO → RCH2CH2CHO
- RCH2CH2CHO + 3 H2 → RCH2CH2CH2OH
Такви процеси производе масне алкохоле, који су корисни при формирању детерџената.
Хидрационе реакције[уреди | уреди извор]
Индустријски важни алкохоли ниске молекулске тежине се производе адицијом воде у алкене. Етанол, изопропанол, 2-бутанол, и терт-бутанол се производе овом општом методом. Користе се два приступа: директни и индиректни методи. Директни метод избегава формирање стабилних интермедијера, типично користећи киселе катализаторе. У индиректном методу, алкен се конвертује до сулфатног естра, који се субсеквентно хидролизује. Директна хидрација користи етилен (етиленска хидрација)[17] или друге алкене из фракција крековања дестиловане сирове нафте.
Хидрација се такође индустријски користи у продукцији диола етилен гликола из етилен оксида.
Биолошки приступи[уреди | уреди извор]
Етанол се добија ферментацијом глукозе произведене хидролизом скроба, у присуству квасца на температури испод 37 °C. На пример, такав процес се може одвијати путем конверзије сахарозе ензимом инвертаза до глукозе и фруктозе, и затим конверзијом глукозе ензимом зимаза до етанола (и угљен-диоксида).
Неколико бенигних типова бактерија у интерстиналном тракту користи ферментацију као облик анаеробног метаболизма. Ова метаболичка реакција производи етанол као нуспроизвод, као што и аеробна респирација производи угљен-диоксид и воду. Стога, људска тела садрже извесну количину алкохола који ендогено производе ове бактерије. У ретким случајевима, то може да буде довољно да узрокује "синдром ауто-врења" услед кога се производе интоксинирајуће количине алкохола.[18][19][20]
Лабораторијска синтеза[уреди | уреди извор]
Постоји неколико метода за лабораторијску припрему алкохола.
Супституција[уреди | уреди извор]
Примарни алкил халиди реагују са воденим раствором NaOH или KOH углавном као примарни алкохоли у нуклеофилној алифатичној супституцији. (Секундарни и посебно терцијарни алкил халиди уместо тога производе елиминационе (алкенске) продукте). Грињарови реагенси реагују са карбонил групама до секундарних и терцијарних алкохола. Сродне реакције су Барбијерова реакција и Нозаки-Хијамина реакција.
Редукција[уреди | уреди извор]
Алдехиди или кетони се редукују са натријум борохидридом или литијум алуминијум хидридом (након киселинске припреме). Редукција се може обавити алуминијумизопропилатима у Meerwein-Ponndorf-Verley редукцији. Нојоријева асиметрична хидрогенација је асиметрична редукција β-кето-естера.
Хидролиза[уреди | уреди извор]
Алкени учествују у киселином катализованој реакцији хидратације користећи концентровану сумпорну киселину као катализатор, која обично даје секундарне или терцијарне алкохоле. Хидроборација-оксидација и оксимеркурација-редукција алкена су поузданији процеси органске синтезе. Алкени реагују са NBS и водом у реакцији формирања халохидрина. Амини се могу конвертовати до диазонијум соли, које се затим хидролизују.
Формирање секундарног алкохола путем редукције и хидрације:
Реакције[уреди | уреди извор]
Депротонација[уреди | уреди извор]
Алкохоли се могу понашати као слабе киселине, при чему подлежу депротонацији. Реакција депротонације којом се производе алкоксидне соли се изводи било са јаком базом, као што је натријум хидрат или n-бутиллитијум, или са металом натријум или калијум.
- 2 R-OH + 2 Na → 2 R-O−Na+ + H2
- 2 CH3CH2-OH + 2 Na → 2 CH3-CH2-O−Na+ + H2↑
Вода има сличну pKa вредност са многим алкохолима, тако да се са натријум хидроксидом остварује равнотежа, која је обично померена налево:
- R-OH + NaOH ⇌ R-O−Na+ + H2O
Потребно је напоменути да су базе које се користе за депротонацију алкохола јаке. Те базе и формирани алкоксиди су веома сензитивни на влагу.
На киселост алкохола такође утиче свеукупна стабилност алкоксидног јона. Електрон-одвлачеће групе везане за угљеник који садржи хидроксилну групу стабилизују формирани алкоксид, што доводи до повећане киселости. С друге стране, присуство електрон-донирајуће групе доводи до формирања мање стабилног алкоксидног јона. То ће резултирати у сценарију где формирани нестабилни алкоксидни јон тежи да прими протон и да се претвори у оригинални алкохол.
Са алкил халидима алкоксиди формирају етре путем Вилијамсонове етарске синтезе.
Нуклеофилна супституција[уреди | уреди извор]
OH група није добра одлазећа група у реакцијама нуклеофилне супституције, тако да неутрални алкохоли не реагују у таквим реакцијама. Међутим, ако се кисеоник прво протонира и формира Р−ОХ2+, одлазећа група (вода) је далеко стабилнија, и нуклеофилна супституција се може одвијати. На пример, терцијарни алкохоли реагују са хлороводоничном киселином и производе терцијарне алкил халиде, при чему се хидроксилна група замењује атомом хлора путем унимолекуларне нуклеофилне супституције. Да би примарни и секундарни алкохоли реаговали са хлороводоничном киселином, потребан је активатор као што је цинк хлорид. Алтернативно, конверзија се може извршити директно користећи тионил хлорид.[21][22][23]
Слично томе, алкохоли се могу конвертовати у алкил бромиде користећи бромоводоничну киселину или фосфор трибромид, на пример:
- 3 R-OH + PBr3 → 3 RBr + H3PO3
У Бартон-Макомбијевој деоксигенацији алкохол се деоксигенише до алкана са трибутилкалај хидридом или комплексом триметилборан-воде у реакцији супституције радикала.
Дехидрација[уреди | уреди извор]
Сами алкохоли су нуклеофилни, тако да R−OH2+ може да реагује ROH и да произведе етре и воду у реакцији дехидрације, мада се та реакција ретко користи изузев у производњи диетил етра.
Кориснија је Е1 елиминациона реакција алкохола којом се производе алкени. Реакција генерално подлеже Зајцевљевом правилу, по коме се најстабилнији (обично у највећој мери супституисани) алкен формира. Терцијарни алкохоли лако врше елиминацију на температурама непосредно изнад собне, док су примарним алкохолима неопходне више температуре.
Ово је дијаграм киселином катализоване дехидрације етанола којом се производи етен:
Боље контролисана реакција елиминације је Чугајева елиминација са угљен дисулфидом и јодометаном.
Естерификација[уреди | уреди извор]
Естар се формира из алкохола и карбоксилне киселине применом Фишерове естерификације. Она се обично изводи путем рефлуксирања са концентрованом сумпорном киселином као катализатором:
- R-OH + R'-COOH → R'-COOR + H2O
Да би се равнотежа померила надесно и произвели добри приноси естра, вода се обично уклања, било путем вишка H2SO4 или користећи Деан-Старков апарат. Естри се такође могу припремити реакцијом алкохола са киселим хлоридима у присуству базе као што је пиридин.
Други типови естара се припремају на сличан начин – на пример, тозил (тозилатни) естри се формирају реакцијом алкохола са p-толуенсулфонил хлоридом у пиридину.
Оксидација[уреди | уреди извор]
Примарни алкохоли (R-CH2-OH) се могу оксидовати било до алдехида (R-CHO) или до карбоксилних киселина (R-CO2H), док се оксидација секундарних алкохола (R1R2CH-OH) нормално завршава на кетонима (R1R2C=O). Терцијарни алкохоли (R1R2R3C-OH) су отпорни на оксидацију.
Директна оксидација примарних алкохола до карбоксилних киселина се нормално одвија путем кореспондирајућих алдехида, који се трансформишу преко алдехидног хидрата (R-CH(OH)2) реакцијом са водом, пре даље оксидације до карбоксилне киселине.
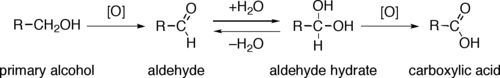
Реагенси који су корисни при трансформацији примарних алкохола до алдехида су нормално подесни и за оксидацију секундарних алкохола до кетона. То су Колинсов реагенс и Дес–Мартинов перјодинан. Директна оксидација примарних алкохола до карбоксилних киселина се може одвијати користећи калијум перманганат или Џонсов реагенс.
Види још[уреди | уреди извор]
Референце[уреди | уреди извор]
- ^ „alcohols”. IUPAC Gold Book. Приступљено 16. 12. 2013.
- ^ Мишић, Милан, ур. (2005). Енциклопедија Британика. А-Б. Београд: Народна књига : Политика. стр. 35. ISBN 86-331-2075-5.
- ^ IUPAC. „Alcohols”. Kompendijum hemijske terminologije (Internet izdanje).
- ^ Nomenclature of Organic Chemistry, Oxford: Pergamon Press, 1979; A Guide to IUPAC Nomenclature of Organic Compounds, Recommendations 1993, Oxford: Blackwell Scientific Publications, 1993.
- ^ Aghababian 2010, стр. 814
- ^ Ahmad 2010, стр. 194
- ^ Behrman & Gopalan 2005, стр. 1791.
- ^ Medical Biochemistry at a Glance @Google books, Blackwell Publishing, 2006, стр. 52, ISBN 978-1-4051-1322-9
- ^ Miller, William Allen (1857). Elements of chemistry pt. 3 1857. J.W. Parker and Son. стр. 52—54.
- ^ а б Reusch, William. „Alcohols”. VirtualText of Organic Chemistry. Архивирано из оригинала 19. 9. 2007. г. Приступљено 14. 9. 2007.
- ^ Organic chemistry IUPAC nomenclature. Alcohols Rule C-201.
- ^ Reusch, William (2. 10. 2013). „Nomenclature of Alcohols”. Приступљено 17. 3. 2015.
- ^ „MetaCyc Compound Class: a short-chain alcohol”. Приступљено 31. 12. 2013.
- ^ „Molecule Gallery - Alcohols”. Архивирано из оригинала 19. 04. 2015. г. Приступљено 31. 12. 2013.
- ^ „alcohol (chemical compound)”. Encyclopædia Britannica. Приступљено 31. 12. 2013.
- ^ а б Falbe, Jürgen; Bahrmann, Helmut; Lipps, Wolfgang; Mayer, Dieter (2000). „Alcohols, Aliphatic”. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH Verlag. ISBN 3527306730. doi:10.1002/14356007.a01_279.
- ^ Lodgsdon J.E. (1994). „Ethanol”. Ур.: Kroschwitz J.I. Encyclopedia of Chemical Technology. 9 (4th изд.). New York: John Wiley & Sons. стр. 820. ISBN 978-0-471-52677-3.
- ^ M, P.. D.. Geertinger; Bodenhoff, J.; K. Helweg-Larsen; Lund, A. (1. 9. 1982). „Endogenous alcohol production by intestinal fermentation in sudden infant death”. Zeitschrift für Rechtsmedizin. Springer-Verlag. 89 (3): 167—172. PMID 6760604. S2CID 29917601. doi:10.1007/BF01873798.
- ^ Logan BK, Jones AW (2000). „Endogenous ethanol 'auto-brewery syndrome' as a drunk-driving defence challenge”. Medicine, Science, and the Law. 40 (3): 206—15. PMID 10976182. S2CID 6926029. doi:10.1177/002580240004000304.
- ^ Adams, Cecil (20. 10. 2006). „Designated drunk: Can you get intoxicated without actually drinking alcohol?”. The Straight Dope. Приступљено 27. 2. 2013.
- ^ Lewis, E.S.; Boozer, C.E. J. Am. Chem. Soc. 1952, 74, 308.
- ^ Cram, D. J., J. Am. Chem. Soc. 1953, 75, 332-338.
- ^ Lee, C. C. ; Clayton, J. W.; Lee, D. G.; Finlayson, A. J. Tetrahedron, 1962, 18 1395-1402
Литература[уреди | уреди извор]
- Miller, William Allen (1857). Elements of chemistry pt. 3 1857. J.W. Parker and Son. стр. 52—54.
- Ahmad, Jawad (2010). Hepatology and Transplant Hepatology: A Case Based Approach. Springer. стр. 194. ISBN 978-1-4419-7085-5.
- Lodgsdon J.E. (1994). „Ethanol”. Ур.: Kroschwitz J.I. Encyclopedia of Chemical Technology. 9 (4th изд.). New York: John Wiley & Sons. стр. 820. ISBN 978-0-471-52677-3.
- Aghababian, Richard V. (2010). Essentials of Emergency Medicine. Jones & Bartlett Publishers. стр. 814. ISBN 978-1-4496-1846-9.
- Metcalf, Allan A. (1999). The World in So Many Words. Houghton Mifflin. ISBN 978-0-395-95920-6.
- Edited by Shelley Minteer, ур. (2006). Alcoholic Fuels. Boca Raton: CRC Press / Taylor & Francis. ISBN 978-0-8493-3944-8.
- Jonathan Clayden, ур. (2008). Alcohols; Science of Synthesis: Houben-Weyl Methods of Molecular Transformations. 36. Georg Thieme Verlag. ISBN 978-1-588-90527-7.
- Editor: Richard G. Herman, ур. (1984). Catalytic Conversions of Synthesis Gas and Alcohols to Chemicals. American Chemical Society, Middle Atlantic Regional Meeting. Plenum Press. ISBN 978-0-306-41614-9.
- Mellan, I. (1962). Polyhydric Alcohols. Spartan Books.
- Monick J. A. (1968). Alcohols: Their Chemistry, Properties, and Manufacture. Reinhold. ISBN 978-0-442-15601-5.
- Edward J. Wickson, ур. (1981). Monohydric Alcohols: Manufacture, Applications, and Chemistry: based on a symposium. ACS symposium series (volume 159). American Chemical Society. ISBN 978-0-8412-0637-3.
- Otera, J.; Nishikido, J. (2010). Esterification: Methods, Reactions, and Applications (Second изд.). Weinheim: Wiley-VCH. ISBN 978-3-527-32289-3.
- Tojo, G.; Fernández, M. (2006). Oxidation of Alcohols to Aldehydes and Ketones (First изд.). New York: Springer. ISBN 978-0-387-23607-0.
- Weissermel, K.; Arpe H-J. (2003). Alcohols - Industrial organic chemistry (4th изд.). Weinheim: Wiley-VCH. стр. 193—266. ISBN 978-3-527-30578-0.
- С. М. Локтева, ур. (1970). Высшие жирные спирты (области применения, методы производства, физико-химические свойства). М.: «Химия». стр. 329.
- Курц, Л. А. Г.; Брусова, П.; Демьянович, М. В. (1999). „Одно- и двухатомные спирты, простые эфиры и их сернистые аналоги”. Учебные материалы. Органическая химия. ChemNet. Химический факультет МГУ. Архивирано из оригинала 04. 03. 2016. г. Приступљено 10. 7. 2010.
- Маркизова Н. Ф.; Гребенюк, Н. А..; Башарин, А. В..; Бонитенко, Ю. Е. (2004). Спирты. Токсикология для врачей. СПб.: «Фолиант». стр. 112. ISBN 978-5-93929-089-0.
- Реутов, А. О.; Курц, Л. А.; Бутин, П. К. (2010). Органическая химия. 2 (3-е изд.). М: Бином. Лаборатория знаний. ISBN 978-5-94774-614-9 Проверите вредност параметра
|isbn=: checksum (помоћ). - „Спирты”. Энциклопедия по охране и безопасности труда. Том IV. Раздел XVIII. Справочники. Обзор химических соединений. Институт промышленной безопасности, охраны труда и социального партнерства. Архивирано из оригинала 04. 03. 2016. г. Приступљено 27. 12. 2010.
Чланци[уреди | уреди извор]
- Behrman, E. J.; Gopalan, Venkat (2005). William M. Scovell, ур. „Cholesterol and Plants” (PDF). Journal of Chemical Education. 82 (12): 1791. Bibcode:2005JChEd..82.1791B. doi:10.1021/ed082p1791. Архивирано из оригинала (PDF) 21. 10. 2012. г. Приступљено 13. 02. 2017.
Спољашње везе[уреди | уреди извор]
- Alcohol (Ethanol) at The Periodic Table of Videos (University of Nottingham)
- Mitschnitte von Vorlesungen der Universität Tübingen, Experimentalchemie II, Organische Chemie.
- Schulversuche zum Thema Alkohole
- „Спирты. Фенолы”. Органическая химия. Видеоопыты. Единая коллекция цифровых образовательных ресурсов. Архивирано из оригинала 21. 8. 2011. г. Приступљено 06. 07. 2010.



