Nitrozil-hlorid
| |

| |
| Nazivi | |
|---|---|
| IUPAC naziv
Nitrozil-hlorid
| |
| Drugi nazivi
Nitrogen-oksihlorid
Nitrozonijum-hlorid | |
| Identifikacija | |
| ECHA InfoCard | 100.018.430 |
| Е-бројеви | E919 (glazing agents, ...) |
| MeSH | Nitrosyl+chloride |
| RTECS | QZ7883000 |
| UN broj | 1069 |
| Svojstva | |
| ClNO | |
| Molarna masa | 65,46 g/mol |
| Agregatno stanje | žuti gas, crvena tečnost |
| Gustina | 1,417 g/cm3 (течност, -12 °C) 2.99 g/L (гас) |
| Tačka topljenja | -59.6 °C |
| Tačka ključanja | -6.4 °C |
| razlaže se | |
| Rastvorljivost u hlorokarbonu | rastvorljiv |
| Struktura | |
| Oblik molekula (orbitale i hibridizacija) | sp2 za N |
| Dipolni moment | 1.90 D |
| Opasnosti | |
| Glavne opasnosti | Veoma otrovan |
| NFPA 704 | |
| Srodna jedinjenja | |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |
| Reference infokutije | |
Nitrozil-hlorid je hemijsko neorgansko jedinjenje hemijske formule ClNO.
Struktura molekula[uredi | uredi izvor]
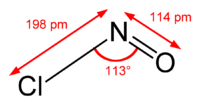
Iako se formula vrlo često piše NOCl, struktura se bolje prikazuje formulom ONCl. Između N i O postoji dvostruka veza (razdaljina = 1,16 Å), a između N i Cl postoji jednostruka (razdaljina = 1,69 Å). Ugao koji zaklapaju O-N-Cl iznosi 113°.[1]
Dobijanje[uredi | uredi izvor]
Može se dobiti na više načina[2]:
1. reakcijom azot-monoksida i hlora na običnoj temperaturi, uz drveni ugalj kao katalizator:
2. reakcijom fosfor-pentahlorida i kalijum-nitrita:
3. u carskoj vodi:
Fizička i hemijska svojstva[uredi | uredi izvor]
To je narandžastožut gas, koji se pretvara u crvenkastu tečnost na temperaturi od -5,5 °C, a pri -65 °C gradi kristale limun-žute boje.[3][4] Reaguje sa vodom gradeći kiseline:
Takođe, reaguje sa živom gradeći merkurohlorid i azot-monoksid, a gradi i dvoguba jedinjenja kao što je SnCl4•NOCl.[2]
Izvori[uredi | uredi izvor]
- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego. 2001. ISBN 978-0-12-352651-9..
- ^ a b Parkes, G.D. & Phil, D. 1973. Melorova moderna neorganska hemija. Naučna knjiga. Beograd.
- ^ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0911910131.





