Kancerski probijajući bol
| Kancerski probijajući bol | |
|---|---|
 | |
| Klasifikacija i spoljašnji resursi | |
| MKB-10 | R52 |
| MKB-9-CM | 338 |
| DiseasesDB | 9503 |
| MedlinePlus | 002164 |
| MeSH | D010146 |
Kancerski probijajući bol ili kancerski bol je prolazno pogoršanje bola u vidu naglih, kratkotrajnih i vrlo intenzivnih napada koji se javljaju spontano ili u sprezi sa specifičnim nepredvidivim ili predvidivim „okidačkim mehanizmom“, i pored relativno stabilnog, dobro kontrolisanog osnovnog (pozadinskog) bola. Za sve bolesnike sa kancerskom bolešću, probijajući bol je jedan od najčešćih sindroma izazvan tumorskom bolešću.[1] Tokom bolesti mnogi bolesnici sa karcinomom više strahuje od bola nego od same smrti, jer se ova vrsta bola javlja sa različiteom učestalošću i prilikom postavljanja dijagnoze maligne bolesti prisutna je u 25 do 50% slučajeva.[2][3]
Kod onkoloških bolesnika razlikujemo dve osnovne komponente bola: perzistentni (stalni) bol koji traje najmanje 12 sati tokom dana, i probijajući bol. Intenzitet probijajućeg bola je srednje jaki do jaki sa vrhuncem bola nakon tri do pet minuta, i prosečnim trajanjem oko 30 minuta. Kako bi se ova vrsta bola razlikovala od slabo kontrolisanog osnovnog bola, on se definiše kao: „četiri, ili manje, epizoda tokom 24 sata.“
Probijajući bol javlja se kao posledica različitih (neuropatskih, nociceptivnih ili kombinovanih) patofizioloških mehanizama. Prema dostupnim podacima iz literature incidenca probijajućeg bola kreće se između 40 i 86% (33% do 90%).[4] Istraživanja su pokazala da je on u 67-76% slučajeva uzrokovana samim zloćudnim rakom (tumorom), u 20-33% epizoda bol se javlja kao posledica onkološke terapije, dok je u oko 4% slučajeva probijajući bol nejasnog uzroka.[5][6]
Kancerski probijajuća bol najčešće se javlja kod bolesnika lečenih fiksnim dozama opioidnih analgetika, sa učestalšću od 13,2-33%.[7][8][9]
Istraživanja dokazuju da i pored savremenih saznanja o patofiziologiji bola, dostupnim lekovima i postojanju smernica za lečenje bola on je i dalje neadekvatno zbrinut kod 50-70% bolesnika sa malignom bolešću pa oni trpe bolove određenog stepena. Vrhunske dijagnostičke, hirurške i radioterapijske metode i tehnike te novi citostatici, omogućili su i duže preživljavanje onkoloških bolesnika, pa su tako maligni tumori postali hronična bolest. Međutim produženje života dovodi, i do produženja patnje zbog stresnih simptoma uzrokovanih malignitetom.[10][11] Sa druge strane, kako Svetska zdravstvena organizacija (SZO) predviđa da će incidencija malignih tumora tipa karcinoma u svetu u sledećih 20 godina porasti za 50% i da će do 2020. biti 15 miliona novootkrivenih slučajeva godišnje,[12] adekvatno lečenje bola postalo je moralni imperativ prihvaćen u svim zdravstvenim službama savremenog sveta. SZO je u postupku antitumorskog lečenja kupiranje karcinomskog bola postavio na četvrto mesto po značaju (prevencija, rana detekcija, uspešno izlečenje, terapija bola) i time upozorio sve svoje članice na njenu važnost.[13] U tom smislu terapijski pristup probijajućem bolu mora biti: multimodalan, individualno podešen, usmeren ka određenom tipu i karakteristikama probijajućeg bola prema svakom pojedinom bolesniku. Sadašnje smernice za lečenje probijajućeg bola uključuju brzodelujući oralne opioide, a neke i fentanilske preparate.
Definicije bola[uredi | uredi izvor]
Prema definiciji Svetske zdravstvene organizacije: „bol je neprijatno čulno ili emocionalno iskustvo povezano sa stvarnim ili potencijalnim oštećenjem tkiva“.
Međunarodno udruženje za proučavanje bola International Association for the Study of Pain(IASP) definiše bol kao: „neprijatno osetno i osećajno iskustvo povezano sa pravom ili potencijalnom povredom tkiva, ili uzrokovano tim oštećenjem ili povredom.“
Četiri dimenzije bola[uredi | uredi izvor]
Uporan bol za onkološke bolesnike ima četiri dimenzije patnje;
- fizičke — izazvane bolom (usled same bolesti ili postupka lečenja),
- psihoemocionalne, socijalne i duhovne.[14]
Ponekad se može čuti od onkoloških bolesnika da oni bol koristi kao način doživljavanja bolesti, „ja sam neizlečiv slučaj i zato umirem“.[15] Kod takvih slučajeva, lekari koji leče bolesnike sa teškim, kancerskim, probijajućim bolom, moraju imati veoma širok pogled na bol ne samo kao fizičkom stanju (bol, nesanica, umor), već i kao psichoemocionalnom poremećaju (osećanje bespomoćnosti, ljutnja na dijagnozu, strah od smrti), socijalnom faktoru (gubitak posla, gubitak finansijske sigurnosti, položaja u društvu, osećaj napuštenosti), i duhovnoj patnji (gubitak svrhe života, zašto me mučite) i na sve navedene komponente bola moraju stalno obraćati pažnju.[16]
Takođe lekari neprestano moraju ceniti karakteristike fizičkog bola, u pogledu kvaliteta, zračenja (prostiranja), ozbiljnosti bola i na osnovu toga ga klasifikavati na nociceptivni, neuropatski i simpatetički prenosivi bol.
Uzrok bola kod pacijenata sa karcinomom može biti i nekarcinogenog porekla kao što su osteoartritis, neuralgija posle herpesa, mišićni grčevi, ili bol kao posledica posthemoterapijska periferne neuropatije. Stoga svaki probijajući bol mora biti pravilno procenjen, kako bi se odredili njegovi uzroci i pristupilo pravilnom lečenju. U oko 15% pacijenata sa invazivnim karcinomom, nijedan od njihovih bolova nije uzrokovan samim karcinomom.[16]
Karakteristike kanacerskog probijajućeg bola[uredi | uredi izvor]
Bol je subjektivni osećaj koji se opisuje korišćenjem nekoliko različitih osobina ili karakteristika (lokalizacijom, kvalitetom, intenzitetom, emocionalnim uticajem, promenom ponašanja, učestalošću,...), koje treba uzeti u obzir u toku terapiju hroničnog bola maligne etiologije. Intenzitet malignog probijajućeg bola je prepoznat i prihvaćen kao najvažnija klinička dimenzija doživljavanja bola.
Kancerski probijajući bol je najčešći simptom koji najteže podnose kod bolesnici sa uznapredovalim malignim ili nekim drugim oboljenjem u terminalnom stadijumu. Za razliku od bolesnicika koji ne pate od probijajućeg bola, kod ovih bolesnika izraženo je smanjenje funkcionalnih kapaciteta i psihološki distres, prvenstveno zbog depresije i teskobe, što značajno narušava kvalitet života kod dela bolesnika.
- Razlike između konstantnog i probijajućeg bola
Osobine prema kojima razlikujemo probijajući bol od konstantnog bola su:
- Povezanost bola sa fiksnim dozama opioidnih analgetika
Kod onkoloških bolesnika kod kojih se primenjuju u lečenju konstantnog bola, fiksne doze opioidnih analgetika ova vrsta bola javlja se sa učestalošću od 13,2-33%.
- Vremenska određenost trajanja bola
Vremenska određenost trajanja bola podrazumeva specifičan nastup, trajanje i učestalost epizoda probijajućeg bola. Nastup je najčešće iznenadan uz postepeno pojačanje intenziteta bola unutar 30 minuta (srednje vreme trajanja oko 3 minute). Broj dnevnih epizoda probijajućeg bola varira od 1-3.600 (prosečno 4-6), a trajanje svake epizode je od 1-240 minuta (srednje vreme trajanja 15-30 minuta).
- Povezanost bola sa provocirajućim činiocima
Napadi probijajućeg boli mogu biti povezane sa nekim provocirajuce činiocem, i kod nekih bolesnika bol može biti predvidiv. Provocirajući faktor kod 55-80% slučajeva je poznat, dok se u 27-38,3% slučajeva ne može identifikovati.
- Predvidivost bola.
U 12-15,3% slučajeva probijajući bol je predvidiv, a u 57% epizoda uopšte se ne može predvideti.
Učestalost javljanja i mogućnosti lečenja kancerskog bola[uredi | uredi izvor]
Prema podacima Svetske zdravstvene organizacije (SZO), 15 miliona ljudi boluje od malignih bolesti, a 66% pacijenata tokom svoje bolesti imaju bolove, ili oko 10 miliona ljudi u svetu u ovom času pati od hroničnog kancerskog bola.[17]
Svake godine u Republici Srbiji dijagnostikuje se oko 32.000 novih slučajeva maligne bolesti, a godišnje od raka umre oko 20.000 ljudi. Bol je najčešći i najteži simptom maligne bolesti, koji najviše plaši bolesnika i porodicu. Kancerski bol javlja se kod oko 60% pacijenata, u svim fazama maligne bolesti, s tim da se učestalost i jačina bola povećavaju kako bolest napreduje. Oko 25-30% pacijenata u Srbiji ima jake probijajuće bolove.
Na osnovu rezultati velikog evropskog istraživanja prevalence i tretmana bola vezanog za kancer pokazali su da je bol prisutan u svim fazama kancera (ranom i metastatski), i da kod velikog broja pacijenata (od 56% do 82,3%) bol nije bio lečen adekvatno.[18]
Prema podacima Svetske zdravstvene organizacije (SZO), kancerske bol moguće je otkloniti kod većine pacijenata (70-90%). Metod otklanjanja kancerskog bola koji preporučuje SZO zasniva se na farmakoterapiji lekovima koji se primenjuju na najmanje invazivan način (oralno, na prvom mestu), po vremenu, u skladu sa jačinom bola i individualnim karakteristikama bolesnika i bolnog sindroma.
U brojnim naučnim radovima o prevalenci kancerskog bola (objavljenih od 1966—2005) Za različite tipove malignoma, došlo se do zaključka da je u jednakoj meri bol zastupljen kod pacijenata koji se aktivno leče i kod onih u uznapredovaloj ili terminalnoj fazi bolesti. Prevalenca bola u tim studijama je 64% kod pacijenata sa uznapredovalom, metastatskim ili terminalnom bolešću, 59% kod pacijenata u toku aktivnog lečenja i u 33% kod pacijenata nakon kurativnog tretmana.[19]
Opioidni analgetici su ključni lekovi, bez kojih uspešna terapija umereno jakog i jakog kancerskog probijajućeg bola nije moguća. Prema tzv. analgetičkim stepenicama SZO, svaki bolesnik sa jačinom bola ≥ 5/10 na numeričkoj skali za jačinu bola (0: bez bola, 10: najjači mogući bol) trebalo bi da bude lečen opioidima.[20]
Oblici probijajućeg bola[uredi | uredi izvor]
Bol se može podeliti na različite načine i to prema:
- Trajanju: na akutni i hronični bol.
- Etiologiji: na maligni i nemaligni bol,
- Patofiziologiji: nociceptivni (koji može biti somatski i visceralni), neuropatski i inflamatorni bol.
Vrste bola prema trajanju[uredi | uredi izvor]
- Akutni bol
Akutni bol ima zaštitnu ulogu i najčešće je uzrokovan povredom i ukazuje na stvarno oštećenje tkiva. Javlja se naglo i prethodno je bio ograničen na period trajanja od šest meseci, dok se danas ograničava na vreme od tri meseca ili na vreme potrebno za lečenje ili oporavak (npr bol kod glavobolje, zubobolje, dismenoreje, nakon udarca ...)
- Hronični bol
Hronični bol traje duže od optimalnog vremena oporavka od povrede, a taj vremenski period može biti od 3 meseca do kraja života kod nekih bolesnika (npr maligni probijajući bol). Hronični bol ponekad uopšte nije izazvan povredom a može biti i bez dijagnostikovanog štetnog uzroka. On po pravilu dovodi do značajnog narušavanja kvaliteta života bolesnika.
Faze kroz koje prolaze bolesnici sa hroničnim bolom
| Faze | Trajanje | karakteristike |
|---|---|---|
| ||
| ||
| ||
|
Karakteristične su dve vrste hroničnog bola bola:
- Kontinuirani pozadinski bol - praćen često i funkcionalnom nesposobnošću,
- Probijajući bol - u vidu naglih, kratkotrajnih i vrlo intenzivnih napada.
Vrste bola prema etiologiji[uredi | uredi izvor]
- Maligni bol
Maligni bol je hronični bol povezan sa progresivnom bolešću koja potencijalno ugrožava život bolesnika (npr kod karcinom, AIDS-a, progresivne neurološke bolesti ...)
- Nemaligni bol
Nemaligno bol je hronični bol povezan sa bolestima koje nisu po život opasne, kao što su bol u trbuhu, bol kod artritisa, osteoartritis, neuropatski bol, bol u krstima...
Patofiziologija kancerskog bola[uredi | uredi izvor]
U zavisnosti od patofiziološkog mehanizma koji dovodi do nastanka bola, kancerski bol možemo podeliti na nociceptivni, neuropatski i inflamatorni.[21] Sva tri mehanizma bola zastupljena su kod karcinomskog bola.[22]
- Nociceptivni bol
Nociceptivni bol nastaje kao posledica nadražaja nociceptora - slobodnih nervnih završetaka za bol. Nociceptore mogu biti nadraženi toplotnim, hemijski i mehaničkim nadražajima.[23] Najznačajniji toplotni receptori su receptori iz porodice TRP-a (engl. Transient Receptor Potential).[24][25]
Nociceptori se dele u dve osnovne grupe: mehaničke i polimodalne.[26]
- Mehanički receptori prenose impulse mijelinskim A-vlaknima, namenjeni provođenju dobro lokalizovanog, ubodnog bola.
- Polimodalni receptori impulse prenose nemijeliniskim C-vlaknima, i služe za provođenje tupog, neoštro lokalizovaneog bola.
Osećaj bola sa periferije prenosi se prema središnjem nervnom sistemu uz pomoću vlakana za bol koja ulaze u kičmenu moždinu preko spinalnih ganglija i zadnjih korenova spinalnih živaca. Ona završavaju u sinapsama dorzalne sive materije koja čini neuron prvog reda. Postsinaptička vlakna za bol prelaze na suprotnu stranu i formiraju dva odvojena puta. Vlakna tipa A koja čine neospinotalamički put, i vlakna tipa C koja obrazuju palospinotalamički put. U neospinotalamičkom putu neurone drugog reda čine ventroposterolateralna talamička jezgra, dok su neuroni trećeg reda somatosenzorna područja I. i II. parijetalnog korteksa. U palospinotalamičkom putu neuroni drugog reda su intralaminarna jedra talamusa, dok neurone trećeg reda čine difuzne kortikalne projekcije ka čeonom, temporalnom i parijetalnom području.[21]
Neuropatski bol nastaje kao posledica oštećenja perifernog ili centralnog nervnog sistema, bez istovremenog nadražaja nociceptora.[27] Ovaj tip bola često se javlja kod primene neurotoksične hemoterapije.
Kako je bol individualan osećaj jednak nadražaj može kod više osoba izazvati bol različite jačine. Objašnjenje delimično leži u činjenici da je aktivaciji analgezijskog sistema ta koja kontroliše ulazak bolnih impulsa u mozak. Analgezijski sistem počinje u sivoj masi oko akvedukta i periventrikularnih područja u mezencefalonu i gornjem delu ponsa.[21] Impuls se nadalje prenosi u veliko jedro rafe i retikularna paragigantocelularna jedra u spoljnjem delu produžene moždine. Na kraju impuls završava u zadnjem rogu kičmene moždine, u području gde je lociran kompleks za inhibiciju bola. U analgezijskom sistemu učestvuju brojne prenosne materije od kojih se posebno izdvajaju endorfini, encefalina i dinorfini, koji čine endogeni opioidni sistem.[28]
Najčešći bolni sindromi u okviru kancerskog bola
| Bolni sindom | Simptomi i znaci |
|---|---|
| |
(sa ili bez pripadajućih seroze) |
|
|
Dijagnoza i procena intenziteta bola[uredi | uredi izvor]
Kako je bol subjektivni osećaj, ne postoji validan objektivni metod za merenje njegovog intenziteta. Na doživljaj bola utiču i kompleksna ljudska iskustva sa funkcionalnim, emotivnim i duhovnim komponentama. Kako lekari vole da imaju odgovarajuće vodiče, oruđa za procenu intenziteta bola (koji treba da im daju podatke o intenzitetu bola) i ponuđene analgetike i dodatne lekove i postupke za terapiju bola u odnosu na intenzitet istog, u mnogim zemljama stalno se razvijaju i usavršavaju jednodimenziona i višedimenziona oruđa za procenu jačine bola.
Klinička procena bola[uredi | uredi izvor]
|
Klinička procena bola, u načelu, obuhvata:
- 1. Detaljna anamneza
U okviru anameneze treba prikupiti podatke o:
- lokalizacija, širenju, kvalitetu i jačini bola
- faktorima koji ga pojačavaju ili ublažavaju,
- ponašanju bola u vremenu, postojanje proboja bola,
- prethodnoj terapiji bola: lekovi, doze, način primene, šema davanja, efikasnost, neželjena dejstva,
- psihosocijalnom statusu pacijenta.
- 2. Fizički pregled, uključujući i neurološki pregled
Ovim pregledi obuhvataju procenu funkcionalnog oštećenja i psihosocijalnu procenu (holistički pristup).
- 3. Dodatna ispitivanja (laboratorijska, vizualizaciona)
Dopunski dijagnostički pregledi mogu biti: laboratorijski testovi, MRT, CT, pregledi specijalista drugih struka. Ovi pregledi uvode se prema potrebi.
Oruđa za merenje intenziteta bola[uredi | uredi izvor]
Jednodimenziona oruđa za merenje intenziteta bola koja se koriste u dijagnostici, su različite skale koje mogu biti numeričke i vizuelne:
Verbalna skala - VS (Categorical Verbal Rating Scales (VRS)).
Ova skala predstavlja listu deskriptora, kojima se opisuje stepen jačine bola, najčešće sa četiri deskriptora (bez bola, blag, umereno jak, jak bol).
Verbalna skala za procenu bola
| Bez bola | Blag bol | Umereno jak bol | Jak bol |
|---|
Numerička skala - NS (Categorical Numerical Rating Scales (NRS)).
Numerička skala (NS) koja se često zove i vizuelna numerička skala (VNRS/VNS), jer je skala objašnjena ili prikazana na papiru, tako da odgovara nekom broju (0-5 ili 0-10). Ona je jednostavna za primenu u proceniu intenziteta bola. Koristiti se kod prvog pregleda i kod kontrolnih pregleda bolesnika radi praćenja delotvornosti terapije. Na skali su označena dva ekstrema u opisu intenziteta bola, na primer od „bola nema uopšte“, do „najgori mogući bol“.

Vizuelno analogna skala - VAS (Visual Analogue Scale (VAS)).
Kako je kod dece veoma teško odrediti karakter bola, primenom kombinovanih slikovno-numeričkih skala od 0-10 ta poteškoća se donekle može ublažiti. U praksi se često koristi Vong Bekerova skala (Wong Baker Scale) za procenu težine bola kod dece.[16]
Izbor skale zavisi od njene praktičnosti, znanja i veštine korisnika, i uobičajeno se koriste u merenju intenziteta bola sa podjednakim uspehom.[29]
Terapija[uredi | uredi izvor]
|
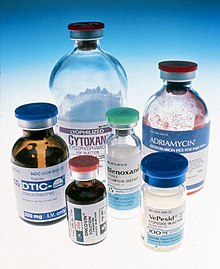
Terapiju kancerskog bola treba sprovoditi postepenim uvođenjem slabijih a potom jačih analgetika. Svetska zdravstvena organizacija (SZO) je, kao izuzetno korisnu preporuku za lečenje bola, u praksu uvela primenu „analgetičkih stepenica“. Mnogi eksperti u razvijenim i nerazvijenim zemljama koriste ih kao jedno veoma korisno oruđe koje se primenjuje u terapiji bola. Stepenice od tri nivoa su odličan model za početnika, jer pokazuju osnovu pristupa terapiji bola. Osnovne pretpostavke, date i u ovoj metodi za lečenje bola su veoma korisne i danas primenljive, ali mnoge promene su potrebne pogotovo na nivou farmakoterapije, posebno kada se radi o terapiji malignog probijajućeg ili karcinomskog bola.
Analgetičke stepenice se veoma koriste u svakodnevnom radu jer su pogodne za primenu i pomažu lekarima koji počinju da se bave terapijom bola. Daju mogućnost da se postepeno uvode lekovi i kontroliše uspeh i napredovanja terapije. Pri tome nivo stepanica jedan, blag bol (NS=1–3), preporučuje primenu neopioidnih analgetika i dodatnu terapiju. Nivo dva, umeren i blag bol (NS=4-7), preporučuje primenu opioida uz primenu neopioida i adjuvantnu terapiju. Na kraju najviši nivo, nivo tri, (NS=8-10), preporučuje jake opioide za umeren i jak bol uz lečenje neopioidima i dodatnu terapiju. [31][32]

Metoda SZO lečenja bola u pet tačaka[uredi | uredi izvor]
Ova metoda SZO može se sažeti u sledećih pet tačaka:
- 1. Lek davati na usta
Optimalan je put unosa morfina na usta. Idealno su potrebna dva oblika: jedan sa normalnim otpuštanjem za titraciju doze i drugi sa modifikovanim otpuštanjem za terapiju održavanja.

- 2. Lek davati na sat
Ispravna je doza analgetika ona doza koja suzbije bol. Nema standardne doze za opioide. Doza oralnog morfina može varirati 5-1.000 mg svakih 4 sata.
Početnu dozu i određuje stanje bolesnika i prethodna terapija. Na prvom stepenu biće dovoljno i 5 mg svakih 4 sata. Na drugom stepenu bola (opioid plus neopioid) terapija će započeti obično sa 10 mg svakih 4 sata, dok će se na trećem stepenu doza povećati. Kod probijajućeg bola „spas-doza“ može se ponavljati svaki sat.
- 3. Lek davati po lestvici,
Na drugom stepenu jačine bola predlaže se upotreba kodeina, tramadola, malih doza oksikodona i buprenorfina. Dodatni analgetski efekat postiže se u kombinaciji sa nesteroidnim antireumaticima (kao što je acetilsalicilna kiselina). Istraživanja pokazuju da ovi slabi opioidi nisu superiorni punim dozama nesteroidnih antireumatika, pa se došlo do ideje da se prvi i drugi stepen jednostavno spoje u jedan (prvi) stepen, dok bi drugi stepen činio onaj za tešku bol.[33]
- 4. Lečenje prilagoditi pojedincu
Izuzetno je važno individualno prilagođavanje lečenja. Tako uz jačinu bola treba uzeti u obzir i prethodno uzimanje opijata, starost pacijenata, obim karcinoma i prisustvo drugih bolesti.
- 5. U toku lečenja pažnju usmerenu na detalje.
Morfin je u početku izabran kao jaki opioid izbora, međutim, raste upotreba oksikodona, hidromorfon, fentanila i metadona. U kliničkim farmakološkim studijama morfin je ostao zlatni standard.[34]
Ovih pet tačaka uključuje i koncept prema kojem je analgetska medikamentozna terapija ključna u lečenju bola većine pacijenata sa kancerom (tumorom), kao i to da su jaki opijati apsolutno potrebni u savladavanju teških bolova kod većine pacijenata.
Terapija opioidima[uredi | uredi izvor]
Opioidi, koji se dele na slabe i jake, polusintetske i sintetske, su farmaceutici iz grupe anelgetika koji imaju aktivnost kao morfin, uključujući i agoniste i antagoniste kao i prirodne i sintetske opioidne peptide.[35][36]
- Slabi opioidi, se nazvaju tako jer imaju gornju granicu efikasnosti, odnosno za njih postoji maksimalna dnevna doza koja se može primeniti i koriste se za bolove na vizuelno analognoj skali od 4-6.
- Jaki opiodi nemaju maksimalnu dnevnu dozu i koriste se za jake bolove, na vizuelno analognoj skali > 6.
Tolerancija na opioide[uredi | uredi izvor]
Tolerancija na opoide podrazumeva: smanjenje analgetičkog efekta opioida posle ponavljanih davanja određene doze tog leka. Tolerancija na analgetički efekt opioida ne razvija se brzo. Potreba da se doza analgetika poveća, najčešće je rezultat pojačanja bola, a ne prave farmakološke tolerancije (tzv. pseudotolerancija).
Do pojačanja bola najčešće dolazi zbog:
- pojačanja bolnog nadražaja (relaps ili progresija maligne bolesti)
- uticaja nemedicinskih faktora na bolesnikov doživljaj bola (prema konceptu tzv totalnog bola to mogu biti psihološki, socijalni, spiritualni faktori).
U slučaju pseudotolerancije, kauzalnom terapijom bola na holistički način, uz učešće nemedicinskih i medicinskih članova tima, moguće je smanjiti jačinu bola i povratiti analgetički efekt leka. Tolerancija na analgetički efekt opioida može da se prevaziđe prelaskom sa slabog na jak opioid ili povećanjem doze jakog opioida. Jaki opioidi nemaju maksimalnu dozu i doza leka se može povećavati koliko god je to potrebno do prestanka bola ili do pojave neželjenih dejstava koja se ne mogu kontrolisati. Tolerancija na jak opioid može se takođe prevazići tzv. rotacijom opioida, ili prelaskom sa jednog jakog opioida na drugi.
Neželjena dejstva opioida[uredi | uredi izvor]
Primenu opioida često u svakodnevnoj praksi sprečava i strah kako bolesnika tako i neiskusnog lekara od mogućih neželjenih dejstava. Neželjena dejstva opioida dobro su poznata, i mogu da se spreče i kontrolišu na osnovu individualnih iskustva onkologa iz prakse i smernicama u odgovarajućim tarapijskim vodičima.[37]
Na većinu neželjenih dejstava opioida razvija se tolerancija i ona se spontano povlače tokom vremena. Trajno neželjeno dejstvo opioida je opstipacija. Neželjena dejstva koja ograničavaju dozu su mioklonus i delirijum. Depresija disanja je potencijalno fatalna, a neželjeno dejstvo opioida, na ovaj efekt brzo razvija toleranciju. Pored toga, bol se suprotstavlja depresornom efektu opioida depresijom disanja. Jedino su pod rizikom da razviju depresiju disanja bolesnici koji nikada ranije nisu bili izloženi opioidima, kao i bolesnici sa oštećenom funkcijom bubrega.
Neželjena dejstva opioida
| Vrste | Znaci i simptomi |
|---|---|
| Inicijalna | • Mučnina i povraćanje • Nesvestica • Sedacija • Konfuzija |
| Trajna | • Opstipacija |
| Retka | • Znojenje • Suvoća usta • Svrab • Delirijum • Retencija mokraće • Depresija disanja • Mioklonus • Hiperalgezija • Halucinacije |
- Strah od upotrebe opoida
Kako se kancerski bol mora i može lečiti opoidima, to ponekad nailazi na otpor kod pacijenata zbog moguće zavisnosti i neželjenih dejstava ovih lekova. U tom smislu neophodno je otvoreno razgovarati sa pacijentima i njihovom porodicom o tome šta ih sprečava da se bol uspešno leči, jer na današnjem stepenu znanja, nijedan bolesnik ne bi trebalo ni da živi ni da umire sa bolom. Lekovi iz grupe opioida (morfin i njemu slični lekovi) neophodni su i nezamenjivi lekovi za uspešno otklanjanje umereno jakog i jakog kancerskog bola. Strah pacijenata i porodice od zavisnosti nakon primene opoida ne bi trebalo da bude prepreka uspešnom otklanjanju bola i uzrok bezrazložne patnje velikog broja pacijenata. Lekovi opioidi su tu da bi se koristili, a ne da bi se permanentno izbegavali. Zbog toga lekar mora da se zapita zašto bolesnici i dalje odbijaju ove lekove, i ukažu im na zablude.
Terapija koanalgeticima (analgetičkim adjuvantima)[uredi | uredi izvor]
Primarna indikacija za primenu lekova iz grupe koanalgetika nije lečenje bola, ali je dokazano da oni deluju analgetički, najčešće na neuropatski bol, hronične glavobolje, mišićnoskeletni i kancerski bol.[38]
Ovi lekovi se mogu primeniti u svakoj stepenici analgetičke lestvice SZO. Oni su zapravo deo multimodalnog terapijskog pristupa hroničnom bola, jer pomažu delovanje i smanjuju potrošnju primarnih analgetika.
Izbor koanalgetička lek treba da je individualno obavljen a njegova primena stalno kontorisana. U praksi nije u potunosti dokazano da u pogledu efikasnosti, jedan koanalgetik ima apsolutnu prednost nad drugim.
U ovu grupu lekova spadaju:[39]
- Antidepresivi (amitriptilin, nortriptilin, duloketin, venlafaksin),
- Antiepileptici (gabapentin, pregabalin, karbamazepin, okskarbazepin),
- Kortikosteroidi (deksametazon),
- Antagonisti NMDA receptora (ketamin, aminobifosfonat, ibandronat, pamidronat, zoledronat).
Izvori[uredi | uredi izvor]
- ^ Renata Dobrila-Dintinjana, Jelena Vukelić, Marijan Dintinjana. Liječenje maligne boli.. Medicus. 23: 93—98. 2014. Nedostaje ili je prazan parametar
|title=(pomoć) - ^ Mishra, S.; Bhatnagar, S.; Chaudhary, P.; Rana, S. P. (2009). „Breakthrough cancer pain: Review of prevalence, characteristics and management”. Indian J Palliat Care. 15 (1): 14—18. PMC 2886208
 . PMID 20606850. doi:10.4103/0973-1075.53506
. PMID 20606850. doi:10.4103/0973-1075.53506  ..
..
- ^ Caraceni A, Davies A, Poulain P, et al. Guidelines for the management of breakthrough pain in patients with cancer. J Natl Compr Canc Netw 2013;11:S-29-S-36.
- ^ Davies, A.; Zeppetella, G.; Andersen, S.; Damkier, A.; Vejlgaard, T.; Nauck, F.; Radbruch, L.; Sjolund, K. F.; Stenberg, M.; Buchanan, A. (2011). „Multi-centre European study of breakthrough cancer pain: Pain characteristics and patient perceptions of current and potential management strategies”. Eur J Pain. 15 (7): 756—763. PMID 21251860. S2CID 221679539. doi:10.1016/j.ejpain.2010.12.004..
- ^ Portenoy, R. K.; Hagen, N. A. (1990). „Breakthrough pain: Definition, prevalence and characteristics”. Pain. 41 (3): 273—81. PMID 1697056. S2CID 30164796. doi:10.1016/0304-3959(90)90004-W.
- ^ Portenoy, R. K.; Payne, D.; Jacobsen, P. (1999). „Breakthrough pain: Characteristics and impact in patients with cancer pain”. Pain. 81 (1–2): 129—34. PMID 10353500. S2CID 8893835. doi:10.1016/S0304-3959(99)00006-8..
- ^ Mishra S, Bhatnagar S, Chaudhary P, Rana SP (januar 2009). „Breakthrough cancer pain: review of prevalence, characteristics and management”. Indian Journal of Palliative Care. 15 (1): 14—8. PMC 2886208
 . PMID 20606850. doi:10.4103/0973-1075.53506
. PMID 20606850. doi:10.4103/0973-1075.53506  .
.
- ^ Caraceni A, Hanks G, Kaasa S, Bennett MI, Brunelli C, Cherny N, Dale O, De Conno F, Fallon M, Hanna M, Haugen DF, Juhl G, King S, Klepstad P, Laugsand EA, Maltoni M, Mercadante S, Nabal M, Pigni A, Radbruch L, Reid C, Sjogren P, Stone PC, Tassinari D, Zeppetella G (februar 2012). „Use of opioid analgesics in the treatment of cancer pain: evidence-based recommendations from the EAPC” (PDF). The Lancet Oncology. 13 (2): e58—68. PMID 22300860. doi:10.1016/S1470-2045(12)70040-2. Arhivirano iz originala (PDF) 19. 10. 2014. g. Pristupljeno 18. 10. 2014.
- ^ Zeppetella G, Davies AN (2013). Zeppetella G, ur. „Opioids for the management of breakthrough pain in cancer patients”. The Cochrane Database of Systematic Reviews. 10 (10): CD004311. PMID 24142465. doi:10.1002/14651858.CD004311.pub3.
- ^ Valdimarsdóttir, U.; Helgason, A. R.; Fürst, C. J.; Adolfsson, J.; Steineck, G. (2002). „The unrecognised cost of cancer patients' unrelieved symptoms:a nationwide follow-up of their surviving partners”. Br J Cancer. 86 (10): 1540—5. PMC 2746591
 . PMID 12085201. doi:10.1038/sj.bjc.6600271..
. PMID 12085201. doi:10.1038/sj.bjc.6600271..
- ^ Winslow, M.; Seymour, J.; Clark, D. (2005). „Stories of cancer pain: A historical perspective”. J Pain Symptom Manage. 29 (1): 22—31. PMID 15652436. doi:10.1016/j.jpainsymman.2004.08.005..
- ^ Frankish H. 15 million new cancer cases per year by 2020, says WHO. Lancet 2003;361(9365):1278.
- ^ Persoli-Gudelj M, Lončarić-Katušin M, Šamija M. Bol u onkoloških bolesnika. U: Šamija M, Nemet D i sur. Potporno i palijativno liječenje onkoloških bolesnika, Medicinska naklada, Zagreb, 2010.
- ^ Kroenke K, Bair MJ, Damush TM; et al. (2009-05-27). „Optimized antidepressant therapy and pain self-management in primary care patients with depression and musculoskeletal pain: a randomized controlled trial”. JAMA. 301 (20): 2099—110. PMC 2884224
 . PMID 19470987. doi:10.1001/jama.2009.723..
. PMID 19470987. doi:10.1001/jama.2009.723..
- ^ Chaturvedi A; Singh P. (2013). „The Unheard Pain of Cancer Patients”. Syst Rev Pharm. 4: 14—9. S2CID 73302527. doi:10.4103/0975-8453.135832
 .
.
- ^ a b v Grossman SA. Undertreatment of Cancer pain: Barriers and remedies. Grossman, Stuart A. (1993). „Undertreatment of cancer pain: Barriers and remedies”. Support Care Cancer. 1 (2): 74—8. PMID 7511475. S2CID 2985911. doi:10.1007/BF00366899..
- ^ World Health Organization: National Cancer Control Programmes, Policies and Managerial Guidelines, Geneva, 2nd ed. 2002.
- ^ Breivik, H.; Cherny, N.; Collett, B.; De Conno, F.; Filbet, M.; Foubert, A.J.; Cohen, R.; Dow, L. (2009). „Cancer-related pain: A pan-European survey of prevalence, treatment, and patient attitudes”. Ann Oncol. 20 (8): 1420—1433. PMID 19244085. doi:10.1093/annonc/mdp001..
- ^ van den Beuken-van Everdingen MH; De Rijke, J. M.; Kessels, A. G.; Schouten, H. C.; Van Kleef, M.; Patijn, J. (2007). „Prevalence of pain in patients with cancer: A systematic review of the past 40 years”. Ann Oncol. 18 (9): 1437—1449. PMID 17355955. doi:10.1093/annonc/mdm056.)
- ^ ESMO: Management of cancer pain: ESMO Clinical Practice Guidelines. Annals of Oncology 22 (Supplement 6): vi69–vi77, 2011.
- ^ a b v Guyton AC, Hall JE. Tjelesni osjeti II: Bol, glavobolja i toplinski osjeti. Medicinska fiziologija, 11. izdanje, Zagreb, Hr, Medicinska naklada. 2006;598–609.
- ^ Benedetti C, Brock C, Cleeland C i sur. NCCN Practice Guidelines for Cancer Pain.. Oncology. 14: 135—50. 2000. Nedostaje ili je prazan parametar
|title=(pomoć). - ^ Persoli M, Juretić A, Lončarić-Katušin M. (2011). „Smjernice za liječenje karcinomske boli odraslih”. Bol. 2: 2—14.
- ^ Caraceni, A.; Cherny, N.; Fainsinger, R.; Kaasa, S.; Poulain, P.; Radbruch, L.; De Conno, F. (2002). „Pain measurement tools and methods in clinical research in palliative care: Recommendations of an Expert Working Group of the European Association of Palliative Care”. J Pain Symptom Manage. 23 (3): 239—55. PMID 11888722. doi:10.1016/S0885-3924(01)00409-2..
- ^ Breivik, H.; Borchgrevink, P. C.; Allen, S. M.; Rosseland, L. A.; Romundstad, L.; Hals, E. K.; Kvarstein, G.; Stubhaug, A. (2008). „Assessment of pain”. Br J Anaesth. 101: 17—24. PMID 18487245. doi:10.1093/bja/aen103..
- ^ Woolf, C. J.; Ma, Q. (2007). „Nociceptors--noxious stimulus detectors”. Neuron. 55 (3): 353—64. PMID 17678850. S2CID 13576368. doi:10.1016/j.neuron.2007.07.016..
- ^ Treede, R. D.; Jensen, T. S.; Campbell, J. N.; Cruccu, G.; Dostrovsky, J. O.; Griffin, J. W.; Hansson, P.; Hughes, R.; Nurmikko, T.; Serra, J. (2008). „Neuropathic pain: Redefinition and a grading system for clinical and research purposes”. Neurology. 70 (18): 1630—5. PMID 18003941. S2CID 30172528. doi:10.1212/01.wnl.0000282763.29778.59..
- ^ Holden, J. E.; Jeong, Y.; Forrest, J. M. (2005). „The endogenous opioid system and clinical pain management”. AACN Clin Issues. 16 (3): 291—301. PMID 16082232. doi:10.1097/00044067-200507000-00003..
- ^ Helme, R. D.; Gibson, S. J. (2001). „The epidemiology of pain in elderly people”. Clin Geriatr Med. 17 (3): 417—431. PMID 11459713. doi:10.1016/S0749-0690(05)70078-1.
- ^ Price, D. D.; Bush, F. M.; Long, S.; Harkins, S. W. (1994). „A comparison of pain measurement characteristics of mechanical visual analogue and simple numerical rating scales”. Pain. 56 (2): 217—226. PMID 8008411. S2CID 8652437. doi:10.1016/0304-3959(94)90097-3..
- ^ Fraenkel L, Falzer P, Fried T, Kohler M, Peters E, Kerns R, Leventhal H. Measuring Pain Impact Versus Pain Severity Using a Numeric Rating Scale.J Gen Intern Med. . 27 (5). 2012: 555—560. Nedostaje ili je prazan parametar
|title=(pomoć). - ^ Lund I, Lundeberg T, Sandberg L, Budh CN, Kowalski J, Svensson E. Lack of interchangeability between visual analogue and verbal rating pain scales: a cross sectional description of pain etiology groups. BMC Medical Research Methodology 2005, 5:31
- ^ Eisenberg E., Berkey C. S., Carr D. B. et al. Efficacy and safety of nonsteroidal antiinflammatory drugs for cancer pain: a meta-analysis. J. Clin Oncol. 12 (12): 2756—2765. 1994. Nedostaje ili je prazan parametar
|title=(pomoć) - ^ Wiffen P. J., Edwards J. E., Barden J., McQuay H. J.: Oral morphine for cancer pain. Cochrane Database of Systematic Reviews(4): CD003868, 2003.
- ^ Kalso E. Clinical Pharmacology of Opioids in the Treatment of Pain. In: Castro-Lopes J, Raja S, Schmelz,eds. Pain 2008. An Updated Review. Refresher Course Syllabus. Seattle:IASP Press; 2008, p. 197-203.
- ^ Wasan, A. D.; Ross, E. L.; Michna, E.; Chibnik, L.; Greenfield, S. F.; Weiss, R. D.; Jamison, R. N. (februar 2012). „Craving of prescription opioids in patients with chronic pain: A longitudinal outcomes trial”. J Pain. 13 (2): 146—54. PMC 3274819
 . PMID 22245713. doi:10.1016/j.jpain.2011.10.010..
. PMID 22245713. doi:10.1016/j.jpain.2011.10.010..
- ^ Jovanović L, Prostran M, Divac N, Žikić Lj. Prevencija i lečenje neželjenih dejstava opioidnih analgetika. u: Bošnjak S, Beleslin DB, Vučković-Đekić Lj. eds.Farmakoterapija kancerskog bola. Monografije naučnih skupova. Beograd: AMN SLD, seija B, vol 1, broj 1, 2007, p.139-155.
- ^ Irving, G.; Jensen, M.; Cramer, M.; Wu, J.; Chiang, Y. K.; Tark, M.; Wallace, M. (mart 2009). „Efficacy and tolerability of gastric-retentive gabapentin for the treatment of postherpetic neuralgia: Results of a double-blind, randomized, placebo-controlled clinical trial”. Clin J Pain. 25 (3): 185—92. PMID 19333167. S2CID 24318727. doi:10.1097/AJP.0b013e3181934276..
- ^ „True Koanalgetika – Übersicht”. Pharm. ZTG. 159 (16): 40—45. 2014..
Spoljašnje veze[uredi | uredi izvor]
- Bol : medicalcg.me
- Hronična bolna stanja maligne etiologije, kliničko terapijski vodič
- Suvremeno liječenje boli : plivamed.net
- Radije trpe bol nego što prihvataju morfin : politika.rs, objavljeno: 19.10.2014
- Opiofobija - Šta plaši bolesnika i porodicu, brošura
| Klasifikacija |
|---|
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
