Растварање — разлика између измена
. |
. |
||
| Ред 23: | Ред 23: | ||
! Име !! Композиција |
! Име !! Композиција |
||
|- |
|- |
||
| |
| Растварач 645 || толуен 50%, бутил ацетат 18%, етил ацетат 12%, бутанол 10%, етанол 10%. |
||
|- |
|- |
||
| |
| Растварач 646 || [[толуен]] 50%, [[етанол]] 15%, [[бутанол]] 10%, бутил- или [[амил ацетат]] 10%, [[етил целосолв]] 8%, [[ацетон]] 7%<ref>[https://www.dcpt.ru/rastvoritel-646/#tab3 dcpt.ru Solvent 646 Characteristics (ru)]</ref> |
||
|- |
|- |
||
| |
| Растварач 647 || бутил- или амил ацетат 29,8%, [[етил ацетат]] 21,2%, бутанол 7,7%, толуен или [[пиробензен]] 41,3%<ref>[https://www.dcpt.ru/rastvoritel-647/#tab3 dcpt.ru Solvent 647 Characteristics (ru)]</ref> |
||
|- |
|- |
||
| |
| Растварач 648 || [[бутил ацетат]] 50%, етанол 10%, бутанол 20%, толуен 20%<ref>[https://www.dcpt.ru/rastvoritel-marki-r-648/ dcpt.ru Solvent 648 Characteristics (ru)]</ref> |
||
|- |
|- |
||
| |
| Растварач 649 || етил целосолв 30%, бутанол 20%, [[ксилен]] 50% |
||
|- |
|- |
||
| |
| Растварач 650 || етил целосолв 20%, бутанол 30%, ксилен 50%<ref>[https://www.dcpt.ru/primenenie-r-650-ximicheskogo-rastvoritelya/ dcpt.ru Solvent 650 Characteristics (ru)]</ref> |
||
|- |
|- |
||
| |
| Растварач 651 || [[white spirit|вајт спирит]] 90%, бутанол 10% |
||
|- |
|- |
||
| |
| Растварач KR-36 || бутил ацетат 20%, бутанол 80% |
||
|- |
|- |
||
| |
| Растварач P-4 || толуен 62%, ацетон 26%, бутил ацетат 12%. |
||
|- |
|- |
||
| |
| Растварач P-10 || ксилен 85%, ацетон 15%. |
||
|- |
|- |
||
| |
| Растварач P-12 || толуен 60%, бутил ацетат 30%, ксилен 10%. |
||
|- |
|- |
||
| |
| Растварач P-14 || циклохексанон 50%, толуен 50%. |
||
|- |
|- |
||
| |
| Растварач P-24 || растварач 50%, ксилен 35%, ацетон 15%. |
||
|- |
|- |
||
| |
| Растварач P-40 || толуен 50%, етил целосолв 30%, ацетон 20%. |
||
|- |
|- |
||
| |
| Растварач P-219 || толуен 34%, циклохексанон 33%, ацетон 33%. |
||
|- |
|- |
||
| |
| Растварач P-3160 || бутанол 60%, етанол 40%. |
||
|- |
|- |
||
| |
| Растварач RCC || ксилен 90%, бутил ацетат 10%. |
||
|- |
|- |
||
| |
| Растварач RML || етанол 64%, етилцелосолв 16%, толуен 10%, бутанол 10%. |
||
|- |
|- |
||
| |
| Растварач PML-315 || толуен 25%, ксилен 25%, бутил ацетат 18%, етил целосолф 17%, бутанол 15%. |
||
|- |
|- |
||
| |
| Растварач PC-1 || толуен 60%, бутил ацетат 30%, ксилен 10%. |
||
|- |
|- |
||
| |
| Растварач PC-2 || вајт спирит 70%, ксилен 30%. |
||
|- |
|- |
||
| |
| Растварач RFG || етанол 75%, бутанол 25%. |
||
|- |
|- |
||
| |
| Растварач RE-1 || ксилен 50%, ацетон 20%, бутанол 15%, етанол 15%. |
||
|- |
|- |
||
| |
| Растварач RE-2 || растварач 70%, етанол 20%, ацетон 10%. |
||
|- |
|- |
||
| |
| Растварач RE-3 || растварач 50%, етанол 20%, ацетон 20%, етил целосолв 10%. |
||
|- |
|- |
||
| |
| Растварач RE-4 || растварач 50%, ацетон 30%, етанол 20%. |
||
|- |
|- |
||
| |
| Растварач FK-1 (?) || апсолутни алкохол (99,8%) 95%, етил ацетат 5% |
||
|} |
|} |
||
| Ред 83: | Ред 83: | ||
! Име !! Композиција |
! Име !! Композиција |
||
|- |
|- |
||
| |
| Разређивач RKB-1 || бутанол 50%, ксилен 50% |
||
|- |
|- |
||
| |
| Разређивач RKB-2 || бутанол 95%, ксилен 5% |
||
|- |
|- |
||
| |
| Разређивач RKB-3 || ксилен 90%, бутанол 10% |
||
|- |
|- |
||
| |
| Разређивач M || етанол 65%, бутил ацетат 30%, етил ацетат 5%. |
||
|- |
|- |
||
| |
| Разређивач P-7 || циклохексанон 50%, етанол 50%. |
||
|- |
|- |
||
| |
| Разређивач R-197 || ксилен 60%, бутил ацетат 20%, етил целосолв 20%. |
||
|- |
|- |
||
| |
| Разређивач WFD || толуен 50%, бутил ацетат (или амил ацетат) 18%, бутанол 10%, етанол 10%, етил ацетат 9%, ацетон 3%. |
||
|} |
|} |
||
Верзија на датум 28. фебруар 2020. у 16:43

Растварање је процес диспереговања (равномерног разређивања, распоређивања) једне супстанце или више њих у другој. Осим код правих смеша, увек је праћено разменом енергије са околином.[1][2]
Један корисник управо ради на овом чланку. Молимо остале кориснике да му допусте да заврши са радом. Ако имате коментаре и питања у вези са чланком, користите страницу за разговор.
Хвала на стрпљењу. Када радови буду завршени, овај шаблон ће бити уклоњен. Напомене
|
Растварач је супстанца која раствара растворак, чиме се формира раствор. A solvent is usually a liquid but can also be a solid, a gas, or a supercritical fluid. The quantity of solute that can dissolve in a specific volume of solvent varies with temperature. Common uses for organic solvents are in dry cleaning (e.g. tetrachloroethylene), as paint thinners (e.g. toluene, turpentine), as nail polish removers and glue solvents (acetone, methyl acetate, ethyl acetate), in spot removers (e.g. hexane, petrol ether), in detergents (citrus terpenes) and in perfumes (ethanol). Water is a solvent for polar molecules and the most common solvent used by living things; all the ions and proteins in a cell are dissolved in water within a cell. Solvents find various applications in chemical, pharmaceutical, oil, and gas industries, including in chemical syntheses and purification processes.
Растварач
Растварач, релативан и конвенционални појам, назив за средину у којој је нека супстанца дисперегована. Идеалан раствор, смеша, без хемијског међудејства средине и растворене супстанце или са међудејством. Може бити чврст, течан или гасовит. Вода је универзалан растварач. Растварачи као вода веома су значајни за живот, такође и у индустрији, а нарочито важну улогу имају селективни растварачи.
Растварачи у дегазацији
Растварачи у дегазацији су органска једињења с двојаком наменом - за растварање дегазитора у току њихове припреме за употребу и за растварање самих бојних отрова, односно за дагазацију физичким путем. Као растварачи дегазатора најчешће се употребљавају дихлоретан, тетрахлоругљеник и титрохлоретилен, а као растварачи бојних отрова бензин и петролеум.
Раствор
Раствор (чврст, течан или гасовит) настаје мешањем двеју или више супстанци. Засићен раствор за дату температуру има максималну концетрацију растворене супстанце. Незасићен раствор је раствор у коме се може растворити још извесна количина већ растворене супстанце све док се не добије засићен простор. Презасићен простор је раствор у коме је растворено више супстанци него што одговара засићеном раствору. Нестабилан је и из њега се лако издваја, у облику талога, вишак растворене супстанце.
Растворљивост
Растворљивост неке супстанце представља број грама супстанције који се раствара у 100г растварача на одређеној темпаратури.
Вишекомпонентни
Растварачи
| Име | Композиција |
|---|---|
| Растварач 645 | толуен 50%, бутил ацетат 18%, етил ацетат 12%, бутанол 10%, етанол 10%. |
| Растварач 646 | толуен 50%, етанол 15%, бутанол 10%, бутил- или амил ацетат 10%, етил целосолв 8%, ацетон 7%[3] |
| Растварач 647 | бутил- или амил ацетат 29,8%, етил ацетат 21,2%, бутанол 7,7%, толуен или пиробензен 41,3%[4] |
| Растварач 648 | бутил ацетат 50%, етанол 10%, бутанол 20%, толуен 20%[5] |
| Растварач 649 | етил целосолв 30%, бутанол 20%, ксилен 50% |
| Растварач 650 | етил целосолв 20%, бутанол 30%, ксилен 50%[6] |
| Растварач 651 | вајт спирит 90%, бутанол 10% |
| Растварач KR-36 | бутил ацетат 20%, бутанол 80% |
| Растварач P-4 | толуен 62%, ацетон 26%, бутил ацетат 12%. |
| Растварач P-10 | ксилен 85%, ацетон 15%. |
| Растварач P-12 | толуен 60%, бутил ацетат 30%, ксилен 10%. |
| Растварач P-14 | циклохексанон 50%, толуен 50%. |
| Растварач P-24 | растварач 50%, ксилен 35%, ацетон 15%. |
| Растварач P-40 | толуен 50%, етил целосолв 30%, ацетон 20%. |
| Растварач P-219 | толуен 34%, циклохексанон 33%, ацетон 33%. |
| Растварач P-3160 | бутанол 60%, етанол 40%. |
| Растварач RCC | ксилен 90%, бутил ацетат 10%. |
| Растварач RML | етанол 64%, етилцелосолв 16%, толуен 10%, бутанол 10%. |
| Растварач PML-315 | толуен 25%, ксилен 25%, бутил ацетат 18%, етил целосолф 17%, бутанол 15%. |
| Растварач PC-1 | толуен 60%, бутил ацетат 30%, ксилен 10%. |
| Растварач PC-2 | вајт спирит 70%, ксилен 30%. |
| Растварач RFG | етанол 75%, бутанол 25%. |
| Растварач RE-1 | ксилен 50%, ацетон 20%, бутанол 15%, етанол 15%. |
| Растварач RE-2 | растварач 70%, етанол 20%, ацетон 10%. |
| Растварач RE-3 | растварач 50%, етанол 20%, ацетон 20%, етил целосолв 10%. |
| Растварач RE-4 | растварач 50%, ацетон 30%, етанол 20%. |
| Растварач FK-1 (?) | апсолутни алкохол (99,8%) 95%, етил ацетат 5% |
Разређивачи
| Име | Композиција |
|---|---|
| Разређивач RKB-1 | бутанол 50%, ксилен 50% |
| Разређивач RKB-2 | бутанол 95%, ксилен 5% |
| Разређивач RKB-3 | ксилен 90%, бутанол 10% |
| Разређивач M | етанол 65%, бутил ацетат 30%, етил ацетат 5%. |
| Разређивач P-7 | циклохексанон 50%, етанол 50%. |
| Разређивач R-197 | ксилен 60%, бутил ацетат 20%, етил целосолв 20%. |
| Разређивач WFD | толуен 50%, бутил ацетат (или амил ацетат) 18%, бутанол 10%, етанол 10%, етил ацетат 9%, ацетон 3%. |
Физичка својства
Табела својстава уобичајених растварача
The solvents are grouped into nonpolar, polar aprotic, and polar protic solvents, with each group ordered by increasing polarity. The properties of solvents which exceed those of water are bolded.
| Solvent | Chemical formula | Boiling point[7] (°C) |
Dielectric constant[8] | Density (g/mL) |
Dipole moment (D) |
|---|---|---|---|---|---|
Nonpolar solvents | |||||
| Pentane | CH3CH2CH2CH2CH3 | 36 | 1.84 | 0.626 | 0.00 |
| Cyclopentane | 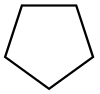 C5H10 |
40 | 1.97 | 0.751 | 0.00 |
| Hexane | CH3CH2CH2CH2CH2CH3 | 69 | 1.88 | 0.655 | 0.00 |
| Cyclohexane |  C6H12 |
81 | 2.02 | 0.779 | 0.00 |
| Benzene | 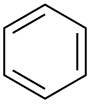 C6H6 |
80 | 2.3 | 0.879 | 0.00 |
| Toluene | C6H5-CH3 | 111 | 2.38 | 0.867 | 0.36 |
| 1,4-Dioxane |  C4H8O2 |
101 | 2.3 | 1.033 | 0.45 |
| Chloroform | CHCl3 | 61 | 4.81 | 1.498 | 1.04 |
| Diethyl ether | CH3CH2-O-CH2CH3 | 35 | 4.3 | 0.713 | 1.15 |
| Dichloromethane (DCM) | CH2Cl2 | 40 | 9.1 | 1.3266 | 1.60 |
Поларни апротични растварачи | |||||
| Tetrahydrofuran (THF) | 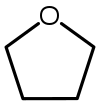 C4H8O |
66 | 7.5 | 0.886 | 1.75 |
| Ethyl acetate |  CH3-C(=O)-O-CH2-CH3 |
77 | 6.02 | 0.894 | 1.78 |
| Acetone |  CH3-C(=O)-CH3 |
56 | 21 | 0.786 | 2.88 |
| Dimethylformamide (DMF) | 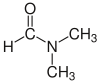 H-C(=O)N(CH3)2 |
153 | 38 | 0.944 | 3.82 |
| Acetonitrile (MeCN) | CH3-C≡N | 82 | 37.5 | 0.786 | 3.92 |
| Dimethyl sulfoxide (DMSO) |  CH3-S(=O)-CH3 |
189 | 46.7 | 1.092 | 3.96 |
| Nitromethane | CH3-NO2 | 100–103 | 35.87 | 1.1371 | 3.56 |
| Propylene carbonate | C4H6O3 | 240 | 64.0 | 1.205 | 4.9 |
Поларни протични растварачи | |||||
| Formic acid |  H-C(=O)OH |
101 | 58 | 1.21 | 1.41 |
| n-Butanol | CH3CH2CH2CH2OH | 118 | 18 | 0.810 | 1.63 |
| Isopropyl alcohol (IPA) |  CH3-CH(-OH)-CH3 |
82 | 18 | 0.785 | 1.66 |
| n-Propanol | CH3CH2CH2OH | 97 | 20 | 0.803 | 1.68 |
| Ethanol | CH3CH2OH | 79 | 24.55 | 0.789 | 1.69 |
| Methanol | CH3OH | 65 | 33 | 0.791 | 1.70 |
| Acetic acid |  CH3-C(=O)OH |
118 | 6.2 | 1.049 | 1.74 |
| Water | H-O-H |
100 | 80 | 1.000 | 1.85 |
Вредности параметра Хансенове растворљивости
The Hansen solubility parameter values[9][10] are based on dispersion bonds (δD), polar bonds (δP) and hydrogen bonds (δH). These contain information about the inter-molecular interactions with other solvents and also with polymers, pigments, nanoparticles, etc. This allows for rational formulations knowing, for example, that there is a good HSP match between a solvent and a polymer. Rational substitutions can also be made for "good" solvents (effective at dissolving the solute) that are "bad" (expensive or hazardous to health or the environment). The following table shows that the intuitions from "non-polar", "polar aprotic" and "polar protic" are put numerically – the "polar" molecules have higher levels of δP and the protic solvents have higher levels of δH. Because numerical values are used, comparisons can be made rationally by comparing numbers. For example, acetonitrile is much more polar than acetone but exhibits slightly less hydrogen bonding.
| Растварач | Chemical formula | δD Dispersion | δP Polar | δH Hydrogen bonding |
|---|---|---|---|---|
Неполарни растварачи | ||||
| n-Hexane | CH3CH2CH2CH2CH2CH3 | 14.9 | 0.0 | 0.0 |
| Benzene | C6H6 | 18.4 | 0.0 | 2.0 |
| Toluene | C6H5-CH3 | 18.0 | 1.4 | 2.0 |
| Diethyl ether | CH3CH2-O-CH2CH3 | 14.5 | 2.9 | 4.6 |
| Chloroform | CHCl3 | 17.8 | 3.1 | 5.7 |
| 1,4-Dioxane | /-CH2-CH2-O-CH2-CH2-O-\ | 17.5 | 1.8 | 9.0 |
Поларни апротични растварачи | ||||
| Ethyl acetate | CH3-C(=O)-O-CH2-CH3 | 15.8 | 5.3 | 7.2 |
| Tetrahydrofuran (THF) | /-CH2-CH2-O-CH2-CH2-\ | 16.8 | 5.7 | 8.0 |
| Dichloromethane | CH2Cl2 | 17.0 | 7.3 | 7.1 |
| Acetone | CH3-C(=O)-CH3 | 15.5 | 10.4 | 7.0 |
| Acetonitrile (MeCN) | CH3-C≡N | 15.3 | 18.0 | 6.1 |
| Dimethylformamide (DMF) | H-C(=O)N(CH3)2 | 17.4 | 13.7 | 11.3 |
| Dimethyl sulfoxide (DMSO) | CH3-S(=O)-CH3 | 18.4 | 16.4 | 10.2 |
Поларни протични растварачи | ||||
| Acetic acid | CH3-C(=O)OH | 14.5 | 8.0 | 13.5 |
| n-Butanol | CH3CH2CH2CH2OH | 16.0 | 5.7 | 15.8 |
| Isopropanol | CH3-CH(-OH)-CH3 | 15.8 | 6.1 | 16.4 |
| n-Propanol | CH3CH2CH2OH | 16.0 | 6.8 | 17.4 |
| Ethanol | CH3CH2OH | 15.8 | 8.8 | 19.4 |
| Methanol | CH3OH | 14.7 | 12.3 | 22.3 |
| Formic acid | H-C(=O)OH | 14.6 | 10.0 | 14.0 |
| Water | H-O-H | 15.5 | 16.0 | 42.3 |
If, for environmental or other reasons, a solvent or solvent blend is required to replace another of equivalent solvency, the substitution can be made on the basis of the Hansen solubility parameters of each. The values for mixtures are taken as the weighted averages of the values for the neat solvents. This can be calculated by trial-and-error, a spreadsheet of values, or HSP software.[9][10] A 1:1 mixture of toluene and 1,4 dioxane has δD, δP and δH values of 17.8, 1.6 and 5.5, comparable to those of chloroform at 17.8, 3.1 and 5.7 respectively. Because of the health hazards associated with toluene itself, other mixtures of solvents may be found using a full HSP dataset.
Види још
Референце
- ^ Peter Atkins; Julio de Paula (2001). Physical Chemistry (7th изд.). W. H. Freeman. ISBN 0716735393.
- ^ Donald A. McQuarrie; John D. Simon (1997). Physical Chemistry: A Molecular Approach (1st изд.). University Science Books. ISBN 0935702997.
- ^ dcpt.ru Solvent 646 Characteristics (ru)
- ^ dcpt.ru Solvent 647 Characteristics (ru)
- ^ dcpt.ru Solvent 648 Characteristics (ru)
- ^ dcpt.ru Solvent 650 Characteristics (ru)
- ^ Solvent Properties – Boiling Point Архивирано 14 јун 2011 на сајту Wayback Machine. Xydatasource.com. Retrieved on 26 January 2013.
- ^ Dielectric Constant Архивирано 4 јул 2010 на сајту Wayback Machine. Macro.lsu.edu. Retrieved on 26 January 2013.
- ^ а б Abbott S, Hansen CM (2008). Hansen solubility parameters in practice. Hansen-Solubility. ISBN 978-0-9551220-2-6.
- ^ а б Hansen CM (јануар 2002). Hansen solubility parameters: a user's handbook. CRC press. ISBN 978-0-8493-7248-3.
Литература
- Lowery TH, Richardson KS (1987). Mechanism and Theory in Organic Chemistry (3rd изд.). Harper Collins Publishers. ISBN 978-0-06-364044-3.
Спољашње везе
- "European Solvents Industry Group - ESIG - ESIG European Solvents Industry Group" Solvents in Europe.
- Table and text O-Chem Lecture
- Tables Properties and toxicities of organic solvents
- CDC – Organic Solvents – NIOSH Workplace Safety and Health Topic
- EPA – Solvent Contaminated Wipes
