Hloroamin
Appearance
| |

| |
| Nazivi | |
|---|---|
| Drugi nazivi
monohloroamin
hloramid | |
| Identifikacija | |
| |
| ECHA InfoCard | 100.031.095 |
| MeSH | Chloramine |
| Svojstva | |
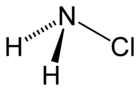
| NH2Cl | |
| Molarna masa | 51,48 g/mol |
| Agregatno stanje | bezbojan gas |
| Tačka topljenja | −66 °C |
| Tačka ključanja | °C |
| Rastvorljivost u drugim rastvaračima | rastvorljiv |
| Srodna jedinjenja | |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |
| Reference infokutije | |
Hloroamin (NH2Cl) je toksičan gas koji nastaje u reakciji amonijaka i natrijum-hlorida.
Hloroamin je popularno sredstvo za dezinfekciju koje se koristi u vodenim rastvorima. Ima bolje dezinfekciono dejstvo od samog rastvora hlora, jer je hloroamin postojaniji u rastvorima, a sa organskim jedinjenjima ne gradi po zdravlje štetne halometane (kao na primer tetrahlorid ugljenika).[1][2]
Reference
[uredi | uredi izvor]- ^ Lide David R., ur. (2006). CRC Handbook of Chemistry and Physics (87th izd.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ Susan Budavari, ur. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th izd.). Merck Publishing. ISBN 0911910131.
