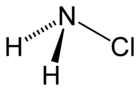
Хлороамин
Изглед
| |

| |
| Називи | |
|---|---|
| Други називи
монохлороамин
хлорамид | |
| Идентификација | |
| |
| ECHA InfoCard | 100.031.095 |
| MeSH | Chloramine |
| Својства | |
| NH2Cl | |
| Моларна маса | 51,48 g/mol |
| Агрегатно стање | безбојан гас |
| Тачка топљења | −66 °C |
| Тачка кључања | °C |
| Растворљивост у другим растварачима | растворљив |
| Сродна једињења | |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Хлороамин (NH2Cl) је токсичан гас који настаје у реакцији амонијака и натријум-хлорида.
Хлороамин је популарно средство за дезинфекцију које се користи у воденим растворима. Има боље дезинфекционо дејство од самог раствора хлора, јер је хлороамин постојанији у растворима, а са органским једињењима не гради по здравље штетне халометане (као на пример тетрахлорид угљеника).[1][2]
Референце[уреди | уреди извор]
- ^ Lide David R., ур. (2006). CRC Handbook of Chemistry and Physics (87th изд.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.
- ^ Susan Budavari, ур. (2001). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (13th изд.). Merck Publishing. ISBN 0911910131.
