Epitelni tumor jajnika
| Epitelni tumori jajnika | |
|---|---|
| Sinonimi | Surface epithelial-stromal tumor |
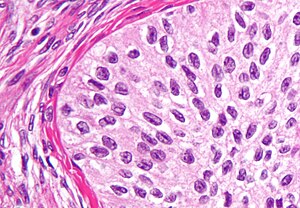 | |
| Mikrografija Brenerovog tumora | |
| Specijalnosti | onkologija, akušerstvo i ginekologija |
Epitelni tumori jajnika (ovarijuma) (akronim ETJ) čini 25% svih malignih oboljenja ženskog genitalnog trakta i najčešći je uzrok smrti među ženama obolelim od maligne bolesti genitalnog trakta. Prema dosadašnjim saopštenjima, najmanje 20% epitelnih tumora jajnika su karcinomi, koji se dijagnostikuju u stadijumu I bolesti. Epitelni tumori predstavljaju veliki izazov za ginekološkog onkologa, jer neneoplastične lezije jajnika mogu stvoriti karličnu masu i potencijalno oponašati neoplazmu. Njihovo pravilno prepoznavanje i histopatološka klasifikacija neophodni su za odgovarajuće lečenje, jer se maligni tumori obično javljaju u poodmakloj fazi zbog njihove asimptomatske prirode i nepristupačni mesta za aspiracijsku citologiju i biopsiju. I pored toha histopatološki pregled i dalje ostaje glavni oslonac u dijagnozi ovih neoplazmi.
Usled tendencije da žene danas rađaju svoje prvo dete u poznijim reproduktivnim godinama i veće dostupnosti različitih dijagnostičkih metoda, dijagnoza epitelnih tumora jajnika pre ostvarivanja reprodukcije postaje sve češća. Shodno tome, sve su i veći zahtevi struke da se hirurgijom očuva fertilitet u ranim stadijumima epitelnih tumora jajnika.[1]
Epidemiologija[уреди | уреди извор]

U žena svih dobnih skupina jajničke mase su česta pojava, s približno 8% asimptomatskih žena u dobi između 25 i 40 godina. Oko 80% tumora jajnika je dobroćudno, a javljaju se uglavnom kod mladih žena između 20 i 45 godina, dok se granični tumori javljaju u nešto starijoj dobi.
Incidencija malignih tumora raste sa godinama, javljajući se pretežno u žena u menopauzi i perimenopauzi.
Rak jajnika je šesti najčešći rak među ženama, a ujedno je i sedmi uzrok smrtnosti od raka među ženama širom sveta.[2][3] Jajnici su treća vodeća lokalizacija raka među ženama koja je u zaostatku iza raka vrata maternice i raka dojke prema nekim registrima za rak.[2][4]
Oko 90% svih karcinoma jajnika i dve trećine svih novotvorina jajnika čine tumori površinskog epitela. Ovi tumori imaju širok spektar histoloških obrazaca što ga čini zanimljivom temom za proučavanje. Poznavanje vrste tumora i diferencijacija pomaže u razumnom upravljanju pacijentom u smislu odgovarajućeg lečenja i praćenja.[5][6][7]
Među epitelni ovarijalnim tumorima najopasniji su karcinomi (EOK) koji čine 25% svih malignih oboljenja ženskog genitalnog trakta i najčešći su uzrok smrti među ženama obolelim od maligne bolesti genitalnog trakta.[8] Među EOK, invazivni mucinozni adenokarcinom javlja se kod oko 10% obolelih.[9] Prema dosadašnjim saopštenjima, bar 20% dijagnostikuje se u stadijumu I bolesti.[8][10]
Desetogodišnja stopa preživljavanja žena obolelih od mucinoznih tumora je odlična u odsustvu invazije. U slučaju graničnih tumora ograničenih na jajnike i malignih tumora bez invazije, stope preživljavanja su 90% ili veće. Kod invazivnih karcinoma preživljavanje je približno 30%.
Klasifikacija[уреди | уреди извор]

Epitelno-stromalni tumori jajnika su klasifikovani na osnovu tipa epitelne ćelije, relativne količine epitela i strome, prisustva papilarnih procesa i lokacije epitelnih elemenata.[11]
Mikroskopske patološke osobine određuju da li je površinski epitelno-stromalni tumor benigni, granični ili maligni (dokaz maligniteta i stromalne invazije). Granični tumori su neizvesnog malignog potencijala.
Ovu grupu čine serozni, mucinozni, endometrioidni, bistroćelijski i Brenerоv (prelazni) tumori, mada postoji nekoliko mešovitih, nediferenciranih i neklasifikovanih tipova.[12][13][14][15]
Serozni tumori[уреди | уреди извор]
Histopatologija obloge benignog seroznog tumora jajnika.
Benigni serozni tumori jajnika su jednostruke ciste tankih zidova koje su obložene trepljičastim pseudostratifikovanim kuboidnim ili stubastim epitelom.[16]
Ovi tumori variraju u veličini, od malih i gotovo neprimetnih do velikih, ispunjavajući trbušnu šupljinu.
Benigni, granični i maligni tipovi seroznih tumora čine oko 30% svih tumora jajnika.
Oko 75% je benignih ili graničnih maligniteta, a 25% je malignih
Maligni oblik ovog tumora, serozni cistadenokarcinom, čini približno 40% svih karcinoma jajnika i najčešći su maligni tumori jajnika.
Benigni i granični tumori su najčešći su u dobi između 20 i 50 godina.
Maligni serozni tumori javljaju se u proseku kasnije u životu, mada nešto i ranije u porodičnim slučajevima.[17]
Oko 20% benignih, 30% graničnih i 66% malignih tumora je obostrano (pogađa oba jajnika).
Komponente ovih tumora mogu da uključuju:
- cistična područja
- cistična i vlaknasta područja
- pretežno vlaknasta područja
Šansa za malignitet tumora raste sa količinom prisutnih čvrstih područja, uključujući i papilarne strukture i bilo koje prisutno nekrotičnog tkiva.
Patologija[уреди | уреди извор]

- Ova vrsta tumora obložena je visokim, stubičastim i trepljastim epitelnim ćelijama.
- Ispunjen je bistrom seroznom tečnošću
- Pojam seroza koji opisuje tečnosti ciste, počeo je da se primewnjuje za određeni tip epitelne ćelije viđen u ovim tumorima
- može zahvatiti površinu jajnika.[18]
Podela između benignih, graničnih i malignih utvrđuje se procenom:[19]
- ćelijska atipija (bez obzira da li pojedinačne ćelije izgledaju abnormalno)
- invazija strome okolnih jajnika (bilo da se ćelije infiltriraju u okolno tkivo ili ne)
- granični tumori mogu imati ćelijsku atipiju, ali nema dokaza o invaziji,
- prisustvo tela psamoma je karakterističan mikroskopski nalaz cistadenokarcinoma.[20]
Prognoza[уреди | уреди извор]
Prognoza seroznog tumora, kao i većina neoplazmi, zavisi od:
- stepen diferencijacije
- koliko bliske tumorske ćelije podsećaju na benigne ćelije
- dobro diferencirani tumor veoma liči na benigne tumore
- slabo diferencirani tumor možda uopšte ne podseća na tip porekla ćelije
- umereno diferencirani tumor obično podseća na ćelijski tip porekla, ali deluje iskreno maligno
- proširenje tumora na druge strukture
- posebno kod seroznih malignih bolesti, prisustvo malignog širenja na peritoneum je važno s obzirom na prognozu.
Petogodišnja stopa preživljavanja graničnih tumora i malignih tumora ograničenih na jajnike iznosi 100%, odnosno 70%. Ako je zahvaćen peritoneum, ove stope postaju 90% i 25%.
Iako su petogodišnje stope preživljavanja graničnih tumora odlične, ovo ne treba smatrati dokazom izlečenja, jer se recidivi mogu javiti mnogo godina kasnije.
Mucinozni tumori[уреди | уреди извор]

Mucinozni tumori zrazito podsećaju na njihove serozne kolege, ali verovatno neće biti bilateralni
Nešto ređe, čini oko 25% svih novotvorina na jajnicima
U nekim slučajevima mucinozne tumore karakterišu više cista promenljive veličine i retkost površinskog zahvaćanja u poređenju sa seroznim tumorima
Takođe u poređenju sa seroznim tumorima, mucinski tumori su ređe obostrani, približno 5% primarnih mucinoznih tumora je obostrano.
Može formirati vrlo velike cistične mase, sa zabeleženom težinom većom od 25 kg
Patologija[уреди | уреди извор]
Mucinozne tumore karakteriše obloga visokih ćelijskih epitelnih ćelija sa apikalnim mucinom i odsustvom trepavica, sličnih po izgledu sa benignim cervikalnim ili crevnim epitelom. Izgled može izgledati slično raku debelog creva ili jajnika, ali tipično potiče iz slepog creva (vidi mucinozni adenokarcinom sa kliničkim stanjem Pseudomikoma peritonei). Jasna stromalna invazija koristi se za razlikovanje graničnih tumora od malignih.
Prognoza[уреди | уреди извор]
Stope preživljavanja od 10 godina za granične tumore sadržane u jajniku, maligne tumore bez invazije i invazivne maligne tumore veće su od 95%, 90%, odnosno 66%. Jedno retko, ali vredno pažnje, povezano sa mucinoznim novotvorinama jajnika je pseudomiksom peritonej. Kako su primarni mucinozni tumori jajnika obično jednostrani (u jednom jajniku), prezentacija bilateralnih mucinoznih tumora zahteva izuzeće ne-jajničkog porekla, obično slepog creva.
Endometrioidni tumori[уреди | уреди извор]
Endometrioidni tumori jajnika mogu biti benigni, sa proliferacijom i maligni.
- Benigni endometrioidni tumori
Benigni endometrioidni tumori su relativno retki i obično se javljaju obostrano. Dostižu veličinu ženske pesnice i izazivaju zapaljenjsku reakciju na svojoj površini, pa su često srasli sa okolinom. Zbog toga se kod ovih tumora ne javlja komplikacija u vidu torzije. Po građi potiču od tkiva endometrijuma čije poreklo u ovim tumorima nije razjašnjeno. Postoji više hipoteza o tome. U svakom slučaju ćelije endometrijuma iz kojih potiču ovi tumori, zadržavaju svoje funkcionalne osobine i pod uticajem seksualnih hormona u njima se dešavaju redovne ciklične promene, praćene krvarenjem. Na taj način sadržaj ciste dobija hemoragičan karakter i kasnije poprima čokoladnu boju ili boju katrana. Pacijentkinje osećaju dismenoreične tegobe, a često pate od dispareunije. Takođe, ovi tumori mogu biti uzrok neplodnosti.
Endometrioidni tumori mogu po histološkoj građi biti:
- adenomi, u obliku solidnih tumora,
- cistadenomi, u obliku mešovitih solidno cističnih tumora
- Tumori sa proliferacijom
Neki od tumora jajnika spadaju u granično maligne tumore tumore sa proliferacijama, čije ćelije pokazuju izvesne osobine svojstvene malignim neoplazmama. Ovi tumori vremenom postaju pravi maligni tumori endometrioidni adenokarđnomi.
- Maligni endometrioidni tumori
Endometrioidni tumori cistični ili solidni mogu biti maligni od samog početka (endometroidni karcinomi), i čine približno 20% svih karcinoma jajnika Napravljene su od cevastih žlezda koje podsećaju na benigni ili maligni endometrijum. Od 15 do 30% endometrioidnih karcinoma jajnika javlja se kod osoba sa karcinomom endometrijuma i ovi pacijenti imaju lošiju prognozu. Izgledaju slično ostalim površinskim epitelno-stromalnim tumorima, sa čvrstim i cističnim područjima. Oko 40% ovih tumora je obostrano, kada su obostrane metastaze često prisutne.
Patologija[уреди | уреди извор]
Benigni tumori imaju zrele žlezde u fibroznoj stromi.
Granični tumori imaju složen obrazac grananja bez stromalne invazije.
Karcinomi (maligni tumori) imaju invazivne žlezde sa prepunim, atipičnim ćelijama, čestim mitozama. Sa lošijom diferencijacijom, tumor postaje čvršći (kompaktniji).
Prognoza[уреди | уреди извор]
Prognoza u mnogome zavisi od širenja tumora, kao i od toga koliko se tumor razlikuje. Ukupna prognoza je nešto lošija nego za serozne ili mucinozne tumore, a petogodišnja stopa preživljavanja kod pacijenata sa tumorima ograničenim na jajnik iznosi približno 75%.
Bistroćelijski tumori[уреди | уреди извор]

Bistroćelijske tumore karakterišu velike epitelne ćelije sa obilnom bistrom citoplazmom i mogu se videti u vezi sa endometriozom ili endometrioidnim karcinomom jajnika, što ima sličnost sa karcinomom bistrih ćelija endometrijuma. Mogu biti pretežno čvrsti ili cistični. Ako su čvrste, bistre ćelije imaju tendenciju da budu raspoređene u čaršave ili tubule. Kod cistične sorte, neoplastične ćelije čine oblogu ciste.
Prognoza[уреди | уреди извор]
Ovi tumori imaju tendenciju da budu agresivni, petogodišnja stopa preživljavanja tumora ograničenih na jajnike iznosi približno 65%. Ako se tumor prilikom dijagnoze proširio izvan jajnika, prognoza je loša
Brenerov tumor[уреди | уреди извор]

Brenerovi tumori su neuobičajeni tumori površinskih epitelnih stromalnih ćelija u kojima je epitelna ćelija (koja definiše ove tumore) prelazna ćelija. Po izgledu su slični epitelima bešike. Tumori mogu biti vrlo mali do vrlo veliki i mogu biti čvrsti ili cistični. Histološki se tumor sastoji od gnezda pomenutih prelaznih ćelija unutar okolnog tkiva koje podseća na normalan jajnik. Brenerovi tumori mogu biti benigni ili maligni, u zavisnosti od toga da li tumorske ćelije napadaju okolno tkivo.[22][23][24]
Tumori malih ćelija[уреди | уреди извор]
Dvoćelijski rak jajnika (SCCO) obično se klasifikuju u epitelne tumore[тражи се извор] povezane sa prepoznatljivim endokrinim karakteristikama.[25]
Svetska zdravstvena organizacija (VHO) prepoznaje SCCO kao dva različita entiteta: rak jajnika malih ćelija hiperkalcemičnog tipa (SCCOHT) i rak jajnika malih ćelija plućnog tipa (SCCOPT).[25]
Sitnoćelijski tumori su retki i agresivni, oni doprinose manje od 2% svih ginekoloških malignih bolesti.[25] Prosečna starost dijagnoze je 24 godine, a većina pacijenata takođe ima hiperkalcemiju (62%).[26] Tipično se javlja sa jednostranim velikim tumorom.[26] Većina žena umire u roku od godinu dana od postavljanja dijagnoze.[26]
Dijagnoza[уреди | уреди извор]
Napredak u molekularnoj biologiji i velika količina literature o upotrebi pomoćnih tehnika za bolje razumijevanje tumora površinskog epitela jajnika su u porastu, ali još uvijek su morfološke studije histopatološkim tehnikama i dalje okosnica za dijagnozu ovih tumora.[27][28]
Histopatološka dijagnoza tumora jajnika zasniva se na određivanju iz uzorka ćelijskog tipa tumora. Na osnovu tipova ćelija, prema jednoj studiji iz Indije,[27] dijagnostikovano je 61,7% seroznih tumora, 34,8% mucinoznih tumora, jedan karcinom bistrih ćelija, jedan endometrioidni karcinom i 3 benigna tumora prijelaznih ćelija. Učestalost pojave ovih tumora iz ove studije uporediva sa studijama koje su radili drugi istraživači.[29][30][31][32]
Terapija[уреди | уреди извор]
Istraživanja sugerišu da se u prvoj liniji za lečenja raka jajnika endometrijuma koristi pegilovani liposomski doksorubicin zajedno sa karboplatinom, zadovoljavajuća alternativa paklitakselu sa karboplatinom.[33] Kod osoba sa relapsom EOC osetljivim na platinu, istraživanje je otkrilo da je pegilovani liposomski doksorubicin sa karboplatinom bolji tretman od paklitaksela sa karboplatinom.[34]
Za uznapredovale oblike ove histologije, Američki nacionalni institut za rak preporučuje metod hemoterapije koji kombinuje intravensku (IV) i intraperitonealnu (IP) administraciju.[35] Poželjna hemoterapeutska sredstva uključuju platinu sa taksanom.
Prema vodičima Internacionalne asocijacije za ginekologiju i akušerstvo (FIGO) standardni tretman žena sa epitelnim ovarijalnim karcinomom sastoji se od kompletnog hirurškog stadiranja koje podrazumeva:[1]
- totalnu abdominalnu histerektomiju,
- bilateralnu salpingooforektomiju,
- disekciju pelvičnih i paraaortnih limfnih čvorova,
- infrakoličnu omentektomiju,
- multiplu pelvičnu citologiju ispiraka,
- multiple peritonealne biopsije,
- maksimalnu citoreduktivnu hirurgiju.
Standardni hirurški postupak, međutim, bolesnicu u potpunosti lišava fertilnosti.
Promene stava o radikalnoj onkološkoj hirurgiji, vođene su sa idejom da ne bi trebalo određivati koristi samo prema kontroli bolesti, već i prema kvalitetu života, a pre svega prema očuvanju fertilnosti mlađih bolesnica sa karcinomom ovarijuma.[36]
Zbog tendencije da žene danas rađaju svoje prvo dete u poznijim reproduktivnim godinama i veće dostupnosti različitih dijagnostičkih metoda, dijagnoza EOK pre ostvarivanja reprodukcije postaje sve češća. Shodno tome, sve su veći zahtevi za hirurgijom očuvanja fertiliteta u ranim stadijumima EOK.[1]
Da li je kompletno hirurško stadiranje uvek neophodno?[уреди | уреди извор]
U studiji Cho i sar.[37] utvrđeno je da su morbiditet i incidencija postoperativnih komplikacija bili viši kod kompletno stadiranih, nego nekompletno stadirane bolesnice. Histološki podtip tumora trebalo bi da utiče na procedure koje zahteva hirurško stadiranje. Ova studija odnosila se na mucinozne adenokarcinome stadijuma I, među bolesnicama koje nisu bile inicijalno hirurški stadirane; 5,9% njih bilo je supstadirano u odnosu na peritonealnu citologiju, a nije bilo supstadiranih u pogledu prisustva okultnih limfnonodusnih metastaza. Oni su, takođe, utvrdili da nema značajnih razlika u rekurentnosti, periodu bez bolesti i ukupnom preživljavanju u odnosu na kompletnost stadiranja kod bolesnica sa mucinoznim adenokarcinomom u stadijumu I bolesti. Ovi autori smatraju da kompletno hirurško stadiranje sa disekcijom limfnih čvorova nema uticaja na preživljavanje bolesnica sa mucinoznim adenokarcinomom u stadijumu I bolesti i da bi, verovatno, moglo biti izostavljeno kod ovih bolesnica.[38]
Metastaze[уреди | уреди извор]
Za površinske epitelno-stromalne ovarijalne tumore (posebno karcinome), najčešća mesta metastaziranja su, u:[39]
- 33% slučajeva pleuralna šupljina,
- 26% slučajeva jetra pluća
- 3% slučaja pluća.
Uticaj na plodnost[уреди | уреди извор]
Plodnost nakon tretmana površinskih epitelnih ovarijalnih tumora uglavnom zavisi od histologije i početnog stadijuma tumora koji se dele na benigniji, i one u naprednijim stadijuma (ili više maligne).[40]
Procenjuje se da konzervativno lečenje (bez bilateralne ooforektomije) graničnih tumora u ranoj fazi ima šansu za preko 50% spontanih trudnoća sa malim rizikom od pojave smrtnosne ponovne pojave tumora (0,5%).[40] S druge strane, u slučajevima konzervativnog lečenja u poodmakloj fazi graničnih tumora, procenjuje se da su stope spontane trudnoće 35%, a rizik od letalnog recidiva 2%.[40]
Incidencija metastaza u limfnim čvorovima kod bolesnica u stadijumu I mucinoznog adenokarcinoma iznosila je 3%, u poređenju sa 27% kod onih sa seroznim adenokarcinomom 20.
Prognoza[уреди | уреди извор]
Prognoza seroznog tumora, kao i većina neoplazmi, zavisi od stepen diferencijacije i obima malignog proširenje tumora na druge strukture posebno kod seroznih malignih oboljenja, prisustvo malignog širenja na peritoneum je važno s obzirom na prognozu.[41]
Petogodišnja stopa preživljavanja graničnih i malignih tumora ograničenih na jajnike iznosi 100%, odnosno 70%. Ako je zahvaćen peritoneum, ove stope postaju 90% i 25%.
Iako su petogodišnje stope preživljavanja graničnih tumora odlične, ovo ne treba smatrati dokazom izlečenja, jer se recidivi mogu javiti mnogo godina kasnije.
Izvori[уреди | уреди извор]
- ^ а б в Milošević J, et al.Trudnoća nakon konzervativnog hirurškog lečenja mucinoznog adenokarcinoma jajnika, Vojnosanitetski pregled 2011; 68(1): 77–80.
- ^ а б Global cancer statistics, 2002. Parkin DM, Bray F, Ferlay J, Pisani P CA Cancer J Clin. 2005 Mar-Apr; 55(2):74-108.[PubMed] [Ref list]
- ^ Study of 'patterns of care' of ovarian cancer patients in a specialized cancer institute in Kolkata, eastern India. Basu P, De P, Mandal S, Ray K, Biswas J Indian J Cancer. 2009 Jan-Mar; 46(1):28-33.
- ^ Consolidated Report of Population Based Cancer Registries 2001-2004. National Cancer Registry Program Bangalore: Indian Council of Medical Research. 2006. [Ref list]
- ^ Tavassoli FA, Devilee P. Tumours of Breast and Female Genital Organs. Lyon: IARC Press; 2003. WHO classification of tumours. Pathology and Genetics. [Google Scholar]
- ^ Clement PB, Young HR. Sternberg’s Diagnostic Surgical Pathology, 5th Edition. Ovarian Surface Epithelial-Stromal Tumours. Lippincott Williams & Wilkins; 2010. pp. 2272–306. [Google Scholar]
- ^ Scully RE. International Histological Classification of Tumours: Histological Typing of Ovarian Tumours. 2nd edition. Heidelberg: Springer-Verlag; 1998. [Google Scholar]
- ^ а б Jemal A, Siegel R, Ward E, Murray T, Xu J, Smigal C, et al. Cancer statistics, 2006. CA Cancer J Clin 2006; 56(2): 106–30.
- ^ McGuire V, Jesser CA, Whittemore AS. Survival among U.S. women with invasive epithelial ovarian cancer. Gynecol Oncol 2002; 84(3): 399–403
- ^ Green JA. Early ovarian cancer-time for a rethink on stage? Gynecol Oncol 2003; 90(2): 235–7.
- ^ „Benign Ovarian Surface Epithelial-Stromal Tumor”. www.ebi.ac.uk. Приступљено 2021-03-25.
- ^ Ishioka S-I, Sagae S, Terasawa K, Sugimura M, Nishioka Y, Tsukada K, Kudo R. Comparison of the usefulness between a new universal grading system for epithelial ovarian cancer and the FIGO grading system. Gynecol Oncol 2003;89:447-452.
- ^ Kaimaktchiev V, Terracciano L, Tornillo L, Spichtin H, Stoios D, Bundi M, Korcheva V, Mirlacher M, Loda M, Sauter G, Corless CL. The homeobox intestinal differentiation factor CDX2 is selectively expressed in gastrointestinal adenocarcinomas. Mod Pathol 2004;17:1392-1399.
- ^ Kurman RJ, Shih LM. Pathogenesis of ovarian cancer. Lessons from morphology and molecular biology and their clinical implications. Int J Gynecol Pathol 2008;27:151- 160.
- ^ Logani S, Oliva E, Amin MB, Folpe AL, Cohen C, Young RH. Immunoprofile of ovarian tumors with putative transitional cell (urothelial) differentiation using novel urothelial markers. Histogenetic and diagnostic implications. Am J surg pathol 2003;27:1434-1441.
- ^ Baradwan, Saeed; Alalyani, Haneen; Baradwan, Amira; Baradwan, Afnan; Al-Ghamdi, Maram; Alnemari, Jameel; Al-Jaroudi, Dania (2018). "Bilateral ovarian masses with different histopathology in each ovary". Clinical Case Reports. 6 (5): 784–787.
- ^ McCluggage WG, Lyness RW, Atkinson RJ, Dobbs SP, Harley I, McClelland HR, Price JH. Morphological effects of chemotherapy on ovarian carcinoma. J Clin Pathol 2002;55:27-31.
- ^ Dobbs SP, McClelland RH, Kennedy K, McCluggage WG. An immunohistochemical and morphological analysis of past-chemotherapy ovarian carcinoma. J clin Pathol 2008;61:652-657.
- ^ McCluggage WG. The pathology of and controversial aspects of ovarian borderline tumours. Curr Opin Oncol 2010; 22:462-472. Miller K, Price JH,
- ^ Cotran RS, Kumar V, Nelson F, Robbins SL, Abbas AK (2005). Robbins and Cotran pathologic basis of disease (7th ed.). St. Louis, Mo: Elsevier Saunders. . ISBN 978-0-7216-0187-8. Недостаје или је празан параметар
|title=(помоћ). - ^ Baradwan, Saeed; Alalyani, Haneen; Baradwan, Amira; Baradwan, Afnan; Al-Ghamdi, Maram; Alnemari, Jameel; Al-Jaroudi, Dania (2018). „Bilateral ovarian masses with different histopathology in each ovary”. Clinical Case Reports. 6 (5): 784—787. PMC 5930217
 . PMID 29744056. doi:10.1002/ccr3.1466.
. PMID 29744056. doi:10.1002/ccr3.1466.
- ^ F. Brenner: Das Oophoroma folliculare. Frankfurter Zeitschrift für Pathologie, München, 1907, 1: 150-171.
- ^ Philipp, Elliot Elias; O'Dowd, Michael J. (2000). The history of obstetrics and gynaecology. Carnforth, Lancs: Parthenon. p. 586
- ^ Pelusi G, Taroni B, Flamigni C. Benign ovarian tumors. Front Biosci 1996;1:16-9.
- ^ а б в Kaphan AA, Castro CM (2014-01-01). MPH rG, FRCPATH RH, MD JO, MD MJ (eds.). Small Cell and Neuroendocrine Cancers of the Ovary. John Wiley & Sons, Ltd. pp. 139–147. Kaphan, Ariel A.; Castro, Cesar M. (2014). „Small Cell and Neuroendocrine Cancers of the Ovary”. Uncommon Gynecologic Cancers. стр. 139—147. ISBN 9781118655351. doi:10.1002/9781118655344.ch12.. . ISBN 9781118655344. Недостаје или је празан параметар
|title=(помоћ). - ^ а б в Bakhru A, Liu JR, Lagstein A (2012). "A case of small cell carcinoma of the ovary hypercalcemic variant in a teenager". Bakhru, Arvind; Liu, J. Rebecca; Lagstein, Amir (2012). „A case of small cell carcinoma of the ovary hypercalcemic variant in a teenager”. Gynecologic Oncology Case Reports. 2 (4): 139—142. PMC 3861231
 . PMID 24371647. doi:10.1016/j.gynor.2012.09.001.
. PMID 24371647. doi:10.1016/j.gynor.2012.09.001.
- ^ а б Modepalli, Nalini; Venugopal, Suguna Belur (1. 10. 2016). „Clinicopathological Study of Surface Epithelial Tumours of the Ovary: An Institutional Study”. Journal of Clinical and Diagnostic Research : JCDR. 10 (10): EC01—EC04. ISSN 2249-782X. PMC 5121679
 . PMID 27891341. doi:10.7860/JCDR/2016/21741.8716.
. PMID 27891341. doi:10.7860/JCDR/2016/21741.8716.
- ^ Zhao C, Bratthauer GL, Barner R, Vang R. Diagnostic utility of WT1 immunostianing in ovarian Sertoli cell tumor. Am J Surg Pathol 2007;31:1378-1386.
- ^ Kanthikar SN, Dravid NV, Deore PN, Nikumbh DB, Suryawanshi KH. Clinico-Histopathological analysis of neoplastic and non-neoplastic lesions of the ovary: A 3-Year prospective study in Dhule, North Maharashtra, India. Journal of Clinical and Diagnostic Research : JCDR. 2014;8(8):FC04–FC07. [PMC free article] [PubMed] [Google Scholar]
- ^ >Dawar R. Surface epithelial tumours of ovary. Indian Journal of Medical & Paediatric Oncology. 2004;25(1):5–9. [Google Scholar]
- ^ Tushar K, Asanranthi K, Mohapatra PC. Intraoperative cytology of ovarian tumours. J Obstet Gynecol India. 2005;55(4):345–49. [Google Scholar]
- ^ Swamy GG, Satyanarayana N. Clinicopathological analysis of ovarian tumours – A study on five years samples. Nepal Medical College Journal. 2010;12(4):221–23.
- ^ Lawrie TA, Rabbie R, Thoma C, Morrison J, et al. (The Cochrane Collaboration) (October 2013). Lawrie TA (ed.). "Pegylated liposomal doxorubicin for first-line treatment of epithelial ovarian cancer". The Cochrane Database of Systematic Reviews. John Wiley & Sons, Ltd (10): CD010482. Lawrie, Theresa A.; Rabbie, Roy; Thoma, Clemens; Morrison, Jo (2013). „Pegylated liposomal doxorubicin for first-line treatment of epithelial ovarian cancer”. Ур.: Lawrie, Theresa A. Cochrane Database of Systematic Reviews. 2013. стр. CD010482. PMC 6457824
 . PMID 24142521. doi:10.1002/14651858.cd010482.pub2..
. PMID 24142521. doi:10.1002/14651858.cd010482.pub2..
- ^ Lawrie, Theresa A.; Bryant, Andrew; Cameron, Alison; Gray, Emma; Morrison, Jo (2013). „Pegylated liposomal doxorubicin for relapsed epithelial ovarian cancer”. Cochrane Database of Systematic Reviews. 2016 (9): CD006910. PMC 6457816
 . PMID 23835762. doi:10.1002/14651858.cd006910.pub2..
. PMID 23835762. doi:10.1002/14651858.cd006910.pub2..
- ^ „Intraperitoneal Therapy for Ovarian Cancer - National Cancer Institute”. 2009-01-13. Архивирано из оригинала 13. 01. 2009. г. Приступљено 2021-03-15.
- ^ Park JY, Kim DY, Suh DS, Kim JH, Kim YM, Kim YT, et al. Outcomes of fertility-sparing surgery for invasive epithelial ovarian cancer: oncologic safety and reproductive outcomes. Gynecol Oncol 2008; 110(3): 345–53.
- ^ Cho YH, Kim DY, Kim JH, Kim YM, Kim KR, Kim YT, et al. Is complete surgical staging necessary in patients with stage I mucinous epithelial ovarian tumors? Gynecol Oncol 2006; 103: 878–82.
- ^ 20. Di Re F, Fontaneli R, Raspagliesi F, Di Re E. Pelvic and paraaortic lymphadenectomy in cancer of the ovary. Bailliéres Clin Obstet Gynaecol 1989; 3: 131–42.
- ^ Kolomainen, Desiree F.; Larkin, James M.G.; Badran, Mohammad; a'Hern, Roger P.; King, D. Michael; Fisher, Cyril; Bridges, Jane E.; Blake, Peter R.; Barton, Desmond P.J.; Shepherd, John H.; Kaye, Stanley B.; Gore, Martin E. (2002). „Epithelial Ovarian Cancer Metastasizing to the Brain: A Late Manifestation of the Disease with an Increasing Incidence”. Journal of Clinical Oncology. 20 (4): 982—986. PMID 11844820. doi:10.1200/JCO.2002.20.4.982..
- ^ а б в Daraï, Emile; Fauvet, Raffaèle; Uzan, Catherine; Gouy, Sébastien; Duvillard, Pierre; Morice, Philippe (2013). „Fertility and borderline ovarian tumor: A systematic review of conservative management, risk of recurrence and alternative options”. Human Reproduction Update. 19 (2): 151—166. PMID 23242913. doi:10.1093/humupd/dms047..
- ^ Slomovitz BM, Caputo TA, Gretz HF III, Economos K, Tortoriello DV, Schlosshauer PW, Baergen RN, Isacson C, Soslow RA. A comparative analysis of 57 serous borderline tumors with and without a noninvasive micropapillary component. Am J Surg Pathol 2002;26:592-600.
Literatura[уреди | уреди извор]
- E. G. Orthmann: Zur Casuistik einiger seltener Ovarial- und Tuben-Tumoren. Monatsschrift für Geburtshülfe und Gynäkologie, Berlin, 1899, 9: 771-782.
- E. G. Orthmann: Über die Entstehungsweisen der Sacrosalpingen und Tubo-Ovarialcysten. [Virchows] Archiv für pathologische Anatomie und Physiologie, und für klinische Medizin, Berlin, 1899, 155: 220-234.
- Dukic M, Jurisic A, Markovic S, Rakic S, Runic S, Andelić S. Dijagnostićka vrednost kolor dopler ultrasonografije u otkrivanju malignih tumora ovarijuma. Zbornik radova XL ginekol. akus. ned, Beograd: 1996;409-15.
Spoljašnje veze[уреди | уреди извор]
| Klasifikacija |
|---|
- Johns Hopkins: "Surface Epithelial Tumors" Архивирано на сајту Wayback Machine (19. фебруар 2020) (језик: енглески)
- Diagram: "Epithelial Stromal Ovarian Tumors" (језик: енглески)
- Small Cell Ovarian Cancer Research Collaboration & Patients Registry Архивирано на сајту Wayback Machine (14. фебруар 2019) (језик: енглески)
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
