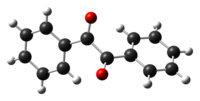
Benzil

| |
| |
| |
| Nazivi | |
|---|---|
| IUPAC naziv
1,2-diphenylethane-1,2-dione
| |
| Drugi nazivi
dibenzoil
bibenzoil difenilglioksal difeniletandion 1,2-difeniletan-1,2-dion 1,2-difenil-etandion difenil-α,β-diketon | |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.004.689 |
| |
| |
| Svojstva | |
| C14H10O2 | |
| Molarna masa | 210,23 g·mol−1 |
| Agregatno stanje | žuti kristali ili prah |
| Gustina | 1,23 g/cm3, чврсти материјал (1.255 g/cm3) |
| Tačka topljenja | 94.43-95.08 °C, 201.97-203.14 °F, 367-368 K |
| Tačka ključanja | 346- 348 °C, 654.8-658.4 °F, 619-621 K |
| nerastvoran | |
| Rastvorljivost u benzen | rastvoran |
| Struktura | |
| Kristalna rešetka/struktura | P31,221[3] |
| Dipolni moment | 3.8 D[4] |
| Opasnosti | |
| Glavne opasnosti | Iritant |
| NFPA 704 | |
| Srodna jedinjenja | |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25°C [77°F], 100 kPa). | |
| Reference infokutije | |
Benzil je aromačni 1,2-diketon, sa hemijskom formulom (С6Н5СО)2 ili kraće (PhCO)2. Njegovo sistemsko ime po IUPAC-u je 1,2-difenil-1,2-etandion. Poznat je i pod drugim imenima kao dibenzoil, bibenzoil, difenilglioksal, difeniletandion, 1,2-difeniletan-1,2-dion, 1,2-difenil-etandion, difenil-α,β-diketon. Nalazi se u čvrstom stanju. Kristali su mu žute boje.
Ovaj diketon se koristi kao intermedijer u organskoj sintezi. Benzil se takođe koristi kao fotoinicijator slobodnih radikala za lečenje polimernih mreža. Ultraljubičasto zračenje rastavlja benzil, stvarajući slobodne radikale koji se kreću kroz polimerni materijal, stvarajući unakrsne veze između indivedualnih polimernih lanaca. Nedavno benzil je identifikovan kao selektivni inhibitor enzima karboksilesteraza, proteina uključenih u metalolizam esterifikovanih lekova i ksenobiotika.
Dobijanje benzila[uredi | uredi izvor]
Benzil se lako može dobiti oksidacijom benzoina azotnom kiselinom, hloridom i jodidom. Čak i blaga oksidaciona sredstva, kao Felingov rastvor ili bakar-sulfat u piridinu mogu dovesti do reakcije. U praksi se za oksidaciju benzoina u benzil najčešće koristi bakar-sulfat u piridinu i azotna kiselina. Kod oksidacije benzoina sa bakar-sulfatom koristi se njegov rastvor u piridinu, jer piridin sprečavava taloženje bakar oksida, nije isparljiv kao amonijak, i ponaša se kao delimični rastvarač za benzoin. Pri oksidaciji benzoina sa azotnom kiselinom izdvajaju se otrovni oksidi azota, pa je sintezu neophodno izvoditi u digestoru.[5]
Izvori[uredi | uredi izvor]
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Acta Cryst. B43 398 (1987)
- ^ Spectrochim. Acta A60 (8-9) 1805 (2004)
- ^ „Benzil”. Organic Syntheses, Coll. 1: 87. 1941.

