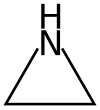
Азиридин
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
Aziridine
| |||
| Други називи
Азациклопропан, Етилен имин
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.005.268 | ||
| EC број | 205-793-9 | ||
| КЕГГ[1] | |||
| |||
| Својства | |||
| C2H5N | |||
| Моларна маса | 43,07 g·mol−1 | ||
| Агрегатно стање | Цлеар цолорлесс оилy лиqуид[2] | ||
| Густина | 0,8321 g/ml 20 °C[3] | ||
| Тачка топљења | -77.9 °C | ||
| Тачка кључања | 56 °C | ||
| мисцибле алл пропортионс | |||
| Опасности | |||
| Тачка паљења | -11°Ц | ||
| Сродна једињења | |||
Сродне хетероциклизација
|
Бориран, Етилен оксид, Етилен сулфид | ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||
Азиридини су органска једињења која садрже азиридинску функционалну групу, трочлано хетероциклично једињење са једном амино групом и две метиленске групе.[4][5] Основно једињење је азиридин (или етилен имин), са молекулском формулом C2H5N.
Структура
[уреди | уреди извор]Углови веза азиридина су приближно 60°, што је знатно мање од нормалног угљоводоничног угла везе од 109.5°. Последица тога је ангуларно напрзање слично молекулима циклопропана и оксирана. Модел савијених веза објашњава везивање таквих једињења. Азиридин је мање базан него ациклични алифатични амини, са пКа од 7.9 за коњуговану киселину, услед повећаног s карактера слободног електронског пара азота. Ангуларно напрезање у азиридину такође повишава баријеру инверзије азота. Висина ове баријере омогућава изолацију засебних инвертомера, на пример цис и транс инвертомери N-хлоро-2-метилазиридина.
Синтеза
[уреди | уреди извор]Постоји више синтетичких путева.
Циклизација халоамина и амино алкохола
[уреди | уреди извор]Аминска функционална група истискује суседни халид у реакцији интрамолекулске нуклеофилне супституције чиме се формира азиридин. Амино алкохоли имају једнаку реактивност, али се хидроксилна група мора прво конвертовати у добру одлазећу групу. Циклизација амино алкохола се зове Венкерова синтеза (1935), а циклизација халоамина Габриелов етиленимински метод (1888)[6].
Адиција нитрена
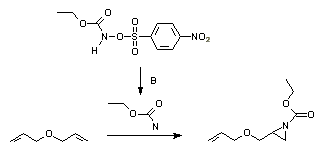
[уреди | уреди извор]Адиција нитрена у алкене је добро-познат метод за синтезу азиридина. Фотолиза или термолиза азида су поуздани начини формирања нитрена. Нитрени такође могу да се припреме ин ситу из јодозобензен диацетата и сулфонамида, или етоксикарбонилнитрен из N-сулфонилокси прецурсора.[7]
Референце
[уреди | уреди извор]- ^ Јоанне Wиxон; Доуглас Келл (2000). „Wебсите Ревиеw: Тхе Кyото Енцyцлопедиа оф Генес анд Геномес — КЕГГ”. Yеаст. 17 (1): 48—55. дои:10.1002/(СИЦИ)1097-0061(200004)17:1<48::АИД-YЕА2>3.0.ЦО;2-Х.
- ^ „Азиридине” (пдф).
- ^ Лиде Давид Р., ур. (2006). ЦРЦ Хандбоок оф Цхемистрy анд Пхyсицс (87тх изд.). Боца Ратон, ФЛ: ЦРЦ Пресс. ISBN 978-0-8493-0487-3.
- ^ Heterocyclic chemistry. Harlow, England: Longman Scientific. 1987. ISBN 978-0-582-01421-3.
- ^ Albert Padwaa and S. Shaun Murphreeb (2006). „Epoxides and aziridines - A mini review”. Arkivoc: 6—33.
- ^ „Gabriel Ethylenimine Method”.
- ^ Addition reactions of ethoxycarbonylnitrene and ethoxycarbonylnitrenium ion to allylic ethers M. Antonietta Loreto, Lucio Pellacani, Paolo A. Tardella, and Elena Toniato Tetrahedron Letters, Volume 25, Issue 38, 1984, Pages 4271-4274 Abstract Архивирано 2012-09-09 на сајту Archive.today
Литература
[уреди | уреди извор]- Хетероцyцлиц цхемистрy. Харлоw, Енгланд: Лонгман Сциентифиц. 1987. ИСБН 978-0-582-01421-3.