Transplantacija krvnih matičnih ćelija u mukopolisaharidozama
| Transplantacija krvnih matičnih ćelija u mukopolisaharidozama | |
|---|---|
 | |
| ICD-10-PCS | Koštani transplant spreman za primenu |
Transplantacija krvnih matičnih ćelija ili transplantacija hematopoetskih matičnih ćelija u mukopolisaharidozama (skraćeno HSCT) je savremena metoda lečenja u transplantologiji u kojoj se multipotentne hematopoetske (krvotvorne) matične ćelije koriste za ponovno uspostavljanje hematopoetske funkcije koja je prisutna na niskim nivoima ili je potpuno izgubljene u 7 tipova mukopolisaharidoza. Naslednioh genskih poremećaja uzrokovanih nedostatkom specifičnih lizozomskih enzima uključenih u degradaciju glikozaminoglikana (skraćeno GAGs ) ili mukopolisaharida, u kojem akumulacija delimično degradiranih produkata glikozaminoglikana izaziva smetnje u ćeliji, tkivu, narušava funkcije pojedinih organa, i izaziva preranu smrt.[1]
Dosadašnje iskustvo sa transplantacija matičnih ćelija je pozitivno, a rizici povezani sa ovom intervencijom takođe su smanjeni. Međutim, rezultati lečenja su često nedovoljni, posebno kod skeletnih simptoma. Decu koja su prošla transplantaciju hematopoetskih matičnih ćelija trebalo bi redovno da prate stručnjaci za mukopolisaharidozne sindrome, kako za procenu rezultata lečenja tako i za sprečavanje eventualnih komplikacija.
Istorija[uredi | uredi izvor]
Hematopoetska transplantacija matičnih ćelija za lečenje mukopolisaharidoza prvi put je primenjena 1980. godine.[2] Narednih godina, korišćena je za lečenje MPS tip II (1981),[3] MPS tip VI (1982),[4] i MPS tip VII (1998).[5]
Trenutno, hematopoetska transplantacija matičnih ćelija je dokazano efikasna, i primenjuje se za lečenje mukopolisaharidoze tip I, mukopolisaharidoze tip II, mukopolisaharidoze tip VI i mukopolisaharidoze tip VII.[6][7][8]
Opšta razmatranja[uredi | uredi izvor]
Hematopoetska transplantacija matičnih ćelija (HSCT) je metod lečenja u kojoj se multipotentne hematopoetske (krvotvorne) matične ćelije koriste za ponovno uspostavljanje hematopoetske funkcije koja je prisutna na niskim nivoima ili je potpuno izgubljena zbog teške bolesti. Ove ćelije (najbolje uzete od autolognih ili alogenih donora) se obično prikupljaju oiz krvi pupčane vrpce, koštane srži ili periferne krvi i intravenozno se injektiraju u pacijenta čiji imuni sistem ili koštana srž nije adekvatan da funkcioniše kako treba.
Matične ćelije[uredi | uredi izvor]

Sve krvne ćelije se proizvode se iz matičnih ćelija krvi (hematopoetske matične ćelije) u koštanoj srži. Matične ćelije koje formiraju krv mogu se razviti u:
- crvene krvne ćelije (eritrocite),
- različite vrste belih krvnih zrnaca uključujući limfocite i
- krvne pločice (trombociti).
Rane i kasne reakcije[uredi | uredi izvor]
Imunski odgovor nakon transplantacija matičnih ćelija obuhvata rani i kasni efekat:
- Rani štetni efekti
Potencijalni rani štetni efekti se sastoje od akutne bolesti, preoperativne bolesti (GVHD), bakteremije/sepse, hemoragičnog cistitisa, venookluzivne bolesti i mukozitisa.
- Kasni štetni efekti
Potencijalni kasni efekti uključuju hroničnu GVHD, kongestivnu srčanu insuficijenciju, endokrine efekte, očne efekte, infekcije kasnog porekla i povećani rizik od maligniteta.[9]
Transplantacija matičnih ćelija je u ranijem periodu primene nosila visok rizik smrtnosti zbog imunoloških reakcija. Međutim, zahvaljujući znatno poboljšanoj podršci, tipu donatora, tipu HLA, režima kondicioniranja i prevenciji i lečenju ozbiljnih infekcija, stopa mortaliteta i morbiditeta značajno je smanjena.[10][11]
Mogućnosti i mere prevencije[uredi | uredi izvor]
Transplantacija matičnih ćelija pruža mogućnost da se zameni koštana srž bolesne osobe sa onom zdravog čoveka. Takođe poželjno je da donor koja se koristi u transplantaciji matičnih ćelija bude autologna osoba, koja je u malom riziku od maligniteta i sa niskom stepeom morbiditeta i mortaliteta. Međutim, ako je autologna transplantacija nije izvodljiva, alogena transplantacija je još jedna opcija.[11] Takođe u cilju prevencija HLA tipizaciju tkiva uvek treba uskladiti što bliže sa donorom kako bi se izbeglo GVHD i druge imunske komplikacije.[10]
Kako bi se optimizovale šanse za uspešnu transplantaciju, primalac srži bi trebalo da bude što više oslobođen od infekcije ili u dobrom fizičkom stanju. Iz tog razloga, važno je izvršiti transplantaciju u ranoj fazi, nakon rođenja deteta, ili što pre nakon postavljanja rane dijagnoze.
Tipovi mukopolisaharidoza za HSCT[uredi | uredi izvor]
Do danas je poznato da jedanaest različitih lizozomskih enzimskih anomalija uzrokuje 7 različitih i priznatih fenotipova i nekoliko podtipova MPS, prikazanih na ovoj tabeli, koji se mogu lečiti transplantacijom krvnih matičnih ćelija:
| Tip | Naziv | Deficijencija enzima | Proizvod akumulacije | Znaci i simptomi |
|---|---|---|---|---|
| MPS I | Hurlerov sindrom Hurler-Scheie sindrom Scheie sindrom |
Alfa-L-induronidaza |
|
|
| MPS II | Hanterov sindrom | Induronat sulfataza |
|
(simptomi slični Harlerovom sindromu, samo blaži) |
| MPS III | Sanfilipov sindrom A | Heparan N-sulfataza |
|
|
| Sanfilipov sindrom B | Alfa-N-acetilglukozaminidaza |
| ||
| Sanfilipov sindrom C | Acetil CoA: alfa-glukozaminid acetiltranferaza |
| ||
| MPS IV | Morqui sindrom | N-acetilgalaktozamin-6-sulfataza |
|
|
| MPS VI | Maroteaux-Lamy sindrom | N-acetilgalaktozamin-4-sulfataza |
|
|
| MPS VII | Sly sindrom | Beta glukuronidaza |
|
|
Način izvođenja[uredi | uredi izvor]
Sama intervencija je prilično jednostavna, ali pripreme, naknadna zaštita i glavni rizici čine metodu veoma zahtevnim pa i rizičnim postupkom.
Da bi se izvršila transplantacija matičnih ćelija, mora se naći adekvatan donor čiji se tip tkiva (HLA antigen) podudara sa primaocem. Kako je tip tkiva nasleđen od oba roditelja, svako dete ima 25% šansi da ima isti tip tkiva kao bolesni brat ili sestra. Zato je najbolje rešenje je transplantacija koštane srži da se ona uzme od zdravog srodnika sa istim tipom tkiva. Ako to nije moguće, odgovarajući donator može biti lociran u nacionalnim i međunarodnim registrima donora koštane srži ili u uskladištenom, zamrznutoj krvi iz pupčanih vrpca.
Tako npr. Tobias Registry u Švedskoj sadrži približno 40.000 registrovanih dobrovoljnih donatora, a imena više od 19 miliona drugih donora mogu se naći u registrima izvan Švedske.
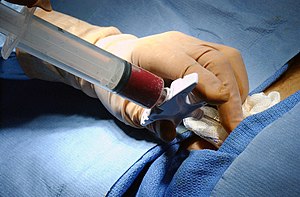
U transplantaciji krvnih matičnih ćelija koriste se tri načina, jedan glavni i dva alternativna:
Glavni — uzimanje koštana srži iz kosti donora usisavanjem, nakon čega se ona sakuplja u kontejneru.
Prvi alternativni — propuštanje donorske krvi kroz specijalnu centrifugu koja filtrira matične ćelije, a ostatak krvi se vraća donoru.
Drugi alternativni — upotreba krvi koja se nalazi u pupčanku novorođenčeta. Krv novorođenčadi ima veoma visok nivo krvnih matičnih ćelija, a mala količina krvi koja se nalazi u pupčanoj vrpci zdravog novorođenčeta može se zamrznuti i sačuvati za kasnije transplantacije.
Bez obzira na izvor ćelija, tako transplantirane krvne matične ćelije pronalaze svoj put u šupljine kostiju primaoca.
Pripremne mere su neophodne kako bi se pomoglo novim matičnim ćelijama da se skupljaju i minimiziraju rizik uništenja od obolelih ćelija koje neprestano napadaju nove donorske ćelije. U tom smislu primalac transplantiranih ćelija se obavezno leči hemoterapijom.
Neželjene reakcije[uredi | uredi izvor]
Ovaj tretman nije bez problema jer;
- Hemoterapija takođe može da ometa barijersku funkciju mukoznih membrana.
- Postoji veliki rizik od razvoja ozbiljne infekcije i iz tog razloga dete mora biti izolovano u trajanju od nekoliko nedelja, ili ponekad meseci pre i posle transplantacije.
Dosadašnja iskustva[uredi | uredi izvor]
Transplantacije hematopoetskih matičnih ćelija izvode se kod pacijenata sa Hurlerovim sindromom oko 25 godina, a ukupno više od 400 dece širom sveta prošlo je kroz ovaj postupak.[13]
Transplantacija krvnih matičnih ćelija poboljšava, respiratornu funkcij, fumnunkcije sluha srca i visceralnih organa, biohemijske nalaze i sprečava deformacije kostiju ako se izvrši dovoljno rano (pre 2 godine starosti deteta) i pre pojavljivanja neuroloških simptoma (ako je relevantno). Međutim, ne smanjuje zamućenje rožnjače. Ako se primeni nakon 2 godine starosti, deformacije se ne mogu preokrenuti, ali se rast poboljšava.[14][15]
Nekoliko dugotrajnih studija zaključilo je da transplantacija matičnih ćelija može sprečiti kognitivno oštećenje kod dece sa Hurlerovim sindromom, samo ako se obavi u ranoj fazi sindroma. Pošto se prevencija intelektualnog invaliditeta smatra primarnom pogodnošću transplantacije u Hurlerovom sindromu, trenutna preporuka je da se izvrši postupak u pre dve i po godine, mada je poželjno da to bude tokom prve godine života, ili čim se postavi osnovna dijagnoza.
Deca čije su kognitivna veština unutar normale u trenutku transplantacije imaju najveću korist, jer ova intervencija sprečava dalje pogoršanje sindroma. Jedan mesec nakon transplantacije nivoi enzima u krvotoku primaoca postaju normalni, mukopolisaharidi se izlučuju u urinu, a štetne akumulacije u ćelijama se smanjuju. Kao posledica toga, zgušnjavanje meninga se takođe smanjuje, čime se sprečava razvoj hidrocefalusa. Transplantacija hematopoetskih matičnih ćelija takođe poboljšava vid, kao i opšte stanje, srca i pluća. Karakteristične promene lica se skoro potpuno normalizuju.[16]
Međutim, intervencija nema uticaja na abnormalnosti skeleta, ako se transplantacija primeni nakon 2 godine starosti, pa se ortopedska operacija, na primer, kukova, mora izvesti kada je dete starije.[17]
Izgledi da se u određenoj meri povećava i rast, su neodređeni. Medicinska literatura ne podržava upotrebu hormona rasta kao efikasnog načina povećanja visine, ali još uviek nisu sprovedene sistematske studije.[18]
Komplikacije[uredi | uredi izvor]
Kako je transplantacija matičnih ćelija komplikovana procedura sa rizikom od ozbiljnih ili čak smrtonosnih komplikacija, dete mora biti detaljno ispitano pre nego što se preporuči ova intervencija.
Pre intervencije roditelji treba da budu dobro informisani o rizicima i nalazima iz dosadašnjih studija sa decom koja su podvrgnuta transplantaciji matičnih ćelija.
Vidi još[uredi | uredi izvor]
Izvori[uredi | uredi izvor]
- ^ Krivit W. Stemcell bone marrow transplantation in patients with metabolic storage diseases. Adv Pediatr 2002; 49: 359-378.
- ^ Hobbs JR, Hugh-Jones K, Barrett AJ, Byrom N, Chambers D, Henry K, et al. Reversal of clinical features of Hurler's disease and biochemical improvement after treatment by bone-marrow transplantation. Lancet. 1981 Oct 3. 2 (8249):709-12.
- ^ Warkentin PI, Dixon MS Jr, Schafer I, Strandjord SE, Coccia PF. Bone marrow transplantation in Hunter syndrome: a preliminary report. Birth Defects Orig Artic Ser. 1986. 22 (1):31-9.
- ^ Krivit W, Pierpont ME, Ayaz K, Tsai M, Ramsay NK, Kersey JH, et al. Bone-marrow transplantation in the Maroteaux-Lamy syndrome (mucopolysaccharidosis type VI). Biochemical and clinical status 24 months after transplantation. N Engl J Med. 1984 Dec 20. 311 (25):1606-11.
- ^ Yamada Y, Kato K, Sukegawa K, Tomatsu S, Fukuda S, Emura S, et al. Treatment of MPS VII (Sly disease) by allogeneic BMT in a female with homozygous A619V mutation. Bone Marrow Transplant. 1998 Mar. 21 (6):629-34.
- ^ Beck M, Arn P, Giugliani R, Muenzer J, Okuyama T, Taylor J, et al. The natural history of MPS I: global perspectives from the MPS I Registry. Genet Med. 2014 Oct. 16 (10):759-65.
- ^ Turbeville S, Nicely H, Rizzo JD, Pedersen TL, Orchard PJ, Horwitz ME, et al. Clinical outcomes following hematopoietic stem cell transplantation for the treatment of mucopolysaccharidosis VI. Mol Genet Metab. 2011 Feb. 102 (2):111-5.
- ^ Boelens JJ. Trends in haematopoietic cell transplantation for inborn errors of metabolism. J Inherit Metab Dis. 2006 Apr-Jun. 29 (2-3):413-20.
- ^ Wingard JR, Hsu J, Hiemenz JW. Hematopoietic stem cell transplantation: an overview of infection risks and epidemiology. Infect Dis Clin North Am. 2010 Jun. 24 (2):257-72.
- ^ a b Mielcarek M, Storer B, Martin PJ, Forman SJ, Negrin RS, Flowers ME, et al. Long-term outcomes after transplantation of HLA-identical related G-CSF-mobilized peripheral blood mononuclear cells versus bone marrow. Blood. 2012 Mar 15. 119 (11):2675-8.
- ^ a b Horowitz MM, Confer DL. Evaluation of hematopoietic stem cell donors. Hematology Am Soc Hematol Educ Program. 2005. 469-75.
- ^ Marks, Dawn B.; Swanson, Todd; Sandra I Kim; Marc Glucksman (2007) Biochemistry and molecular biology. Wolters Kluwer Health/Lippincott Williams & Wilkins, Philadelphia.
- ^ Bjoraker KJ, Delaney K, Peters C, Krivit W, Shapiro EG. Long-term outcomes of adaptive functions for children with mucopolysaccharidoses I (Hurler Syndrome) treated with haematopoeitic stem cell transplantation. Dev Behav Pediatr 2006; 27: 290-296.
- ^ Khan S, Alméciga-Díaz CJ, Sawamoto K, Mackenzie WG, Theroux MC, Pizarro C, et al. Mucopolysaccharidosis IVA and glycosaminoglycans. Mol Genet Metab. 2017 Jan - Feb. 120 (1-2):78-95.
- ^ Tomatsu S, Sawamoto K, Alméciga-Díaz CJ, Shimada T, Bober MB, Chinen Y, et al. Impact of enzyme replacement therapy and hematopoietic stem cell transplantation in patients with Morquio A syndrome. Drug Des Devel Ther. 2015. 9:1937-53.
- ^ Malm G, Gustafsson B, Berglund G, Lindström M, Naess K, Borgström B et al. Outcome in six children with mucopolysaccharidosis type I, Hurlers syndrome, after haematopoietic stem cell transplantation (HSCT). Acta Paediatr Scand 2008; 97: 1108-1112.
- ^ van der Linden M, Kruyt M, Sakkers R, de Koning TJ, Oner FC, Castelein RM. Orthopaedic management of Hurler’s disease after hematopoietic stem cell transplantation: a systematic review. J Inherit Metab Dis 2011; 34: 657-669.
- ^ Krivit W. Stem cell bone marrow transplantation in patients with metabolic storage diseases. Adv Pediatr. 2002;49:359-78.
Literatura[uredi | uredi izvor]
- Consolini DM, Bayever E. Malatack JJ, The status of hematopoietic stem cell transplantation in lysosomal storage disease. Pediatr Neurol. 2003 Nov; 29(5):391-403.
- Grewal SS, Wynn R, Abdemur JE, Burton BK, Gharib M, Haase C et al. Safety and efficacy of enzyme replacement therapy in combination with hematopoietic stem cell transplantation in Hurler syndrome. Genet Med 2005; 7: 143-146.
Spoljašnje veze[uredi | uredi izvor]
- Diagnosis: Hurler, Hurler-Scheie and Scheie syndromes — Synonyms: Mucopolysaccharidosis type I (IH, IH/S, IS); MPS I (IH, IH/S, IS), Alfa-L-iduronidase deficiency (jezik: engleski)
- VMA: Transplantacija matičnih ćelija od nesrodnog davaoca
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
