Analog prelaznog stanja
Analozi prelaznog stanja (analozi tranzicionog stanja), su hemijska jedinjenja sa hemijskom strukturom koja podseća na prelazno stanje molekula supstrata u enzimski katalizovanoj hemijskoj reakciji. Enzimi formiraju interakcije sa supstratom putem naprezanja i distorzija, čime dovode supstrat do tranzicionog stanja.[1] Analozi tranzicionog stanja se mogu koristiti kao inhibitori enzimski katalizovanih reakcija pošto oni blokiraju aktivno mesto enzima. Iz teorije proističe da bi enzimski inhibitori koji podsećaju na strukture prelaznog stanja trebalo da se čvršće vezuju za enzim nego sam supstrat.[2] Primeri inhibitora koji su analogni prelaznom stanju obuhvataju između ostalog lek protiv gripa iz grupe inhibitora neuraminidaza oseltamivir i inhibitor HIV proteaze sakvinavir koji se koristi u AIDS tretmanu.
Analog prelaznog stanja[уреди | уреди извор]

Prelazno stanje strukture se najbolje može opisati pomoću statističke mehanike, pri čemu energije razlaganja i formiranja veza imaju jednaku verovatnoću kretanja iz prelaznog stanja u nazad do reaktanata ili unapred do produkata. U enzimski katalizovanim reakcijama, sveukupna enrgija aktivacije reakcije je niža kad enzim stabilizuje visoko energetski intermedijer prelaznog stanja. Analozi prelaznog stanja oponašaju taj visoko energijski intermedijer, ali ne podležu katalizovanoj hemijskoj rekciji i stoga se mogu mnogo jače vezati za enzim nego jednostavni supstrat ili analog produkta.
Dizajn analoga prelaznog stanja[уреди | уреди извор]
Da bi se dezajnirao analog prelaznog stanja, ključni korak je eksperimentalna determinacija strukture supstrata u prelaznom stanju datog enzima, koristeći na primer kinetički izotopni efekat. Struktura prelaznog stanja se isto tako može predvideti putem računarskih pristupa, što je komplementarno sa KIE.
Kinetički izotopni efekat[уреди | уреди извор]
Kinetički izotopni efekat (KIE) je mera reakcione brzine izotopski obeleženog reaktanta u odnosu na zastupljeniji prirodni supstrat. Vrednost kinetičkog izotopnog efekta je odnos brojeva konverzija i obuhvata sve korake reakcije.[3] Unutrašnja kinetička vrednost izotopa proističe iz razlike u vibracionom oktuženju veza atoma u reaktantima u osnovnom stanju relativno na atome u prelaznom stanju.[3] Pomoću kinetičkog izotopnog efekta znatan uvid se može dobiti o tome kako prelazno stanje enzimski katalizovane reakcije može da izgleda i to se može koristi za usmeravanja razvoja analoga prelaznog stanja.
Kompjuterske simulacije[уреди | уреди извор]
Računarski pristupi su korisna oruđa za elucidaciju mehanizma dejstva enzima.[4] Sama molekulska mehanika ne može da predvidi transfer elektrona, što je od fundamentalnog značaja za organske reakcije. Molekularno dinamičke simulacije pružaju dovoljno informacija u pogledu fleksibilnosti proteina tokom katalitičke reakcije. Komplementarni metod je kombinacija molekularno mehaničkih/kvantno mehaničkih simulacija (QM/MM metod).[5] U tom pristupu, samo atomi koji su odgovorni za enzimatsku reakciju u katalitičkom regionu su obuhvaćeni QM pristupom, dok se preostali atomi tretiraju koristeći molekularnu mehaniku.[6]
Primeri dizajna analoga prelaznog stanja[уреди | уреди извор]
Nakon određivanja strukture prelaznog stanja koristeći bilo KIE ili računarske simulacije, inhibitor se može dizajnirati po uzoru na utvrđene strukture prelaznog stanja ili intermedijere. Sledeća tri primera ilustruju kako inhibitori oponašaju strukture prelaznog stanja putem promena funkcionalnih grupa koje korespondiraju geometriji i elektrostatičkoj distribuciji struktura prelaznog stanja.
Inhibitor metiltioadenozin nukleozidaze[уреди | уреди извор]
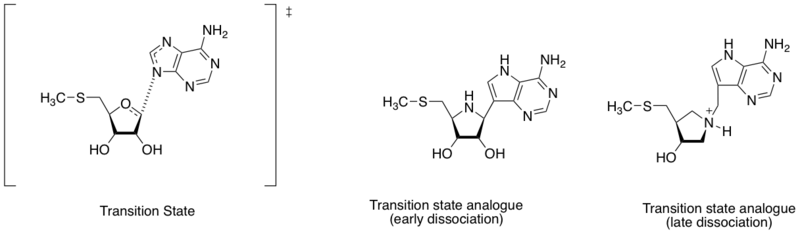
Metiltioadenozin nukleozidaza je enzim koji katalizuje reakciju hidrolitičke deadenilacije 5'-metiltioadenozina i S-adenosilhomocisteina. On se takođe smatra važnom metom za otkrivanje antibakterijskih lekova, jer je važan u metaboličkom sistemu bakterija i jedino se formira u njima.[7] Imajući u vidu različita rastojanja između adeninskog atoma azota i riboznog anomernog ugljenika (pogledajte dijagram u ovoj sekciji), struktura prelaznog stanja se može definisati po ranom ili kasnom stupnju disocijacije. Na bazi nalaza različih struktura prelaznog stanja, Šram i njegovi saradnici su dizajnirali analoge dva prelazna stanja koji oponašaju rano i kasno disocijativno prelazno stanje. Analozi ranog i kasnog prelaznog stanja imaju afinitet vezivanja (Kd) od 360 i 140 pM, respektivno.[8]
Inhibitor termolizina[уреди | уреди извор]

Termolizin je enzim koji katalizuje hidrolizu peptidnih amidnih veza sa hidrofobinim aminokiselinama, i koji proizvodi Bacillus thermoproteolyticus.[9] Iz tog razloga, ovaj enzim je takođe meta za dizajn antibakterijskih agenasa. Enzimatski reakcioni mehanizam započinje zamenom malim peptidnim molekulom molekula vode koji vezuje cink u blizini Glu143 termolizina. Molekul vode koji je aktiviran jonom cinak i Glu143 napada karbonilni ugljenik i formira tetraedralno prelazno stanje. (Pogledajte sliku) Holden i njegovi saradnici su polazeći od tog tetraedralnog prelaznog stanja dezajnirali serije analognih fosfonamidatnih peptida. Među sintetisanim analozima, R = L-Leu ispoljava najpotentniju inhibitornu aktivnost (Ki = 9.1 nM).[10]
Inhibitor arginaze[уреди | уреди извор]
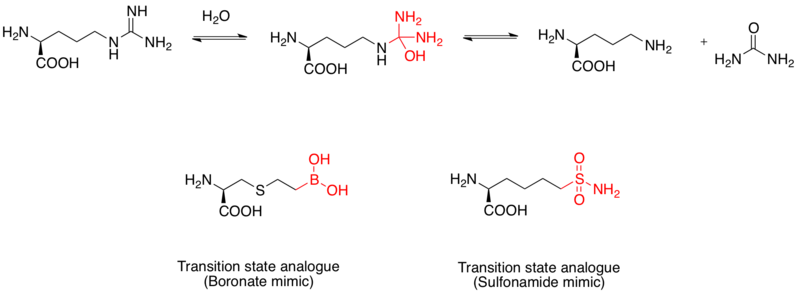
Arginaza je binuklearni manganozni metaloprotein koji katalizuje hidrolizu L-arginina do L-ornitina i ureje. Ona je meta za razvoj lekova za tretman astme.[11] Mehanizam hidrolize L-arginina obuhvata nukleofilni napad molekula vode, čime se formira tetraedralni intermedijar. Studije su pokazale da boronska kiselina može da poprimi tetraedralnu konfiguraciju i da deluje kao inhibitor. Dodatno, sulfonamidna funkcionalna grupa može da oponaša strukturu prelaznog stanja.[12] Evidencija da boronska kiselina deluje kao analog prelaznog stanja proizilazi iz rendgenske kristalne strukture kompleksa sa ljudskom arginazom I.[13]
Vidi još[уреди | уреди извор]
- Enzim
- Strukturni analog, jedinjenje sa sličnom hemijskom strukturom
- Inhibitor enzima
- Analog supstrata
- Samoubilačka inhibicija
- Supstrat
Reference[уреди | уреди извор]
- ^ Silverman, Richard B. (2004). The Organic Chemistry of Drug Design and Drug Action. San Diego, CA: Elsevier Academic Press. ISBN 0-12-643732-7.
- ^ Copeland, R.A.; Davis, J.P.; Cain, G.A.; Pitts, W.J.; Magolda, R.L. (1996). „The Immunosuppressive Metabolite of Leflunomide is a Potent Inhibitor of Human Dihydroorotate Dehydrogenase”. Biochemistry. 35 (4): 1270. doi:10.1021/bi952168g.
- ^ а б Schramm, Vern L> (2011). „Enzymatic Transition States, Transition-State Analogs, Dynamics, Thermodynamics, and Lifetimes”. Annu. Rev. Biochem. 80 (1): 703—732. PMID 21675920. doi:10.1146/annurev-biochem-061809-100742.
- ^ Peter, Kollman; Kuhn, B.; Peräkylä, M. (2002). „Computational Studies of Enzyme-Catalyzed Reactions: Where Are We in Predicting Mechanisms and in Understanding the Nature of Enzyme Catalysis?”. J. Phys. Chem. B. 106 (7): 1537—1542. doi:10.1021/jp012017p.
- ^ Hou, G; Hou, G.; Cui, Q. (2011). „QM/MM Analysis Suggests that Alkaline Phosphatase (AP) and Nucleotide Pyrophosphatase/Phosphodiesterase Slightly Tighten the Transition State for Phosphate Diester Hydrolysis Relative to Solution: Implication for Catalytic Promiscuity in the AP Superfamily”. J. Am. Chem. Soc. 134 (1): 229—246. doi:10.1021/ja205226d.
- ^ Schwartz, S; Saen-oon, S.; Quaytman-Machleder, S.; Schramm, V. L.; Schwartz, S. D. (2008). „Atomic Detail of Chemical Transformation at the Transition State of an Enzymatic Reaction”. PNAS. 105 (43): 16543—16545. Bibcode:2008PNAS..10516543S. doi:10.1073/pnas.0808413105.
- ^ Singh, Vipender; Singh V; Lee JE; Núñez S; Howell PL; Schramm VL. (2005). „Transition state structure of 5'-methylthioadenosine/S-adenosylhomocysteine nucleosidase from Escherichia coli and its similarity to transition state analogues”. Biochemistry. 44 (35): 11647—11659. PMID 16128565. doi:10.1021/bi050863a.
- ^ Guitierrez, Jemy; Luo, M.; Singh, V.; Li, L.; Brown, R. L.; Norris, G. E. (2007). „Picomolar Inhibitors as Transition-State Probes of 5′-Methylthioadenosine Nucleosidases”. ACS Chemical Biology. 2 (11): 725—734. PMID 18030989. doi:10.1021/cb700166z.
- ^ S, Endo (1962). „Studies on protease produced by thermophilic bacteria”. J. Ferment. Technol. 40: 346—353.
- ^ Holden, Hazel; Tronrud, D. E.; Monzingo, A. F.; Weaver, L. H. (1987). „Slow-and fast-binding inhibitors of thermolysin display different modes of binding: crystallographic analysis of extended phosphoramidate transition-state analogs”. Biochemistry. 26 (26): 8542—8553. doi:10.1021/bi00400a008.
- ^ Maarsingh, Harm; Johan Zaagsma; Herman Meurs (2009). „Arginase: a key enzyme in the pathophysiology of allergic asthma opening novel therapeutic perspectives”. Br J Pharmacol. 158 (3): 652—664. PMC 2765587
 . PMID 19703164. doi:10.1111/j.1476-5381.2009.00374.x.
. PMID 19703164. doi:10.1111/j.1476-5381.2009.00374.x.
- ^ E, Cama; Shin H; Christianson DW. (2003). „Design of amino acid sulfonamides as transition-state analogue inhibitors of arginase”. J Am Chem Soc. 125 (43): 13052—7. doi:10.1021/ja036365b.
- ^ Shishova, Ekaterina; Luigi Di Costanzo; David E. Cane; David W. Christianson (2009). „Probing the Specificity Determinants of Amino Acid Recognition by Arginase”. Biochemistry. 48 (1): 121—131. doi:10.1021/bi801911v.
