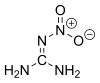
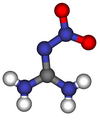
Нитрогванидин
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
1-Nitroguanidine
| |||
| Други називи
Пикрит
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.008.313 | ||
| |||
| Својства | |||
| CH4N4O2 | |||
| Моларна маса | 104,068 | ||
| Агрегатно стање | Безбојна кристална чврста супстанца | ||
| Густина | 1,77 g/cm3 | ||
| Тачка топљења | 257 °C (495 °F; 530 K) | ||
| 3.45 г/кг (у води при 25 °Ц (77 °Ф; 298 К)) | |||
| Експлозивност | |||
| Осетљивост на шок | > 50 Ј | ||
| Осетљивост на трење | > 350 Н | ||
| Брзина детонације | |||
| РЕ фактор | 1.00
| ||
| Опасности | |||
| Главне опасности | Експлозив | ||
| Безбедност приликом руковања | |||
|
| |||
| Сродна једињења | |||
Сродна
|
|||
Сродна једињења
|
Гванидин Гванидин нитрат
| ||
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||
Нитрогванидин - понекад скраћено НГу, такође назван пикрит - је безбојно експлозивно хемијско једињење, кристална чврста супстанца која није директно запаљива, која има веома ниску експлозивну осетљивост и топи се на 257 °Ц (495 °Ф; 530 К) и распада на 254 °Ц (489 °Ф; 527 К), али зато има велику брзину детонације. [3] Нитрогванидин је изузетно неосетљив, али моћан експлозив, такође се користи у бездимном баруту где смањује пламен на излазу из цеви и смањује ерозију цеви и буренцета. [4] Влажење са > 20 теж.% воде утиче на десензибилизацију са ХД 1.1 на ХД 4.1 (запаљива чврста супстанца). [5] Нитрогванидин се користи као енергетски материјал, односно погонско гориво или високо експлозивно средство, прекурсор за инсектициде и за друге сврхе.
Нитрогванидин је такође органско једињење, које садржи 1 атом угљеника и има молекулску масу од 104,068 Da.
Историја[уреди | уреди извор]
Нитрогванидин је први изумео L. Јоусселин 1877. године. Око Другог светског рата почео је да се користи као барут.
Производња[уреди | уреди извор]
Нитрогванидин је синтетисан по први пут 1877. године [3] нитрацијом гванидина [6], а затим је са великим потешкоћама добијен екстракцијом гвана. [7] Од 1930-их, [3] индустријски се производи дехидратацијом сумпорном киселином самог гванидин нитрата [8] добијеног реакцијом цијанамида или дицијандиамида [9] и амонијум нитрата. [3] · [10] · [11] Гванидин нитрат се такође може произвести из уреје и амонијум нитрата са силицијум-диоксидним катализатором [12]али у лабораторији се може припремити од урее О=C(НХ
2)
2 и сулфаминске киселине Х
3НСО
3 да би се добио гванидин сулфат који је накнадно нитрован у нитрогванидин. [13]
Нитрогванидин се производи широм света у великим размерама почевши од реакције дицијандиамида (ДЦД) са амонијум нитратом да би се добила со гванидинијум нитрата, која се затим нитрира третманом са концентрованом сумпорном киселином на ниској температури. [14]
- [C(НХ2)3]НО3 → (НХ2)2ЦННО2 + Х2О
Нитрогванидин се такође може добити третирањем урее амонијум нитратом (преко БМА процеса). Међутим, због проблема поузданости и сигурности, овај процес никада није комерцијализован упркос својим атрактивним економским карактеристикама.
Особине[уреди | уреди извор]
| Особина | Вредност |
|---|---|
| Број акцептора водоника | 3 |
| Број донора водоника | 3 |
| Број ротационих веза | 2 |
| Партициони коефицијент[15] (ALogP) | 1,2 |
| Растворљивост[16] (logS, log(mol/L)) | -0,3 |
| Поларна површина[17] (PSA, Å2) | 107,7 |
Карактеристике[уреди | уреди извор]
Нитрогванидин је веома неосетљив и детонира тек након иницирања детонатором. Важни индикатори експлозије су:
- Топлота експлозије: 3062 кЈ кг−1. [18]
- Температура детонације: при максималној густини 2.530 °Ц (4.590 °Ф; 2.800 К) [19]
- Брзина детонације: при максималној густини 8.546 м/с (28.040 фт/с)−1 [18]
- Нормална запремина гаса: 1075 л·кг−1. [20]
- Специфична енергија: 932 кЈ·кг−1. [20]
- Детонациони притисак: 29 ГПа
- Температура детонације: 2.540 °Ц (4.600 °Ф; 2.810 К) [19]
- Оловни блок: 305 цм3/10 г[20]
- Осетљивост на удар: до 50 Нм без реакције [21]
- Осетљивост на трење: до 353 Н оптерећење игле без реакције [21]
- Критични пречник при густини: при густини од 1,52 г/цм 3 < 14 мм [18]
- Испитивање челичног кућишта: са граничним пречником од 1 мм без паљења. [21]
Као и код свих експлозива, брзина детонације, вD, нитрогванидина расте са његовом густином. вD следи следећи закон у опсегу од 0,3 до 1,78 г·цм−3: вD = 1,44 + 4,015 густина [мм·µс−1] [22] (погледајте и следећу графику)

Нитрогванидин је један од јаких, али тешко детонирајућих експлозива. Ово објашњава снажну зависност брзине детонације од пречника. Пуњење густине 0,95 г/цм3 има брзину детонације од 4.340 м/с (14.240 фт/с) у цеви унутрашњег пречника 20 мм.
Синтеза[уреди | уреди извор]
Нитрогванидин се може добити дехидратацијом гванидин нитрата концентрованом сумпорном киселином. [23]
- Х
2Н-C(=НХ)-Х
2Н·ХНО
3 → Х
2Н-C(-НХ
2)=Н-НО
2 + Х
2О
Реактивност[уреди | уреди извор]
Нитрогванидин постоји у воденој средини у два облика у таутомерној равнотежи један са другим, наиме нитроимино облик (1-нитрогванидин) и нитроамински облик (2-нитрогванидин). I у чврстој фази и у раствору преовлађује имин облик. [24].
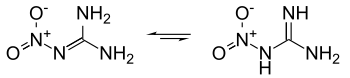
- Х
2Н-C(-НХ
2)=Н-НО
2 ⇄ ХН=C(-НХ
2)-НХ-НО
2
Употреба[уреди | уреди извор]
Експлозиви[уреди | уреди извор]
Нитрогванидин је у употреби од 1930-их као састојак погонских горива са троструком базом у којима смањује температуру пламена, бљесак отвора и ерозију цеви пиштоља, али задржава притисак у комори због високог садржаја азота. Његова екстремна неосетљивост у комбинацији са ниском ценом учинила га је популарним састојком у неосетљивим високоексплозивним формулацијама (нпр. АФX-453, АФX-760, ИМX-101, АЛ-ИМX-101, ИМX-103, итд.). [25]
Експлозивно распадање нитрогванидина је дато следећом једначином:
- Х4Н4ЦО2 (с) → 2 Х2О (г) + 2 Н2 (г) + C (с)
Бездимни прах (барут)[уреди | уреди извор]
Нитрогванидин се користи као компонента у праховима са троструком базом, односно на бази нитроцелулозе, нитроглицерина и амино деривата као што је нитрогванидин. Тамо се користи за смањење температуре блица без утицаја на притисак детонације. Нитрогванидин се уграђује као фина суспензија у бездимни прах који садржи нитроцелулозу, нитроглицерин и често централит. [26] Ови прахови су мање енергетски густи од прахова са двоструком базом, али мање еродирају цев пиштоља. [27].
Под овим условима, додатак нитрогванидина у праху омогућава смањење пламена на отвору цеви упркос повећаном стварању дима. [27] · [4].
Нитрогванидин се такође користи у саставу специфичних такозваних пудера ниске осетљивости (ЛОВА).[28] Ова горива не дефлагрирају или детонирају када су подвргнута топлоти или удару или погођена обликованим пуњењем и стога су безбеднија. Нитрогванидин затим замењује експлозиве као што је ХМX и везује се за везиво као што је нитроцелулоза или поливинил нитрат и пластификатори. [29]
Пестициди[уреди | уреди извор]
Деривати нитрогванидина се користе као инсектициди, који имају упоредиво дејство са никотином. Деривати укључују клотианидин, динотефуран, имидаклоприд и тиаметоксам.
Биохемија[уреди | уреди извор]
Нитрозоиловани дериват, нитрозогванидин, се често користи за мутагеизацију бактеријских ћелија за биохемијске студије.
Структура[уреди | уреди извор]
Након неколико деценија дебате, НМР спектроскопијом и дифракцијом рендгенских зрака и неутрона могло би се потврдити да нитрогванидин постоји искључиво као нитроимин таутомер и у чврстом стању и у раствору. [30][31][32]
Референце[уреди | уреди извор]
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б в г Ernst-Christian, Koch (2021). High explosives, propellants, pyrotechnics. De Gruyter. стр. 510. ISBN 978-3-11-066052-4.
- ^ а б Thomas M., Klapötke (2022-08-01). Chemistry of High-Energy Materials [Chemistry of High-Energy Materials]. De Gruyter. стр. 516. ISBN 978-3-11-073950-3. doi:10.1515/9783110739503. Приступљено 2023-07-30.
- ^ United Nations, Transport of Nitroguanidine, wetted, (UN 1336) in flexible IBCs, ST/SC/AC.10/C.3/2006/52, Geneva, 13 April 2006. Accessed at https://www.unece.org/fileadmin/DAM/trans/doc/2006/ac10c3/ST-SG-AC10-C3-2006-52e.pdf
- ^ M. W., Kirkwood; George F, Wright (1957-06-01). MECHANISM OF GUANIDINE NITRATION: II. TETRAETHYLNITROGUANIDINE. 35. Canadian Journal of Chemistry. стр. 527—540. ISSN 0008-4042. doi:10.1139/v57-074. Приступљено 2023-07-30. Непознати параметар
|issn2=игнорисан (помоћ) - ^ A, Strecker (1861). Untersuchungen über die chemischen Beziehungen zwischen Guanin, Xanthin, Theobromin, Caffein und Kreatinin. 118. Annalen der Chemie und Pharmacie. стр. 151—177. doi:10.1002/jlac.18611180203.
- ^ Synthesis method of superfine nitroguanidine with particle size of less than 4.0um. 2020-03-24. Приступљено 2023-07-30.
- ^ „Organic Syntheses Procedure”. orgsyn.org. Приступљено 2023-07-30.
- ^ William H., Hill; Robert C., Swain; Joseph H., Paden (1941-08-12). Production of guanidine nitrate. Приступљено 2023-07-30.
- ^ Tenney L., Davis (1922-12-26). Guanidine nitrate. Приступљено 2023-07-30.
- ^ One-step safety production method of guanidine nitrate. 2012-04-11. Приступљено 2023-07-30.
- ^ Axt (1. 8. 2007). „Nitroguanidine: from sulphamic acid and urea”. Sciencemadness Discussion Board.
- ^ E.-C. Koch, Insensitive High Explosives: III. Nitroguanidine – Synthesis – Structure – Spectroscopy – Sensitiveness, Propellants Explos. Pyrotech. 2019, 44, 267-292. [1]
- ^ Ghose, A.K.; Viswanadhan V.N. & Wendoloski, J.J. (1998). „Prediction of Hydrophobic (Lipophilic) Properties of Small Organic Molecules Using Fragment Methods: An Analysis of AlogP and CLogP Methods”. J. Phys. Chem. A. 102: 3762—3772. doi:10.1021/jp980230o.
- ^ Tetko IV, Tanchuk VY, Kasheva TN, Villa AE (2001). „Estimation of Aqueous Solubility of Chemical Compounds Using E-State Indices”. Chem Inf. Comput. Sci. 41: 1488—1493. PMID 11749573. doi:10.1021/ci000392t.
- ^ Ertl P.; Rohde B.; Selzer P. (2000). „Fast calculation of molecular polar surface area as a sum of fragment based contributions and its application to the prediction of drug transport properties”. J. Med. Chem. 43: 3714—3717. PMID 11020286. doi:10.1021/jm000942e.
- ^ а б в E.-C. Koch: Sprengstoffe, Treibmittel, Pyrotechnika. 2., vollständig überarbeitete Auflage. de Gruyter, Berlin, 2019, ISBN 978-3-11-055784-8.
- ^ а б R. Doherty, R. L. Simpson: Comparative Evaluation of several insensitive high explosives, 28th International Annual ICT Conference, June 1997, Karlsruhe, Germany. V-32.
- ^ а б в J. Köhler, R. Meyer, A. Homburg: Explosivstoffe. 10., vollständig überarbeitete Auflage. Wiley-VCH, Weinheim 2008, ISBN 978-3-527-32009-7.
- ^ а б в Ernst-Christian Koch (18. 01. 2019), „Insensitive High Explosives: III. Nitroguanidine – Synthesis – Structure – Spectroscopy – Sensitiveness”, Propellants, Explosives, Pyrotechnics (на језику: немачки), 44 (3), pp. 267–292, doi:10.1002/prep.201800253
- ^ Terry R. Gibbs, Alphonse Popolato (1984), LASL explosive property data (на језику: немачки), University of California Press, pp. 52–60, ISBN 0-520-04012-0}}
- ^ „Nitroguanidine”. National Institutes of Health. Приступљено 10. 06. 2015.
- ^ „Nitroguanidine”. 04. 01. 2012. Приступљено 10. 06. 2015.
- ^ E.-C. Koch, Insensitive High Explosives: IV. Nitroguanidine - Initiation & detonation, Def. Tech. 2019, 15, 467-487.[2]
- ^ ARMY RESEARCH LABORATORY Extraction of Nitroguanidine (NQ) From Triple-Base Gun Propellant by Jeffrey B. Morris February 2002 lire en ligne
- ^ а б Rudolf, Meyer; Josef, Köhler; Axel, Homburg; Rudolf, Meyer (2007). Explosives. Wiley-VCH. стр. 236. ISBN 978-3-527-31656-4. Приступљено 2023-07-30.
- ^ Ernst‐Christian, Koch (20. 01. 2021). Insensitive High Explosives: V. Ballistic Properties and Vulnerability of Nitroguanidine Based Propellants. 46. Propellants, Explosives, Pyrotechnics. стр. 174—206. ISSN 0721-3115. doi:10.1002/prep.202000220. Приступљено 2023-07-30. Непознати параметар
|issn2=игнорисан (помоћ) - ^ Rudolf, Meyer; Josef, Köhler; Axel, Homburg (2007). Explosives. Wiley - VCH Verlag. стр. 211. ISBN 978-3-527-31656-4. Приступљено 2023-07-30.
- ^ Bulusu, S.; Dudley, R. L.; Autera, J. R. (1987). „Structure of nitroguanidine: nitroamine or nitroimine? New NMR evidence from nitrogen-15 labeled sample and nitrogen-15 spin coupling constants”. Magnetic Resonance in Chemistry. 25 (3): 234—238. S2CID 97416890. doi:10.1002/mrc.1260250311.
- ^ Murmann, R. K.; Glaser, Rainer; Barnes, Charles L. (2005). „Structures of nitroso- and nitroguanidine x - ray crystallography and computational analysis”. Journal of Chemical Crystallography. 35 (4): 317—325. S2CID 96090647. doi:10.1007/s10870-005-3252-y.
- ^ S. Choi, Refinement of 2-Nitroguanidine by Neutron Powder Diffraction, Acta Crystallogr. B 1981, 37, 1955-1957.[3]
Literatura[уреди | уреди извор]
- Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- Katritzky A.R.; Pozharskii A.F. (2000). Handbook of Heterocyclic Chemistry (Second изд.). Academic Press. ISBN 0080429882.