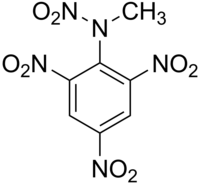
Тетрил
| |
| Идентификација | |
|---|---|
3Д модел (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.006.848 |
| УНИИ | |
| |
| Својства | |
| C7H5N5O8 | |
| Моларна маса | 287,143 |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25 °C [77 °F], 100 kPa). | |
| Референце инфокутије | |
Тетрил је експлозив за појачавање нитрамина, иако је његову употребу у великој мери заменио РДX. Тетрил је осетљив секундарни високи експлозив који се користи као појачивач, мало пуњење постављено поред детонатора како би се детонација проширила у главно пуњење експлозива. Такође, Тетрил је органско једињење, које садржи 7 атома угљеника и има молекулску масу од 287,143 Da.
У животној средини је екотоксичан и представља мутагено средство.[3].
Историја
[уреди | уреди извор]
Тетрил, који је открио и описао Ромбург 1883[4], углавном је коришћен током Првог светског рата (као погонско гориво, с тим што се за његову производњу нису трошили исти производи као код многих других експлозива) и користио се током Другог светског рата и у каснијим сукобима. Упркос предузетим мерама предострожности, посебно током 1940-их, многи радници који су се бавили тиме су се разболели[4] или су патили од алергија[4].
Тетрил је затим помешан са стеаринском киселином, графитом или другим везивним средством да би се могао пресовати у пелете, облик у којем се најчешће користио у муницији. Обично се користи сам, али се понекад користи и у комбинацији са другим хемикалијама, на пример у тетритолу.
Особине
[уреди | уреди извор]| Особина | Вредност |
|---|---|
| Број акцептора водоника | 8 |
| Број донора водоника | 0 |
| Број ротационих веза | 5 |
| Партициони коефицијент[5] (ALogP) | 3,7 |
| Растворљивост[6] (logS, log(mol/L)) | -5,8 |
| Поларна површина[7] (PSA, Å2) | 186,5 |
Хемијска својства
[уреди | уреди извор]Тетрил је жути кристални чврсти материјал у праху, практично нерастворљив у води, али растворљив у ацетону, бензену и другим растварачима. Када се тетрил загреје, он се прво топи, а затим се распада и експлодира. Лако гори и лакше се детонира од амонијум пикрата[8] или ТНТ-а, осетљив је отприлике као пикринска киселина. Детонира се трењем, ударом или варницом. Остаје стабилан на свим температурама које се могу наћи у складиштењу. Углавном се користи у облику пресованих куглица, и одобрен је као стандардно распрскавајуће пуњење за пројектиле малог калибра, јер даје много бољу фрагментацију од ТНТ-а. Има експлозивну брзинуод 23.600–23.900 стопа у секунди (7200–7300 м/с). Тетрил је основа за сервисне тетрилне капице за пескарење неопходне за позитивну детонацију ТНТ-а. Мешавина живиног фулмината и калијум хлората је укључена у поклопац да би се обезбедила детонација тетрила.[8]
Физичко-хемијска својства
[уреди | уреди извор]Тетрил је нитрамин. Појављује се као жути кристални материјал (чврсти прах), чија структура је објављена од 1967. године: кристалише у моноклинском систему, просторна група П21/ц са параметрима решетке
- а = 1,4129 нм
- б = 0,7374 нм
- ц = 1,0614 нм
- β = 97,07° и
- 4 јединице/месх 4 .
Лако гори и лакше експлодира него амонијум пикрат[9] или ТНТ, осетљив је отприлике као пикринска киселина коју је често замењивао.
Експлозивна својства
[уреди | уреди извор]Тетрил је веома осетљив експлозив[10] Међу важним показатељима експлозије су следећи:[10]
- Енталпија експлозије: 4251 кЈ · кг-1 (Х2О (л)), 4153 кЈ · кг-1 (Х2О (г))
- Брзина детонације: 7850 м · с-1 а уна денсидад де 1,71 г · цм -3
- Запремина експлозивних гасова: 939 л · кг-1
- Специфична енергија: 1213 кЈ · кг-1
- Температура дефлаграције: 185 а 195 °Ц
- Траузл тест: 41 цм³ / 10 г
- Осетљивост на удар: 3 Н · м
- Осетљивост на трење: 353 пин оптерећење Н
- Испитивање челичне чауре: критични пречник 6 мм
Судбина животне средине
[уреди | уреди извор]Најтоксичнија једињења убојних средстава, тетрил и 1,3,5-ТНБ, су такође и најразградљивија и биоразградив од стране микроорганизама у земљишту, укључујући бактерије[11]. Стога се очекује да ће ове хемикалије бити краткотрајне природе, а утицаји на животну средину не би се очекивали у областима које тренутно нису предмет хроничног уноса ових хемикалија. Тетрил се брзо разлаже у растворима метанола / воде, као и са топлотом. Све водене узорке за које се очекује да садрже тетрил треба разблажити ацетонитрилом пре филтрације и закисељено до пХ < 3. Сви узорци за које се очекује да садрже тетрил не треба да се излажу температурама изнад собне температуре. Поред тога, производи разградње тетрила се појављују као раме на пику 2,4,6-ТНТ.[8]
Његови остаци и одређени међупродукти разградње или метаболити, на пример анилин који производе сулфат-редуцирајуће бактерије из остатака тетрила, су стога токсични или екотоксични. Али се сматра да у природи не трају дуго. Дуго се претпостављало да су њени утицаји на животну средину ограничени на подручја која га хронично примају.
Начин разградње варира у зависности од тога да ли се одвија у аеробном или анаеробном окружењу[12].
Скоро век након што је Ромбургов први опис овог молекула 1883. године, амерички токсиколози показали 1980. да је тетрил доказао (за разлику од других експлозива као што су ПЕТН (пентаеритритол тетранитрат), РДX (1,3,5-тринитрохексахидро-1,35, -триазин) и ХМX (октахидро-1,3,5,7-тетранитро-1,3,5,7-тетразоцин)), који је снажан мутаген, који делује директно и у веома малим дозама 1 на три микробна система која се конвенционално користе за тестове мутагености (Неуроспора црасса, Салмонелла типхимуриум и Саццхаромицес церевисиае).[3] Изложеност људи овом производу и његовим производима разградње стога може довести до ризика по здравље.[3]
Коришћење
[уреди | уреди извор]Уопштено се користи у облику пресованих куглица и одобрен је као стандардно распрскавајуће пуњење за пројектиле малог калибра, јер производи бољу фрагментацију од ТНТ-а и његова разбијање је већа од снаге било ког другог војног експлозива овог типа.
Његова брзина детонације је 7200 - 7300 метара у секунди.
Тетрил се користи у детонаторима потребним за детонацију ТНТ-а. Затим се наноси на капсулу која садржи мешавину живиног фулмината и калијум хлората [8]. Такође улази у састав тетритола.
Тетрил је коришћен углавном током Првог и Другог светског рата и каснијих сукоба. Тетрил се обично користи самостално, мада се понекад може наћи у композицијама као што је тетритол. Тетрил се више не производи нити користи у Сједињеним Државама, али се и даље може наћи у застарелој муницији као што је противпешадијска мина М14.[13]
Производња
[уреди | уреди извор]Полазни материјали за припрему тетрила су: диметиланилин, сумпорна киселина и азотна киселина. Азотна киселина се користи у облику нитрозе са саставом од 85-86% азотне киселине, 6-8% сумпорне киселине и 8% воде. Сумпорна киселина која се овде користи је 92-96% монохидрат.
Процес добијања тетрила састоји се од следећих операција:
- добијање диметиланилин сулфата
- нитрација диметиланилин сулфата
- прање тетрила од киселина
- кристализација тетрила
- сушење и просејавање.
Диметиланилин сулфат се добија третирањем диметиланилина сумпорном киселином на температури од 33—40 °Ц (91—104 °Ф) у апаратима који су по конструкцији слични обичним нитраторима.
Реакција се одвија према једначини:
- C6Х5Н(ЦХ3)2 + Х2СО4 → C6Х5Н(ЦХ3)2 * Х2СО4
Операцију добијања диметиланилин сулфата треба спровести јер услед повећања активности бензенског прстена изазваног присуством Н(ЦХ3)2 групе, реакција нитрације чистог диметиланилина тече веома енергично и велики број настају нуспроизводи. Диметиланилин сулфат нитрати спорије и даје тетрил у већем приносу. Тетрил се добија нитрацијом диметиланилин сулфата са смешом за нитрирање на 50—55 °Ц (122—131 °Ф). Нитрација диметиланилин сулфата је опаснија од нитрирања толуена јер се нитрација и оксидација одвијају истовремено. Ове реакције су праћене ослобађањем велике количине топлоте. Стога се тетрил добија у малим нитраторима.
Реакција нитрирања највероватније следи једначину:
- C6Х5Н(ЦХ3)2 + 10 ХНО3 → C6Х2(НО2)3НЦХ3НО2 + 6НО2 + ЦО2+8Х2О
- C6Х5Н(ЦХ3)2 + 6ХНО3 → C6Х2(НО2)3НЦХ3НО2 + 2НО + ЦО2 + 6Х2О
Након што је нитрација завршена, тетрил се одваја од киселина на филтеру и испере са малом количином воде; затим се шаље у станицу за прање где се пере без киселина у бачвама опремљеним мешалицама. Производ се пере неколико пута у почетку хладном водом, а затим топлом водом. Вода садржана у испраном тетрилу се извлачи на вакуум филтерима; стога се тетрил шаље да се кристалише из бензена или дихлоретана. У кристализацији из ацетона, тетрил се претходно осуши.
Да би се тетрил рекристализовао, он се топло раствори у бензену или дихлоретану да би се добио засићени раствор у апаратима који се називају растварачи. Додатно испирање топлом водом се обично врши у растварачу како би се што потпуније уклонили остаци киселине. Врући раствор се шаље кроз филтере у кристализатор где се раствор постепено хлади и тетрил преципитира. Садржај кристализатора се шаље у вакуум филтер, где се тетрил одваја од кристалне течности, а затим испере водом и алкохолом.
Пречишћени тетрил се суши у посудама постављеним на полице на 40—60 °Ц (104—140 °Ф); након што је сушење завршено, материјал се просијава да се одвоје грудвице и пакује.
Здравствени проблеми
[уреди | уреди извор]Иако је тетрил међу најотровнијим експлозивним једињењима, веома је краткотрајан. Ово у комбинацији са чињеницом да су утицаји овог једињења на здравље углавном непроучени, не зна се много о здравственим проблемима које ово једињење може изазвати.
Епидемиолошки подаци показују да тетрил највише делује на кожу, делујући као јак иритант.[14] Могу се јавити симптоми сензибилизације коже као што су дерматитис, свраб, еритем итд.[15] Тетрил такође може да утиче на слузокоже, горње дисајне путеве, а можда и на јетру.
Током рата, 30% радника у фабрикама муниције у контакту са овим производом било је сензибилизирано на њега[16] за 10 до 14 дана опћенито[16]. Амерички радници морали су да користе немасне креме и да се перу са 1% сапуна.сулфити који су разлагали тетрил[16]. Током Другог светског рата значајан број алергија. Контактни дерматитис је примећен код радника у фабрикама муниције, а посебно код оних који су руковали или припремали експлозиве или који су руковали фулминатом живе. Пикринска киселина (лидит) и тринитротолуен (ТНТ) били су познати алергени, али је утврђено да је тетрил још више алергенски. У овом периоду проучаван је механизам настанка ових алергија, а да није дошло до решења за заштиту радника.
Види јпш
[уреди | уреди извор]Референце
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б в Whong Wen-Zong, Norman D. Speciner, Gordon S. Edwards, Mutagenic activity of tetryl, a nitroaromatic explosive, in three microbial test systems ; Toxicology Letters Volume 5, Issue 1, January 1980, Pages 11–17 (résumé)
- ^ а б в Leon J. Witkowski, M.D.; Carl N. Fisher, M.D.; Howard D. Murdock, M.S, Industrial illness due to tetryl report of 1258 cases ; AMA. 1942;119(17):1406-1409. doi: 10.1001/jama.1942.02830340018005 (Début du texte)
- ^ Ghose, A.K.; Viswanadhan V.N. & Wendoloski, J.J. (1998). „Prediction of Hydrophobic (Lipophilic) Properties of Small Organic Molecules Using Fragment Methods: An Analysis of AlogP and CLogP Methods”. J. Phys. Chem. A. 102: 3762—3772. doi:10.1021/jp980230o.
- ^ Tetko IV, Tanchuk VY, Kasheva TN, Villa AE (2001). „Estimation of Aqueous Solubility of Chemical Compounds Using E-State Indices”. Chem Inf. Comput. Sci. 41: 1488—1493. PMID 11749573. doi:10.1021/ci000392t.
- ^ Ertl P.; Rohde B.; Selzer P. (2000). „Fast calculation of molecular polar surface area as a sum of fragment based contributions and its application to the prediction of drug transport properties”. J. Med. Chem. 43: 3714—3717. PMID 11020286. doi:10.1021/jm000942e.
- ^ а б в г „Боостер Еxплосивес”.
- ^ Боостерс еxплосифс
- ^ а б Кöхлер, Ј.; Меyер, Р.; Хомбург, А.: Еxплосивстоффе, зехнте, воллстäндиг üберарбеитете Ауфлаге, Wилеy-ВЦХ, Wеинхеим 2008, ISBN 978-3-527-32009-7.
- ^ R Boopathy, Formation of aniline as a transient metabolite during the metabolism of tetryl by a sulfate-reducing bacterial consortium ;- Current microbiology, 2000 ([Résumé])
- ^ Manish M. Shah, Jim C. Spain (1996), Regular Article Elimination of Nitrite from the Explosive 2,4,6-Trinitrophenylmethylnitramine (Tetryl) Catalyzed by Ferredoxin NADP Oxidoreductase from Spinach ; Biochemical and Biophysical Research Communications Volume 220, Issue 3, 27 March 1996, Pages 563–568 (Résumé)
- ^ “A Military Guide to Terrorism in the 21st Century.” August 2003. P. 171. U.S. Army Training and Doctrine Command, Fort Leavenworth, Kansas. http://smallwarsjournal.com/documents/terrorismhandbook.pdf. Аццессед Маy 11, 2010.
- ^ ЦДЦ - Доцументатион фор Иммедиателy Дангероус То Лифе ор Хеалтх Цонцентратионс (ИДЛХс)
- ^ ЦДЦ - НИОСХ Поцкет Гуиде то Цхемицал Хазардс
- ^ а б в ПГХ Гелл, Сенситизатион то “тетрyл” ; Натионал Институте фор Медицал Ресеарцх, Хампстеад ; Бритисх Јоурнал оф Еxпериментал Патхологy, 1944 [ПДФ] à партир де них.гов
Литература
[уреди | уреди извор]- Цлаyден, Јонатхан; Греевес, Ницк; Wаррен, Стуарт; Wотхерс, Петер (2001). Органиц Цхемистрy (I изд.). Оxфорд Университy Пресс. ИСБН 978-0-19-850346-0.
- Смитх, Мицхаел Б.; Марцх, Јеррy (2007). Адванцед Органиц Цхемистрy: Реацтионс, Мецханисмс, анд Струцтуре (6тх изд.). Неw Yорк: Wилеy-Интерсциенце. ИСБН 0-471-72091-7.
- Катритзкy А.Р.; Позхарскии А.Ф. (2000). Хандбоок оф Хетероцyцлиц Цхемистрy (Сецонд изд.). Ацадемиц Пресс. ИСБН 0080429882.
Спољашње везе
[уреди | уреди извор]- Tetryl
- Тетрyл Архивирано на сајту Wayback Machine (15. август 2000), Агенцy фор Тоxиц Субстанцес анд Дисеасе Регистрy
- Оццупатионал Сафетy анд Хеалтх Гуиделине фор Тетрyл Архивирано 2009-02-27 на сајту Wayback Machine, Оццупатионал Сафетy & Хеалтх Администратион
