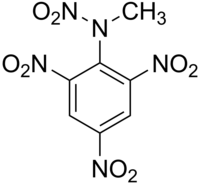
Tetril
| |
| Identifikacija | |
|---|---|
3D model (Jmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.006.848 |
| UNII | |
| |
| Svojstva | |
| C7H5N5O8 | |
| Molarna masa | 287,143 |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Tetril je eksploziv za pojačavanje nitramina, iako je njegovu upotrebu u velikoj meri zamenio RDX. Tetril je osetljiv sekundarni visoki eksploziv koji se koristi kao pojačivač, malo punjenje postavljeno pored detonatora kako bi se detonacija proširila u glavno punjenje eksploziva. Takođe, Tetril je organsko jedinjenje, koje sadrži 7 atoma ugljenika i ima molekulsku masu od 287,143 Da.
U životnoj sredini je ekotoksičan i predstavlja mutageno sredstvo.[3].
Istorija
[уреди | уреди извор]
Tetril, koji je otkrio i opisao Romburg 1883[4], uglavnom je korišćen tokom Prvog svetskog rata (kao pogonsko gorivo, s tim što se za njegovu proizvodnju nisu trošili isti proizvodi kao kod mnogih drugih eksploziva) i koristio se tokom Drugog svetskog rata i u kasnijim sukobima. Uprkos preduzetim merama predostrožnosti, posebno tokom 1940-ih, mnogi radnici koji su se bavili time su se razboleli[4] ili su patili od alergija[4].
Tetril je zatim pomešan sa stearinskom kiselinom, grafitom ili drugim vezivnim sredstvom da bi se mogao presovati u pelete, oblik u kojem se najčešće koristio u municiji. Obično se koristi sam, ali se ponekad koristi i u kombinaciji sa drugim hemikalijama, na primer u tetritolu.
Osobine
[уреди | уреди извор]| Osobina | Vrednost |
|---|---|
| Broj akceptora vodonika | 8 |
| Broj donora vodonika | 0 |
| Broj rotacionih veza | 5 |
| Particioni koeficijent[5] (ALogP) | 3,7 |
| Rastvorljivost[6] (logS, log(mol/L)) | -5,8 |
| Polarna površina[7] (PSA, Å2) | 186,5 |
Hemijska svojstva
[уреди | уреди извор]Tetril je žuti kristalni čvrsti materijal u prahu, praktično nerastvorljiv u vodi, ali rastvorljiv u acetonu, benzenu i drugim rastvaračima. Kada se tetril zagreje, on se prvo topi, a zatim se raspada i eksplodira. Lako gori i lakše se detonira od amonijum pikrata[8] ili TNT-a, osetljiv je otprilike kao pikrinska kiselina. Detonira se trenjem, udarom ili varnicom. Ostaje stabilan na svim temperaturama koje se mogu naći u skladištenju. Uglavnom se koristi u obliku presovanih kuglica, i odobren je kao standardno rasprskavajuće punjenje za projektile malog kalibra, jer daje mnogo bolju fragmentaciju od TNT-a. Ima eksplozivnu brzinuod 23.600–23.900 stopa u sekundi (7200–7300 m/s). Tetril je osnova za servisne tetrilne kapice za peskarenje neophodne za pozitivnu detonaciju TNT-a. Mešavina živinog fulminata i kalijum hlorata je uključena u poklopac da bi se obezbedila detonacija tetrila.[8]
Fizičko-hemijska svojstva
[уреди | уреди извор]Tetril je nitramin. Pojavljuje se kao žuti kristalni materijal (čvrsti prah), čija struktura je objavljena od 1967. godine: kristališe u monoklinskom sistemu, prostorna grupa P21/c sa parametrima rešetke
- a = 1,4129 nm
- b = 0,7374 nm
- c = 1,0614 nm
- β = 97,07° i
- 4 jedinice/mesh 4 .
Lako gori i lakše eksplodira nego amonijum pikrat[9] ili TNT, osetljiv je otprilike kao pikrinska kiselina koju je često zamenjivao.
Eksplozivna svojstva
[уреди | уреди извор]Tetril je veoma osetljiv eksploziv[10] Među važnim pokazateljima eksplozije su sledeći:[10]
- Entalpija eksplozije: 4251 kJ · kg-1 (H2O (l)), 4153 kJ · kg-1 (H2O (g))
- Brzina detonacije: 7850 m · s-1 a una densidad de 1,71 g · cm -3
- Zapremina eksplozivnih gasova: 939 l · kg-1
- Specifična energija: 1213 kJ · kg-1
- Temperatura deflagracije: 185 a 195 °C
- Trauzl test: 41 cm³ / 10 g
- Osetljivost na udar: 3 N · m
- Osetljivost na trenje: 353 pin opterećenje N
- Ispitivanje čelične čaure: kritični prečnik 6 mm
Sudbina životne sredine
[уреди | уреди извор]Najtoksičnija jedinjenja ubojnih sredstava, tetril i 1,3,5-TNB, su takođe i najrazgradljivija i biorazgradiv od strane mikroorganizama u zemljištu, uključujući bakterije[11]. Stoga se očekuje da će ove hemikalije biti kratkotrajne prirode, a uticaji na životnu sredinu ne bi se očekivali u oblastima koje trenutno nisu predmet hroničnog unosa ovih hemikalija. Tetril se brzo razlaže u rastvorima metanola / vode, kao i sa toplotom. Sve vodene uzorke za koje se očekuje da sadrže tetril treba razblažiti acetonitrilom pre filtracije i zakiseljeno do pH < 3. Svi uzorci za koje se očekuje da sadrže tetril ne treba da se izlažu temperaturama iznad sobne temperature. Pored toga, proizvodi razgradnje tetrila se pojavljuju kao rame na piku 2,4,6-TNT.[8]
Njegovi ostaci i određeni međuprodukti razgradnje ili metaboliti, na primer anilin koji proizvode sulfat-reducirajuće bakterije iz ostataka tetrila, su stoga toksični ili ekotoksični. Ali se smatra da u prirodi ne traju dugo. Dugo se pretpostavljalo da su njeni uticaji na životnu sredinu ograničeni na područja koja ga hronično primaju.
Način razgradnje varira u zavisnosti od toga da li se odvija u aerobnom ili anaerobnom okruženju[12].
Skoro vek nakon što je Romburgov prvi opis ovog molekula 1883. godine, američki toksikolozi pokazali 1980. da je tetril dokazao (za razliku od drugih eksploziva kao što su PETN (pentaeritritol tetranitrat), RDX (1,3,5-trinitroheksahidro-1,35, -triazin) i HMX (oktahidro-1,3,5,7-tetranitro-1,3,5,7-tetrazocin)), koji je snažan mutagen, koji deluje direktno i u veoma malim dozama 1 na tri mikrobna sistema koja se konvencionalno koriste za testove mutagenosti (Neurospora crassa, Salmonella tiphimurium i Saccharomices cerevisiae).[3] Izloženost ljudi ovom proizvodu i njegovim proizvodima razgradnje stoga može dovesti do rizika po zdravlje.[3]
Korišćenje
[уреди | уреди извор]Uopšteno se koristi u obliku presovanih kuglica i odobren je kao standardno rasprskavajuće punjenje za projektile malog kalibra, jer proizvodi bolju fragmentaciju od TNT-a i njegova razbijanje je veća od snage bilo kog drugog vojnog eksploziva ovog tipa.
Njegova brzina detonacije je 7200 - 7300 metara u sekundi.
Tetril se koristi u detonatorima potrebnim za detonaciju TNT-a. Zatim se nanosi na kapsulu koja sadrži mešavinu živinog fulminata i kalijum hlorata [8]. Takođe ulazi u sastav tetritola.
Tetril je korišćen uglavnom tokom Prvog i Drugog svetskog rata i kasnijih sukoba. Tetril se obično koristi samostalno, mada se ponekad može naći u kompozicijama kao što je tetritol. Tetril se više ne proizvodi niti koristi u Sjedinjenim Državama, ali se i dalje može naći u zastareloj municiji kao što je protivpešadijska mina M14.[13]
Proizvodnja
[уреди | уреди извор]Polazni materijali za pripremu tetrila su: dimetilanilin, sumporna kiselina i azotna kiselina. Azotna kiselina se koristi u obliku nitroze sa sastavom od 85-86% azotne kiseline, 6-8% sumporne kiseline i 8% vode. Sumporna kiselina koja se ovde koristi je 92-96% monohidrat.
Proces dobijanja tetrila sastoji se od sledećih operacija:
- dobijanje dimetilanilin sulfata
- nitracija dimetilanilin sulfata
- pranje tetrila od kiselina
- kristalizacija tetrila
- sušenje i prosejavanje.
Dimetilanilin sulfat se dobija tretiranjem dimetilanilina sumpornom kiselinom na temperaturi od 33—40 °C (91—104 °F) u aparatima koji su po konstrukciji slični običnim nitratorima.
Reakcija se odvija prema jednačini:
- C6H5N(CH3)2 + H2SO4 → C6H5N(CH3)2 * H2SO4
Operaciju dobijanja dimetilanilin sulfata treba sprovesti jer usled povećanja aktivnosti benzenskog prstena izazvanog prisustvom N(CH3)2 grupe, reakcija nitracije čistog dimetilanilina teče veoma energično i veliki broj nastaju nusproizvodi. Dimetilanilin sulfat nitrati sporije i daje tetril u većem prinosu. Tetril se dobija nitracijom dimetilanilin sulfata sa smešom za nitriranje na 50—55 °C (122—131 °F). Nitracija dimetilanilin sulfata je opasnija od nitriranja toluena jer se nitracija i oksidacija odvijaju istovremeno. Ove reakcije su praćene oslobađanjem velike količine toplote. Stoga se tetril dobija u malim nitratorima.
Reakcija nitriranja najverovatnije sledi jednačinu:
- C6H5N(CH3)2 + 10 HNO3 → C6H2(NO2)3NCH3NO2 + 6NO2 + CO2+8H2O
- C6H5N(CH3)2 + 6HNO3 → C6H2(NO2)3NCH3NO2 + 2NO + CO2 + 6H2O
Nakon što je nitracija završena, tetril se odvaja od kiselina na filteru i ispere sa malom količinom vode; zatim se šalje u stanicu za pranje gde se pere bez kiselina u bačvama opremljenim mešalicama. Proizvod se pere nekoliko puta u početku hladnom vodom, a zatim toplom vodom. Voda sadržana u ispranom tetrilu se izvlači na vakuum filterima; stoga se tetril šalje da se kristališe iz benzena ili dihloretana. U kristalizaciji iz acetona, tetril se prethodno osuši.
Da bi se tetril rekristalizovao, on se toplo rastvori u benzenu ili dihloretanu da bi se dobio zasićeni rastvor u aparatima koji se nazivaju rastvarači. Dodatno ispiranje toplom vodom se obično vrši u rastvaraču kako bi se što potpunije uklonili ostaci kiseline. Vrući rastvor se šalje kroz filtere u kristalizator gde se rastvor postepeno hladi i tetril precipitira. Sadržaj kristalizatora se šalje u vakuum filter, gde se tetril odvaja od kristalne tečnosti, a zatim ispere vodom i alkoholom.
Prečišćeni tetril se suši u posudama postavljenim na police na 40—60 °C (104—140 °F); nakon što je sušenje završeno, materijal se prosijava da se odvoje grudvice i pakuje.
Zdravstveni problemi
[уреди | уреди извор]Iako je tetril među najotrovnijim eksplozivnim jedinjenjima, veoma je kratkotrajan. Ovo u kombinaciji sa činjenicom da su uticaji ovog jedinjenja na zdravlje uglavnom neproučeni, ne zna se mnogo o zdravstvenim problemima koje ovo jedinjenje može izazvati.
Epidemiološki podaci pokazuju da tetril najviše deluje na kožu, delujući kao jak iritant.[14] Mogu se javiti simptomi senzibilizacije kože kao što su dermatitis, svrab, eritem itd.[15] Tetril takođe može da utiče na sluzokože, gornje disajne puteve, a možda i na jetru.
Tokom rata, 30% radnika u fabrikama municije u kontaktu sa ovim proizvodom bilo je senzibilizirano na njega[16] za 10 do 14 dana općenito[16]. Američki radnici morali su da koriste nemasne kreme i da se peru sa 1% sapuna.sulfiti koji su razlagali tetril[16]. Tokom Drugog svetskog rata značajan broj alergija. Kontaktni dermatitis je primećen kod radnika u fabrikama municije, a posebno kod onih koji su rukovali ili pripremali eksplozive ili koji su rukovali fulminatom žive. Pikrinska kiselina (lidit) i trinitrotoluen (TNT) bili su poznati alergeni, ali je utvrđeno da je tetril još više alergenski. U ovom periodu proučavan je mehanizam nastanka ovih alergija, a da nije došlo do rešenja za zaštitu radnika.
Vidi jpš
[уреди | уреди извор]Reference
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ а б в Whong Wen-Zong, Norman D. Speciner, Gordon S. Edwards, Mutagenic activity of tetryl, a nitroaromatic explosive, in three microbial test systems ; Toxicology Letters Volume 5, Issue 1, January 1980, Pages 11–17 (résumé)
- ^ а б в Leon J. Witkowski, M.D.; Carl N. Fisher, M.D.; Howard D. Murdock, M.S, Industrial illness due to tetryl report of 1258 cases ; AMA. 1942;119(17):1406-1409. doi: 10.1001/jama.1942.02830340018005 (Début du texte)
- ^ Ghose, A.K.; Viswanadhan V.N. & Wendoloski, J.J. (1998). „Prediction of Hydrophobic (Lipophilic) Properties of Small Organic Molecules Using Fragment Methods: An Analysis of AlogP and CLogP Methods”. J. Phys. Chem. A. 102: 3762—3772. doi:10.1021/jp980230o.
- ^ Tetko IV, Tanchuk VY, Kasheva TN, Villa AE (2001). „Estimation of Aqueous Solubility of Chemical Compounds Using E-State Indices”. Chem Inf. Comput. Sci. 41: 1488—1493. PMID 11749573. doi:10.1021/ci000392t.
- ^ Ertl P.; Rohde B.; Selzer P. (2000). „Fast calculation of molecular polar surface area as a sum of fragment based contributions and its application to the prediction of drug transport properties”. J. Med. Chem. 43: 3714—3717. PMID 11020286. doi:10.1021/jm000942e.
- ^ а б в г „Booster Explosives”.
- ^ Boosters explosifs
- ^ а б Köhler, J.; Meyer, R.; Homburg, A.: Explosivstoffe, zehnte, vollständig überarbeitete Auflage, Wiley-VCH, Weinheim 2008, ISBN 978-3-527-32009-7.
- ^ R Boopathy, Formation of aniline as a transient metabolite during the metabolism of tetryl by a sulfate-reducing bacterial consortium ;- Current microbiology, 2000 ([Résumé])
- ^ Manish M. Shah, Jim C. Spain (1996), Regular Article Elimination of Nitrite from the Explosive 2,4,6-Trinitrophenylmethylnitramine (Tetryl) Catalyzed by Ferredoxin NADP Oxidoreductase from Spinach ; Biochemical and Biophysical Research Communications Volume 220, Issue 3, 27 March 1996, Pages 563–568 (Résumé)
- ^ “A Military Guide to Terrorism in the 21st Century.” August 2003. P. 171. U.S. Army Training and Doctrine Command, Fort Leavenworth, Kansas. http://smallwarsjournal.com/documents/terrorismhandbook.pdf. Accessed May 11, 2010.
- ^ CDC - Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs)
- ^ CDC - NIOSH Pocket Guide to Chemical Hazards
- ^ а б в PGH Gell, Sensitization to “tetryl” ; National Institute for Medical Research, Hampstead ; British Journal of Experimental Pathology, 1944 [PDF] à partir de nih.gov
Literatura
[уреди | уреди извор]- Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- Smith, Michael B.; March, Jerry (2007). Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6th изд.). New York: Wiley-Interscience. ISBN 0-471-72091-7.
- Katritzky A.R.; Pozharskii A.F. (2000). Handbook of Heterocyclic Chemistry (Second изд.). Academic Press. ISBN 0080429882.
Spoljašnje veze
[уреди | уреди извор]- Tetryl
- Tetryl Архивирано на сајту Wayback Machine (15. август 2000), Agency for Toxic Substances and Disease Registry
- Occupational Safety and Health Guideline for Tetryl Архивирано 2009-02-27 на сајту Wayback Machine, Occupational Safety & Health Administration
