Herpes simpleks virus
| Herpes simpleks virus | |
|---|---|
| |
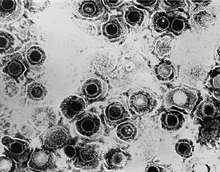
| Mikrografija herpes simpleks virusa | |
| Naučna klasifikacija | |
| (nerangirano): | Virus |
| Realm: | Duplodnaviria |
| Carstvo: | Heunggongvirae |
| Tip: | Peploviricota |
| Klasa: | Herviviricetes |
| Red: | Herpesvirales |
| Porodica: | Herpesviridae |
| Potporodica: | Alphaherpesvirinae |
| Rod: | Simplexvirus |
| Uključene grupe | |
| Kladistički uključene, mada tradicionalno isključene iz taksona | |
|
All other Simplexvirus spp.:
| |
Herpes simplek virus (akronim HSV) ili HSV-1 i HSV-2, takođe poznati pod svojim taksonomskim nazivima Ljudski alfaherpesvirus 1 i Ljudski alfaherpesvirus 2, su dva člana iz humane porodice Herpesviridae, grupe novijih virusa koji proizvode virusne infekcije kod većine ljudi.[1][2] I HSV-1 (koji proizvodi većinu herpesa) i HSV-2 (koji proizvodi većinu genitalnog herpesa) su uobičajeni i zarazni, i mogu se preneti kada zaražena osoba počne da prenosi virus.
Oko 67% svetske populacije mlađe od 50 godina ima HSV-1.[3] U Sjedinjenim Američkim Državama se veruje da je oko 47,8% osoba zaraženo HSV-1, a 11,9% osoba HSV-2.[4] Pošto se može preneti bilo kojim intimnim kontaktom, spada u grupu izazivača najčešćih polno prenosivih infekcija.[5]
Prenošenje
[uredi | uredi izvor]HSV-1 i HSV-2 se prenose kontaktom sa zaraženom osobom koja ima reaktivaciju virusa.
HSV-2 se periodično izlučuje preko ljudskih genitalnih organa, najčešće kod asimptomatskih oblika. Većina seksualnih prenosa se dešava tokom perioda asimptomatske reaktivacije infekcije.[6] Asimptomatska reaktivacija znači da virus izaziva atipične, suptilne ili teško uočljive simptome koji nisu identifikovani kao aktivna herpes infekcija, tako da je sticanje virusa moguće čak i ako nema aktivnih HSV plikova ili ranica.
U jednoj studiji, dnevni uzorci briseva genitalnih organa otkrili su HSV-2 u proseku u 12–28% slučajeva među onima koji su imali epidemiju i u 10% među onima koji pate od asimptomatske infekcije, pri čemu su se mnoge od ovih epizoda dešavale bez vidljivih manifestacija („subklinički osip“).[7]
U drugoj studiji, 73 subjekta su randomizovana da primaju valaciklovir 1 gram dnevno ili placebo tokom 60 dana svaki u dvosmernom unakrsnom dizajnu. Dnevni bris genitalnog područja je samostalno uzet za detekciju HSV-2 lančanom reakcijom polimeraze, da bi se uporedio efekat valaciklovira u odnosu na placebo na asimptomatskim izlučivanjem virusa kod imunokompetentnih, HSV-2 seropozitivnih subjekata bez istorije simptomatske infekcije genitalnog herpesa. Studija je otkrila da je valaciklovir značajno smanjio izlučivanje tokom subkliničkih dana u poređenju sa placebom, pokazujući smanjenje od 71%; dok 84% ispitanika nije imalo osip dok su primali valaciklovir u odnosu na 54% ispitanika koji su bili a placebu. Oko 88% pacijenata lečenih valaciklovirom nije imalo prepoznate znakove ili simptome u odnosu na 77% kod placeba.[8]
Za HSV-2, subkliničko izlučivanje može predstavljati najznačajniji način prenošenja.[7] Studije na neskladnim partnerima (jedan zaražen HSV-2, jedan ne) pokazuju da je stopa prenošenja približno 5 na 10.000 seksualnih kontakata.[9] Atipični simptomi se često pripisuju drugim uzrocima, kao što je gljivična infekcija.
HSV-1 se često dobija oralno tokom detinjstva. Takođe se može preneti polno, uključujući kontakt sa pljuvačkom, kao što je ljubljenje i kontakt usta sa genitalijama (oralni seks).[10]
HSV-2 je prvenstveno polno prenosiva infekcija, ali stopa genitalnih infekcija HSV-1 sve više raste.[11]
Oba virusa se takođe mogu prenositi vertikalno tokom porođaja,[12] pa se često virus naziva „negenitalni herpes simpleks virus“.[13] Međutim, rizik od prenošenja infekcije je minimalan ako majka nema simptome ili plikove tokom porođaja. Rizik je značajniji kada se majka prvi put zarazi virusom tokom kasne trudnoće.[14]
Suprotno popularnim mitovima, herpes se ne može preneti sa površina kao što su toaletne daske jer virus herpesa počinje da umire odmah po izlasku iz tela.[15] Iako herpes simpleks virusi mogu uticati na delove kože koji su izložena kontaktu sa zaraženom osobom. Primer za to je herpes infekcija prstiju, npr. stomatologa pre rutinske upotrebe rukavica prilikom lečenja pacijenata.[16] Rukovanje sa zaraženom osobom ne prenosi ovu bolest.
Infekcija HSV-2 povećava rizik od dobijanja HIV-a.[17]
Virologi
[uredi | uredi izvor]Virusna struktura
[uredi | uredi izvor]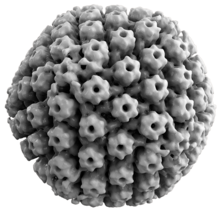

Svi virusi herpesa kod životinja imaju neka zajednička svojstva. Struktura herpes virusa sastoji se od relativno velikog, dvolančanog, linearnog DNK genoma umotanog u ikosaedarski proteinski kavez koji se zove kapsid, koji je umotan u lipidni dvosloj koji se naziva omotač. Koverta je spojena sa kapsidom pomoću tegumenta. Ova potpuna čestica je poznata kao virion.[18] Svaki od HSV-1 i HSV-2 sadrži najmanje 74 gena (ili otvorenih okvira čitanja, ORF) unutar svojih genoma,[19] iako spekulacije o gomilanju gena dozvoljavaju čak 84 jedinstvena gena koji kodiraju proteine pomoću 94 navodna ORF-a.[20] Ovi geni kodiraju različite proteine uključene u formiranje kapsida, tegumenta i omotača virusa, kao i kontrolu replikacije i infektivnosti virusa. Ovi geni i njihove funkcije su prikazani u tabeli ispod.
Genomi HSV-1 i HSV-2 su složeni i sadrže dva jedinstvena regiona koji se nazivaju dugi jedinstveni region (UL) i kratki jedinstveni region (US). Od 74 poznata ORF-a, UL sadrži 56 virusnih gena, dok US sadrži samo 12.[19] Transkripciju HSV gena katalizuje RNK polimeraza II inficiranog domaćina.[19] Neposredni rani geni, koji kodiraju proteine koji regulišu ekspresiju ranih i kasnih virusnih gena, prvi su koji se eksprimiraju nakon infekcije. Sledi rana ekspresija gena, kako bi se omogućila sinteza enzima uključenih u replikaciju DNK i proizvodnju određenih glikoproteina omotača. Ekspresija kasnih gena se dešava poslednja; ova grupa gena pretežno kodira proteine koji formiraju virionsku česticu.[19]
Pet proteina iz (UL) formiraju virusni kapsid - UL6, UL18, UL35, UL38 i glavni kapsid protein UL19.[18]
Ulaz u ćeliju
[uredi | uredi izvor]Ulazak HSV-a u ćeliju domaćina uključuje vezivanje nekoliko glikoproteina na površini virusa sa omotačem za njihove transmembranske receptore na površini ćelije. Mnogi od ovih receptora se zatim povlače prema unutra od strane ćelije, za koju se smatra da otvara prsten od tri heterodimera gHgL koji stabilizuju kompaktnu konformaciju gB glikoproteina, tako da on izbija i probija ćelijsku membranu.[21] Omotač koji pokriva virusnu česticu se zatim spaja sa ćelijskom membranom, stvarajući poru kroz koju sadržaj virusnog omotača ulazi u ćeliju domaćina.
Uzastopne faze ulaska HSV-a su analogne onima kod drugih virusa. U početku, komplementarni receptori na virusu i na površini ćelije dovode virus i ćelijske membrane u blizinu. Interakcije ovih molekula zatim formiraju stabilnu ulaznu poru kroz koju se sadržaj virusnog omotača unosi u ćeliju domaćina. Virus se takođe može endocitozirati nakon vezivanja za receptore, a fuzija se može desiti na endosomu. Na elektronskim mikrografijama, spoljni listići virusnog i ćelijskog lipidnog dvosloja su viđeni spojeni;[22] ova hemifuzija može biti na uobičajenom putu ka ulasku ili obično može biti zaustavljeno stanje koje je verovatnije da će biti zarobljeno nego prolazni mehanizam ulaska.
U slučaju herpes virusa, početne interakcije se javljaju kada se dva virusna glikoproteina omotača nazvana glikoprotein C (gC) i glikoprotein B (gB) vežu za česticu na površini ćelije koja se zove heparan sulfat. Zatim, glavni protein koji vezuje receptore, glikoprotein D (gD), vezuje se specifično za najmanje jedan od tri poznata ulazna receptora.[traži se izvor] Ovi ćelijski receptori uključuju posrednik ulaska herpesvirusa (HVEM), nektin-1 i 3-O sulfatni heparan sulfat. Nektinski receptori obično proizvode adheziju ćelija-ćelija, da bi obezbedili jaku tačku vezivanja virusa za ćeliju domaćina.[21] Ove interakcije dovode površine membrane u međusobnu blizinu i omogućavaju drugim glikoproteinima ugrađenim u omotač virusa da stupe u interakciju sa drugim molekulima površine ćelije. Jednom vezan za HVEM, gD menja svoju konformaciju i stupa u interakciju sa virusnim glikoproteinima H (gH) i L (gL), koji formiraju kompleks. Interakcija ovih membranskih proteina može dovesti do stanja hemifuzije. gB interakcija sa gH/gL kompleksom stvara ulazne pore za virusni kapsid.[22] gB stupa u interakciju sa glikozaminoglikanima na površini ćelije domaćina
Genetska inokulacija
[uredi | uredi izvor]Nakon što virusni kapsid uđe u ćelijsku citoplazmu, transportuje se do jezgra ćelije. Jednom kada se zakači za jezgro u nuklearnoj ulaznoj poru, kapsid izbacuje svoj DNK sadržaj preko kapisnog portala. Kapsidni portal je formiran od 12 kopija portalnog proteina, UL6, raspoređenih u obliku prstena; proteini sadrže leucinski rajsferšlus sekvencu aminokiselina, što im omogućava da se prianjaju jedni za druge.[23] Svaki ikosaedarski kapsid sadrži jedan portal, smešten u jednom tjemenu.[24] DNK izlazi iz kapsida u jednom linearnom segmentu.[25]
Imunološko izbegavanje
[uredi | uredi izvor]HSV izbegava imunološki sistem preko interferencije sa prezentacijom antigena MHC klase I na površini ćelije, blokiranjem transportera povezanog sa obradom antigena (TAP) indukovanog sekrecijom ICP-47 od strane HSV. U ćeliji domaćinu, TAP prenosi digestivne peptide epitopa virusnog antigena iz citosola u endoplazmatski retikulum, omogućavajući da se ovi epitopi kombinuju sa molekulima MHC klase I i predstave na površini ćelije. Prezentacija virusnog epitopa sa MHC klase I je preduslov za aktivaciju citotoksičnih T-limfocita (CTL), glavnih efektora imunog odgovora posredovanog ćelijama protiv ćelija inficiranih virusom. ICP-47 sprečava pokretanje CTL odgovora na HSV, omogućavajući virusu da preživi duži period u domaćinu.[26] HSV obično proizvodi citopatski efekat (CPE) u roku od 24-72 sata nakon infekcije u permisivnim ćelijskim linijama, što se primećuje klasičnim formiranjem plaka. Međutim, prijavljeni su i klinički izolati HSV-1 koji nisu pokazali nikakav CPE u Vero i A549 ćelijskim kulturama tokom nekoliko pasusa sa niskim nivoom ekspresije proteina virusa. Verovatno ovi izolati HSV-1 evoluiraju ka „zagonetnijem“ obliku da bi se uspostavila hronična infekcija i na taj način otkrila još jednu strategiju za izbegavanje imunološkog sistema domaćina, osim neuronske latencije.[27]
Replikacija
[uredi | uredi izvor]
Nakon infekcije ćelije, proizvodi se kaskada proteina virusa herpesa, koji se nazivaju neposredno rani, rani i kasni. Istraživanje pomoću protočne citometrije na drugom članu porodice herpes virusa, herpesvirusu povezanom sa Kaposijevim sarkomom, ukazuje na mogućnost dodatnog litičkog stadijuma, odloženo-kasno.[28] Ove faze litičke infekcije, posebno kasne litičke, razlikuju se od faze latencije. U slučaju HSV-1, proteinski proizvodi se ne detektuju tokom latencije, dok se detektuju tokom litičkog ciklusa.
Rani transkribovani proteini se koriste u regulaciji genetske replikacije virusa. Prilikom ulaska u ćeliju, α-TIF protein se pridružuje virusnoj čestici i pomaže u neposrednoj ranoj transkripciji. Protein za zatvaranje viriona (VHS ili UL41) je veoma važan za replikaciju virusa.[29] Ovaj enzim isključuje sintezu proteina u domaćinu, razgrađuje mRNK domaćina, pomaže u replikaciji virusa i reguliše ekspresiju gena virusnih proteina. Virusni genom odmah putuje u jezgro, ali VHS protein ostaje u citoplazmi.[30][29]
Kasni proteini formiraju kapsid i receptore na površini virusa. Pakovanje virusnih čestica - uključujući genom, jezgro i kapsid - se dešava u jezgru ćelije. Ovde se konkatemeri virusnog genoma razdvajaju cepanjem i stavljaju u formirane kapside. HSV-1 prolazi kroz proces primarnog i sekundarnog omotača. Primarni omotač se dobija pupanjem u unutrašnju nuklearnu membranu ćelije. Ovo se zatim spaja sa spoljnom nuklearnom membranom. Virus dobija svoj konačni omotač pupanjem u citoplazmatske vezikule.[31]
Latentna infekcija
[uredi | uredi izvor]HSV-ovi mogu opstati u mirnom, ali upornom obliku poznatom kao latentna infekcija, posebno u nervnim ganglijama.[1] HSV-1 ima tendenciju da boravi u trigeminalnim ganglijima, dok HSV-2 ima tendenciju da boravi u sakralnim ganglijima, ali to su samo tendencije, a ne fiksno ponašanje. Tokom latentne infekcije ćelije, HSV eksprimiraju RNK transkripta povezanu sa latencijom (LAT). LAT reguliše genom ćelije domaćina i ometa prirodne mehanizme ćelijske smrti. Održavanjem ćelija domaćina, ekspresija LAT čuva rezervoar virusa, što omogućava naknadne, obično simptomatske, periodične recidive ili „izbijanja“ karakteristične za nelatentnost. Bez obzira na to da li su recidivi simptomatski ili ne, dolazi do oslobađanja virusa da bi se inficirao novi domaćin.
Protein koji se nalazi u neuronima može se vezati za DNK virusa herpesa i regulisati latenciju. DNK virusa herpesa sadrži gen za protein nazvan ICP4, koji je važan transaktivator gena povezanih sa litičkom infekcijom kod HSV-1.[32] Elementi koji okružuju gen za ICP4 vezuju protein poznat kao humani neuronski protein neuronski restriktivni faktor utišavanja (NRSF) ili faktor transkripcije utišavanja elementa represora čoveka (REST). Kada se veže za elemente virusne DNK, deacetilacija histona se dešava na vrhu ICP4 genske sekvence kako bi se sprečilo pokretanje transkripcije sa ovog gena, čime se sprečava transkripcija drugih virusnih gena uključenih u litički ciklus.[32] Drugi HSV protein preokreće inhibiciju sinteze proteina ICP4. ICP0 odvaja NRSF od ICP4 gena i na taj način sprečava utišavanje virusne DNK.[33]
Genom
[uredi | uredi izvor]HSV genom se sastoji od dva jedinstvena segmenta, nazvana jedinstveni dugi (UL) i jedinstveni kratki (US), kao i terminalnih invertiranih ponavljanja pronađenih na dva kraja nazvana dugo ponavljanje (RL) i kratko ponavljanje (RS). Postoje i manji elementi „zaliha terminala“ (α) koji se nalaze na daljim krajevima RS. Ukupan raspored je RL-UL-RL-α-RS-US-RS-α sa svakim parom ponavljanja koji se međusobno invertuju. Cela sekvenca se zatim kapsulira u terminalnu direktnu ponavljanje. Dugi i kratki delovi imaju svoje poreklo replikacije, pri čemu se OriL nalazi između UL28 i UL30 i OriS koji se nalazi u paru blizu RS.[34] Kako se L i S segmenti mogu sastaviti u bilo kom smeru, oni se mogu slobodno okretati jedan u odnosu na drugi, formirajući različite linearne izomere.[35]
| ORF | Lažni protein | HSV-1 | HSV-2 | Funkcija/opis |
|---|---|---|---|---|
| Dugo ponavljanje (RL) | ||||
| ICP0/RL2 | ICP0; IE110; α0 | P08393 | P28284 | E3 ubikvitin ligaza koja aktivira transkripciju virusnog gena suprotstavljajući se hromatinizaciji virusnog genoma i suprotstavlja se intrinzičnim i antivirusnim odgovorima zasnovanim na interferonu. |
| RL1 | RL1; ICP34.5 | O12396 | Faktor neurovirulencije. Antagonizira PKR defosforilacijom eIF4a. Veže se za BECN1 i inaktivira autofagiju. | |
| LAT | LRP1, LRP2 | P17588
P17589 |
Transkript povezan sa kašnjenjem i proteinski proizvodi (proteini povezani sa kašnjenjem) | |
| Jedinstvena duga (UL) | ||||
| UL1 | Glycoprotein L | P10185 | Površina i membrana | |
| UL2 | UL2 | P10186 | Uracil-DNK glikozilaza | |
| UL3 | UL3 | P10187 | Nepoznat | |
| UL4 | UL4 | P10188 | Nepoznat | |
| UL5 | UL5 | Q2MGV2 | DNK replikacija | |
| UL6 | Portalni protein UL-6 | P10190 | Dvanaest od ovih proteina čine kapisdni portalni prsten kroz koji DNK ulazi i izlazi iz kapsida. | |
| UL7 | UL7 | P10191 | Sazrevanje viriona | |
| UL8 | UL8 | P10192 | Protein povezan sa kompleksom DNK virusa helikaze i primaze | |
| UL9 | UL9 | P10193 | Protein koji se vezuje poreko replikacije | |
| UL10 | Glycoprotein M | P04288 | Površina i membrana | |
| UL11 | UL11 | P04289 | Izlaz viriona i sekundarni omotač | |
| UL12 | UL12 | Q68978 | Alkalna eksonukleaza | |
| UL13 | UL13 | Q9QNF2 | Serin-treonin protein kinaza | |
| UL14 | UL14 | P04291 | Tegument protein | |
| UL15 | Terminase | P04295 | Obrada i pakovanje DNK | |
| UL16 | UL16 | P10200 | Tegument protein | |
| UL17 | UL17 | P10201 | Obrada i pakovanje DNK | |
| UL18 | VP23 | P10202 | Kapsidni protein | |
| UL19 | VP5; ICP5 | P06491 | Glavni kapsidni protein | |
| UL20 | UL20 | P10204 | Membranski protein | |
| UL21 | UL21 | P10205 | Tegument protein | |
| UL22 | Glycoprotein H | P06477 | Površina i membrana | |
| UL23 | Thymidine kinase | O55259 | Periferna replikacija DNK | |
| UL24 | UL24 | P10208 | Nepoznat | |
| UL25 | UL25 | P10209 | Obrada i pakovanje DNK | |
| UL26 | P40; VP24; VP22A; UL26.5 (HHV2 kratka izoforma) | P10210 | P89449 | Kapsidni protein |
| UL27 | Glycoprotein B | A1Z0P5 | Površina i membrana | |
| UL28 | ICP18.5 | P10212 | Obrada i pakovanje DNK | |
| UL29 | UL29; ICP8 | Q2MGU6 | Glavni protein koji vezuje DNK | |
| UL30 | DNA polymerase | Q4ACM2 | DNK replikacija | |
| UL31 | UL31 | Q25BX0 | Protein nuklearnog matriksa | |
| UL32 | UL32 | P10216 | Glikoprotein omotača | |
| UL33 | UL33 | P10217 | Obrada i pakovanje DNK | |
| UL34 | UL34 | P10218 | Protein unutrašnje nuklearne membrane | |
| UL35 | VP26 | P10219 | Kapsidni protein | |
| UL36 | UL36 | P10220 | Protein velikog tegumenta | |
| UL37 | UL37 | P10216 | Sastavljanje kapsida | |
| UL38 | UL38; VP19C | P32888 | Sastavljanje kapsida i sazrevanje DNK | |
| UL39 | UL39; RR-1; ICP6 | P08543 | Ribonukleotid reduktaza (mala podjedinica) | |
| UL40 | UL40; RR-2 | P06474 | Ribonukleotid reduktaza (mala podjedinica) | |
| UL41 | UL41; VHS | P10225 | Tegument protein; isključivanje domaćina viriona | |
| UL42 | UL42 | Q4H1G9 | Faktor procesivnosti DNK polimeraze | |
| UL43 | UL43 | P10227 | Mambranski protein | |
| UL44 | Glycoprotein C | P10228 | Površina i membrana | |
| UL45 | UL45 | P10229 | Membranski protein; C-tip lektina | |
| UL46 | VP11/12 | P08314 | Tegument proteini | |
| UL47 | UL47; VP13/14 | P10231 | Tegument proteini | |
| UL48 | VP16 (Alpha-TIF) | P04486 | Sazrevanje viriona; aktiviraju IE gene interakcijom sa ćelijskim transkripcionim faktorima Oct-1 i HCF. Vezuje se za sekvencu5'TAATGARAT3'. | |
| UL49 | UL49A | O09800 | Protein omotača | |
| UL50 | UL50 | P10234 | dUTP difosfataza | |
| UL51 | UL51 | P10234 | Tegument proteini | |
| UL52 | UL52 | P10236 | Protein kompleksa DNK helikaze/primaze | |
| UL53 | Glycoprotein K | P68333 | Površina i membrana | |
| UL54 | IE63; ICP27 | P10238 | Regulacija transkripcije i inhibicija STING signaloma | |
| UL55 | UL55 | P10239 | Nepoznat | |
| UL56 | UL56 | P10240 | Nepoznat | |
| Obrnuto ponavljanje dugo (IRL) | ||||
| Obrnuto ponavljanje kratko (IRS) | ||||
| Jedinstveno kratko (US) | ||||
| US1 | ICP22; IE68 | P04485 | Replikacija virusa | |
| US2 | US2 | P06485 | Nepoznat | |
| US3 | US3 | P04413 | Serin/treonin-protein kinaza | |
| US4 | Glycoprotein G | P06484 | Površina i membrana | |
| US5 | Glycoprotein J | P06480 | Površina i membrana | |
| US6 | Glycoprotein D | A1Z0Q5 | Površina i membrana | |
| US7 | Glycoprotein I | P06487 | Površina i membrana | |
| US8 | Glycoprotein E | Q703F0 | Površina i membrana | |
| US9 | US9 | P06481 | Tegument protein | |
| US10 | US10 | P06486 | Kapsid/Tegument protein | |
| US11 | US11; Vmw21 | P56958 | Vezuje DNK i RNK | |
| US12 | ICP47; IE12 | P03170 | Inhibira put MHC klase 1 sprečavanjem vezivanja antigena za TAP | |
| Kratko ponavljajući terminal (TRS) | ||||
| RS1 | ICP4; IE175 | P08392 | Glavni aktivator transkripcije. Neophodan za napredovanje nakon neposredne rane faze infekcije. IEG represor transkripcije. | |
Evolucija
[uredi | uredi izvor]Genomi herpes simpleksa 1 mogu se klasifikovati u šest klasa.[36] Četiri od njih se javljaju u istočnoj Africi, jedan u istočnoj Aziji i jedan u Evropi i Severnoj Americi. Ovo sugeriše da virus možda potiče iz istočne Afrike. Čini se da je najnoviji zajednički predak evroazijskih sojeva evoluirao pre oko 60.000 godina.[37] Istočnoazijski izolati HSV-1 imaju neobičan obrazac koji se trenutno najbolje objašnjava sa dva talasa migracija odgovornih za naseljavanje Japana.[37]
Herpes simplek 2 genomi se mogu podeliti u dve grupe: jedna je globalno rasprostranjena, a druga je uglavnom ograničena na podsaharsku Afriku.[38] Globalno rasprostranjeni genotip je prošao kroz četiri drevne rekombinacije sa herpes simpleksom 1. Takođe je objavljeno da HSV-1 i HSV-2 mogu imati savremene i stabilne događaje rekombinacije kod domaćina koji su istovremeno inficirani sa oba patogena. Svi slučajevi su HSV-2 koji preuzima delove HSV-1 genoma, ponekad menjajući u evolucionom procesu delove epitopa antigena.[39]
Stopa mutacije je procenjena na ~1,38×10−7 supstitucija/lokaciji/godini.[36] U kliničkom okruženju, mutacije u genu timidin kinaze ili genu DNK polimeraze izazvale su otpornost na aciklovir. Međutim, većina mutacija se javlja u genu timidin kinaze, a ne u genu DNK polimeraze.[40]
Druga analiza je procenila da je stopa mutacije u genomu herpes simpleksa 1 1,82×10−8 supstitucija nukleotida po mestu godišnje. Ova analiza je postavila najnovijeg zajedničkog pretka ovog virusa pre ~710.000 godina.[41]
Herpes simpleks 1 i 2 su se razdvojili u dva posebna podtipa pre oko 6 miliona godina.[39]
Klinička slika infekcije
[uredi | uredi izvor]Mnogi od onih koji su zaraženi nikada ne razviju simptome.[traži se izvor] Simptomi, kada se pojave, mogu uključivati vodenaste plikove na koži ili sluzokoži usta, usana, nosa ili genitalija,[1] ili očiju (očni herpes).[traži se izvor] Lezije leče krastama karakterističnim za herpetičnu bolest. Ponekad virusi izazivaju blage ili atipične simptome tokom izbijanja. Međutim, oni takođe mogu izazvati problematičnije oblike herpes simpleksa. Kao neurotropni i neuroinvazivni virusi, HSV-1 i -2 opstaju u telu skrivajući se od imunog sistema u ćelijskim telima neurona. Nakon početne ili primarne infekcije, neki zaraženi ljudi doživljavaju sporadične epizode virusne reaktivacije ili izbijanja. U izbijanju, virus u nervnoj ćeliji postaje aktivan i transportuje se preko aksona neurona do kože, gde dolazi do umnožavanja i izbacivanja virusa i izaziva nove rane.[traži se izvor]
Terapija
[uredi | uredi izvor]

Herpes virusi uspostavljaju doživotne infekcije (i stoga se ne mogu iskoreniti iz tela).[42]
Tretman obično uključuje antivirusne lekove opšte namene koji ometaju replikaciju virusa, smanjuju fizičku težinu lezija povezanih sa epidemijom i smanjuju mogućnost prenošenja na druge. Studije ranjivih populacija pacijenata su pokazale da svakodnevna upotreba antivirusnih lekova kao što su aciklovir[43] valaciklovir može smanjiti stope reaktivacije.[44] Ekstenzivna upotreba antiherpetičkih lekova dovela je do razvoja rezistencije na lekove, što zauzvrat dovodi do neuspeha lečenja. Stoga se novi izvori lekova široko istražuju kako bi se rešio problem. U januaru 2020. objavljen je opsežan pregledni članak koji je pokazao efikasnost prirodnih proizvoda kao obećavajućih lekova protiv HSV.[45]
Pirition, jonofor cinka, pokazuje antivirusnu aktivnost protiv virusa herpes simpleksa.[46]
Reaktivacija višestrukosti
[uredi | uredi izvor]Reaktivacija višestrukosti (MR) je proces kojim virusni genomi koji sadrže oštećenje međusobno deluju unutar zaražene ćelije da bi stvorili održivi virusni genom. MR je prvobitno otkriven sa bakterijskim virusom bakteriofagom T4, ali je potom pronađen i kod patogenih virusa, uključujući virus gripa, HIV-1, adenovirusni simian virus 40, virus vakcinije, reovirus, poliovirus i virus herpes simpleksa.[47]
Kada su HSV čestice izložene dozama agensa koji oštećuje DNK koji bi bio smrtonosan u pojedinačnim infekcijama, ali im se zatim dozvoli da se podvrgnu višestrukoj infekciji (dva ili više virusa u ćeliji domaćina), primećuje se reaktivacija višestrukosti. Poboljšano preživljavanje HSV-1 usled reaktivacije višestrukosti nastaje nakon izlaganja različitim agensima koji oštećuju DNK, uključujući metil metansulfonat,[48] trimetilpsoralen (koji uzrokuje umrežavanje DNK u lancima)[49][50] i UV svetlost.[51]
Nakon tretmana genetski obeleženog HSV trimetilpsoralenom, povećava se rekombinacija između obeleženih virusa, što sugeriše da oštećenje trimetilpsoralena stimuliše rekombinaciju. Izgleda da reaktivacija višestrukosti HSV delimično zavisi od rekombinacionih funkcija za popravku ćelija domaćina, jer ćelije fibroblasta kože oštećene u okviru ove funkcije (ćelije pacijenata sa Blumovim sindromom) nemaju reaktivaciju višestrukosti.[51]
Ova zapažanja sugerišu da reaktivacija višestrukosti kod HSV infekcija uključuje genetsku rekombinaciju između oštećenih virusnih genoma što rezultuje proizvodnjom održivih virusa potomaka. HSV-1, nakon zaraze ćelija domaćina, izaziva upalu i oksidativni stres.[52] Stoga se čini da genom HSV može biti izložen oksidativnom oštećenju DNK tokom infekcije, a da reaktivacija višestrukosti može poboljšati preživljavanje virusa i virulenciju pod ovim uslovima.
Izvori
[uredi | uredi izvor]- ^ a b v Ryan KJ, Ray CG, ur. (2004). Sherris Medical Microbiology (4th izd.). McGraw Hill. str. 555–62. ISBN 978-0-8385-8529-0.
- ^ Chayavichitsilp P, Buckwalter JV, Krakowski AC, Friedlander SF (april 2009). „Herpes simplex”. Pediatr Rev. 30 (4): 119—29; quiz 130. PMID 19339385. S2CID 34735917. doi:10.1542/pir.30-4-119.
- ^ „Herpes simplex virus”. www.who.int (na jeziku: engleski). Pristupljeno 2022-03-15.
- ^ Geraldine McQuillan, Ph.D., Deanna Kruszon-Moran, M.S., Elaine W. Flagg, Ph.D., M.S., and Ryne Paulose-Ram, Ph.D., M.A. Prevalence of Herpes Simplex Virus Type 1 and Type 2 in Persons Aged 14–49: United States, 2015–2016, NCHS Data Brief No. 304 February 2018
- ^ Straface, Gianluca; Selmin, Alessia; Zanardo, Vincenzo; De Santis, Marco; Ercoli, Alfredo; Scambia, Giovanni (2012). „Herpes Simplex Virus Infection in Pregnancy”. Infectious Diseases in Obstetrics and Gynecology. 2012: 385697. PMC 3332182
 . PMID 22566740. doi:10.1155/2012/385697
. PMID 22566740. doi:10.1155/2012/385697  ..
..
- ^ Schiffer, Joshua T.; Mayer, Bryan T.; Fong, Youyi; Swan, David A.; Wald, Anna (2014). „Herpes simplex virus-2 transmission probability estimates based on quantity of viral shedding”. Journal of the Royal Society Interface. 11 (95). PMC 4006256
 . PMID 24671939. doi:10.1098/rsif.2014.0160..
. PMID 24671939. doi:10.1098/rsif.2014.0160..
- ^ a b Johnston, Christine; Koelle, David M.; Wald, Anna (2011). „HSV-2: In pursuit of a vaccine”. Journal of Clinical Investigation. 121 (12): 4600—4609. PMC 3223069
 . PMID 22133885. doi:10.1172/JCI57148..
. PMID 22133885. doi:10.1172/JCI57148..
- ^ Sperling, Rhoda S.; Fife, Kenneth H.; Warren, Terri J.; Dix, Lynn P.; Brennan, Clare A. (2008). „The Effect of Daily Valacyclovir Suppression on Herpes Simplex Virus Type 2 Viral Shedding in HSV-2 Seropositive Subjects Without a History of Genital Herpes”. Sexually Transmitted Diseases. 35 (3): 286—290. PMID 18157071. S2CID 20687438. doi:10.1097/OLQ.0b013e31815b0132.
- ^ Wald, Anna; Langenberg, A. G.; Link, K.; Izu, A. E.; Ashley, R.; Warren, T.; Tyring, S.; Douglas Jr, J. M.; Corey, L. (2001). „Effect of Condoms on Reducing the Transmission of Herpes Simplex Virus Type 2 from Men to Women”. JAMA. 285 (24): 3100—3106. PMID 11427138. doi:10.1001/jama.285.24.3100..
- ^ „FAQ: Herpes”. MIT Medical (na jeziku: engleski). Pristupljeno 2022-03-15.
- ^ Gupta, Rachna; Warren, Terri; Wald, Anna (2007). „Genital herpes”. The Lancet. 370 (9605): 2127—2137. PMID 18156035. S2CID 40916450. doi:10.1016/S0140-6736(07)61908-4.
- ^ Corey, Lawrence; Wald, Anna (2009). „Maternal and Neonatal Herpes Simplex Virus Infections”. New England Journal of Medicine. 361 (14): 1376—1385. PMC 2780322
 . PMID 19797284. doi:10.1056/NEJMra0807633..
. PMID 19797284. doi:10.1056/NEJMra0807633..
- ^ Usatine, Richard P.; Tinitigan, Rochelle (2010-11-01). „Nongenital herpes simplex virus”. American Family Physician. 82 (9): 1075—1082.
- ^ Kimberlin DW (2007). „Herpes simplex virus infections of the newborn”. Semin. Perinatol. 31 (1): 19—25..
- ^ „Can You Catch STDs From A Toilet Seat? | myLAB Box™”. myLAB Box™ - At Home Wellness Tests & At Home Health Testing (na jeziku: engleski). 2019-02-12. Pristupljeno 2022-03-15.
- ^ Regezi, Joseph A.; Sciubba, James J.; Jordan, Richard C. K., eds. (2012-01-01), "Chapter 1 - Vesiculobullous Diseases", Oral Pathology (Sixth Edition), St. Louis: W.B. Saunders, pp. 1–21, „Vesiculobullous Diseases”. Oral Pathology. 2012. str. 1—21. ISBN 9781455702626. doi:10.1016/B978-1-4557-0262-6.00001-X., Regezi, Joseph A.; Sciubba, James J.; Jordan, Richard C. K. (2012). Oral Pathology: Clinical Pathologic Correlations. Elsevier/Saunders. ISBN 978-1-4557-0262-6.,
- ^ Looker, Katharine J.; Elmes, Jocelyn A R.; Gottlieb, Sami L.; Schiffer, Joshua T.; Vickerman, Peter; Turner, Katherine M E.; Boily, Marie-Claude (2017). „Effect of HSV-2 infection on subsequent HIV acquisition: An updated systematic review and meta-analysis”. The Lancet Infectious Diseases. 17 (12): 1303—1316. PMC 5700807
 . PMID 28843576. doi:10.1016/S1473-3099(17)30405-X..
. PMID 28843576. doi:10.1016/S1473-3099(17)30405-X..
- ^ a b Mettenleiter, Thomas C.; Klupp, Barbara G.; Granzow, Harald (2006). „Herpesvirus assembly: A tale of two membranes”. Current Opinion in Microbiology. 9 (4): 423—429. PMID 16814597. doi:10.1016/j.mib.2006.06.013..
- ^ a b v g McGeoch, Duncan J.; Rixon, Frazer J.; Davison, Andrew J. (2006). „Topics in herpesvirus genomics and evolution”. Virus Research. 117 (1): 90—104. PMID 16490275. doi:10.1016/j.virusres.2006.01.002..
- ^ Rajčáni, Július; Andrea, Vojvodová; Ingeborg, Režuchová (2004). „Peculiarities of Herpes Simplex Virus (HSV) Transcription: An overview”. Virus Genes. 28 (3): 293—310. PMID 15266111. S2CID 19737920. doi:10.1023/B:VIRU.0000025777.62826.92.
- ^ a b Clarke, Richard W. (2015). „Forces and Structures of the Herpes Simplex Virus (HSV) Entry Mechanism”. ACS Infectious Diseases. 1 (9): 403—415. PMID 27617923. doi:10.1021/acsinfecdis.5b00059.
- ^ a b Subramanian, Ravi P.; Geraghty, Robert J. (2007). „Herpes simplex virus type 1 mediates fusion through a hemifusion intermediate by sequential activity of glycoproteins D, H, L, and B”. Proceedings of the National Academy of Sciences. 104 (8): 2903—2908. Bibcode:2007PNAS..104.2903S. PMC 1815279
 . PMID 17299053. doi:10.1073/pnas.0608374104
. PMID 17299053. doi:10.1073/pnas.0608374104  ..
..
- ^ Cardone, Giovanni; Winkler, Dennis C.; Trus, Benes L.; Cheng, Naiqian; Heuser, John E.; Newcomb, William W.; Brown, Jay C.; Steven, Alasdair C. (2007). „Visualization of the herpes simplex virus portal in situ by cryo-electron tomography”. Virology. 361 (2): 426—434. PMC 1930166
 . PMID 17188319. doi:10.1016/j.virol.2006.10.047..
. PMID 17188319. doi:10.1016/j.virol.2006.10.047..
- ^ Trus, Benes L.; Cheng, Naiqian; Newcomb, William W.; Homa, Fred L.; Brown, Jay C.; Steven, Alasdair C. (2004). „Structure and Polymorphism of the UL6 Portal Protein of Herpes Simplex Virus Type 1”. Journal of Virology. 78 (22): 12668—12671. PMC 525097
 . PMID 15507654. doi:10.1128/JVI.78.22.12668-12671.2004..
. PMID 15507654. doi:10.1128/JVI.78.22.12668-12671.2004..
- ^ Newcomb, William W.; Booy, Frank P.; Brown, Jay C. (2007). „Uncoating the Herpes Simplex Virus Genome”. Journal of Molecular Biology. 370 (4): 633—642. PMC 1975772
 . PMID 17540405. doi:10.1016/j.jmb.2007.05.023..
. PMID 17540405. doi:10.1016/j.jmb.2007.05.023..
- ^ Berger, Carolina; Xuereb, Suzanne; Johnson, David C.; Watanabe, Kathe S.; Kiem, Hans-Peter; Greenberg, Philip D.; Riddell, Stanley R. (2000). „Expression of Herpes Simplex Virus ICP47 and Human Cytomegalovirus US11 Prevents Recognition of Transgene Products by CD8+Cytotoxic T Lymphocytes”. Journal of Virology. 74 (10): 4465—4473. PMC 111967
 . PMID 10775582. doi:10.1128/jvi.74.10.4465-4473.2000..
. PMID 10775582. doi:10.1128/jvi.74.10.4465-4473.2000..
- ^ Roy, Subrata; Sukla, Soumi; De, Abhishek; Biswas, Subhajit (2022). „Non-cytopathic herpes simplex virus type-1 isolated from acyclovir-treated patients with recurrent infections”. Scientific Reports. 12 (1): 1345. Bibcode:2022NatSR..12.1345R. PMC 8789845
 . PMID 35079057. doi:10.1038/s41598-022-05188-w..
. PMID 35079057. doi:10.1038/s41598-022-05188-w..
- ^ Adang, Laura A.; Parsons, Christopher H.; Kedes, Dean H. (2006). „Asynchronous Progression through the Lytic Cascade and Variations in Intracellular Viral Loads Revealed by High-Throughput Single-Cell Analysis of Kaposi's Sarcoma-Associated Herpesvirus Infection”. Journal of Virology. 80 (20): 10073—10082. PMC 1617294
 . PMID 17005685. doi:10.1128/JVI.01156-06..
. PMID 17005685. doi:10.1128/JVI.01156-06..
- ^ a b Taddeo, Brunella; Roizman, Bernard (2006). „The Virion Host Shutoff Protein (U L 41) of Herpes Simplex Virus 1 is an Endoribonuclease with a Substrate Specificity Similar to That of RNase A”. Journal of Virology. 80 (18): 9341—9345. PMC 1563938
 . PMID 16940547. doi:10.1128/JVI.01008-06..
. PMID 16940547. doi:10.1128/JVI.01008-06..
- ^ Skepper, J. N.; Whiteley, A.; Browne, H.; Minson, A. (2001). „Herpes Simplex Virus Nucleocapsids Mature to Progeny Virions by an Envelopment → Deenvelopment → Reenvelopment Pathway”. Journal of Virology. 75 (12): 5697—5702. PMC 114284
 . PMID 11356979. doi:10.1128/JVI.75.12.5697-5702.2001..
. PMID 11356979. doi:10.1128/JVI.75.12.5697-5702.2001..
- ^ Granzow, Harald; Klupp, Barbara G.; Fuchs, Walter; Veits, Jutta; Osterrieder, Nikolaus; Mettenleiter, Thomas C. (2001). „Egress of Alphaherpesviruses: Comparative Ultrastructural Study”. Journal of Virology. 75 (8): 3675—3684. PMC 114859
 . PMID 11264357. doi:10.1128/JVI.75.8.3675-3684.2001..
. PMID 11264357. doi:10.1128/JVI.75.8.3675-3684.2001..
- ^ a b Pinnoji, Rajeswara C.; Bedadala, Gautam R.; George, Beena; Holland, Thomas C.; Hill, James M.; Hsia, Shao-Chung V. (2007). „Repressor element-1 silencing transcription factor/Neuronal restrictive silencer factor (REST/NRSF) can regulate HSV-1 immediate-early transcription via histone modification”. Virology Journal. 4: 56. PMC 1906746
 . PMID 17555596. doi:10.1186/1743-422X-4-56
. PMID 17555596. doi:10.1186/1743-422X-4-56  ..
..
- ^ Roizman, Bernard; Gu, Haidong; Mandel, Gail (2005). „The First 30 Minutes in the Life of a Virus: UnREST in the Nucleus”. Cell Cycle. 4 (8): 1019—1021. PMID 16082207. S2CID 46444480. doi:10.4161/cc.4.8.1902..
- ^ Davidson AJ (2007-08-16). "Comparative analysis of the genomes". Human Herpesviruses. Cambridge University Press. Arvin, Ann; Campadelli-Fiume, Gabriella; Mocarski, Edward; Moore, Patrick S.; Roizman, Bernard; Whitley, Richard; Yamanishi, Koichi (16. 8. 2007). Human Herpesviruses: Biology, Therapy, and Immunoprophylaxis. Cambridge University Press. ISBN 978-0-521-82714-0..
- ^ Slobedman, B.; Zhang, X.; Simmons, A. (1999). „Herpes Simplex Virus Genome Isomerization: Origins of Adjacent Long Segments in Concatemeric Viral DNA”. Journal of Virology. 73 (1): 810—813. PMC 103895
 . PMID 9847394. doi:10.1128/JVI.73.1.810-813.1999..
. PMID 9847394. doi:10.1128/JVI.73.1.810-813.1999..
- ^ a b Kolb, Aaron W.; Ané, Cécile; Brandt, Curtis R. (2013). „Using HSV-1 Genome Phylogenetics to Track Past Human Migrations”. PLOS ONE. 8 (10): e76267. Bibcode:2013PLoSO...876267K. PMC 3797750
 . PMID 24146849. doi:10.1371/journal.pone.0076267
. PMID 24146849. doi:10.1371/journal.pone.0076267  ..
..
- ^ a b Bowden, Rory; Sakaoka, Hiroshi; Ward, Ryk; Donnelly, Peter (2006). „Patterns of Eurasian HSV-1 molecular diversity and inferences of human migrations”. Infection, Genetics and Evolution. 6 (1): 63—74. PMID 16376841. doi:10.1016/j.meegid.2005.01.004..
- ^ Burrel, Sonia; Boutolleau, David; Ryu, Diane; Agut, Henri; Merkel, Kevin; Leendertz, Fabian H.; Calvignac-Spencer, Sébastien (2017). „Ancient Recombination Events between Human Herpes Simplex Viruses”. Molecular Biology and Evolution. 34 (7): 1713—1721. PMC 5455963
 . PMID 28369565. doi:10.1093/molbev/msx113..
. PMID 28369565. doi:10.1093/molbev/msx113..
- ^ a b Casto, Amanda M.; Roychoudhury, Pavitra; Xie, Hong; Selke, Stacy; Perchetti, Garrett A.; Wofford, Haley; Huang, Meei-Li; Verjans, Georges M G M.; Gottlieb, Geoffrey S.; Wald, Anna; Jerome, Keith R.; Koelle, David M.; Johnston, Christine; Greninger, Alexander L. (2019). „Large, Stable, Contemporary Interspecies Recombination Events in Circulating Human Herpes Simplex Viruses”. The Journal of Infectious Diseases. 221 (8): 1271—1279. PMC 7325804
 . PMID 31016321. doi:10.1093/infdis/jiz199..
. PMID 31016321. doi:10.1093/infdis/jiz199..
- ^ Hussin, Ainulkhir; Md Nor, Norefrina Shafinaz; Ibrahim, Nazlina (2013). „Phenotypic and genotypic characterization of induced acyclovir-resistant clinical isolates of herpes simplex virus type 1”. Antiviral Research. 100 (2): 306—313. PMID 24055837. doi:10.1016/j.antiviral.2013.09.008..
- ^ Norberg, Peter; Tyler, Shaun; Severini, Alberto; Whitley, Rich; Liljeqvist, Jan-Åke; Bergström, Tomas (2011). „A Genome-Wide Comparative Evolutionary Analysis of Herpes Simplex Virus Type 1 and Varicella Zoster Virus”. PLOS ONE. 6 (7): e22527. Bibcode:2011PLoSO...622527N. PMC 3143153
 . PMID 21799886. doi:10.1371/journal.pone.0022527
. PMID 21799886. doi:10.1371/journal.pone.0022527  ..
..
- ^ „STD Facts - Genital Herpes”. www.cdc.gov (na jeziku: engleski). 2022-01-18. Pristupljeno 2022-03-15.
- ^ Kimberlin, David W.; et al. (2011). „Oral Acyclovir Suppression and Neurodevelopment after Neonatal Herpes”. New England Journal of Medicine. 365 (14): 1284—1292. PMC 3250992
 . PMID 21991950. doi:10.1056/NEJMoa1003509..
. PMID 21991950. doi:10.1056/NEJMoa1003509..
- ^ Koelle, David M.; Corey, Lawrence (2008). „Herpes Simplex: Insights on Pathogenesis and Possible Vaccines”. Annual Review of Medicine. 59: 381—395. PMID 18186706. doi:10.1146/annurev.med.59.061606.095540.
- ^ Treml, Jakub; Gazdová, Markéta; Šmejkal, Karel; Šudomová, Miroslava; Kubatka, Peter; Hassan, Sherif T. S. (2020). „Natural Products-Derived Chemicals: Breaking Barriers to Novel Anti-HSV Drug Development”. Viruses. 12 (2): 154. PMC 7077281
 . PMID 32013134. doi:10.3390/v12020154
. PMID 32013134. doi:10.3390/v12020154  ..
..
- ^ Qiu, Min; Chen, Yu; Chu, Ying; Song, Siwei; Yang, Na; Gao, Jie; Wu, Zhiwei (2013). „Zinc ionophores pyrithione inhibits herpes simplex virus replication through interfering with proteasome function and NF-κB activation”. Antiviral Research. 100 (1): 44—53. PMID 23867132. doi:10.1016/j.antiviral.2013.07.001..
- ^ Michod, Richard E.; Bernstein, Harris; Nedelcu, Aurora M. (2008). „Adaptive value of sex in microbial pathogens”. Infection, Genetics and Evolution. 8 (3): 267—285. PMID 18295550. doi:10.1016/j.meegid.2008.01.002.
- ^ Das, Shishir K. (1982). „Multiplicity reactivation of alkylating agent damaged herpes simplex virus (Type I) in human cells”. Mutation Research Letters. 105 (1–2): 15—18. PMID 6289091. doi:10.1016/0165-7992(82)90201-9..
- ^ Hall, J. D.; Scherer, K. (1981). „Repair of psoralen-treated DNA by genetic recombination in human cells infected with herpes simplex virus”. Cancer Research. 41 (12 Pt 1): 5033—5038. PMID 6272987.
- ^ Coppey, J.; Sala-Trepat, M.; Lopez, B. (1989). „Multiplicity reactivation and mutagenesis of trimethylpsoralen-damaged herpes virus in normal and Fanconi's anaemia cells”. Mutagenesis. 4 (1): 67—71. PMID 2541311. doi:10.1093/mutage/4.1.67..
- ^ а б Selsky, C. A.; Henson, P.; Weichselbaum, R. R.; Little, J. B. (1979). „Defective reactivation of ultraviolet light-irradiated herpesvirus by a Bloom's syndrome fibroblast strain”. Cancer Research. 39 (9): 3392—3396. PMID 225021.
- ^ Valyi-Nagy, Tibor; Olson, Sandra J.; Valyi-Nagy, Klara; Montine, Thomas J.; Dermody, Terence S. (2000). „Herpes Simplex Virus Type 1 Latency in the Murine Nervous System is Associated with Oxidative Damage to Neurons”. Virology. 278 (2): 309—321. PMID 11118355. doi:10.1006/viro.2000.0678..
Литература
[uredi | uredi izvor]- Tronstein E, Johnston C, Huang ML, Selke S, Magaret A, Warren T,; et al. „Genital shedding of herpes simplex virus among symptomatic and asymptomatic persons with HSV-2 infection”. JAMA. 305 (14): 1441—9.. 2011.
- Ryder N, Jin F, McNulty AM, Grulich AE, Donovan B. „Increasing role of herpes simplex virus type 1 in first-episode anogenital herpes in heterosexual women and younger men who have sex with men, 1992–2006”. Sex Transm Infect. 85 (6): 416—9.. 2009.
- Bernstein DI, Bellamy AR, Hook EW 3rd, Levin MJ, Wald A, Ewell MG, „Epidemiology, clinical presentation, and antibody response to primary infection with herpes simplex virus type 1 and type 2 in young women”. Clin Infect Dis. 56 (3): 344—51.. 2013.
- Xu F, Sternberg MR, Kottiri BJ, McQuillan GM, Lee FK, Nahmias AJ,; et al. „Trends in herpes simplex virus type 1 and type 2 seroprevalence in the United States”. JAMA. 296 (8): 964—73.. 2006.
- Bradley H, Markowitz LE, Gibson T, McQuillan GM. „Seroprevalence of herpes simplex virus types 1 and 2—United States, 1999–2010”. The Journal of Infectious Diseases. 209 (3): 325—33.. 2014.
- Dickson N, Righarts A, van Roode T, Paul C, Taylor J, Cunningham AL. „HSV-2 incidence by sex over four age periods to age 38 in a birth cohort”. Sex Transm Infect. 90 (3): 243—5.. 2014.
- Dukers NH, Bruisten SM, van den Hoek JA, de Wit JB, van Doornum GJ, Coutinho RA. „Strong decline in herpes simplex virus antibodies over time among young homosexual men is associated with changing sexual behavior”. Am J Epidemiol. 152 (7): 666—73.. 2000
 | Molimo Vas, obratite pažnju na važno upozorenje u vezi sa temama iz oblasti medicine (zdravlja). |
