Litijum nikl mangan kobaltni oksidi
Litijum nikl mangan kobaltni oksidi (skraćeno NMC, Li-NMC, LNMC, ili NCM) su mešani metalni oksidi litijuma, nikla, mangana i kobalta sa opštom formulom LiNixMnyCo1-x-yO2. Ovi materijali se obično koriste u litijum-jonskim baterijama za mobilne uređaje i električna vozila, delujući kao pozitivno naelektrisana katoda.

Postoji poseban interes za optimizaciju NMC-a za aplikacije u električnim vozilima zbog velike gustine energije materijala i radnog napona. Smanjenje sadržaja kobalta u NMC-u je takođe jedan od ciljeva, zbog etičkih problema sa iskopavanjem kobalta i visoke cene metala.[1] Štaviše, povećan sadržaj nikla obezbeđuje veći kapacitet u okviru stabilnog radnog perioda.[2]
Struktura
[уреди | уреди извор]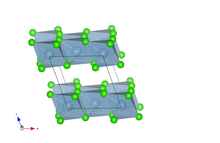
NMC materijali imaju slojevitu strukturu sličnu individualnom jedinjenju metalnog oksida litijum kobalt oksidu (LiCoO2).[3] Litijumski joni se interkaliraju između slojeva nakon pražnjenja, ostajući između ravni rešetke sve dok se baterija ne napune, u kom trenutku se litijum deinterkalira i kreće ka anodi.[4]
Tačke u faznom dijagramu čvrstog rastvora između krajnjih članova LiCoO2, LiMnO2, i LiNiO2 predstavljaju stehiometrijske NMC katode.[5] Tri broja odmah iza NMC skraćenice označavaju relativnu stehiometriju tri definišuća metala. Na primer, molarni sastav NMC od 33% nikla, 33% mangana i 33% kobalta bio bi skraćene označen sa NMC111 (takođe NMC333 ili NCM333) i imao bi hemijsku formulu LiNi 0.33Mn0.33Co 0.33O2. Kompozicija od 50% nikla, 30% mangana i 20% kobalta bi se nazvala NMC532 (ili NCM523) i imala bi formulu LiNi0.5Mn0.3Co0.2O2. Druge uobičajene kompozicije su NMC622 i NMC811.[4] Opšti sadržaj litijuma obično ostaje oko 1:1 sa ukupnim sadržajem prelaznog metala, pri čemu komercijalni NMC uzorci obično sadrže manje od 5% viška litijuma.[6][7]
Za NMC111, idealna oksidaciona stanja za raspodelu naelektrisanja su Mn4+, Co3+, i Ni2+. Kobalt i nikl se delimično oksiduju do Co4+ i Ni4+ tokom punjenja, dok Mn4+ ostaje neaktivan i održava strukturnu stabilnost.[8] Modifikovanje stehiometrije prelaznog metala menja svojstva materijala, obezbeđujući način za prilagođavanje performansi katode.[3] Najvažnije, povećanje sadržaja nikla u NMC-u povećava njegov početni kapacitet pražnjenja, ali smanjuje njegovu termičku stabilnost i zadržavanje kapaciteta. Povećanje sadržaja kobalta dolazi po cenu zamene nikla više energije ili hemijski stabilnog mangana, a istovremeno je skupo. Kiseonik može da se generiše iz metalnog oksida na 300 °C kada se potpuno isprazni, degradirajući rešetku. Veći sadržaj nikla smanjuje temperaturu stvaranja kiseonika dok takođe povećava proizvodnju toplote tokom rada baterije.[3] Mešanje katjona, proces u kome Li+ zamenjuje Ni2+ jone u rešetki, takođe se povećava kako se povećava koncentracija nikla.[9] Slična veličina Ni2+ (0.69 Å) i Li+ (0.76 Å) olakšava mešanje katjona. Izmeštanje nikla iz slojevite strukture može da promeni karakteristike vezivanja materijala, formirajući nepoželjne faze i snižavajući njegov kapacitet.[10][11]
Reference
[уреди | уреди извор]- ^ Warner, John T. (2019-01-01), Warner, John T., ур., „Chapter 8 - The materials”, Lithium-Ion Battery Chemistries (на језику: енглески), Elsevier, стр. 171—217, ISBN 978-0-12-814778-8, S2CID 239383589, doi:10.1016/b978-0-12-814778-8.00008-9, Приступљено 2023-04-02
- ^ Oswald, Stefan; Gasteiger, Hubert A. (2023-03-01). „The Structural Stability Limit of Layered Lithium Transition Metal Oxides Due to Oxygen Release at High State of Charge and Its Dependence on the Nickel Content”. Journal of the Electrochemical Society. 170 (3): 030506. Bibcode:2023JElS..170c0506O. ISSN 0013-4651. S2CID 258406065. doi:10.1149/1945-7111/acbf80
 .
.
- ^ а б в Manthiram, Arumugam; Knight, James C.; Myung, Seung-Taek; Oh, Seung-Min; Sun, Yang-Kook (2015-10-07). „Nickel-Rich and Lithium-Rich Layered Oxide Cathodes: Progress and Perspectives”. Advanced Energy Materials (на језику: енглески). 6 (1): 1501010. S2CID 97342610. doi:10.1002/aenm.201501010.
- ^ а б Warner, John T. (2019-01-01), Warner, John T., ур., „Chapter 5 - The Cathodes”, Lithium-Ion Battery Chemistries (на језику: енглески), Elsevier, стр. 99—114, ISBN 978-0-12-814778-8, S2CID 239420965, doi:10.1016/b978-0-12-814778-8.00005-3, Приступљено 2023-04-02
- ^ Houchins, Gregory; Viswanathan, Venkatasubramanian (2020-01-01). „Towards Ultra Low Cobalt Cathodes: A High Fidelity Computational Phase Search of Layered Li-Ni-Mn-Co Oxides”. Journal of the Electrochemical Society. 167 (7): 070506. Bibcode:2020JElS..167g0506H. ISSN 0013-4651. S2CID 201303669. arXiv:1805.08171
 . doi:10.1149/2.0062007JES.
. doi:10.1149/2.0062007JES.
- ^ Julien, Christian; Mauger, Alain; Zaghib, Karim; Groult, Henri (2016-07-19). „Optimization of Layered Cathode Materials for Lithium-Ion Batteries”. Materials (на језику: енглески). 9 (7): 595. Bibcode:2016Mate....9..595J. ISSN 1996-1944. PMC 5456936
 . PMID 28773717. doi:10.3390/ma9070595
. PMID 28773717. doi:10.3390/ma9070595  .
.
- ^ Li, Xuemin; Colclasure, Andrew M.; Finegan, Donal P.; Ren, Dongsheng; Shi, Ying; Feng, Xuning; Cao, Lei; Yang, Yuan; Smith, Kandler (2019-02-20). „Degradation mechanisms of high capacity 18650 cells containing Si-graphite anode and nickel-rich NMC cathode”. Electrochimica Acta (на језику: енглески). 297: 1109—1120. OSTI 1491439. S2CID 104299816. doi:10.1016/j.electacta.2018.11.194
 .
.
- ^ Yoon, Won-Sub; Grey, Clare P.; Balasubramanian, Mahalingam; Yang, Xiao-Qing; Fischer, Daniel A.; McBreen, James (2004). „Combined NMR and XAS Study on Local Environments and Electronic Structures of Electrochemically Li-Ion Deintercalated Li[sub 1−x]Co[sub 1/3]Ni[sub 1/3]Mn[sub 1/3]O[sub 2] Electrode System”. Electrochemical and Solid-State Letters (на језику: енглески). 7 (3): A53. doi:10.1149/1.1643592.
- ^ Zhang, Xiaoyu; Jiang, W. J.; Mauger, A.; Qilu; Gendron, F.; Julien, C. M. (2010-03-01). „Minimization of the cation mixing in Li1+x(NMC)1−xO2 as cathode material”. Journal of Power Sources (на језику: енглески). 195 (5): 1292—1301. Bibcode:2010JPS...195.1292Z. ISSN 0378-7753. doi:10.1016/j.jpowsour.2009.09.029.
- ^ Xu, Bo; Fell, Christopher R.; Chi, Miaofang; Meng, Ying Shirley (2011). „Identifying surface structural changes in layered Li-excess nickel manganese oxides in high voltage lithium ion batteries: A joint experimental and theoretical study”. Energy & Environmental Science (на језику: енглески). 4 (6): 2223. ISSN 1754-5692. doi:10.1039/c1ee01131f.
- ^ Zhao, Enyue; Fang, Lincan; Chen, Minmin; Chen, Dongfeng; Huang, Qingzhen; Hu, Zhongbo; Yan, Qing-bo; Wu, Meimei; Xiao, Xiaoling (2017-01-24). „New insight into Li/Ni disorder in layered cathode materials for lithium ion batteries: a joint study of neutron diffraction, electrochemical kinetic analysis and first-principles calculations”. Journal of Materials Chemistry A (на језику: енглески). 5 (4): 1679—1686. ISSN 2050-7496. doi:10.1039/C6TA08448F.
Literatura
[уреди | уреди извор]- Giles Parkinson (2019-08-12). „Alinta sees sub 5-year payback for unsubsidised big battery at Newman”. RenewEconomy (на језику: енглески).
- „Energy Storage Solution Provider” (PDF) (на језику: енглески). Архивирано из оригинала (PDF) 2020-02-23. г. Приступљено 2020-03-01.
