Стаклена електрода
Стаклена електрода је тип јон-селективне електроде направљене од доповане стаклене мембране која је осетљива на специфични јон. Најчешћа примена јон-селективних стаклених електрода је мерење pH вредности раствора, односно, активитета хидронијум јона у њему. Стаклене електроде играју важну улогу у опреми за хемијску анализу и физичко-хемијска истраживања. Напон који стаклена електрода генерише у поређењу са неком референтном вредношћу, пропорционалан је промени активитета одређеног типа јона.
Историјат[уреди | уреди извор]
Прва проучавања стаклених електрода довеле су до закључка да различити типови стакла различито реагују на промену киселости раствора због ефекта који јони алкалних метала убачених у стакло имају.
Године 1906, М. Кремер, отац Ерике Кремер, утврдио је да је електрични потенцијал који настаје између течности на супротним крајевима мембране пропорционалан концентрацији хидронијум јона у њима.[1]
Године 1909, С. П. Л. Соренсен је увео концепт pH вредности, а исте године Ф. Хабер и З. Клеменсиевиц обавестили су Друштво хемије у Карлсруеу о својим истраживањима стаклене електроде.[2] [3] Године 1922. В. С. Хјугс је показао да су алкално-силикатне стаклене електроде сличне водониковој електроди, реверзибилне у односу на хидронијум јон.[4]
Године 1925. Филис Маргарет Туки Кериџ је развила прву стаклену електроду за анализу узорака крви. Она је истакла неке од проблема ове опреме, као што је висока отпорност стакла (50–150 MΩ).[5] Током свог доктората, Кериџ је развила минијатурну стаклену електроду. Њен дизајн је био претходник многих стаклених електрода које се данас користе.[6][7]
Примене[уреди | уреди извор]
Стаклене електроде се најчешће користе за мерење киселости. Постоје и специјализоване стаклене електроде за мерење концентрација катјона литијума, натријума, амонијака и других. Стаклене електроде се користе у широком распону примена, од хемијских истраживања, до индустријске контроле провере квалитета при производњи хране и козметике. Честа је и употреба у праћењу киселости земљишта или природних вода.
Врсте[уреди | уреди извор]
Готово све комерцијално доступне електроде реагују на јоне са наелектрисањем +1, као што у катјони водоника, натријума или злата. Постоје и специјализоване стаклене електроде које реагују на јоне са наелектрисањем +2, мада су оне ређе.
Постоје два главна система формирања стакла за овакве електроде: силикатни матрикс заснован на молекуларној мрежи силицијум-диоксида са примесама оксида метала, најчешће натријума, калијума или литијума, и халкогенидни матрикс, заснован на мрежи од AsS, AsSe и AsTe.
Сметње при мерењу[уреди | уреди извор]

Због начина рада ове електроде заснован на размени јона, постоји могућност да неки метални јони утичу на мерења и да поремете линеарну везу активитета хидронијум јона са електродни потенцијалом.
Ефекти ових сметњи су приметни у растворима са високом концентрацијом металних јона. Јачина ефекта се може израчунати Николски-Ајзенмановом једначином, која је проширење Нернстове једначине. Она је:
где је Е електромоторна сила, Е0 стандардни електродни потенцијал, z јонска валенца укључујући знак, а активност, i јон који се мере, j јони који уносе сметњу и kij коефицијент селективности. Што је мањи коефицијент селективности, то је мање сметње од стране ј.
Распон pH стаклене електроде[уреди | уреди извор]

Распон pH при константној концентрацији може се поделити у 3 дела:
- Део где се мерења слажу са електродном једначином, где потенцијал зависи линеарно од pH. Ова једначина за стаклену електроде је:
где је F Фарадејева константа.
- Део у коме су честе алкалне грешке - при ниској концентрацији водоникових јона (високе pH вредности), неки јони алкалних метала (као што су литијум, натријум и калијум) се региструју као водоникови, што доводи до показивања ниже вредности од реалне. У овој ситуацији зависност потенцијала од киселости постаје непредвидива и нелинеарна.
Ефекат је обично уочљив при вредности pH > 12, и концентрацији јона литијума или натријума од 0,1 молова по литру или више. Калијумови јони обично изазивају мање грешке од натријумових и литијумових јона.
- Део у коме су честе киселе грешке - при веома високој концентрацији водоникових јона (веома ниске вредности pH), зависност електроде од pH постаје нелинеарна, а утицај анјона у раствору постаје приметан. Ови ефекти обично постају уочљиви при вредности pH < -1, а проузроковани су засићеношћу стаклене мембране.
Постоје специјализоване електроде за рад у екстремним опсезима pH.
Конструкција[уреди | уреди извор]
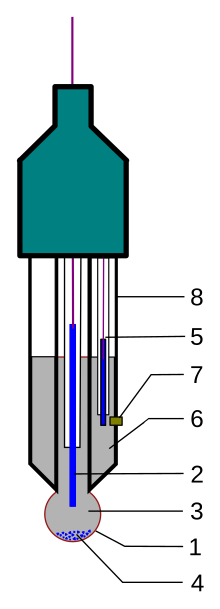
Типична модерна pH електрода је комбинована електрода, која садржи и стаклену и референтну електроду у једном телу. Комбинована електрода се састоји од следећих делова (види цртеж):
- сензорски део електроде, мехур направљена од специфичног стакленог матрикса
- унутрашња електрода, обично среброхлоридна или каломелна електрода
- унутрашњи раствор, обично неутрални пуфер раствор од 0,1 mol/l KCl.
- када се користи електрода са сребро-хлоридом, мала количина AgCl се исталожи на дну мехура.
- референтна електрода, обично исте врсте као и унутрашња (2).
- референтан унутрашњи раствор, обично 0,1М KCl.
- фрита од керамике или капилара са азбестним или кварцним влакнима.
- тело електроде, направљено од изолационог стакла или пластике.
Дно стаклене електроде се завршава танким округлим мехуром. Најбоље је посматрати ову електроду као цев унутар цеви. Унутрашња цев садржи непроменљив раствор HCl од 1 × 10 - 7 М. Унутар унутрашње цеви налази се и катодни крај референтне електроде. Анодни крај се омотава око спољне стране унутрашње цеви и завршава се истом врстом референтне електроде као што је она са унутрашње стране унутрашње цеви. Напуњен је референтним раствором калијум-хлорида и има контакт са раствором на спољашњој страни стаклене електроде преко фрите који служи као слани мост .
Концепт рада[уреди | уреди извор]
Стаклена електрода ради на принципу галванске ћелије, који генерише напон при разлици активитета јона унутар и ван раствора. Насупрот ономе што су старији извори наводили, не долази до трансфера јона између испитиваног раствора, и унутрашњих течности електроде.[8] Због посебне структуре стакленог матрикса, хидронијум јони испитиваног раствора попуњавају поре хидратисаног спољашњег слоја стакла. Овим се спољашност стакла позитивно наелектрише. Ово доводи до стварања мембранског потенцијала између унутрашњости и спољашности мехура, који се преноси преко слободних јона у стаклу, најчешће .
Складиштење[уреди | уреди извор]
Када није у употреби, стаклена електрода би требало да се чува у једномоларном раствору јона који се налази у њој (уобичајено калијум-хлорида). Ово је неопходно, јер се хидратисана стаклена мембрана суши, а без ње, електрода нема способност прецизног мерења.
Референце[уреди | уреди извор]
- ^ Grundner, Friedrich (1882). Untersuchungen über die Querflächen-Ermittlung der Holzbestände; ein Beitrag zur Lehre von der Bestands-Massenaufnahme. Berlin: [J. Springer].
- ^ First publication — The Journal of Physical Chemistry by W. Ostwald and J. H. van 't Hoff) — 1909).
- ^ F. Haber und Z. Klemensiewicz. Über elektrische Phasengrenzkräft. Zeitschrift für Physikalische Chemie. Leipzig. 1909 (Vorgetragen in der Sitzung der Karlsruher chemischen Gesellschaft am 28. Jan. 1909), 67, 385.
- ^ W. S. Hughes, J. Am. Chem. Soc., 44, 2860. 1922; J. Chem. Soc. Lond., 491, 2860. 1928
- ^ Yartsev, Alex. „History of the Glass Electrode”. Deranged Physiology. Приступљено 26. 6. 2016.
- ^ Blake-Coleman, Barrie. „Phyllis Kerridge And The Miniature Ph Electrode”. Inventricity. Приступљено 26. 6. 2016.
- ^ Kerridge, Phyllis Margaret Tookey (1925). „The Use of the Glass Electrode in Biochemistry” (PDF). Biochemical Journal. 19 (4): 611—617. PMC 1259230
 . PMID 16743549. doi:10.1042/bj0190611. Приступљено 23. 6. 2016.
. PMID 16743549. doi:10.1042/bj0190611. Приступљено 23. 6. 2016.
- ^ Verbić; Pešić; Obradović; Cvijetić (2018). Praktikum sa zbirkom zadataka iz instrumentalne analitičke hemije - optičke i elektroanalitičke metode. Beograd: Hemijski fakultet univerziteta u Beogradu.
Литература[уреди | уреди извор]
- Bates, Roger G. (1954). „Chapter 10, Glass Electrodes”. Determination of pH. Wiley.
- Bates, Roger G. (1973). Determination of pH: theory and practice. Wiley.

![{\displaystyle E=E^{0}+{\frac {RT}{z_{i}F}}\ln \left[a_{i}+\sum _{j}\left(k_{ij}a_{j}^{z_{i}/z_{j}}\right)\right]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/173a9dcfbed1bd62faa8126ce218e846c1aabc03)

