Fibronektin
Fibronektin je glikoprotein ekstracelularnog matriksa visoke molekulske težine koji se vezuje za proteinske receptore integrine koji premoštavaju membrane.[1] Pored integrina, fibronektin se isto vezuje za komponente ekstracelularnog matriksa kao što su kolagen[2], fibrin i heparan sulfate proteoglukani (e.g. sindekani). Fibronektin protein je kodiran jednim genom, ali alternativno splajsovanje njegove pre-iRNK dovodi do kreiranja nekoliko proteinskih izoformi.
Dve vrste fibronektina su prisutne u kičmenjacima:[1]
- rastvorljivi plazma fibronektin (ranije poznat kao hladno-nerastvorljivi globulin, ili Clg) je jedna od glavnih proteinskih komponenti krvne plazme (300 μg/ml). On se još proizvodi u jetri i u hepatocitima.
- nerastvorljivi ćelijski fibronektin je značajna komponenta ekstracelularnog matriksa. Ona se izlučuje is različitih ćelija, a primarno iz fibroblasta, kao rastvorljivi dimer, i potom se sakuplja kao nerastvorni ekstracelularni matriks u kompleksnom ćelijski-posredovanim procesu.
Fibronektin igra važnu ulogu u ćelijskoj adheziji, migraciji, i diferencijaciji. On je važan u procesima zarastanja rana i embrionskog razvoja.[1] Nepravilno ekspresija, degeneracija, i organizacija fibronektin gena su bili povezani sa brojnim patološkim okolnostima, uključujući rak i fibrozu.[3]
Struktura
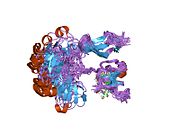
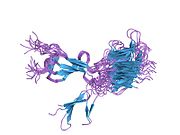
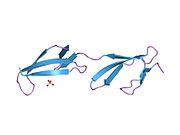
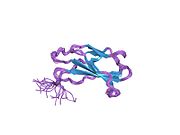
[уреди | уреди извор]Fibronektin postoji kao dimer, koji se sastoji od dva skoro identična monomera povezanih parom disulfidnih veza.[1][4] Svaki fibronektinski monomer ima molekulsku težinu od 230-250 kDa, i sadrži tri tipa proteinskih modula: tip I, II, i III. Sva tri modula se sastoje of dve antiparalelne β-ploče; međutim, tip I i tip II su stabilizovani intra-lančanim disulfidnim mostovima, dok tip III modul ne sadrži disulfidne mostove. Odsustvo disulfidnih intra-lanaca u tipu III modulima dozvoljava im da se delimično razviju pod uticajem sile.[5]
Tri regiona promenljivog RNK sjedinjavanja se javljaju duž fibronektin monomera.[4] Jedan ili oba "ekstra" tipa III modula (EIIIA i EIIIB) mogu biti prisutna u ćelijskom fibronektinu, ali oni nisu nikad prisutni u fibronektinu iz krvne plazme. Promenljivi V-region postoji između III14-15 (14tog i 15tog tipa III modula). V-region strukture je različit of tipa I, II, i III modula, a njegovo prisustvo i dužina mogu varirati. V-region sadrži vezujuće mesto za α4β1 integrine. Ono je prisutno u većini ćelijskih fibronektina, ali samo jedna of dve pod-jedinice fibronektin dimera plazme sadrži V-region sekvencu.
Moduli su aranžirani u nekoliko funkcionalnih i protein-vezujućih domena duž fibronektin monomera. Postoje četiri fibronektin-vezujuća domena, što dozvoljava fibronektinu da se asocira sa drugim fibronektin molekulima.[4] Jedan of tih fibronektin-vezujućih domena, I1-5, se naziva "saborni domen", i on je neophodan za inicijaciju fibronektin matriks konstrukcije. Moduli III9-10 su "ćelijski vezujući domeni" fibronektina. RGD sekvenca (Arg-Gly-Asp) je locirana III10 i one je mesto ćelijskog pripajanja putem αVβ1 i αVβ3 integrina na ćelijskoj površini. "Mesto sjedinjavanja" je na III9 i ima ulogu u modulaciji fibronektinove asocijacije sa αVβ1 integrinima.[6] Fibronektin isto sadrži domene za fibrin-vezivanje (I1-5, I10-12), kolagen-vezivanje (I6-9), fibulin-1-vezivanje (III13-14), i sindekan-vezivanje (III12-14).[4]

Funkcija
[уреди | уреди извор]Fibronektin ima brojne funkcije koje osiguravaju normalno funkcionisanje kičmenjačkih organizama.[1] On je posreduje ćelijsku adheziju, rast, migraciju i diferencijaciju. Ćelijski fibronektin je konstruisan u ekstra-ćelijskom matriksu, jednoj nerastvornoj mreži koja odvaja i podržava organe i tkiva organizma.
Fibronektin igra presudnu ulogu u lečenju rana.[7] Zajedno sa fibrinom, plazma fibronektin se deponuje na mestu povrede, formirajući krvnu grudvu koja zaustavlja krvarenje i zaštićuje potporno tkivo. Dok se popravka tkiva nastavlja, fibroblasti i makrofage počinju da preuređuju površinu, degradirajući proteine koji formiraju privremeni matriks krvne grudve i zamenjujući ih sa matriksom koji više podseća normalnom okružujećem tkivu. Fibroblasti izlučuju proteaze, uključujući matriks metaloproteaze, koje svaruju fibronektin is plazme, i potom fibroblasti izlučuju ćelijski fibronektin i sklapaju ga u nerastvorni matriks. Fragmentacija fibronektina proteazama je bila predložena da promoviše kontrakciju rane, što je kritičan korak u zarastanju rane. Fragmentacija fibronektina isto tako izlaže njegov V-region, koji sadrži mesto za vezivanje α4β1 integrina. Ti fragmenti fibronektina se veruje da uvećavaju vezivanje ćelija koje izražavaju α4β1 integrin, što im dozvoljava da se priljube i kontraktuju okružujući matriks.
Fibronektin je neophodan za embriogenezu, i inaktiviranje gena fibronektina uzrokuje ranu embrionsku letalnost.[8] Fibronektin je važan u upravljanju ćelijskom adhezijom i migracijom u toku embrionskog razvoja. U razvoju sisara, odsustvo fibronektina dovodi do defekata mezoderma, i nervne cevi, i vaskularnog razvoja.
Fibronektin se isto nalazi u normalnoj ljudskog pljuvački, što pomaže sprečavanju kolonizacije usne šupljine i grla potencijalno patogenim bakterijama.[9]
Matriks konstrukcija
[уреди | уреди извор]Ćelijski fibronektin formira nerastvorni fibrilarni matriks u kompleksnom ćelijski-posedovanom procesu.[10] Formiranje fibronektin matriksa počinje kad se rastvorljivi, kompaktni fibronektin dimeri izluče is ćelija, obično fibroblasta. Ti rastvorljivi dimeri se vežu za α5β1 integrin receptore na ćelijskoj površini i pomažu u grupisanju integrina. Lokalna koncentracija integrin-vezanog fibronektina se povećava, dozvoljavajući vezanim fibronektin molekulima da lakše uzajamno deluju. U daljem progresu formiranja fibronektina, rastvorljivi filamenti se pretvaraju u veće nerastvorne filamente koji sačinjavaju ekstra ćelijski matriks.
Promena fibronektina od rastvorne u nerastvorne filamente se odvija kad su prikrivena fibronektin-vezujuća mesta izložena duž vezanih fibronektin molekula. Veruje se da ćelije rastežu fibronektin povlačenjem njihovih fibronektin-vezanih integrin receptorima. Ta sila delimično razvija fibronektin ligand, otkrivajući skrivena fibronektin-vezujuća mesta i dozvoljavajući obližnjim fibronektin molekulima da se vežu. Ta fibronektin-fibronektin interakcija omogućava rastvorljivom, ćelijski-asociranim filamentima da se granaju i stabilizuju u nerastvorni fibronektin matriks.
Uloga u raku
[уреди | уреди извор]Nekoliko morfoloških promena primećenih u tumorima i tumor-izvedenim ćelijskim linijama je pripisano smanjenoj fibronektin ekspresiji, povećanoj fibronektin degradaciji, i smanjenoj ekspresiji fibronektin-vezujućeg receptora, kao što su α5β1 integrini.[11] Fibronektin je impliciran u razvoju karcinoma.[12] U karcinomu plućima, fibronektin ekspresija je povećana, posebno u plućnom karcinomu ne-malih ćelija.
Interakcije
[уреди | уреди извор]Pokazano je da fibronektin stupa u interakcije sa kolagenom, tip VII, alfa 1,[13][14] TRIB3,[15] lipoproteinom (a),[16] Tenascin C,[17] CD44[18] i IGFBP3.[19][20]
Vidi još
[уреди | уреди извор]Reference
[уреди | уреди извор]- ^ а б в г д Pankov R, Yamada KM (2002). „Fibronectin at a glance”. Journal of cell science. 115 (Pt 20): 3861—3. PMID 12244123. doi:10.1242/jcs.00059.
- ^ Donald Voet; Judith G. Voet (2005). Biochemistry (3 изд.). Wiley. стр. 233—240. ISBN 9780471193500.
- ^ Williams CM, Engler AJ, Slone RD, Galante LL, Schwarzbauer JE (2008). „Fibronectin expression modulates mammary epithelial cell proliferation during acinar differentiation”. Cancer research. 68 (9): 3185—92. PMC 2748963
 . PMID 18451144. doi:10.1158/0008-5472.CAN-07-2673.
. PMID 18451144. doi:10.1158/0008-5472.CAN-07-2673.
- ^ а б в г Mao Y, Schwarzbauer JE (2005). „Fibronectin fibrillogenesis, a cell-mediated matrix assembly process”. Matrix biology : journal of the International Society for Matrix Biology. 24 (6): 389—99. PMID 16061370. doi:10.1016/j.matbio.2005.06.008.
- ^ Erickson, H. P. (2002). „Stretching fibronectin”. Journal of muscle research and cell motility. 23 (5-6): 575—80. PMID 12785106. doi:10.1023/A:1023427026818.
- ^ Sechler JL, Corbett SA, Schwarzbauer JE (1997). „Modulatory roles for integrin activation and the synergy site of fibronectin during matrix assembly”. Molecular biology of the cell. 8 (12): 2563—73. PMC 25728
 . PMID 9398676.
. PMID 9398676.
- ^ Valenick LV, Hsia HC, Schwarzbauer JE (2005). „Fibronectin fragmentation promotes alpha4beta1 integrin-mediated contraction of a fibrin-fibronectin provisional matrix”. Experimental cell research. 309 (1): 48—55. PMID 15992798. doi:10.1016/j.yexcr.2005.05.024.
- ^ George EL, Georges-Labouesse EN, Patel-King RS, Rayburn H, Hynes RO (1993). „Defects in mesoderm, neural tube and vascular development in mouse embryos lacking fibronectin”. Development (Cambridge, England). 119 (4): 1079—91. PMID 8306876.
- ^ Hasty DL, Simpson WA (1987). „Effects of fibronectin and other salivary macromolecules on the adherence of Escherichia coli to buccal epithelial cells”. Infection and immunity. 55 (9): 2103—9. PMC 260663
 . PMID 3305363. Архивирано из оригинала 08. 03. 2009. г. Приступљено 13. 03. 2010.
. PMID 3305363. Архивирано из оригинала 08. 03. 2009. г. Приступљено 13. 03. 2010.
- ^ Wierzbicka-Patynowski I, Schwarzbauer JE (2003). „The ins and outs of fibronectin matrix assembly”. Journal of cell science. 116 (Pt 16): 3269—76. PMID 12857786. doi:10.1242/jcs.00670.
- ^ Hynes, Richard O. (1990). Fibronectins. Berlin: Springer-Verlag. ISBN 978-0-387-97050-9.
- ^ Han S, Khuri FR, Roman J (2006). „Fibronectin stimulates non-small cell lung carcinoma cell growth through activation of Akt/mammalian target of rapamycin/S6 kinase and inactivation of LKB1/AMP-activated protein kinase signal pathways”. Cancer research. 66 (1): 315—23. PMID 16397245. doi:10.1158/0008-5472.CAN-05-2367.
- ^ Lapiere JC, Chen JD, Iwasaki T, Hu L, Uitto J, Woodley DT (1994). „Type VII collagen specifically binds fibronectin via a unique subdomain within the collagenous triple helix”. J. Invest. Dermatol. UNITED STATES. 103 (5): 637—41. ISSN 0022-202X. PMID 7963647. doi:10.1111/1523-1747.ep12398270.
- ^ Chen M, Marinkovich MP, Veis A, Cai X, Rao CN, O'Toole EA, Woodley DT (1997). „Interactions of the amino-terminal noncollagenous (NC1) domain of type VII collagen with extracellular matrix components. A potential role in epidermal-dermal adherence in human skin”. J. Biol. Chem. UNITED STATES. 272 (23): 14516—22. ISSN 0021-9258. PMID 9169408. doi:10.1074/jbc.272.23.14516.
- ^ Zhou, Ying; Lu, Li; et al. (2008). „E3 ubiquitin ligase SIAH1 mediates ubiquitination and degradation of TRB3”. Cell. Signal. England. 20 (5): 942—8. ISSN 0898-6568. PMID 18276110. doi:10.1016/j.cellsig.2008.01.010.
- ^ Salonen, E M; Jauhiainen, M.; et al. (1989). „Lipoprotein(a) binds to fibronectin and has serine proteinase activity capable of cleaving it”. EMBO J. ENGLAND. 8 (13): 4035—40. ISSN 0261-4189. PMC 401578
 . PMID 2531657.
. PMID 2531657.
- ^ Chung, C Y; Zardi, L.; Erickson H P (1995). „Binding of tenascin-C to soluble fibronectin and matrix fibrils”. J. Biol. Chem. UNITED STATES. 270 (48): 29012—7. ISSN 0021-9258. PMID 7499434. doi:10.1074/jbc.270.48.29012.
- ^ Jalkanen, S; Jalkanen, M. (1992). „Lymphocyte CD44 binds the COOH-terminal heparin-binding domain of fibronectin”. J. Cell Biol. UNITED STATES. 116 (3): 817—25. ISSN 0021-9525. PMC 2289325
 . PMID 1730778. doi:10.1083/jcb.116.3.817.
. PMID 1730778. doi:10.1083/jcb.116.3.817.
- ^ Martin, J A; Miller B A; et al. (2002). „Co-localization of insulin-like growth factor binding protein 3 and fibronectin in human articular cartilage”. Osteoarthr. Cartil. England. 10 (7): 556—63. ISSN 1063-4584. PMID 12127836. doi:10.1053/joca.2002.0791.
- ^ Gui, Y; Murphy L J (2001). „Insulin-like growth factor (IGF)-binding protein-3 (IGFBP-3) binds to fibronectin (FN): demonstration of IGF-I/IGFBP-3/fn ternary complexes in human plasma”. J. Clin. Endocrinol. Metab. United States. 86 (5): 2104—10. ISSN 0021-972X. PMID 11344214. doi:10.1210/jc.86.5.2104.
Literatura
[уреди | уреди извор]Dodatni izvori
[уреди | уреди извор]- ffrench-Constant C (1996). „Alternative splicing of fibronectin--many different proteins but few different functions.”. Exp. Cell Res. 221 (2): 261—71. PMID 7493623. doi:10.1006/excr.1995.1374.
- Snásel J, Pichová I (1997). „The cleavage of host cell proteins by HIV-1 protease.”. Folia Biol. (Praha). 42 (5): 227—30. PMID 8997639. doi:10.1007/BF02818986.
- Schor SL, Schor AM (2003). „Phenotypic and genetic alterations in mammary stroma: implications for tumour progression.”. Breast Cancer Res. 3 (6): 373—9. PMC 138703
 . PMID 11737888. doi:10.1186/bcr325.
. PMID 11737888. doi:10.1186/bcr325. - Przybysz M, Katnik-Prastowska I (2002). „[Multifunction of fibronectin]” [Multifunction of fibronectin]. Postȩpy higieny i medycyny doświadczalnej (на језику: Polish). 55 (5): 699—713. PMID 11795204.
- Rameshwar, P.; Oh, H. S.; Yook, C.; et al. (2003). „Substance p-fibronectin-cytokine interactions in myeloproliferative disorders with bone marrow fibrosis.”. Acta Haematol. 109 (1): 1—10. PMID 12486316. doi:10.1159/000067268.
- Cho J, Mosher DF (2006). „Role of fibronectin assembly in platelet thrombus formation.”. J. Thromb. Haemost. 4 (7): 1461—9. PMID 16839338. doi:10.1111/j.1538-7836.2006.01943.x.
- Schmidt DR, Kao WJ (2007). „The interrelated role of fibronectin and interleukin-1 in biomaterial-modulated macrophage function.”. Biomaterials. 28 (3): 371—82. PMID 16978691. doi:10.1016/j.biomaterials.2006.08.041.
- Dallas SL, Chen Q, Sivakumar P (2006). „Dynamics of assembly and reorganization of extracellular matrix proteins.”. Curr. Top. Dev. Biol. 75: 1—24. PMID 16984808. doi:10.1016/S0070-2153(06)75001-3.
- Hynes, Richard O. (1990). Fibronectins. Berlin: Springer-Verlag.
Spoljašnje veze
[уреди | уреди извор]- [3]
- Fibronektin protein
- Fibronectin на US National Library of Medicine Medical Subject Headings (MeSH)
- Molekulske interakcije fibronektina
![]() Mediji vezani za članak Fibronektin na Vikimedijinoj ostavi
Mediji vezani za članak Fibronektin na Vikimedijinoj ostavi