Пирол
| |||
| |||
| Називи | |||
|---|---|---|---|
| IUPAC назив
1H-Pyrrole
| |||
| Идентификација | |||
3Д модел (Jmol)
|
|||
| Бајлштајн | 1159 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.387 | ||
| EC број | 203-724-7 | ||
| Гмелин Референца | 1705 | ||
| RTECS | УX9275000 | ||
| УНИИ | |||
| УН број | 1992, 1993 | ||
| |||
| Својства | |||
| C4H5N | |||
| Моларна маса | 67,09 g·mol−1 | ||
| Густина | 0,967 g cm-3 | ||
| Тачка топљења | −23 °C (−9 °F; 250 K) | ||
| Напон паре | 7 mmHg at 23°C | ||
| Вискозност | 0.001225 Pa s | ||
| Термохемија | |||
| Специфични топлотни капацитет, C | 1.903 J k-1 mol k-1 | ||
Стд енталпија
формирања (ΔfH⦵298) |
108.2 kJ mol-1 (гас) | ||
| Стд енталпија сагоревања ΔcH |
2242 kJ mol-1 | ||
| Opasnosti | |||
| NFPA 704 | |||
| Tačka paljenja | 33.33°C | ||
| 550 °C (1.022 °F; 823 K) | |||
| Eksplozivni limiti | 3.1-14.8% | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |||
| Референце инфокутије | |||
Пирол је хетероциклично ароматично органско једињење. То је петочлани прстен са формулом C4H4NH.[3][4] Он је безбојна испарљива течност која потамни након излагања ваздуху. Супституисани деривати се такође називају пиролима, нпр., N-метилпирол, C4H4NCH3. Порфобилиноген, трисупституисани пирол, је биосинтетички прекурзор многих природних производа као што је хем.[5]
Особине
[уреди | уреди извор]Пирол има веома ниску базност у поређењу са конвенционалним аминима и неким другим ароматичним једињењима као што је пиридин. Ова умањена базност је последица делокализације слободног пара електрона атома азота у ароматичном прстену. Пирол је веома слаба база са pKaH вредношћу од око −4. Протонација доводи до губитка ароматичности, и стога није спонтана.
Као и многи други амини, пирол потамни при излагању ваздуху и светлости, и неоходно је да се дестилише непосредно пре употребе.[6]
Синтеза
[уреди | уреди извор]Пирол се индустријски припрема третманом фурана са амонијаком у присуству чврстог киселог катализатора.[7]
Један синтетички пут пирола је декарбоксилација амонијум муката, амонијумове соли галактозне киселине. Со се типично загрева под дестилационом условима са глицеролом као растварачом.[8]
Супституисани пироли
[уреди | уреди извор]Многи методи постоје за органску синтезу деривата пиола. Класичне „именоване реакције“ су Кнорова синтеза пирола, Хантзсцхова синтеза пирола, и Пал-Кнорова синтеза.
Почетни материјали Пилоти-Робинсонове синтезе пирола су 2 еквивалента алдехида и хидразин.[9][10] Производ је пирол са специфичним супституентима у позицијама 3 и 4. Алдехид реагује са диамином да формира интермедијар ди-имин (R–C=N−N=C–R), који са хлороводоничном киселином затвара прстен и губи амонијак.
У једној модификацији, пропионалдехид се третира прво са хидразином, а онда са бензоил хлоридом на високим температурама и уз помоћ микроталасног озрачивања:[11]
У другом ступњу, долази до [3,3]сигматропне реакције између два интермедијара.
Пирол може да буде полимеризован у полипирол.
Реактивност
[уреди | уреди извор]NH протон пирола је умерено кисео са pKa вредношћу од 16.5. Пирол се може депротоновати са јаким базама као што је бутил литијум и натријум хидрид. Резултујући алкални пиролид је нуклеофилан. Треатирање те коњуговане басе са електрофилима као што је метил јодид даје N-метилпирол.
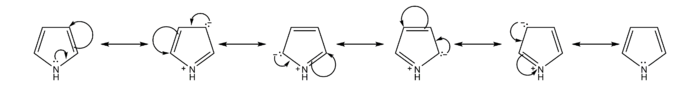
Резонантни облици пирола дају увид у реактивност овог једињења. Попут фурана и тиофена, пирол је реактивнији од бензена у електрофилној ароматичној супституцији, јер има способност стабилизације позитивно наелектрисаних карбокатјонских интермедијара.
Пирол подлеже електрофилној ароматичној супституцији предоминантно у 2 и 5 позицијама. Две такве реакције од посебног значаја за формирање функционализованих пирола су Маницхова реакција и Вилсмеиер-Хакова реакција,[12] обе од којих су компатибилне са мноштвом пиролних супстрата.

Формилација деривата пирола[12])
Види још
[уреди | уреди извор]Литература
[уреди | уреди извор]- Армарего, Wилфред, L.Ф.; Цхаи, Цхристина, L.L. (2003). Пурифицатион оф Лабораторy Цхемицалс (5тх изд.). Елсевиер. стр. 346.
- Лоудон, Марц Г. (2002). „Цхемистрy оф Напхтхалене анд тхе Ароматиц Хетероцyцлес.”. Органиц Цхемистрy (Фоуртх изд.). Неw Yорк: Оxфорд Университy Пресс. стр. 1135-1136. ИСБН 978-0-19-511999-2.
Референце
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Loudon, Marc G. (2002). „Chemistry of Naphthalene and the Aromatic Heterocycles.”. Organic Chemistry (Fourth изд.). New York: Oxford University Press. стр. 1135-1136. ISBN 978-0-19-511999-2.
- ^ Katritzky A.R.; Pozharskii A.F. (2000). Handbook of Heterocyclic Chemistry (Second изд.). Academic Press. ISBN 0080429882.
- ^ David L. Nelson; Michael M. Cox (2005). Principles of Biochemistry (IV изд.). New York: W. H. Freeman. ISBN 0-7167-4339-6.
- ^ Armarego, Wilfred, L.F.; Chai, Christina, L.L. (2003). Purification of Laboratory Chemicals (5th изд.). Elsevier. стр. 346.
- ^ Albrecht Ludwig Harreus "Pyrrole" in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. . doi:10.1002/14356007.a22_453. Недостаје или је празан параметар
|title=(помоћ) - ^ Practical Organic Chemistry, Vogel, 1956, Page 837, Link (12 MB)
- ^ Oskar Piloty (1910). „Synthese von Pyrrolderivaten: Pyrrole aus Succinylobernsteinsäureester, Pyrrole aus Azinen”. Chem. Ber. 43: 489. doi:10.1002/cber.19100430182. Текст „Piloty, O. ” игнорисан (помоћ)
- ^ Robinson, Gertrude Maud; Robinson, Robert (1918). „LIV.—A new synthesis of tetraphenylpyrrole”. J. Chem. Soc. 113: 639. doi:10.1039/CT9181300639.
- ^ Benjamin C. Milgram; Katrine Eskildsen; Steven M. Richter; W. Robert Scheidt & Karl A. Scheidt (2007). „Microwave-Assisted Piloty-Robinson Synthesis of 3,4-Disubstituted Pyrroles” (Note). J. Org. Chem. 72 (10): 3941—3944. PMC 1939979
 . PMID 17432915. doi:10.1021/jo070389.
. PMID 17432915. doi:10.1021/jo070389.
- ^ а б Jose R. Garabatos-Perera; Benjamin H. Rotstein & Alison Thompson (2007). „Comparison of Benzene, Nitrobenzene, and Dinitrobenzene 2-Arylsulfenylpyrroles”. J. Org. Chem. 72 (19): 7382—7385. PMID 17705533. doi:10.1021/jo070493r.