Piridin
| |||
| |||
| Nazivi | |||
|---|---|---|---|
| IUPAC naziv
Pyridine
| |||
| Drugi nazivi
Azabenzen
Azin py | |||
| Identifikacija | |||
3D model (Jmol)
|
|||
| ChemSpider | |||
| ECHA InfoCard | 100.003.464 | ||
| EC broj | 203-809-9 | ||
| UNII | |||
| |||
| Svojstva | |||
| C5H5N | |||
| Molarna masa | 79,10 g·mol−1 | ||
| Agregatno stanje | bezbojna tečnost | ||
| Gustina | 0,9819 g/cm3, tečnost | ||
| Tačka topljenja | −416 °C (−717 °F; −143 K) | ||
| Tačka ključanja | 1.152 °C (2.106 °F; 1.425 K) | ||
| meša se | |||
| Napon pare | 18 mmHg | ||
| Kiselost (pKa) | 5.25,[3][4] | ||
| Indeks refrakcije (nD) | 1.5093 | ||
| Viskoznost | 0.88 cP | ||
| Opasnosti[7] | |||
EU klasifikacija (DSD)
|
Zapaljiv (F) Štetan (Xn) | ||
| R-oznake | R20 R21 R22 R34 R36 R38 | ||
| NFPA 704 | |||
| Tačka paljenja | 21 °C (70 °F; 294 K) | ||
| Eksplozivni limiti | 1.8%–12.4%[5] | ||
| 5 ppm (TWA) | |||
| Letalna doza ili koncentracija (LD, LC): | |||
LD50 (LD50)
|
891 mg/kg (rat, oral) 1500 mg/kg (mouse, oral) 1580 mg/kg (rat, oral)[6] | ||
LC50 (LC50)
|
9000 ppm (rat, 1 hr)[6] | ||
| SAD zdravstvene granice izlaganja (NIOSH): | |||
PEL (dozvoljivo)
|
TWA 5 ppm (15 mg/m3)[5] | ||
REL (preporučeno)
|
TWA 5 ppm (15 mg/m3)[5] | ||
IDLH (neposredna opasnost)
|
1000 ppm[5] | ||
| Srodna jedinjenja | |||
Srodne amini
|
Pikolin Hinolin | ||
Srodna jedinjenja
|
Anilin Pirimidin Piperidin | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |||
| Reference infokutije | |||
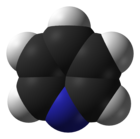
Piridin je heterociklično organsko jedinjenje sa hemijskom formulom C5H5N. On je strukturno srodan sa benzenom. Jedna CH grupa je zamenjena atomom azota.[8] On se koristi kao prekurzor agrohemikalija i lekova. On je isto tako važan rastvarač i reagens. Piridin je bezbojna lako zapaljiva tečnost sa specifičnim mirisom, koji podseća na ribu. Piridinov prsten se se javlja u mnogim važnim jedinjenjima, kao što su vitamini nikotinamid i piridoksal.
Priprema i pojava[уреди | уреди извор]
Piridin je originalno industrijski proizvođen ekstrakcijom iz ugljene smole. U današnje vreme se sintetizuje iz formaldehida, amonijaka, i acetaldehida:
Reakcije[уреди | уреди извор]
Baza[уреди | уреди извор]
U organskim reakcijama piridin se ponaša kao tercijarni amin, podleže protonaciji, alkilaciji, acilaciji, i N-oksidaciji na svom atomu azota, i kao aromatično jedinjenje, podleže nukleofilnim supstitucijama.

Azotni atom piridina poseduje bazni slobodni elektronski par. Pošto ovaj slobodni elektronski par nije delokalizovan u aromatični pi-sistem, piridin je baza sa hemijskim osobinama sličnim tercijarnim aminima. pKa vrednost konjugovane kiseline je 5.21. Piridin se protonizuje reakcijom sa kiselinama i formira pozitivno naelektrisani aromatični poliatomiski jon, koji se naziva piridinijum. Dužine veza i uglovi veza piridina i piridinijum jona su skoro identični.[9] Piridinijum katjon i benzen imaju isti broj elektrona. Piridinijum p-toluen sulfonat (PPTS) je ilustrativna piridinijumska so; ona se formira tretiranjem piridina sa p-toluen sulfonskom kiselinom.
N-nukleofil i ligand[уреди | уреди извор]
Piridin je dobar nukleofil sa donorskim brojem 33.1. On lako reaguje sa alkilujućim reagensima i daje N-alkil-piridinijum soli. Primer takve soli je cetil-piridinijum hlorid, katjonski surfaktant koji je u širokoj upotrebi kao dizinfikujući i antiseptički agens. Piridinijum soli se mogu pripremiti Zinckovom reakcijom. Korisni adukti piridina su piridin-boran, C5H5NBH3 (m.p. 10–11°C), blago redukujući reagens sa poboljšanom stabilnošću u odnosu na NaBH4 u protičkim rastvaračima, i poboljšanom ratvorljivošću u aprotičkim organskim rastvaračima. Piridin-sumpor trioksid, C5H5NSO3 (mp 175°C) je sulfonacioni reagens koji se koristi za konvertovanje alkohola u sulfonate, koji zatim podležu rascepu C-O veze posle redukcije sa hidridnim reagensima.
Piridin se koristi kao ligand u koordinacionoj hemiji. Takođe su važni njegovi helatni derivati 2,2'-bipiridin, koji se sastoje od dva molekula piridina spojena jednostrukom vezom, i terpiridin, molekul sa tri spojena piridinska prstena.
MSDS[уреди | уреди извор]
Piridin izaziva negativne posledice po čoveka i to, u dodiru sa kožom iritaciju, u neposrednom kontaktu sa očima izaziva iritaciju, odnosno suzenje, kao i depresiju CNS, što se manifestuje usporenim pulsom, disanjem, i gubljenjem svesti. Sa piridinom se mora pažljivo rukovati jer je i u tečnom i u gasovitom agregatnom stanju lako zapaljiva supstanca.
Respiratorni sistem[уреди | уреди извор]
Ukoliko je žrtva izložena udisanju piridina, nakon kraćeg vremena, osetiće glavobolju, pospanost, vrtoglavicu, i gubitak koordinacije. Nakon dužeg vremena, posledice su stomačni problemi, mučnina, povraćanje, dijareja, bol u stomaku, gubitak apetita, potom vrtoglavica, poremećaji sna, nagle promene raspoloženja, gubitak koordinacije pokreta i oštećenje nerava. Prva pomoć se ukazuje tako što se odmah uklanja izvor isparavanja piridina, žrtvi se mora obezbediti čisti vazduh, a ukoliko diše otežano ili u potpunosti ne diše, potrebno joj je ukazati pomoć u vidu veštačkog disanja. Takođe, poželjno je pozvati i lekara.
Koža[уреди | уреди извор]
Čovek čija je koža izložena delovanju piridina, prouzrokovaće iritaciju i alergijske reakcije. Kako bi se pomoglo tom čoveku, potrebno je prati iritiranu kožu vodom i sapunom oko 15 minuta. Obratiti se lekaru u slučaju dužem izlaganju kože dejstvu piridina. Obavezno dubinski očistiti kontaminiranu odeću i obuću pre ponovne upotrebe.
Oči[уреди | уреди извор]
Kontakt sa očima može prouzrokovati suzenje, iritaciju i, eventualno, trajno oštećenje čula vida. Važno je obavezno pozvati lekarsku pomoć, a pre toga 15 minuta dobro isprati mlazom vode.
Konzumiranje[уреди | уреди извор]
Osoba koja proguta piridin osetiće prvenstveno mučninu, potom povraćanje, dijareju, dezorjentisanost u prostoru, nagle promene raspoloženja, kao i kongestiju pluća. Ukoliko se ne ukaže prva pomoć i žrtvi se ne ispere želudac, mogući problemi su poput oštećenja nastalih nakon dužeg udisanja, a mogu se i trajno oštetiti pojedini organi, poput jetre, bubrega, srca. Vrlo je verovatno da će ta osoba ostati bez svesti, pa je neophodno odmah pozvati lekarsku pomoć. Nikako ne dozvoliti da onesvešćena osoba povraća i ne treba joj davati nikakvu tečnost.
Preventiva[уреди | уреди извор]
Preventiva bilo kakve povrede ili ozlede od piridina je adekvatna oprema, koja obuhvata rad u digestoru, hemijski otporna odeća, naočare i rukavice otporne na hemikalije. Mora se skladištiti i rukovati po važećim propisima i standardima. Piridin je potrebno zaštiti od fizičkih oštećenja, plamena, varnica, paljenja, kao i bilo kakvog izvora toplote. Boce i kontejneri u kojima se čuva piridin mogu eksplodirati pri neodgovarajućim uslovima. Čuvati od nekompitabilnih supstanci, i to kiselina, zapaljivih materija, oksidirajućih materija, oksida ugljenika i azota.
Reference[уреди | уреди извор]
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ Linnell, R. H., J. Org. Chem., 1960, 25, 290.
- ^ Pearson, R., Williams, F., J. Amer. Chem. Soc., 1953, 75, 3073.
- ^ а б в г NIOSH Džepni vodič hemijskih hazarda 0541
- ^ а б „Pyridine”. Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ „Pyridine MSDS”. fishersci.com. Fisher.
- ^ Katritzky A.R.; Pozharskii A.F. (2000). Handbook of Heterocyclic Chemistry (Second изд.). Academic Press. ISBN 0080429882.
- ^ T. M. Krygowski; H. Szatyowicz & J. E. Zachara (2005). „How H-bonding Modifies Molecular Structure and π-Electron Delocalization in the Ring of Pyridine/Pyridinium Derivatives Involved in H-Bond Complexation†”. J. Org. Chem. 70 (22): 8859. PMID 16238319. doi:10.1021/jo051354h.
Spoljašnje veze[уреди | уреди извор]
![]() Mediji vezani za članak Piridin na Vikimedijinoj ostavi
Mediji vezani za članak Piridin na Vikimedijinoj ostavi




