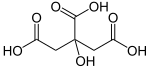
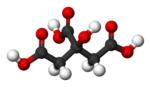
Limunska kiselina
| |||
| Nazivi | |||
|---|---|---|---|
| IUPAC naziv
Citrusna kiselina[1]
| |||
| Sistemski IUPAC naziv
2-Hidroksipropan-1,2,3-trikarboksilna kiselina | |||
| Identifikacija | |||
3D model (Jmol)
|
|||
| ChEBI | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.973 | ||
| EC broj | 201-069-1 | ||
| E-brojevi | E330 (antioksidansi, ...) | ||
| KEGG[2] | |||
| RTECS | GE7350000 | ||
| UNII | |||
| |||
| Svojstva | |||
| C6H8O7 | |||
| Molarna masa | 192,123 g/mol (anhidrat), 210,14 g/mol (monohidrat)[5] | ||
| Agregatno stanje | bela čvrsta materija | ||
| Miris | bez mirisa | ||
| Gustina | 1,665 g/cm3 (anhidrat) 1,542 g/cm3 (18 °C, monohidrat) | ||
| Tačka topljenja | 156 °C (313 °F; 429 K) | ||
| Tačka ključanja | 310 °C (590 °F; 583 K) razlaže se na 175 °C[6] | ||
| 54% w/w (10 °C) 59,2% w/w (20 °C) 64,3% w/w (30 °C) 68,6% w/w (40 °C) 70,9% w/w (50 °C) 73.5% w/w (60 °C) 76,2% w/w (70 °C) 78,8% w/w (80 °C) 81,4% w/w (90 °C) 84% w/w (100 °C)[7] | |||
| Rastvorljivost | Rastvorana u acetonu, alkoholu, etru, etil acetatu, DMSO Nerastvorana u C 6H 6, CHCl3, CS2, toluene[6] | ||
| Rastvorljivost u etanol | 62 g/100 g (25 °C)[6] | ||
| Rastvorljivost u amil acetat | 4,41 g/100 g (25 °C)[6] | ||
| Rastvorljivost u dietil etar | 1,05 g/100 g (25 °C)[6] | ||
| Rastvorljivost u 1,4-Dioksan | 35,9 g/100 g (25 °C)[6] | ||
| log P | −1,64 | ||
| Kiselost (pKa) | pKa1 = 3,13[8] pKa2 = 4,76[8] pKa3 = 6,39,[9] 6.40[10] | ||
| Indeks refrakcije (nD) | 1.493–1.509 (20 °C)[7] 1,46 (150 °C)[6] | ||
| Viskoznost | 6.5 cP (50% aq. sol.)[7] | ||
| Struktura | |||
| Kristalna rešetka/struktura | Monoklinična | ||
| Termohemija | |||
| Specifični toplotni kapacitet, C | 226,51 J/(mol·K) (26,85 °C)[11] | ||
| Standardna molarna entropija S |
252,1 J/(mol·K)[11] | ||
Std entalpija
formiranja (ΔfH⦵298) |
−1543,8 kJ/mol[7] | ||
| 1985,3 kJ/mol (474,5 kcal/mol, 2,47 kcal/g),[7] 1960.6 kJ/mol[11] 1972,34 kJ/mol (471,4 kcal/mol, 2,24 kcal/g) (monohidrat)[7] | |||
| Farmakologija | |||
| A09AB04 (WHO) | |||
| Opasnosti | |||
| Opasnost u toku rada | Iritant kože i očiju | ||
| Bezbednost prilikom rukovanja | HMDB | ||
| GHS grafikoni |  [8] [8]
| ||
| GHS signalna reč | Upozorenje | ||
| H319[8] | |||
| P305+351+338[8] | |||
| NFPA 704 | |||
| Tačka paljenja | 155 °C (311 °F; 428 K) | ||
| 345 °C (653 °F; 618 K) | |||
| Eksplozivni limiti | 8%[8] | ||
| Letalna doza ili koncentracija (LD, LC): | |||
LD50 (LD50)
|
3000 mg/kg (pacovi, oralno) | ||
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |||
| Reference infokutije | |||
Limunska kiselina, C6H8O7, trobazna je organska kiselina[12][13], prisutna u mnogim vrstama voća (u limunovom soku 5–6%).
Bela je kristalna supstanca kiselog ukusa, lako rastvorljiva u vodi. Industrijski se dobija iz limuna (u južnoj Italiji i Kaliforniji) ili iz šećera fermentacijom pomoću plesni Aspergillus niger. Upotrebljava se u proizvodnji bezalkoholnih napitaka i u medicini. Njene soli su citrati. Normalan je sastojak ljudske krvi i urina (mokraće). Koristi se u proizvodnji šumećih tableta i vitaminskih napitaka, voćnih sokova, smrznutog voća itd... Uzorci krvi i tkiva čuvaju se u rastvorima limunske kiseline.

Prirodni izvori i industrijska proizvodnja[уреди | уреди извор]

Limunske kiseline ima u raznom voću i povrću, a najviše u citrusnim plodovima. Limun i limete imaju posebno visoke koncentracije kiseline; može činiti čak 8% suve mase ovog voća (u sokovima oko 47 g/L[14]). To još uvek ne čini limun posebno jako kiselim. To je zato što, kao slaba kiselina, većina njenih molekula nije disocirana, te ne doprinosi kiselosti unutar limuna ili njegovog soka. Koncentracije limunske kiseline u limunskim plodovima kreću se od 0,005 mol/L za narandže i grejpfrut do 0,30 mol/L u limunu i limeti; ove vrednosti variraju unutar vrsta, zavisno od sorte i okolnostima u kojima je voće uzgajano.
Proizvodnja limunske kiseline u industrijskim razmerama prvi je put započela 1890. Godine, u italijanskoj industriji citrusnih plodova, gde je sok tretiran hidratiziranim krečom (kalcijum hidroksid) da se istaloži kalcijum citrat, koji je izolovan i preveden nazad u kiselinu pomoću razblažene sumporne kiseline.[15] Godine 1893, Karl Vemer otkrio je da gljivice, plesni roda Penicillium mogu proizvesti limunsku kiselinu iz šećera. Međutim, mikrobna proizvodnja limunske kiseline nije postala industrijski važna sve dok Prvi svetski rat nije poremetio italijanski izvoz limuna.
Nakon što se plesan filtrira iz rezultujućeg rastvora, limunska kiselina se izolira pomoću taloženja kalcijum hidroksidom, dajući kalcijumovu citratnu so, iz koje se limunska kiselina obnavlja tretiranjem sumpornom kiselinom, kao u direktnoj ekstrakciji soka citrusnih plodova.
Preduzeću Lever Broders je 1977. godine odobren patent za hemijsku sintezu limunske kiseline, polazeći od akonitne ili izocitratne / aloizocitratne soli kalcijuma, pod uslovima visokog pritiska; ovo je stvorilo limunsku kiselinu u blizu kvantitativnoj konverziji onoga što se činilo obrnutim, neenzimskim reakcijama Krebsovog ciklusa.[16]
Godine 2018, globalna proizvodnja limunske kiseline dostigla je 2,000.000 tona.[17] Više od 50% ovog obima proizvedeno je u Kini. Više od 50% korišteno je kao regulator kiselosti u pićima, oko 20% u drugim namirnicama, a 20% u deterdžentima i 10% u aplikacijama koje nisu hrana, poput kozmetike, farmaceutskih proizvoda i hemijske industrije.
Hemijska obeležja[уреди | уреди извор]


Limunsku kiselinu je prvi put izolovao Karl Vilhelm Šele 1784. godine, hemičar koji ju je kristalizovao iz limunovog soka.[15][18][19]
Limunska kiselina može postojati ili u bezvodnom (anhidridnom) obliku ili kao monohidrat. Bezvodni oblik se kristalizuje iz vruće vode, dok monohidrat nastaje kada se limunska kiselina kristalizuje iz hladne vode. Monohidrat se može pretvoriti u bezvodni oblik na oko 78 °C. Limunska kiselina se takođe rastvara u apsolutnom (bezvodnom) etanolu (76 delova limunske kiseline na 100 delova etanola) na 15 °C. Razgrađuje se gubitkom ugljen dioksida, iznad oko 175 °C.
Limunska kiselina se obično smatra troosnovnom kiselinom, sa pKa, ekstrapoliranom na nultu ionsku snagu, od 2,92, 4,28 i 5,21 na 25 °C.[20] Konstanta pKa hidroksil grupe nađena je spektroskopski (13C NMR), a iznosi prosečno 14,4.[21]
Specijacijski dijagram pokazuje da su rastvori limunske kiseline puferski rastvori , sa i pH između oko 2 i pH 8. U biološkim sistemima pH je oko 7, u obe prisutne vrste: citratni i monovodonik-citratni jon.[22][23] Dostupne su i kompilirane tabele za studij biohemije[24]
Citratni jon formira komplekse sa metalnim katjonima. Konstante stabilnosti za stvaranje ovih kompleksa prilično su velike zbog helatnog efekta. On stvara komplekse čak i sa katjonima alkalnih metala. Međutim, kada se helatni kompleks formira pomoću sve tri karboksilatne grupe, helatni prstenovi imaju 7 i 8 članova, koji su generalno termodinamički manje stabilni od manjih helatnih prstenova. Kao posledica toga, hidroksilna grupa može se deprotonovati, čineći deo stabilnijeg petočlanog prstena, kao u amonijum-željeznom citratu, (NH
4)
5Fe(C
6H
4O
7)
2·2H
2O.[25]
Ciklus limunske kiseline[уреди | уреди извор]
Citrat je međuprodukat u TCA-ciklusu (Tri C (od carboxyl) A (od acid = kiselina) ili Krebsov ciklus, a po Sent Đerđiju, centralni metabolički put za životinje, biljke i bakterije. Citrat-sintaza katalizuje kondenzaciju oksaloacetata sa acetil-KoA dajući citrat. Citrat tada deluje kao supstrat za akonitazu i pretvara se u akonitnu kiselinu. Ciklus se završava regeneracijom oksaloacetata. Ova serija hemijskih reakcija, kod viših organizama, izvor je dve trećine energije dobijene hranom. Za ovo otkriće, Hans Adolf Krebs dobio je 1953. Nobelovu nagradu za fiziologiju ili medicinu.
Neke bakterije (posebno E. coli) mogu proizvesti i konzumirati citrat iznutra kao deo svog TCA ciklusa, ali ga ne mogu koristiti kao hranu, jer im nedostaju enzimi potrebni za unos u ćeliju. Nakon desetina hiljada evolucija u minimalnom mediju glukoze koji je takođe sadržavao citrat tokom dugoročnog evolucijskog eksperimenta, koji je izveo Ričard Lenski na E. coli evoluirao je sposobnošću aerobnog rasta na citratu. Zahari Blant, student Lenskog i njegove kolege proučavali su ove „Cit+” E. coli,[26][27] kao model za razvoj novih osobina. Pronašli su dokaze da je, u ovom slučaju, inovacija uzrokovana retkom mutacijom dupliranja usled nakupljanja nekoliko prethodnih „potencirajućih” mutacija, čiji su identitet i učinci još uvek u fazi proučavanja. Evolucija obeležja Cit+ smatrana je značajnim primerom uloge istorijskog kontingenta u evoluciji.
Ostale biološke uloge[уреди | уреди извор]
Citrat se može transportovati iz mitohondrija u citoplazmu, zatim razgraditi na acetil-KoA za sintezu masnih kiselina i u oksaloacetat. Citrat je pozitivni modulator ove konverzije i alosterno reguliše enzim acetil-KoA karboksilaza, koji je regulatorni enzim u konverziji acetil-KoA u malonil-KoA (korak ulaganja u sintezu masne kiseline). Ukratko, citrat se transportuje u citoplazmu, pretvara u acetil KoA, koji se zatim pretvara u malonil KoA pomoću acetil KoA karboksilaze, koju citrat alosterno moduliše.
Visoke koncentracije citosolnog citrata mogu inhibirati fosfofruktokinazu, katalizator koraka koji ograničava brzinu glikolize. Ovaj je učinak povoljan: visoke koncentracije citrata ukazuju na to da postoji velika količina molekula biosintetskih prekursora, pa nema potrebe da fosfofruktokinaza i dalje šalje molekule svog supstrata, fruktoza 6-fosfata u glikolizu. Citrat deluje pojačavajući inhibitorni učinak visokih koncentracija ATP, još jedan znak da nema potrebe za provođenjem glikolize.[28]
Reference[уреди | уреди извор]
- ^ ChemSpider lists 'citric acid' as the expert-verified IUPAC name.
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ PubChem CID 22230
- ^ а б в г д ђ е „citric acid”. chemister.ru. Архивирано из оригинала 29. 11. 2014. г. Приступљено 1. 6. 2014.
- ^ а б в г д ђ PubChem CID 311
- ^ а б в г д ђ Fisher Scientific, Citric acid. Retrieved on 2014-06-02.
- ^ „Data for Biochemical Research”. ZirChrom Separations, Inc. Приступљено 11. 1. 2012.
- ^ „Ionization Constants of Organic Acids”. Michigan State University. Приступљено 11. 1. 2012.
- ^ а б в Citric acid in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-06-02)
- ^ Clayden, Jonathan; Greeves, Nick; Warren, Stuart; Wothers, Peter (2001). Organic Chemistry (I изд.). Oxford University Press. ISBN 978-0-19-850346-0.
- ^ Thomas L. Lemke; David A. Williams, ур. (2007). Foye's Principles of Medicinal Chemistry (6. изд.). Baltimore: Lippincott Willams & Wilkins. ISBN 0781768799.
- ^ Penniston KL, Nakada SY, Holmes RP, Assimos DG (2008). „Quantitative Assessment of Citric Acid in Lemon Juice, Lime Juice, and Commercially-Available Fruit Juice Products”. Journal of Endourology. 22 (3): 567—570. PMC 2637791
 . PMID 18290732. doi:10.1089/end.2007.0304.
. PMID 18290732. doi:10.1089/end.2007.0304.
- ^ а б Frank H. Verhoff (2005). „Citric Acid”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH.
- ^ US 4056567-V.Lamberti and E.Gutierrez
- ^ „Global Citric Acid Markets Report, 2011-2018 & 2019-2024”. prnewswire.com. 19. 3. 2019. Приступљено 28. 10. 2019.
- ^ Scheele, Carl Wilhelm (1784). „Anmärkning om Citron-saft, samt sätt at crystallisera densamma” [Note about lemon juice, as well as ways to crystallize it]. Kungliga Vetenskaps Academiens Nya Handlingar [New Proceedings of the Royal Academy of Science]. 2nd series. 5: 105—109.
- ^ Graham, Thomas (1842). Elements of chemistry, including the applications of the science in the arts. Hippolyte Baillière, foreign bookseller to the Royal College of Surgeons, and to the Royal Society, 219, Regent Street. стр. 944. Приступљено 4. 6. 2010.
- ^ Goldberg, Robert N.; Kishore, Nand; Lennen, Rebecca M. (2002). „Thermodynamic Quantities for the Ionization Reactions of Buffers”. J. Phys. Chem. Ref. Data. 31 (1): 231—370. Bibcode:2002JPCRD..31..231G. doi:10.1063/1.1416902.
- ^ Silva, Andre M. N.; Kong, Xiaole; Hider, Robert C. (2009). „Determination of the pKa value of the hydroxyl group in the α-hydroxycarboxylates citrate, malate and lactate by 13C NMR: implications for metal coordination in biological systems”. Biometals. 22 (5): 771—778. PMID 19288211. doi:10.1007/s10534-009-9224-5.
- ^ SSC 20X hybridization buffer je primer uobičajene upotrebe.
- ^ Maniatis, T.; Fritsch, E. F.; Sambrook, J. 1982. Molecular Cloning: A Laboratory Manual. Cold Spring Harbor Laboratory, Cold Spring Harbor, NY.
- ^ Gomori, G. (1955). „16 Preparation of buffers for use in enzyme studies”. Methods in Enzymology Volume 1. Methods in Enzymology. 1. стр. 138–146. ISBN 9780121818012. doi:10.1016/0076-6879(55)01020-3.
- ^ Matzapetakis, M.; Raptopoulou, C. P.; Tsohos, A.; Papaefthymiou, V.; Moon, S. N.; Salifoglou, A. (1998). „Synthesis, Spectroscopic and Structural Characterization of the First Mononuclear, Water Soluble Iron−Citrate Complex, (NH4)5Fe(C6H4O7)2·2H2O”. J. Am. Chem. Soc. 120 (50): 13266—13267. doi:10.1021/ja9807035.
- ^ Powell, Alvin (14. 2. 2014). „59,000 generations of bacteria, plus freezer, yield startling results”. phys.org. Приступљено 13. 4. 2017.
- ^ Blount, Z. D.; Borland, C. Z.; Lenski, R. E. (4. 6. 2008). „Historical contingency and the evolution of a key innovation in an experimental population of Escherichia coli” (PDF). Proceedings of the National Academy of Sciences. 105 (23): 7899—7906. Bibcode:2008PNAS..105.7899B. PMC 2430337
 . PMID 18524956. doi:10.1073/pnas.0803151105. Архивирано из оригинала (PDF) 21. 10. 2016. г. Приступљено 13. 4. 2017.
. PMID 18524956. doi:10.1073/pnas.0803151105. Архивирано из оригинала (PDF) 21. 10. 2016. г. Приступљено 13. 4. 2017.
- ^ Stryer, Lubert; Berg, Jeremy; Tymoczko, John (2003). „Section 16.2: The Glycolytic Pathway Is Tightly Controlled”. Biochemistry (5. ed., international ed., 3. printing изд.). New York: Freeman. ISBN 978-0716746843.
Spoljašnje veze[уреди | уреди извор]
- British Pharmacopoeia Commission Secretariat (2009). „Index, BP 2009” (PDF). Архивирано из оригинала (PDF) 11. 4. 2009. г. Приступљено 4. 2. 2010.
- „Japanese Pharmacopoeia, Fifteenth Edition” (PDF). 2006. Архивирано из оригинала (PDF) 22. 7. 2011. г. Приступљено 4. 2. 2010.