Фосфораста киселина

| |
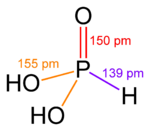
| |
| Називи | |
|---|---|
| IUPAC називs
Фосфитна киселина
хидридодихидроксидооксидофосфит | |
| Други називи
фосфораста киселина
| |
| Идентификација | |
| ECHA InfoCard | 100.033.682 |
| MeSH | Phosphorous+acid |
| RTECS | SZ6400000 |
| Својства | |
| H3PO3 | |
| Моларна маса | 82,00 g/mol |
| Агрегатно стање | безбојна чврста супстанца |
| Густина | 1,65 g/cm3 |
| Тачка топљења | 70.1 °C |
| Тачка кључања | разлаже се |
| меша се | |
| Структура | |
| Облик молекула (орбитале и хибридизација) | тетраедар |
| Опасности | |
| Главне опасности | иритира кожу |
| R-ознаке | R22-R35 |
| S-ознаке | S26-S36/37/39-S45 |
| NFPA 704 | |
| Сродна једињења | |
Уколико није другачије напоменуто, подаци се односе на стандардно стање материјала (на 25°C [77°F], 100 kPa). | |
| Референце инфокутије | |
Фосфораста (фосфитна) киселина, H3PO3, је безбојна кристална супстанца која се добро раствара у води. Припада групи дипротонских киселина (иако садржи 3 водоникова атома), и као таква гради два различита типа соли: фосфите и хидрогенфосфите.[1]
При загревању се из 4 мола ове киселине добијају фосфин и фосфорна киселина. Фосфораста киселина има изараженије редукционе особине.
Фосфити натријума, NaHPHO3 и Na2PHO3 могу да се користе као антисептици. У реакцији са слабим база показује киселу реакцију.
Извори[уреди | уреди извор]
- ^ Lide David R., ур. (2006). CRC Handbook of Chemistry and Physics (87th изд.). Boca Raton, FL: CRC Press. ISBN 978-0-8493-0487-3.

