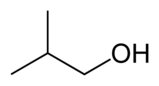
Izobutanol
| |

| |
| Nazivi | |
|---|---|
| IUPAC naziv
2-metil-1-propanol
| |
| Drugi nazivi
Izobutil alkohol, IBA, 2-metilpropil alkohol
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.001.044 |
| KEGG[1] | |
| RTECS | NP9625000 |
| UNII | |
| |
| Svojstva | |
| C4H10O | |
| Molarna masa | 74,122 g/mol |
| Agregatno stanje | Bezbojna tečnost |
| Gustina | 0,802 g/cm3, tečnost |
| Tačka topljenja | −1.019 °C (−1.802 °F; −746 K) |
| Tačka ključanja | 10.789 °C (19.452 °F; 11.062 K) |
| 8,7 mL/100 mL[4] | |
| log P | 0.8 |
| Indeks refrakcije (nD) | 1,3959 |
| Viskoznost | 3,95 cP na 20 °C |
| Opasnosti[5] | |
| Bezbednost prilikom rukovanja | ICSC 0113 |
EU klasifikacija (DSD)
|
Iritant (Xi) |
| R-oznake | R10 R37/38 R41, R67 |
| S-oznake | (S2) S7/9 S13 S26 S37/39 S46 |
| NFPA 704 | |
| Tačka paljenja | 28 °C (82 °F; 301 K) |
| 415 °C (779 °F; 688 K) | |
| Eksplozivni limiti | 1.7–10.9% |
| Letalna doza ili koncentracija (LD, LC): | |
LDLo (LDLo)
|
3750 mg/kg (zec, oralno) 2460 mg/kg (pacov, oralno)[7] |
| SAD zdravstvene granice izlaganja (NIOSH): | |
PEL (dozvoljivo)
|
TWA 100 ppm (300 mg/m3)[6] |
REL (preporučeno)
|
TWA 50 ppm (150 mg/m3)[6] |
IDLH (neposredna opasnost)
|
1600 ppm[6] |
| Srodna jedinjenja | |
Srodne materije
|
n-Butanol sec-Butanol tert-Butanol |
Srodna jedinjenja
|
Izobutiraldehid Izobutirna kiselina |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
Isobutanol (IUPAC: 2-metil-1-propanol) je organsko jedinjenje sa formulom (CH3)2CHCH2OH. Ova bezbojna, zapaljiva tečnost sa karakterističnim mirisom se uglavnom koristi kao rastvarač. Njegovi izomeri su n-butanol, 2-butanol, i tert-butanol, svi od kojih su industrijski značajni.
Proizvodnja[уреди | уреди извор]
Isobutanol se proizvodi karbonilacijom propilena. Dva methoda se koriste u industriji, hidroformilacija se češće primenjuje. Ona formira smešu normalnog i izobutiraldehida, koji se hidrogenišu do alkohola i zatim razdvajaju. Repova karbonilacija se takođe koristi.[8]
Reference[уреди | уреди извор]
- ^ Joanne Wixon; Douglas Kell (2000). „Website Review: The Kyoto Encyclopedia of Genes and Genomes — KEGG”. Yeast. 17 (1): 48—55. doi:10.1002/(SICI)1097-0061(200004)17:1<48::AID-YEA2>3.0.CO;2-H.
- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ „Iso-butanol”. ChemicalLand21.
- ^ а б Isobutanol, International Chemical Safety Card 0113, Geneva: International Programme on Chemical Safety, april 2005.
- ^ а б в NIOSH Džepni vodič hemijskih hazarda 0352
- ^ „Isobutyl alcohol”. Immediately Dangerous to Life and Health. National Institute for Occupational Safety and Health (NIOSH).
- ^ „Butanols”. Ullmann’s Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. 2005. doi:10.1002/14356007.a04_463..

