Arsenitna kiselina
| |
| |
| Nazivi | |
|---|---|
| IUPAC naziv
Arsenitna kiselina
| |
| Drugi nazivi
Arsenitna kiselina
| |
| Identifikacija | |
3D model (Jmol)
|
|
| ChEBI | |
| ChemSpider | |
| DrugBank | |
| |
| Svojstva | |
| H3AsO3 | |
| Molarna masa | 125,94 g/mol |
| Agregatno stanje | Postoji samo u vodenom rastvoru |
| Opasnosti | |
| Opasnost u toku rada | Toksična, korozivna |
| Srodna jedinjenja | |
Srodna jedinjenja
|
Arsenatna kiselina |
Ukoliko nije drugačije napomenuto, podaci se odnose na standardno stanje materijala (na 25 °C [77 °F], 100 kPa). | |
| Reference infokutije | |
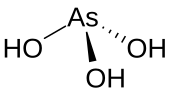
Arsenitna kiselina je neorgansko jedinjenje sa formulom H3AsO3. Ona je javlja u vodenim rastvorima. Ona nije bila izdvojena kao čist materijal.[3]
Osobine
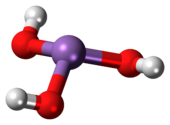
[уреди | уреди извор]As(OH)3 je piramidalni molekul koji sadrži tri hidroksilne grupe vezane za arsen. 1H NMR spektar rastvora arsenitne kiseline potvrđuje simetriju molekula.[4] U kontrastu s tim, srodna fosforna kiselina H3PO3 uglavnom poprima strukturu HPO(OH)2. P(OH)3 je manje zastupljena komponenta rastvora. Različito ponašanje jedinjenja As i P odražava trend da su viša oksidaciona stanja stabilnija za kod lakših elemenata grupe.[5]
Reakcije
[уреди | уреди извор]Priprema As(OH)3 se odvija putem spore hidrolize arsen trioksida u vodi. Dodatak baze konvertuje arsenitnu kiselinu u arsenitne jone [AsO(OH)2]-, [AsO2(OH)]2-, i [AsO3]3-. Prva pKa vrednost je 9.2. Reakcije vodenog arsenik trioksida su posledica prisustva arsenitne kiseline i njenih konjugovanih baza.
Toksikologija
[уреди | уреди извор]Jedinjenja arsenika su visoko toksična i kancerogena. Anhidridna forma arsenitne kiseline, arsenik trioksid, se koristi kao herbicid i pesticid.
Reference
[уреди | уреди извор]- ^ Li Q, Cheng T, Wang Y, Bryant SH (2010). „PubChem as a public resource for drug discovery.”. Drug Discov Today. 15 (23-24): 1052—7. PMID 20970519. doi:10.1016/j.drudis.2010.10.003.
- ^ Evan E. Bolton; Yanli Wang; Paul A. Thiessen; Stephen H. Bryant (2008). „Chapter 12 PubChem: Integrated Platform of Small Molecules and Biological Activities”. Annual Reports in Computational Chemistry. 4: 217—241. doi:10.1016/S1574-1400(08)00012-1.
- ^ King, R. Bruce "(ed.)" (1994). Encyclopedia of Inorganic Chemistry. Chichester: John Wiley & Sons.
- ^ András Kolozsi; Andrea Lakatos; Gábor Galbács; Anders Østergaard Madsen; Erik Larsen & Béla Gyurcsik (2008). „A pH-Metric, UV, NMR, and X-ray Crystallographic Study on Arsenous Acid Reacting with Dithioerythritol” (PDF). Inorg. Chem. 47: 3832—3840. Архивирано из оригинала (PDF) 25. 04. 2012. г. Приступљено 18. 12. 2011.
- ^ Greenwood, N.N.; A. Earnshaw (1997). Chemistry of the Elements. Oxford: Butterworth-Heinemann.
