Radioaktivni nizovi

Radioaktivni nizovi, su skupovi prirodnih radionuklida koji nastaju jedni iz drugih sukcesijom radioaktivnih raspada. Članovi niza su međusobno povezani svojim poreklom jer nastaju jedni od drugih, a svi imaju zajedničkog rodonačelnika – početni radionuklid. Početni radionuklid u nizu ima najduži period poluraspada i najveću masu a poslednji članovi niza su stabilni radionuklidi. Većina prirodnih radionuklida koji postoje na Zemlji (rednog broj Z>82) se grupišu u tri radioaktivna niza. To su uranov, aktinijumov i torijumov niz. Rodonačelnici nizova (radioizotopi urana i torijuma) imaju ekstremno duge periode poluraspada koji su nekoliko redova veličine duži od perioda poluraspada njihovih dugoživećih potomaka. To često ima za posledicu uspostavljanje sekularne radioaktivne ravnoteže u nizovima pri kojoj je aktivnost svakog potomka jednaka aktivnosti rodonačelnika niza. Za svaki niz je karakteristična pojava grananje niza koja nastaje usled toga što neki radionuklidi imaju dvostruku mogućnost raspada sa odgovarajućom verovatnoćom (alfa-raspad i beta-raspad), pri čemu potomak može da nastane pomoću dva kanala raspada. Druga zajednička karakteristika radioaktivnih nizova je prisustvo izotopa inertnog gasa radona koji u većoj ili manjoj meri emanira iz smeše u kojoj se generiše.
Istorijat
[уреди | уреди извор]Radioaktivni izotopi koji prirodno postoje na Zemlji mogu se podeliti u dve grupe:primordijalni (prvobitni)ikosmogeni koji su nastali kao rezultat interakcije kosmičkih zraka sa materijom. Prvu grupu čine dugoživeći izotopi, koji potiču još iz vremena nastanka Sunčevog sistema. Najvažniji izotopi ove grupe svakako su U-238, U-235, Th-232 i K-40. Primordijalni radionuklidi inače predstavljaju najznačajniji izvor jonizujućeg zračenja u životnoj sredini. Radionuklidi sa periodom poluraspada uporedivim sa starošću Zemlje i njihovi produkti raspada su zastupljeni u materijalima u životnoj sredini (stenama, zemljištu, vodi, ljudskom telu[1]. Drugu grupu čine radioaktivni izotopi koji se stalno proizvode. To su potomci raspada dugoživećih izotopa iz prve grupe, kao što su recimo radijum (Ra-226) i radon (Rn-222) i izotopi koji nastaju u različitim nuklearnim reakcijama koje se odvijaju u atmosferi od kojih su najpoznatiji tricijum (H-3) i radioaktivni ugljenik (C-14)[2]. Do otkrića radioaktivnih nizova došlo je tek nakon otkrića čuvenog radijuma Marije Kiri[3]. Merenja su pokazala da je period poluraspada radijuma 1600 godina. S obzirom na to da se starost Zemlje procenjuje na nekoliko miliona godina, oičgledno je da bi sve koliične radijuma na Zemlji već odavno iščezle da se u prirodi stalno ne stvaraju atomi radijuma. Činjenica da se radijum nalazi u uranovim rudama navela je na zaključak da radioaktivni raspad urana dovodi do obrazovanja atoma radijuma[4]
Nizovi
[уреди | уреди извор]Radioaktivni nizovi nose naziv po svojim rodonačelnicima: uranov, aktinijumov, torijumov i neptunijumov. Na Zemlji postoje produkti samo prva tri radioaktivna niza: uranovog, aktinijumovog i torijumovog, jer su se svi članovi neptunijumovog niza odavno raspali zbog relativno kratkoga perioda poluraspada. Periodi poluraspada U-238, U-235 i Th-232 su 4.5 milijardi godina, 700 miliona godina i 14 milijardi godina respektivno. Sva tri izotopa su alfa radioaktivni. Potomci ovih izotopa su takođe nestabilni pa se raspadaju, stvarajući nova lakša, takođe nestabilna jezgra, sve dok se ne postigne konfiguracija stabilnih izotopa olova, sa kojima se nizovi završavaju.
Pošto se prirodnom radioaktivnošću maseni broj može promeniti samo za 4, ovi radionuklidi mogu se svrstati u četiri niza sa masenim brojevima A koji zadovoljavaju relaciju: A = 4n + k, gdje je n prirodan broj, a k = 0, 1, 2, 3.
| Niz | Rodonačelnik (prvi član) | Period poluraspada rodonačelnika (godina) |
|---|---|---|
| Uranov | U-238 | 4,47·109 |
| Aktinijumov | U-235 | 7,04·108 |
| Torijumov | Th-232 | 1,41·1010 |
| Neptunijumov | Np-237 | 2,14·106 |
Uranov niz
[уреди | уреди извор]
"Rodonačelnik" uranovog niza je izotop urana U-238. Posle niza alfa i beta raspada, na kraju se dobija stabilni izotop olova Pb-206. Interesantno je da se atomska masa svakog izotopa ovog niza može napisati u obliku 4n+2, gde je n prirodan broj. Zbog toga se ovaj prirodni radioaktivni niz često i naziva "4n+2" niz. Izotop urana sa masenim brojem 238 emituje alfa-čestice sa vremenom poluraspada od 4,5 milijarde godina. Prema tome, od trenutka nastanka Zemlje uran se raspao veoma malo. Alfa-raspad U-238 dovodi do obrazovanja novog jzgra, sa rednim brojem 90 i masenim brojem 234, tj. izotopa Th-234 koji je radioaktivan i raspada se beta-raspadom čime se stvara, izotop protaktinijuma sa masenim brojem 234 (Pa-243). Ovaj izotop je takodje radioaktivan. Na taj naičn obrazuje se lanac radioaktivnih izotopa. Posle 14 uzastopnih radioaktivnih transmutacija U-238, on prelazi u neradioaktivan tj. stabilan izotop olova Pb-206. Sva radioaktivna jezgra između urana i olova su izotopi elemenata koji, uopšte i nemaju nijedan stabilni izotop. Razlika atomskih brojeva prvog i poslednjeg člana u ovom nizu je 238-206=32, što znači da u ovom nizu postoji 8 alfa-raspada, pošto beta raspadi ne menjaju maseni broj. Tih osam alfa-raspada promenilo bi redni broj urana za 16, a kako je razlika rednih brojeva prvog i poslednjeg člana niza 92-82=10, znači da pored osam alfa raspada postoji i 6 beta- raspada.
Aktinijumov niz
[уреди | уреди извор]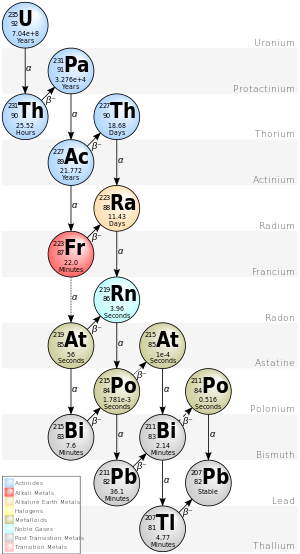
Aktinijumov niz ne počinje aktinijumom, nego izotopom urana U-235. Nekada se U-235 nazivao aktin-uran, pa otuda i naziv celog niza. Izotopu U-235 je prethodio radioaktivni izotop Pu-239, ali se on u međuvremenu raspao i danas ne postoji u prirodi. Ovaj niz se završava stabilnim izotopom Pb-207. Maseni brojevi svih članova zadovoljavaju izraz 4n+3. U aktinijumovom nizu ima 7 alfa-raspada и 4 beta-raspada[5].
Torijumov niz
[уреди | уреди извор]Torijumov niz počinje radioizotopom Th-232, a završava se stabilnim izotopom Pb-208. Atomske mase članova ovog niza zadovoljavaju izraz 4n. Treba reći da je ovaj niz započinjao izotopom Cf-252, ali su se od svog nastanka do danas svi članovi niza koji prethode torijumu (Cf-252, Cm-248, Pu-244, U-240, Np-240, Pu-240, U-236) raspali, i danas ne postoje u prirodi. U torijumovom nizu ima 6 alfa-raspada и 4 beta-raspada[6]
Neptunijumov niz
[уреди | уреди извор]Logično je bilo očekivati da će se naći i niz "4n+1". Taj niz je nekada zaista postojao i počinjao je izotopom Cf-249, a završavao se stabilnim izotopom Bi-209. Izotop ovog niza sa najdužim vremenom poluraspada bio je Np-237, pa otuda i naziv "neptunijumov niz". Svi članovi ovog niza su se do danas raspali i ovaj niz u prirodi više ne postoji.[7]]. Tačnije, postoji još samo njegov poslednji član. Nedavno je otkriveno da Bi-209 nije stabilan, već da se i on raspada alfa-raspadom dajući Tl-205. Ovaj raspad se odvija izuzetno lagano (period poluraspada = 1,9 · 1019 godina).
Raspadi i aktvnost
[уреди | уреди извор]Osnovni procesi transformacije jezgara kod ovih nizova su alfa i beta raspadi. U sva tri radioaktivna niza alfa-emiteri su raspoređeni relativno ravnomerno[8]. To su prvi članovi (začetnici) svih serija, svi gasoviti produkti (izotopi radona) i svi poslednji radioaktivni produkti raspada niza. Sto se tiče gama-aktivnosti u svakom nizu ističe se nekoliko glavnih gama-emitera. U torijumovom nizu to je Ac i neki njegovi potomci, u uranovom nizu to su Ra, Pb i Bi, a u aktinijumovom nizu sam uran i njegov potomak Ra. U torijumovom nizu, gama-emiteri su raspodeljeni relativno ravnomerno duž celog lanca. U aktinijumovom nizu glavni gama-emiteri su prvi, preradonski članovi, all ovu povoljnost sa stanovišta analize gama-spektra potire ukupna smanjena gama-aktivnost ovog niza koja je posledica niske izotopske obilnosti U-235.
Radioaktivno grananje
[уреди | уреди извор]Za svaki niz je karakteristična pojava grananje niza koja nastaje usled toga što neki radionuklidi imaju dvostruku mogućnost raspada sa odgovarajućom verovatnoćom (alfa-raspad i beta-raspad). Ti članovi u nizu ne raspadaju se uz emisiju samo jedne čestice, već je radioaktivni raspad propraćen emisijom različitih čestica. To može biti alfa čestica ili beta čestica. Emisija dve čestice je u stvari nastaje iz dva nezavisna radioaktivna raspada koji konkurišu jedan drugom.
Radioaktvna ravnoteža
[уреди | уреди извор]Aktivnost ill brzina raspada nestabilnih izotopa određena je brojem neraspadnutih jezgara u datom trenutku[9]. Svi potomci u radioaktivnim nizovima imaju daleko kraći period poluraspada od prvih članova niza i ne bi ni postojali na Zemlji da se stalno ne proizvode raspadima svojih dugoživećih rodonačelnika[10] . U ovoj situaciji kada se potomci znatno brže raspadaju od rodonačelnika niza, posle nekoliko vremena poluraspada potomaka uspostavlja se režim koji se zove vekovna ili sekularna ravnoteža. U ravnoteži aktivnost svih članova u nizu postaje jednaka aktivnosti rodonačelnika niza.
Ravnoteža nastaje kada se brzina nastajanja izjednačava sa brzinom nestajanja za sve članove u nizu, osim prvog i poslednjeg. Na taj način se broj atoma za svaki izotop u nizu održava stalnim. Količine izotopa potomaka nalaze u direktnoj srazmeri sa njihovim periodima poluraspada što znači da atoma dugoživećih izotopa ima mnogo, a kratkoživećih malo. Jedino poslednjeg, stabilnog, člana niza stalno ima sve više, dok se konačno svi atomi rodonačelnika niza ne transformišu u u atome poslednjeg člana. Ako nema narušavanje ravnoteže, količina poslednjeg stabilnog člana niza u smeši izotopa svih članova niza, u odnosu na preostalu količinu rodonačelnika niza govori o starosti te smeše. Kada je radioaktivni niz u ravnoteži, aktivnosti svih radionuklida u nizu su iste, te se koncentracija predaka može odrediti merenjem intenziteta gama zračenja bilo kog potomka.
U mnogim mineralima i stenama u Zemljinoj kori ravnoteža se praktično ne narušava što je osnova nuklearne geohronologije. Budući da je na tempo radioaktivnih raspada praktično nemoguće uticati, ovo je najpouzdaniji metod za objektivno merenje starosti stena i minerala odnosno način kojim je određena starost ne samo Zemlje, nego i Meseca i mnogih meteorita.
Narušavanje ravnoteže
[уреди | уреди извор]Do narušavanja ravnoteže dolazi kada se iz ove smeše izotopa neki od njih uklanjaju različitim različitim hemijskim ili fizičkim procesima. Jedan od načešćih uzroka narušavanja ravnoteže je emanacija radona. Narušavanje ravnoteže usled geohemijskih procesa dešava se kod dugoživećih članova niza - torijuma Th-230 i radijuma Ra-226 u uranovom nizu. U prirodnim geohemijskim procesima dolazi do raspadanja i ispiranja radijuma iz minerala i ruda urana, on se rastvara u vodi, migrira i gradi sekundarrne minerale, tako da često radijuma u uzorku ima manje ili više nego što odgovara njegovoj radioaktivnoj ravnoteži sa uranom.
Emanacija radona
[уреди | уреди извор]U prvoj polovini lanca svake serije preovlađuje alfa-raspad, a u drugoj polovini beta-raspad. U sredini lanca svake serije nastaje radioaktivni izotop radon koji je u gasovitom agregatnom stanju i može da isparava što dovodi do narušavanja ravnoteže. Iza radona[11], u sva tri niza, sledi grupa kratkoživućih elemenata koji nisu gasovi, a deo njihovih jezgara raspada se alfa-raspadom, a u drugi deo beta-raspadom. U prirodi su najzastupljenija dva izotopa radioaktivnog gasa radona: radon Rn-222 sa periodom poluraspada od 3.824 dana i toron Rn-220 sa periodom poluraspada od 55.6 s. 222Rn je prisutan u nizu uranijuma 238U i predstavlja najznačajniji radonov izotop. Rn-222 je prisutan u nizu torijuma i uzima se u obzir u situacijama kada on ili njegovi potomci dostižu veće koncentracije kod merenja emanacije radona iz zemljišta i pronalaženja mesta ulaska radona. Gаsoviti produkti u rаdiоаktivnim nizovimа urаnijumа i torijumа: rаdon Rn-222 i toron Rn-220 nаpuštајu mesto generisаnја i kао inertni gаsovi difuzijom dospevајu u vаzduh ili vodu i nа tај nаčin nekada obrаzuju znаčајne koncentrаcije u zаtvorenim prostorimа, što može biti i rаdiјаcioni rizik za izloženo stаnovništvo. Emanacija gasa radona iz uzoraka narušava ravnotežu nizova uranijuma i torijuma kod članova Rn-222 i Rn-220. Držanjem uzoraka u hermetički zatvorenim sudovima u trajanju od oko 10 perioda poluraspada (za Rn-222 je to približno 40 dana, a za toron Rn-220 oko 10 minuta) ova se ravnoteža može ponovo uspostaviti.
Reference
[уреди | уреди извор]- ^ UNSCEAR (2000) United Nations Scientific Committee on the Effects of Atomic Radiation. Sources and effects of ionizing radiation. UNSCEAR 2000 Report to the General Assembly, with scientific annexes
- ^ S. Macura, J. Radić-Perić, Atomistika, Fakultet za fizičku hemiju Univerziteta u Beogradu/Službeni list, Beograd, 2004. glava 11
- ^ Her 1911 Nobel Prize in Chemistry was granted to "Marie Sklodowska Curie" File:Dyplom Sklodowska-Curie.jpg
- ^ Frederick Soddy, "The Radio Elements and the Periodic Law", Chem. News, Nr. 107, (1913). стр. 97–99 ^ Jump up to: a b L'Annunziata, Michael F. . Radioactivity: Introduction and History. Amsterdam, Netherlands: Elsevier Science. 2007. ISBN 9780080548883. стр. 2.
- ^ Kasimir Fajans, "Radioactive transformations and the periodic system of the elements". Berichte der Deutschen Chemischen Gesellschaft, Nr. 46, (1913). стр. 422–439
- ^ Frederick Soddy, "The Radio Elements and the Periodic Law", Chem. News, Nr. 107, (1913). стр. 97–99
- ^ Koch, Lothar (2000). „Transuranium Elements”. Ullmann's Encyclopedia of Industrial Chemistry. ISBN 9783527303854. doi:10.1002/14356007.a27_167..
- ^ NUBASE evaluation of nuclear and decay properties
- ^ />Patel, S.B. . Nuclear physics: an introduction. New Delhi: New Age International. 2000. ISBN 978-81-224-0125-7. стр. 62–72.
- ^ "Decay and Half Life". Retrieved 2009-12-14. http://www.iem-inc.com/prhlfr.html].
- ^ Sturrock, P.A.; Steinitz, G.; Fischbach, E.; Javorsek, D.; Jenkins, J.H. (2012). „Analysis of gamma radiation from a radon source: Indications of a solar influence”. Astroparticle Physics. 36 (1): 18—25. Bibcode:2012APh....36...18S. S2CID 119163371. arXiv:1205.0205
 . doi:10.1016/j.astropartphys.2012.04.009.
. doi:10.1016/j.astropartphys.2012.04.009.
