Електролиза
Електролиза је разлагање хемијског једињења под утицајем електричне струје.[1] Процес не треба мешати са електролитичком дисоцијацијом.
Кратак преглед[уреди | уреди извор]
Када се јонско једињење раствори у адекватном растварачу, или истопи топлотом тако да су јони доступни у води. Електрична струја се примени кроз пар инертних електрода уроњених у течност. Негативно наелектрисана електрода се назива катода а позитивно наелектрисана анода. Свака електрода привлачи јоне супротног наелектрисања. Позитивно наелектрисани јони (катјони) крећу се ка катоди, док негативно наелектрисани јони (анјони) крећу се ка аноди. Енергија потребна да се јонска веза раскине и проузрокује њихово скупљање код одговарајућих електрода, омогућује електрична струја. Код електрода, електрони се апсорбују и додају јонима, формирајући жељени елемент или једињење.
У електролизи, анода је позитивна електрода, што значи да има мањак електрона; једињења која долазе у контакт са анодом отпуштају електроне(оксидују се). Катода је негативна електрода, што значи да има вишак електрона. Једињења која долазе у контакт са катодом теже да приме електроне (редукују се).
Количина електричне енергије која мора бити додата једнака је промени у Гибсовој слободној енергији у реакцији плус губитак у систему. Губици могу(у теорији) бити близу нуле, па максимални термодинамички добитак је једнак промени термодинамичког потенцијала подељеног са слободном енергијом. У већини случајева електрична енергија је већа од промене термодинамичког потенцијала, па се нешто енергије ослободи у виду топлоте. У неким случајевима, на пример у електролизи водене паре у водоник и кисеоник на виској температури, тачно је обрнуто. Топлота се апсорбује од околине, и топлотна енергија водоника је већа од електричне енергије. У овом случају се мисли да је коефицијент ефикасности већи од 100%. Онда је могуће направити машину са перпетуалним покретима (Перпетуум мобиле прве класе је још бољи од ове машине, он ствара енергију да притом не троши ништа, а то је немогуће).
Јачи проток струје (у амперима) подразумева већи проток електрона у истом интервалу времена. То значи да се катода брже редукује а анода брже оксидује. То је директно пропорционало броју молова добијеног производа. Јачина струје која пролази зависи од електричне проводљивости електрода и електролита, али јачина струје такође зависи од тога колико струје сам извор може створити. Процес електролизе са само два или три реактанта може бити веома комплексан. У већини случајева је најбоље потражити литературу и погледати која јачина струје је најповољнија за жељени процес. На пример код неких метала може доћи до различитих типова галванизације(то је процес пресвлачења једног метала у други, да не би на пример кородирао), користећи струју већег интензитета лако се добија лош галванизован метал, а користећи слабију много бољи.
Већа разлика у електричним потенцијалима би проузроковала већу разлику у потенцијалима да би омогућила електролитичкој ћелији да оксидује и редукује тешко раскидљиве компоненте. То може драстично утицати на форму(како хемијску тако и физичку) продукта у датом експерименту. Уопштено и јачина струје(у амперима) и напон(у волтима) утиче на то шта ће се створити у ћелији.
Следеће технологије су повезане са електролизом:
- Електрохемијска ћелија, укључујући водоникову ћелију.
- Електрофореза је електролиза где је растварач гел:користи се да раздвоји супстанце, као што су ДНК честице, базирано на њиховом наелектрисању.
Електролиза воде[уреди | уреди извор]
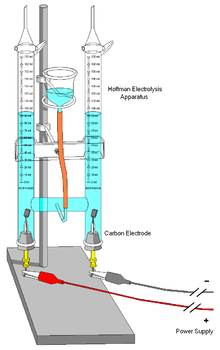
Хофманов апарат за електролизу воде
Важна примена електролизе воде је добијање водоника
2H2O(l) → 2H2(g) + O2(g); E0 = +1.229 V
Овај поступак је предложен за промену друштва ка употреби водоника као главног горива за напајање електричних мотора и мотора са унутрашњим сагоревањем.
Електролиза воде може се посматрати помоћу протока ДС (једносмерне) струје коју ствара батерија или други ДС извор у чаши воде (у пракси се користи слана вода јер повећава интензитет реакције и помоћу ње се та реакција лакше прати). Користећи електроде од платине, водоников гас би се видео да испарава код катоде, а кисеоник код аноде. Ако би се користили други метали кисеоник би реаговао са анодом уместо да се ослободи. На пример користећи електроде од гвожђа у раствору натријум хлорида, гвожђе оксид ће се наградити код аноде који ће да реагује и створиће се гвожђе хидроксид. Када се створе велике количине водоника електролитичка ћелија се загађује и због тога се гвожђе не користи у комерцијалној електролизи.
Ефикасност енергије која се добија електролизом воде веома варира. Неки извештаји тврде да је ефикасност између 50%-70%. Други извештаји тврде да је теоријски максимална ефикасност између 80%-94%. Теоријски максимум подразумева тоталну количину енергије коју су водоник и кисеоник апсорбовали. Ове вредности се односе на конвертовање електричне енергије у водоникову хемијску енергију. Енергија која је изгубљена током стварања електрицитета се не рачуна. На пример, ефикасност електране која конвертује топлоту нуклеарне реакције у водоник помоћу електролизе је 25%-50%.
Око четири процента водоника се у свету добија електролизом. Водоник се користи за прављење амонијака за ђубриво, и конвертовање тешких нафтних ресурса у лакше фракције.
Типично у индустрији, напон већи од 17 kV може да елиминише потребу да електроде буду физички близу, и да се јонски састојци, као што је со, не морају додавати.
Историја[уреди | уреди извор]
Почетком деветнаестог века, Вилијам Николсон и Ентони Карлајл настојали су да продуже Волтине експерименте. Они су причврстили две жице на супротним странама напонске гомиле и ставили друге крајеве у цев напуњену водом. Приметили су да када су жице спојене да свака жица производи мехуриће. Једна врста је била водоник, друга је био кисеоник.[2]
Године 1785, холандски научник по имену Мартин ван Марум створио је електростатички генератор који је користио да редукује калај, цинк и антимон из њихових соли користећи процес касније познат као електролиза. Иако је он несвесно произвео електролизу, тек 1800. године Вилијам Николсон и Ентони Карлајл су открили како електролиза функционише.[3]
Године 1791, Луиђи Галвани је експериментисао са жабљим ногама. Тврдио је да је стављање животињског мишића између два различита метална лима резултирало струјом. Одговарајући на ове тврдње, Алесандро Волта је спровео сопствене тестове.[4][5] Ово би дало увид у идеје Хамфрија Дејвија о електролизи. Током прелиминарних експеримената, Хамфри Дејви је претпоставио да када се два елемента комбинују и формирају једињење, електрична енергија се ослобађа. Хамфри Дејви је наставио да креира табеле разлагања из својих прелиминарних експеримената на електролизи. Табеле разлагања су дале увид у енергије потребне за разлагање одређених једињења.[6]
Године 1817, Јохан Август Арфведсон је утврдио да постоји још један елемент, литијум, у неким од његових узорака; међутим, није могао да изолује компоненту. Тек 1821. године, Вилијам Томас Бранд је користио електролизу да га издвоји. Две године касније, он је поједноставио процес користећи литијум хлорид и калијум хлорид са електролизом за производњу литијума и литијум хидроксида.[7][8]
Током каснијих година истраживања Хамфрија Дејвија, Мајкл Фарадеј је постао његов помоћник. Док је проучавао процес електролизе под Хамфријем Дејвијем, Мајкл Фарадеј је открио два закона електролизе.[5] У време Максвела и Фарадаја, појавила се забринутост за електропозитивне и електронегативне активности.[9] У новембру 1875, Паул Емил Лекок де Буабодран је открио галијум помоћу електролизе галијум хидроксида, давијујући 3,4 mg галијума. Следећег децембра представио је своје откриће галијума Академији наука у Паризу.[10]
Дана 26. јуна 1886. године, Фердинанд Фредерик Хенри Мојсан се разрадио процес ивођења електролизе на анхидрованом флуороводонику да би створио гасовити флуор као чист елемент. Пре него што је користио флуороводоник, Хенри Мојсан је користио соли флуорида за електролизу. Тако је 28. јуна 1886. извео свој експеримент пред Академијом наука да покаже своје откриће новог елемента флуора.[11] Док су покушавали да пронађу елементарни флуор путем електролизе флуоридних соли, многи хемичари су страдали, укључујући Паулин Лује и Жерома Никлеса.[12]
Године 1886, Шарл Мартин Хол из Америке и Пол Еро из Француске су поднели захтеве за америчке патенте за електролизу алуминијума, при чему је Еро поднео свој у мају, а Хол у јулу.[13] Хол је успео да добије свој патент доказујући кроз писма свом брату и породици доказе да је његов метод откривен пре него што је поднет француски патент.[14] Ово је постало познато као Хол–Еров процес који је био користан за многе индустрије, јер је цена алуминијума тада пала са четири долара на тридесет центи по фунти.[15]
Научници[уреди | уреди извор]
Научни пионири електролизе су:
- Хамфри Дејви
- Мајкл Фарадеј
- Пол Еру
- Сванте Архенијус
- Адолф Вилхелм Херман Колбе
- Вилијам Николсон
- Жозеф Луј Геј-Лисак
- Александар фон Хумболт
- Вилијам Чјанг
- Дејвид Конднер
Електролиза тешке воде у познатом експерименту у ком се јављају аномалије у стварању топлоте и контроверзна тврдња хладне фузије.
Први закон електролизе[уреди | уреди извор]
У 1832. години, Мајкл Фарадеј је открио да је количина елемената раздвојена помоћу једносмерне струје пропорционална количини електричне струје која пролази кроз коло.[16] Ова тврдња је постала основа првог закона електролизе
Други закон електролизе[уреди | уреди извор]
Фарадеј је такође открио да су масе раздвојених елемената директно пропорционалне атомским масама елемената када се примени одговарајући целобројни делилац. То је пружило снажан доказ да делићи електрицитета заиста постоје као делови атома елемената.
Индустријске примене[уреди | уреди извор]
- Индустријска производња алуминијума, литијума, натријума, калијума, аспирина.
- Индустријска производња водоника за аутомобиле.
- Електролиза на високој температури се такође користи у те сврхе.
- Индустријска производња хлора и натријум хидроксида.
- Индустријска производња калијум хлорида.
Електролиза има више примена:
- Електрометалургија је процес редукције метала од других једињења да би се добио чист метал. На пример: Натријум Хидроксид се у овој форми дели помоћу електролизе на натријум и водоник од којих оба имају важну примену.
- Електрична рафинација се користи да се метал очисти од непожељних примеса електролизом. Као на пример у једињењу бакра и неких примеса. При електролизи бакар се формира око катоде а нечистоће око аноде.
- Електролизована вода је једна од најчистијих вода која се користи у здравству и стоматологији.
- Дисање у свемиру је још једна примена електролизе. Кисеоник који астронаути удишу се ствара електролизом воде, помоћу сунчеве светлости, енергије.
- Научници су већ спремили план за будућу примену електролизе. Верује се да би водоник могао да буде гориво будућности (водоник потпуно сагорева и не ослобађају се никакви штетни гасови). Процес електролизе воде се може користити да би се добио водоник. Све што је потребно је мало јефтине струје да би се отпочео процес.
Референце[уреди | уреди извор]
- ^ „Електролиза”. Енциклопедија. Приступљено 21. 1. 2019.
- ^ Fabbri, Emiliana; Schmidt, Thomas J. (5. 10. 2018). „Oxygen Evolution Reaction—The Enigma in Water Electrolysis”. ACS Catalysis (на језику: енглески). 8 (10): 9765—9774. doi:10.1021/acscatal.8b02712
 .
.
- ^ Ashworth, William (20. 3. 2015). „Martinus van Marum - Scientist of the Day”. Linda Hall Library.
- ^ Ihde, Aaron J. (1964). The Development of Modern Chemistry. Harper & Row. стр. 125–127.
- ^ а б „The History of Electrochemistry: From Volta to Edison”. ECS (на језику: енглески). Приступљено 2019-10-11.
- ^ Thorpe, Thomas (1896). Humphry Davy, Poet and Philosopher. New York: Macmillan & Co., Limited.
- ^ „Lithium - periodicstats.com”. www.periodicstats.com. Архивирано из оригинала 15. 4. 2021. г.
- ^ Helmenstine, Todd (11. 1. 2018). „Today in Science History - January 12 - Johan August Arfwedson and Lithium”. Science Notes and Projects.
- ^ Ede, Andrew (2017). A History of Science in Society (3rd изд.). Toronto, Canada: University of Toronto Press. стр. 251. ISBN 978-1-4426-3499-2.
- ^ Marshall, James and Virginia. „Rediscovery of the Elements – Gallium” (PDF). University of North Texas. Архивирано (PDF) из оригинала 2022-10-09. г.
- ^ Wisniak, Jaime (2018-08-26). „Henri Moissan: The discoverer of fluorine”. Educación Química. 13 (4): 267. ISSN 1870-8404. S2CID 92299077. doi:10.22201/fq.18708404e.2002.4.66285.
- ^ Marshall, James and Virginia. „Rediscovery of the Elements- Fluorine and Henri Moissan” (PDF). University of North Texas. Архивирано (PDF) из оригинала 2022-10-09. г.
- ^ Beck, Theodore R. (21. 8. 2015). „ECS Classics: Hall and Héroult and the Discovery of Aluminum Electrolysis”. ECS. Interface.
- ^ Hall Process Production and Commercialization of Aluminum - National Historic Chemical Landmark (на језику: енглески). Oberlin, Ohio: American Chemical Society. 1997.
- ^ „Paul Héroult and Charles M. Hall”. Science History Institute (на језику: енглески). 1. 6. 2016.
- ^ „Фарадејеви закони електролизе”. Хемијски речник. Приступљено 21. 1. 2019.
Литература[уреди | уреди извор]
- LaConti AB, Molter TM, Zagaja JA (мај 1986). Electrochemical Reduction of Carbon Dioxide. Online: Information for the Defense Industry. Архивирано из оригинала 27. 3. 2012. г.
- Fujita E (јануар 2000). Carbon Dioxide (Reduction). Upton, NY (United States): Brookhaven National Lab. (BNL).
- Neelameggham NR. „Carbon Dioxide Reduction Technologies: A Synopsis of the Symposium at TMS 2008”. The Minerals, Metals & Materials Society (TMS).
